Наночастица, содержащая рапамицин и альбумин, в качестве противоракового агента
Иллюстрации
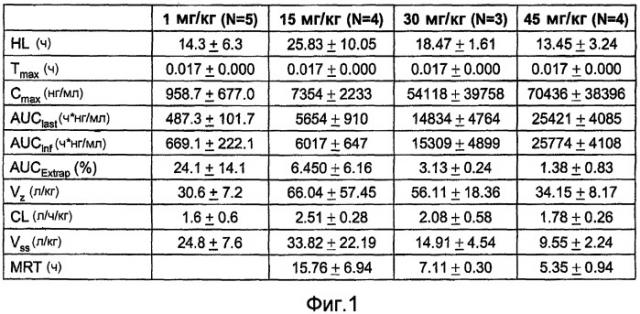
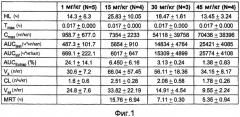
Показать всеГруппа изобретений относится к медицине, а именно к онкологии, и может быть использована для лечения рака. Для этого пациенту вводят эффективное количество фармацевтической композиции, содержащей наночастицы, которые содержат рапамицин и белок носитель, где количество рапамицина в композиции составляет от приблизительно 54 мг до приблизительно 540 мг. Группа изобретений также относится к единичной лекарственной форме, содержащей вышеуказанный состав и фармацевтически приемлемый носитель, и к набору для лечения рака. Использование данной композиции позволяет подавлять, стабилизировать и/или задерживать развитие рака и дополнительно обеспечивает способы комбинированной терапии лечения рака. 3 н. и 78 з.п. ф-лы, 2 табл., 7 ил., 15 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Эта заявка заявляет приоритет относительно предварительной заявки с порядковым номером 60/905,669, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,662, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,735, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,672, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,787, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,663, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/905,767, поданной 7 марта 207 года, предварительной заявки с порядковым номером 60/905,750, поданной 7 марта 2007 года, предварительной заявки с порядковым номером 60/923,248, поданной 13 апреля 2007 года, и предварительной заявки с порядковым номером 60/923,456, поданной 13 апреля 2007 года, полные описания которых включены здесь в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Эта заявка относится к способам и композициям для лечения, стабилизации, предотвращения и/или задержки рака с использованием наночастиц, которые содержат рапамицин или его производное. Эта заявка дополнительно обеспечивает способы комбинированной терапии лечения рака, предусматривающие введение индивидууму эффективного количества наночастиц, которые содержат рапамицин или его производное, и второй терапии.
УРОВЕНЬ ТЕХНИКИ
Неспособность значительного числа опухолей отвечать на лекарственное средство и/или лучевую терапию является серьезной проблемой в лечении рака. Фактически это является одной из главных причин, почему многие из наиболее преобладающих форм рака человека все еще противостоят эффективному химиотерапевтическому вмешательству, несмотря на определенные успехи в области химиотерапии.
В настоящее время рак лечат прежде всего одной или комбинацией из трех типов терапий: хирургии, лучевой терапии и химиотерапии. Хирургия является традиционным подходом, в котором всю опухоль или часть опухоли удаляют из тела. Обычно хирургия является эффективной только для лечения ранних стадий рака. Хотя хирургия иногда является эффективной в удалении опухолей, локализованных в определенных участках, например в молочной железе, ободочной кишке и коже, она не может быть использована в лечении опухолей, локализованных в других участках, недоступных для хирургов, или в лечении диссеминированных неопластических состояний, таких как лейкоз. Для более чем 50% индивидуумов, имеющих рак, ко времени установления их диагноза они уже не являются кандидатами для эффективного хирургического лечения. Хирургические процедуры могут увеличивать метастазы опухоли через кровоток во время хирургии. Большинство раковых индивидуумов не умирают в момент установления диагноза или хирургии, но чаще умирают от метастазов и рецидива рака.
Другие терапии часто являются также неэффективными. Лучевая терапия является эффективной только для индивидуумов, которые обнаруживают клинически локализованное заболевание на ранней или средней стадиях рака, и она неэффективна для поздних стадий рака с метастазированием. Облучение обычно применяют к определенному участку тела субъекта, который содержит патологическую пролиферативную ткань, для максимизации дозы, абсорбируемой этой патологической тканью, и минимизации дозы, абсорбируемой соседней нормальной тканью. Однако селективное применение терапевтического облучения к патологической ткани является трудным (если не невозможным). Так, нормальная ткань, ближайшая к патологической ткани, также подвергается потенциально повреждающим дозам облучения в ходе обработки. Таким образом, эффективность способов лучевой терапии в разрушении патологических пролиферативных клеток пропорциональна ассоциированным цитотоксическим действиям на близлежащие нормальные клетки. Вследствие этого, способы радиотерапии имеют свойственный им узкий терапевтический индекс, который приводит к неадекватному лечению большинства опухолей. Даже наилучшие радиотерапевтические способы могут приводить к неполному уменьшению опухоли, рецидиву опухоли, увеличенной опухолевой массе и индукции устойчивых к облучению опухолей.
Химиотерапия включает в себя нарушение репликации клеток или метаболизма клеток. Химиотерапия может быть эффективной, но имеются тяжелые побочные эффекты, например рвота, низкое количество лейкоцитов, выпадение волос, потеря массы и другие токсичные эффекты. Вследствие этих чрезвычайно токсичных эффектов, многие имеющие рак индивидуумы не могут успешно завершить полную схему химиотерапии. Индуцируемые химиотерапией побочные эффекты существенным образом влияют на качество жизни индивидуума и могут разительным образом влиять на согласие индивидуума на это лечение. Кроме того, вредные побочные эффекты, ассоциированные с химиотерапевтическими агентами, являются обычно главной ограничивающей дозу токсичностью в введении этих лекарственных средств. Например, воспаление слизистой оболочки является одной из главных ограничивающих дозу токсичностей для некоторых противораковых агентов, включающих в себя 5-ФУ, метотрексат и противоопухолевые антибиотики, такие как доксорубицин. Многие из этих индуцируемых химиотерапией побочных эффектов, если они тяжелые, могут приводить к госпитализации или требовать лечения анальгезирующими средствами для лечения боли. Некоторые раковые индивидуумы умирают от химиотерапии вследствие слабой переносимости химиотерапии. Эти чрезвычайно высокие побочные эффекты противораковых лекарственных средств вызваны плохой специфичностью нацеливания таких лекарственных средств. Эти лекарственные средства циркулируют через большинство здоровых органов индивидуумов, так же как и через предполагаемые опухоли-мишени. Эта плохая специфичность нацеливания, которая вызывает побочные эффекты, уменьшает также эффективность химиотерапии, так как лишь часть этих лекарственных средств точно поражает цель. Эффективность химиотерапии дополнительно уменьшается слабым удерживанием противораковых лекарственных средств в опухолях-мишенях.
Другой проблемой, ассоциированной с химиотерапией, является развитие устойчивости к лекарственным средствам. Устойчивость к лекарственным средствам является термином, относящимся к обстоятельствам, когда заболевание не отвечает на лекарственное средство или лекарственные средства, используемые в лечении. Устойчивость к лекарственным средствам может быть либо неотъемлемой, что означает, что заболевание никогда не отвечало на это лекарственное средство или на эти лекарственные средства, либо она может быть приобретенной, что означает, что заболевание перестало отвечать на лекарственное средство или лекарственные средства, на которые это заболевание ранее отвечало. Комбинированная терапия, в том числе комбинированная химиотерапия, имеет потенциальные преимущества как в отношении избежания возникновения устойчивых клеток, так и в отношении убивания предсуществующих клеток, которые уже являются устойчивыми.
Вследствие этих недостатков существующих терапий для рака, тяжести и распространенности неоплазмы, опухоли и рака, существует по-прежнему значительная заинтересованность в дополнительных или альтернативных терапиях и потребность в них для лечения, стабилизации, предотвращения и/или задержки рака. Предпочтительно, эти терапии должны преодолевать недостатки существующих способов хирургии, химиотерапии и облучения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение обеспечивает способы лечения рака с использованием наночастиц, которые содержат рапамицин или его производное. Таким образом, это изобретение в некоторых вариантах осуществления обеспечивает способ лечения рака у индивидуума за счет введения этому индивидууму (например, человеку) эффективного количества композиции, содержащей наночастицы, которые содержат рапамицин или его производное и белок-носитель. В некоторых вариантах осуществления этим раком является рак ранней стадии, неметастатический рак, рак в ремиссии, рецидивирующий рак, рак в адъювантном сеттинге, рак в неоадъювантном сеттинге или рак, по существу не поддающийся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак не является солидной опухолью (т.е. он является другим, чем солидная опухоль). В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является карциномой (т.е. является другим, чем карцинома). В некоторых вариантах осуществления этот рак не является раком ободочной кишки (т.е. является другим, чем рак ободочной кишки). В некоторых вариантах осуществления этот рак не является раком молочной железы (т.е. является другим, чем рак молочной железы). В некоторых вариантах осуществления этот рак не является раком яичника, раком предстательной железы или раком головного мозга. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производного в эффективном количестве этой композиции находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления рапамицин или его производное вводят парентерально (например, внутривенно). В некоторых вариантах осуществления таксан не вводят индивидууму (т.е. вводят отличающееся от таксана лекарственное средство). В некоторых вариантах осуществления вводимый таксан не является композицией, содержащей таксан в наночастицах. В некоторых вариантах осуществления рапамицин или его производное является единственным фармацевтически активным агентом для лечения рака, который вводят этому индивидууму. В некоторых вариантах осуществления вводят рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления белком-носителем является альбумин, например сывороточный альбумин человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах равно менее чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих композициях наночастиц является меньшим, чем приблизительно 18:1.
Это изобретение обеспечивает также фармацевтические композиции, такие как единичные (стандартные) лекарственные формы, которые применимы для лечения рака. Таким образом, это изобретение в некоторых вариантах осуществления обеспечивает фармацевтическую композицию (например, единичную (стандартную) лекарственную форму фармацевтической композиции), которая включает в себя наночастицы, которые содержат рапамицин или его производное и белок-носитель. В некоторых вариантах осуществления эта композиция включает в себя фармацевтически приемлемый носитель. В различных вариантах осуществления рак является раком ранней стадии, неметастатическим раком, первичным раком, запущенным раком, локально прогрессирующим раком, метастатическим раком, раком в ремиссии, рецидивирующим раком, раком в адъювантном сеттинге, раком в неоадъювантном сеттинге или раком, по существу не поддающимся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак не является солидной опухолью (т.е. он является другим, чем солидная опухоль). В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является карциномой (т.е. является другим, чем карцинома). В некоторых вариантах осуществления этот рак не является раком ободочной кишки (т.е. является другим, чем рак ободочной кишки). В некоторых вариантах осуществления этот рак не является раком молочной железы (т.е. является другим, чем рак молочной железы). В некоторых вариантах осуществления этот рак не является раком яичника, раком предстательной железы или раком головного мозга. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производных в композиции (например, в дозе или в единичной (стандартной) лекарственной форме) находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления рапамицин или его производное является единственным фармацевтически активным агентом для лечения рака, который содержится в этой композиции. В некоторых вариантах осуществления эта композиция содержит рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления белок-носитель является альбумином, таким как сывороточный альбумин человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах является меньшим, чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих композициях наночастиц равно менее чем приблизительно 18:1.
Еще в одном аспекте, это изобретение включает в себя набор с (i) композицией, содержащей наночастицы, которые содержат рапамицин или его производное и белок-носитель, и (ii) инструкции для применения в лечении рака. В различных вариантах осуществления этот рак является раком ранней стадии, неметастатическим раком, первичным раком, запущенным раком, локально прогрессирующим раком, метастатическим раком, раком в ремиссии, рецидивирующим раком, раком в адъювантном сеттинге, раком в неоадъювантном сеттинге или раком, по существу не поддающимся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является раком ободочной кишки. В некоторых вариантах осуществления этот рак не является раком молочной железы. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производного в этом наборе находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления рапамицин или его производное вводят парентерально (например, внутривенно). В некоторых вариантах осуществления этот набор не содержит таксан. В некоторых вариантах осуществления рапамицин или его производное является единственным фармацевтически активным агентом для лечения рака, который содержится в этом наборе. В некоторых вариантах осуществления этот набор содержит другой фармацевтически активный агент для лечения рака. В некоторых вариантах осуществления этим другим фармацевтически активным агентом является химиотерапевтический агент. В некоторых вариантах осуществления этот набор содержит рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления белок-носитель является альбумином, таким как сывороточный альбумин человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах равно менее чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного является меньшим, чем приблизительно 18:1.
Данное изобретение обеспечивает также способы лечения рака с использованием комбинированных терапий. Это изобретение обеспечивает способ лечения рака, предусматривающий: а) первую терапию, предусматривающую введение индивидууму эффективного количества композиции, содержащей наночастицы, содержащие рапамицин или его производное и белок-носитель, и b) вторую терапию, такую как хирургия, облучение, генотерапия, иммунотерапия, трансплантация костного мозга, трансплантация стволовых клеток, гормональная терапия, прицельная терапия, криотерапия, ультразвуковая терапия, фотодинамическая терапия и/или химиотерапия (например, одно или несколько соединений или их фармацевтически приемлемых солей, применимых для лечения рака).
В некоторых вариантах осуществления это изобретение обеспечивает способ лечения рака у индивидуума, предусматривающий введение этому индивидууму а) эффективного количества композиции, содержащей наночастицы, содержащие рапамицин или его производное и белок-носитель, и b) эффективного количества по меньшей мере одного другого химиотерапевтического агента. В некоторых вариантах осуществления этот химиотерапевтический агент является любым из (и в некоторых вариантах осуществления выбран из группы, состоящей из) антиметаболитов (в том числе аналогов нуклеозидов), агентов на основе платины, алкилирующих агентов, ингибиторов тирозинкиназ, антрациклиновых антибиотиков, винкаалкалоидов, ингибиторов протеасом, модуляторов HER2/neu, модуляторов EGFR, модуляторов VEGFR и ингибиторов топоизомераз. В некоторых вариантах осуществления этот химиотерапевтический агент является агентом на основе платины, таким как карбоплатин. В некоторых вариантах осуществления этот химиотерапевтический агент является модулятором HER2/neu (таким как ингибитор HER2/neu, например, Herceptin®). В некоторых вариантах осуществления этот химиотерапевтический агент является модулятором EGFR (таким как ингибитор EGFR, например, Erbitux®). В некоторых вариантах осуществления этот химиотерапевтический агент является анти-VEGF-антителом (таким как бевацизумаб, например, Avastin®). В некоторых вариантах осуществления эффективные количества композиции наночастиц и анти-VEGF-антитела синергически ингибируют пролиферацию клеток или метастазирование. В некоторых вариантах осуществления этот химиотерапевтический агент влияет на путь передачи сигнала, включающий в себя рапамицин в качестве мишени. В некоторых вариантах осуществления этот химиотерапевтический агент влияет на путь передачи сигнала, включающий в себя mTOR (такой как путь передачи сигнала PI3K/Akt). В некоторых вариантах осуществления таксан не вводят этому индивидууму. В некоторых вариантах осуществления вводимый таксан не присутствует в композиции наночастиц.
В некоторых вариантах осуществления композицию, содержащую наночастицы, содержащие рапамицин или его производное и белок-носитель, и химиотерапевтический агент вводят одновременно, либо в одной и той же композиции, либо в отдельных композициях. В некоторых вариантах осуществления композицию наночастиц, содержащую рапамицин или его производное и белок-носитель, и этот химиотерапевтический агент вводят последовательно, например композицию наночастиц вводят либо до, либо после введения химиотерапевтического агента. В некоторых вариантах осуществления введение композиции наночастиц, содержащих рапамицин или его производное и белок-носитель, и химиотерапевтического агента является совпадающим, например период введения композиции наночастиц и период введения химиотерапевтического агента перекрываются друг с другом. В некоторых вариантах осуществления введение композиции наночастиц, содержащих рапамицин или его производное и белок-носитель, и химиотерапевтического агента не является совпадающим. Например, в некоторых вариантах осуществления введение композиции наночастиц, содержащих рапамицин или его производное и белок-носитель, заканчивается до введения химиотерапевтического агента. В некоторых вариантах осуществления введение химиотерапевтического агента заканчивается до введения композиции наночастиц, содержащих рапамицин или его производное и белок-носитель.
В некоторых вариантах осуществления обеспечен способ лечения рака у индивидуума, предусматривающий а) первую терапию, предусматривающую введение этому индивидууму композиции, содержащей рапамицин или его производное и белок носитель, и b) вторую терапию, предусматривающую хирургию, облучение, генотерапию, иммунотерапию, трансплантацию костного мозга, трансплантацию стволовых клеток, гормональную терапию, прицельную терапию, криотерапию, ультразвуковую терапию, фотодинамическую терапию или их комбинации. В некоторых вариантах осуществления этой второй терапией является гормональная терапия. В некоторых вариантах осуществления этой второй терапией является лучевая терапия. В некоторых вариантах осуществления этой второй терапией является хирургия. В некоторых вариантах осуществления первую терапию проводят перед второй терапией. В некоторых вариантах осуществления первую терапию проводят после второй терапии.
В некоторых вариантах осуществления раком, который лечат комбинированной терапией, является рак ранней стадии, неметастатический рак, первичный рак, прогрессирующий рак, локально прогрессирующий рак, метастатический рак, рак в ремиссии, рецидивирующий рак, рак в адъювантном сеттинге, рак в неоадъювантном сеттинге или рак, по существу не поддающийся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак не является солидной опухолью (т.е. является другим, чем солидная опухоль). В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является карциномой (т.е. является другим, чем карцинома). В некоторых вариантах осуществления этот рак не является раком ободочной кишки (т.е. является другим, чем рак ободочной кишки). В некоторых вариантах осуществления этот рак не является раком молочной железы (т.е. является другим, чем рак молочной железы). В некоторых вариантах осуществления этот рак не является раком яичника, раком предстательной железы или раком головного мозга. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производного в эффективном количестве этой композиции, используемом в комбинированной терапии, находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления рапамицин или его производное вводят парентерально (например, внутривенно). В некоторых вариантах осуществления таксан не вводят индивидууму (т.е. вводят отличающееся от таксана лекарственное средство). В некоторых вариантах осуществления вводимый таксан не является композицией, содержащей таксан в наночастицах. В некоторых вариантах осуществления вводят рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления белком-носителем является альбумин, например сывороточный альбумин человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах равно менее чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих композициях наночастиц является меньшим, чем приблизительно 18:1.
Это изобретение обеспечивает также фармацевтические композиции, такие как единичные (стандартные) лекарственные формы, которые применимы в комбинированной терапии для лечения рака. Таким образом, это изобретение в некоторых вариантах осуществления обеспечивает фармацевтическую композицию (например, единичную (стандартную) лекарственную форму фармацевтической композиции) для применения в комбинированной терапии, которая включает в себя наночастицы, которые содержат рапамицин или его производное и белок-носитель. В некоторых вариантах осуществления эта фармацевтическая композиция включает в себя а) наночастицы, содержащие рапамицин или его производное и белок-носитель, и b) по меньшей мере один другой терапевтический агент. В некоторых вариантах осуществления этот другой терапевтический агент содержит химиотерапевтический агент. В некоторых вариантах осуществления этот другой терапевтический агент содержит гормональный терапевтический агент. В некоторых вариантах осуществления эта композиция включает в себя также фармацевтически приемлемый носитель. В некоторых вариантах осуществления этим раком является рак ранней стадии, неметастатический рак, первичный рак, прогрессирующий рак, локально прогрессирующий рак, метастатический рак, рак в ремиссии, рецидивирующий рак, рак в адъювантном сеттинге, рак в неоадъювантном сеттинге или рак, по существу не поддающийся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак не является солидной опухолью (т.е. является другим, чем солидная опухоль). В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является карциномой (т.е. является другим, чем карцинома). В некоторых вариантах осуществления этот рак не является раком ободочной кишки (т.е. является другим, чем рак ободочной кишки). В некоторых вариантах осуществления этот рак не является раком молочной железы (т.е. является другим, чем рак молочной железы). В некоторых вариантах осуществления этот рак не является раком яичника, раком предстательной железы или раком головного мозга. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производного в этой композиции (например, в дозе или в единичной (стандартной) лекарственной форме) для применения в комбинированной терапии находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления этот носитель пригоден для парентерального введения (например, внутривенного введения). В некоторых вариантах осуществления таксан не содержится в этой композиции. В некоторых вариантах осуществления рапамицин или его производное является единственным фармацевтически активным агентом для лечения рака, который содержится в этой композиции (например, в виде части набора, который содержит инструкции для применения этой композиции с другой терапией).
В некоторых вариантах осуществления эта композиция содержит рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления этот белок-носитель является альбумином, например сывороточным альбумином человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах равно менее чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах является меньшим, чем приблизительно 18:1.
Еще в одном аспекте, это изобретение включает в себя набор с (i) композицией, содержащей наночастицы, которые содержат рапамицин или его производное и белок-носитель, и (ii) инструкции для применения в комбинированной терапии для лечении рака. Это изобретение обеспечивает также наборы для применения композиций рапамицина (или его производных), описанных здесь, в контексте комбинированной терапии. Например, набор может обеспечивать такую композицию в дополнение к другой терапевтической композиции. В некоторых вариантах осуществления эти инструкции являются инструкциями для обеспечения первой и второй терапии, в которых либо первая, либо вторая терапия предусматривает введение композиции, которая содержит наночастицы рапамицина или его производного и белок-носитель. В некоторых вариантах осуществления этот набор дополнительно содержит по меньшей мере один другой терапевтический агент. В некоторых вариантах осуществления этот другой терапевтический агент включает в себя химиотерапевтический агент. В некоторых вариантах осуществления этот другой терапевтический агент включает в себя гормональный терапевтический агент. В некоторых вариантах осуществления этим раком является рак ранней стадии, неметастатический рак, первичный рак, прогрессирующий рак, локально прогрессирующий рак, метастатический рак, рак в ремиссии, рецидивирующий рак, рак в адъювантном сеттинге, рак в неоадъювантном сеттинге или рак, по существу не поддающийся гормональной терапии. В некоторых вариантах осуществления этот рак является солидной опухолью. В некоторых вариантах осуществления этот рак не является солидной опухолью (т.е. является другим, чем солидная опухоль). В некоторых вариантах осуществления этот рак является плазмацитомой. В некоторых вариантах осуществления этот рак является множественной миеломой, раком почки (почечно-клеточным раком), раком предстательной железы, раком легкого, меланомой, раком головного мозга (например, глиобластомой), раком яичника или раком молочной железы. В некоторых вариантах осуществления этот рак не является карциномой (т.е. является другим, чем карцинома). В некоторых вариантах осуществления этот рак не является раком ободочной кишки (т.е. является другим, чем рак ободочной кишки). В некоторых вариантах осуществления этот рак не является раком молочной железы (т.е. является другим, чем рак молочной железы). В некоторых вариантах осуществления этот рак не является раком яичника, раком предстательной железы или раком головного мозга. В некоторых вариантах осуществления один или несколько симптомов этого рака являются ослабленными. В некоторых вариантах осуществления этот рак задерживается или предупреждается.
В некоторых вариантах осуществления количество рапамицина или его производного в наборе для применения в комбинированной терапии находится в диапазоне приблизительно 54 мг - приблизительно 540 мг, например, приблизительно 180 мг - приблизительно 270 мг или приблизительно 216 мг. В некоторых вариантах осуществления рапамицин или его производное вводят парентерально (например, внутривенно). В некоторых вариантах осуществления этот набор не содержит таксан. В некоторых вариантах осуществления рапамицин или его производное является единственным фармацевтически активным агентом для лечения рака, который содержится в этом наборе. В некоторых вариантах осуществления это набор содержит другой фармацевтически приемлемый агент для лечения рака. В некоторых вариантах осуществления этим другим фармацевтически активным агентом является химиотерапевтический агент. В некоторых вариантах осуществления этот набор содержит рапамицин. В некоторых вариантах осуществления эта композиция содержит более приблизительно 50% рапамицина или его производного в форме наночастиц. В некоторых вариантах осуществления этот белок-носитель является альбумином, например сывороточным альбумином человека. В некоторых вариантах осуществления средний диаметр наночастиц в этой композиции равен не более чем приблизительно 200 нм (например, не более чем приблизительно 100 нм). В некоторых вариантах осуществления композиции наночастиц являются стерильно фильтруемыми. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих наночастицах равно менее чем приблизительно 18:1. В некоторых вариантах осуществления отношение массы белка-носителя к массе рапамицина или его производного в этих композициях наночастиц является меньшим, чем приблизительно 18:1.
Это изобретение обеспечивает также любую из описанных композиций (например, композицию, содержащую наночастицы, которые содержат рапамицин или его производное и белок-носитель) для любого описанного здесь применения, независимо от того, описывается ли она в контексте применения в качестве лекарственного средства и/или в контексте применения для приготовления лекарственного средства. Обеспечены также единичные лекарственные формы описанных здесь композиций, изделия, содержащие композиции или единичные лекарственные формы в подходящей упаковке (например, флаконах или резервуарах, в том числе герметизированных флаконах или резервуарах и стерильных герметизированных флаконах или резервуарах), и наборы, содержащие эти единичные лекарственные формы. Это изобретение обеспечивает также способы приготовления и применения описанных здесь композиций.
Должно быть понятно, что одно, несколько свойств или все свойства