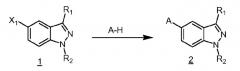
5-замещенные индазолы в качестве ингибиторов киназы
Иллюстрации
Показать всеИзобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям, где A, R1 R2, R3 и m определены в формуле изобретения. Изобретение также относится к ряду конкретных соединений и фармацевтической композиции, содержащей указанные соединения, которые являются полезными для ингибирования киназ, таких как гликогенсинтаза-киназа 3 (GSK-3), Rho киназа (ROCK), Janus Киназы (JAK), AKT, PAK4, PLK, CK2, KDR, MK2, JNK1, aurora, pim 1 и nek 2. 3 н. и 15 з.п. ф-лы, 393 пр.
Реферат
Область изобретения
Настоящее изобретение относится к 5-замещенным индазол- содержащим соединениям, способам получения таких соединений, композициям, содержащим такие соединения, которые являются полезными для ингибирования киназ, таких как гликогенсинтаза-киназа 3 (GSK-3), Rho киназа (ROCK), Janus киназы (JAK), AKT, PAK4, PLK, CK2, KDR, MK2, JNKl, aurora, pim 1 и nek 2.
Предпосылки изобретения
Протеинкиназы представляют собой класс ферментов, которые катализируют перенос фосфатной группы от АТФ к тирозиновому, сериновому, треониновому или гистидиновому остаткам, расположенным на белковом субстрате. Очевидно, что протеинкиназы играют определенную роль в нормальном клеточном росте. Многие белки рецепторов факторов роста содержат внутриклеточные домены, которые функционируют как протеинкиназы, и именно через эту функцию они осуществляют передачу сигнала. Взаимодействие факторов роста с их рецепторами является необходимым событием в нормальной регуляции клеточного роста, и состояние фосфорилирования белков субстрата часто связано с модуляцией клеточного роста.
Хорошо известно, что аномальное фосфорилирование белка может быть непосредственно связано с некоторыми болезненными состояниями или может быть фактором, способствующим началу развития таких заболеваний. Как результат, протеинкиназы являются целями, на которые направлены новые фармацевтические исследования (Cohen, P. Nature Reviews Drug Discovery, 1:309-315, 2002). Различные ингибиторы протеинкиназы имеют клиническое применение для лечения широкого ряда различных заболеваний, таких как рак, хронические воспалительные заболевания, диабет и удар.
Протеинкиназы представляют собой большое и разнообразное семейство ферментов, которые катализируют фосфорилирование белка и играют ключевую роль в клеточной передаче сигнала. Протеинкиназы могут проявлять положительное или отрицательное регуляторное действие, в зависимости от их белков-мишеней. Протеинкиназы участвуют в специфических сигнальных путях, которые регулируют клеточные функции, такие как, но не ограничиваясь этим, метаболизм, развитие клеточного цикла, клеточную адгезию, функцию сосудов, апоптоз и ангиогенез. Как результат, нарушение клеточной сигнальной активности связывают со многими заболеваниями, наиболее характерные из которых включают рак и диабет. Регуляция сигнальной трансдукции цитокинами и связь сигнальных молекул с прото-онкогенами и опухоль-супрессорными генами были в достаточной степени документально подтверждены. Подобным образом, связь между диабетом, вирусными инфекциями и связанными с этим состояниями также относят за счет регуляции протеинкиназ.
Поскольку протеинкиназы регулируют почти каждый клеточный процесс, включая метаболизм, клеточную пролиферацию, клеточную дифференциацию и клеточное выживание, они являются привлекательными мишенями для терапевтического вмешательства при различных болезненных состояниях. Например, контроль клеточного цикла и ангиогенез, где протеинкиназы играют важную роль, представляют собой клеточные процессы, связанные с различными болезненными состояниями, такими как, но не ограничиваясь этим, рак, воспалительные заболевания, аномальный ангиогенез и связанные с этим заболевания, атеросклероз, дегенерация желтого пятна, диабет, ожирение и боль.
Выяснение запутанных путей протеинкиназ и сложности взаимосвязей и взаимодействия между различными протеинкиназами и киназными путями подчеркивает важность разработки фармацевтических средств, способных действовать как модуляторы, регуляторы или ингибиторы протеинкиназ, обладающие благоприятной активностью на различные киназы или различные киназные пути.
Поэтому предполагается, что из-за сложности внутриклеточных сигнальных каскадов протеинкиназных путей, средства, которые влияют на различные пути одновременно, могут быть необходимыми для существенной клинической активности. Хотя считается, что отдельно взятое средство, которое обеспечивает комбинированные эффекты, является привлекательным, существует необходимость в идентификации и применении отдельных средств, которые прицельно действуют на нужные комбинации и различные пути, которые являются клинически эффективными в условиях конкретного заболевания.
Гликогенсинтаза-киназа-3 (GSK-3) представляет собой сериновую/треониновую киназу, кодируемую двумя изоформами, GSK-3α и GSK-3β, с молекулярной массой 51 и 47 кДа, соответственно. Они имеют 97% сходства последовательностей в их киназных каталитических доменах. GSK-3α изоформа имеет вытянутый глицин-обогащенный N-концевой хвост. Был идентифицирован минорный вариант сплайсинга GSK-3β (экспрессируемый на уровне ~15% от общего количества) с вставкой из 13 аминокислот в киназном домене. Этот вариант имел пониженную активность в отношении tau. GSK-3 сохранилась во многих видах в процессе эволюции, и до сих пор присутствует у всех млекопитающих с высокой гомологией в киназном домене. Обе изоформы экспрессируются во многих тканях млекопитающих, включая головной мозг. Фармакологические ингибиторы GSK-3 не могут селективно ингибировать одну из изоформ.
GSK-3β играет важную роль в контроле метаболизма, дифференциации и выживания. Первоначально она была идентифицирована как фермент, способный фосфорилировать и, следовательно, ингибировать гликогенсинтазу. В последствии, было установлено, что GSK-3β является идентичной tau протеинкиназе 1 (TPK1), ферменту, который фосфорилирует tau белок в эпитопах, которые, как было обнаружено, также гиперфосфорилируются при болезни Альцгеймера и некоторых таупатиях.
Интересно, что фосфорилирование GSK-3β протеинкиназой B (AKT) приводит к потере киназной активности, и было сделано предположение, что это ингибирование может опосредовать некоторые эффекты нейротрофических факторов. Более того, фосфорилирование β-катенина (белка, участвующего в клеточном выживании), осуществляемое GSK-3β, приводит к его разрушению зависимым от убихитинилирования протеасомальным путем.
Поэтому оказалось, что ингибирование GSK-3β активности может привести к нейротрофической активности. Существуют доказательства, что литий, неконкурентный ингибитор GSK-3β, усиливает нейритогенез в некоторых моделях и может также повышать выживание нервных клеток через индукцию факторов выживания, таких как Bcl-2, и ингибирование экспрессии проапоптических факторов, таких как P53 и Bax.
Дальнейшие исследования показали, что β-амилоид повышает активность GSK-3β и фосфорилирование белка tau. Более того, это гиперфосфорилирование, а также нейротоксические эффекты β-амилоида блокируются хлоридом лития и антисмысловой мРНК GSK-3β. Взятые вместе, эти наблюдения говорят о том, что GSK-3β может быть звеном между двумя основными патологическим процессами при болезни Альцгеймера: аномальный процессинг APP (амилоидный белок-предшественник) и гиперфосфорилирование белка tau.
Эти экспериментальные наблюдения показывают, что GSK-3β может найти применение в профилактике и лечении нейропатологических последствий и дефицита познавательной способности и внимания, связанных с болезнью Альцгеймера, а также других острых и хронических нейродегенеративных заболеваний. Они включают, но не ограничиваются этим: болезнь Паркинсона, таупатии (например, лобно-височно-теменная деменция, кортикобазальная дегенерация, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; острый удар и другие травматические поражения; цереброваскулярные расстройства (например, возрастная дегенерация желтого пятна); травму головного и спинного мозга; периферические невропатии; ретинопатии и глаукому.
GSK-3β также может найти применение для лечения других заболеваний, таких как: инсулин-независимый диабет и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; воспаления; раковые заболевания, такие как рак молочной железы, немелкоклеточная карцинома легкого, рак щитовидной железы, T или B-клеточный лейкоз и некоторые вирус-индуцированные опухоли.
Rho киназы (ROCK), первые Rho эффекторы, которые были описаны, представляют собой сериновые/треониновые киназы, которые играют важную роль в фундаментальных процессах клеточной миграции, клеточной пролиферации и клеточного выживания. Аномальную активацию Rho/ROCK пути наблюдали при различных расстройствах. Примеры болезненных состояний, где соединения по настоящему изобретению имеют потенциально полезные терапевтические эффекты, благодаря их анти-вазоспазматической активности, включают сердечно-сосудистые заболевания, такие как гипертензия, хроническая и застойная сердечная недостаточность, сердечная гипертрофия, рестеноз, хроническая почечная недостаточность, спазм сосудов головного мозга после субарахноидального кровоизлияния, легочная гипертензия и атеросклероз. Свойство мышечной релаксации также является полезным для лечения астмы, мужских эректильных дисфункций, женских сексуальных дисфункций и синдрома гиперреактивного мочевого пузыря. Повреждение головного и спинного мозга у взрослого позвоночного животного активирует ROCK, ингибируя посредством этого рост и распространение невритов. Ингибирование ROCK приводит к индукции роста новых аксонов, распространению аксонов через поражения в ЦНС, ускоренной регенерации и усиленному функциональному восстановлению после острого нейронного поражения у млекопитающих (повреждение спинного мозга, травматическое повреждение головного мозга). Также было подтверждено, что ингибирование Rho/ROCK пути является эффективным в других животных моделях нейродегенерации, например, удара, воспалительных и демиелинизирующих заболеваний, болезни Альцгеймера, а также для лечения боли. Ингибиторы Rho/ROCK пути поэтому обладают потенциалом для профилактики нейродегенерации и стимуляции нейрорегенерации при различных неврологических расстройствах, включая повреждение спинного мозга, болезнь Альцгеймера, удар, рассеянный склероз, амиотрофический боковой склероз, а также для лечения боли. Было показано, что ингибиторы ROCK обладают противовоспалительными свойствами. Таким образом, соединения по настоящему изобретению можно использовать для лечения нейровоспалительных заболеваний, таких как удар, рассеянный склероз, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона, амиотрофический боковой склероз и воспалительная боль, а также других воспалительных заболеваний, таких как ревматоидный артрит, остеоартрит, астма, синдром раздраженного кишечника, болезнь Крона, псориаз, язвенный колит, обыкновенная волчанка и воспалительное заболевание кишечника. Поскольку ингибиторы ROCK уменьшают клеточную пролиферацию и клеточную миграцию, они могли бы быть полезными для лечения рака и метастазов опухоли. Более того, если свидетельства, говорящие о том, что ингибиторы ROCK подавляют цитоскелетную реаранжировку при вирусной инвазии, таким образом, они также имеют потенциальную терапевтическую ценность для применения в качестве противовирусных и антибактериальных средств. Ингибиторы ROCK также являются полезными для лечения резистентности к инсулину и диабета. Кроме того, было показано, что ингибиторы ROCK уменьшают прогрессирование кистозного фиброза (Abstract S02.3, 8th World Congress on Inflammation, Copenhagen, Denmark, June 16-20, 2007).
Кроме того, было показано, что Rho-ассоциированные закрученные в спираль-образующие спираль протеинкиназы (ROCK)-1 и -2 усиливают фосфорилирование легкой цепи миозина (MLC) путем ингибирования MLC фосфатазы, а также фосфорилирования MLC. Это приводит к регулированию сокращения актина-миозина. Последние сообщения показали, что ингибирование ROCK приводит к прерыванию воспалительного клеточного хемотаксиса, а также ингибированию сокращения гладких мышц в моделях легочного воспаления, связанного с астмой. Поэтому ингибиторы Rho/ROCK пути должны быть полезными для лечения астмы.
Киназы Janus (JAK) представляют собой важное семейство внутриклеточных тирозиновых протеинкиназ (PTK) с 4 членами, присутствующими у млекопитающих, JAK1, JAK2, JAK3 и TYK2, также гомологами у цыпленка, рыб и Drosophila. JAK играют критическую роль в некоторых важных внутриклеточных сигнальных путях, включая основной путь JAK/STAT, центральный для опосредования передачи сигнала цитокинов. Именно эта центральная роль в передаче сигнала цитокинов подкрепляет мнение, что специфические ингибиторы JAK могут найти широкое терапевтическое применение в ситуациях, где активность цитокинов приводит к заболеванию. Важные примеры включают аутоиммунные заболевания, такие как ревматоидный артрит и псориаз, миелопролиферативные синдромы, такие как, лейкозы, лимфомы и сердечно-сосудистые заболевания.
JAK2, член семейства киназ Janus (JAK) тирозиновых протеикиназ (PTK), является важным внутриклеточным медиатором передачи сигнала цитокинов. Мутации JAK2 гена связаны с гематологическими раковыми заболеваниями, и аберрантная JAK активность также связана с различными иммунными заболеваниями, включая ревматоидный артрит.
Киназы Aurora представляют собой семейство мультигенных митотических сериновых-треониновых киназ, которые действуют как класс новых онкогенов. Эти киназы включают в качестве членов aurora-A, aurora-B и aurora-B. Они гиперактивируются и/или сверх-экспрессируются в некоторых солидных опухолях, включая, но, не ограничиваясь этим, рак молочной железы, яичников, предстательной железы, поджелудочной железы и колоректальный рак. В частности, aurora-A представляет собой центросомальную киназу, и ее локализация зависит от клеточного цикла и играет важную роль в развитии клеточного цикла и клеточной пролиферации. Aurora-A расположена в области 20ql3 хромосомы, которая часто амплифицируется в некоторых различных типах злокачественных опухолей, таких как колоректальный рак, рак молочной железы и мочевого пузыря. Ингибирование aurora киназной активности может помочь в уменьшении клеточной пролиферации, роста опухоли и потенциально онкогенеза.
Следовательно, остается потребность в разработке способов, включающих применение лекарственного средства на основе одного активного вещества, способного прицельно действовать на несколько специфических типов киназ или киназных путей. В частности, такие способы воздействуют на нужную комбинацию нескольких мишеней с достижением, таким образом, клинической эффективности.
Краткое описание изобретения
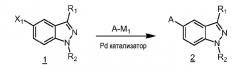
В основном варианте воплощения, настоящее изобретение обеспечивает соединения формулы (I)
или их фармацевтически приемлемые соли, где
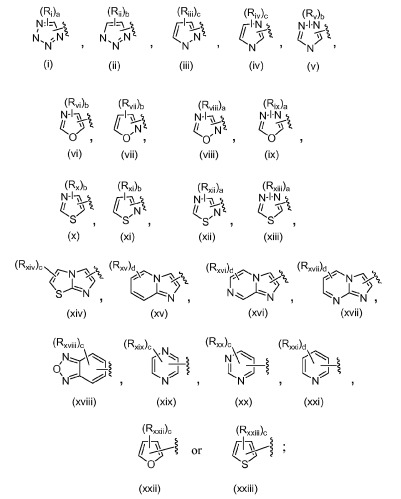
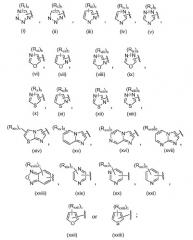
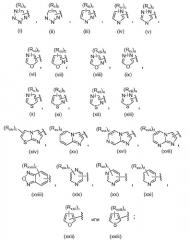
A представляет собой
R1 представляет собой водород, алкил, арил, гетероцикл, гетероарил, RaRbN-, RcRdN-C(O)- или RcRdN-S(O)2-;
R2 представляет собой водород, алкоксикарбонил, алкил, алкилкарбонил, арилкарбонил, гетероциклкарбонил или ReRfN-алкил-C(O)-;
R3 представляет собой алкил, алкокси, арил, циано, циклоалкил, галоген, галогеналкил, гетероарил, нитро или RgRhN-;
R4 представляет собой алкил, алкоксиалкил, арил, циклоалкил, гетероарил, гетероцикл, гетероциклалкил, RjRkN- или RjRkN-алкил-;
R5 представляет собой алкил, арил или гетероарил;
R6 представляет собой алкил, алкоксиалкил, RjRkN-алкил-, арил, циклоалкил или гетероарил;
R7 представляет собой алкил, арил или гетероарил;
Ra и Rb, каждый независимо, представляют собой водород, алкил, арилалкил, циклоалкил, циклоалкилалкил, гетероарилалкил, R4-C(O)- или R5-S(O)2-;
Rc и Rd, каждый независимо, представляют собой водород, алкил или гетероарил;
Re и Rf, каждый независимо, представляют собой водород, алкил, арилалкил, гетероарилалкил, R6-C(O)- или R7-S(O)2-;
Rg и Rh, каждый независимо, представляют собой водород, алкил или алкилкарбонил;
Rj и Rk, каждый независимо, представляют собой водород, алкил, арил, арилалкил, циклоалкил, гетероарил или гетероцикл;
Ri, Rii, Riii, Riv, Rv, Rvi, Rvii, Rviii, Rix, Rx, Rxi, Rxii, Rxiii, Rxiv, Rxv, Rxvi, Rxvii, Rxviii, Rxix, Rxx, Rxxi, Rxxii и Rxxiii, каждый независимо, представляют собой алкил, алкокси, алкоксиалкил, алкоксикарбонил, алкоксикарбонилалкил, арил, арилалкил, арил(гидрокси)алкил, арилоксиалкил, арилкарбонил, арилтиоалкил, карбокси, карбоксиалкил, цианоалкил, циклоалкил, циклоалкилалкил, циклоалкилкарбонил, галоген, гетероарил, гетероарилалкил, гетероцикл, гетероциклалкил, гетероциклкарбонил, гидроксиалкил, триалкилсилилалкил, H2NC(O)-алкил, ZaZbN-, ZaZbNалкил, ZcZdNC(O)- или ZcZdNS(O)2-, где RXiV, Rxv, RXVi и RXVii могут присутствовать по любой открытой валентности в соединениях (xiv), (xv), (xvi) или (xvii);
Za и Zb, каждый независимо, представляют собой водород, алкил, алкоксикарбонилалкил, арил, арилалкил, циклоалкил, H2NC(O)-, H2NалкилC(O)-, H2NC(O)-алкил, диалкилNC(O)- или диалкилNC(O)-алкил-;
Zc и Zd, каждый независимо, представляют собой водород, алкил, алкоксиалкил, арил, арилалкил, арил(гидрокси)алкил, циклоалкил, циклоалкилалкил, гетероарилалкил, гетероцикл, гетероциклалкил, гидроксиалкил, H2NC(O)-алкил-, диалкилNC(O)-алкил-, диалкилN-алкил- или CHZeZf;
Ze представляет собой арил или гетероарил;
Zf представляет собой гетероарилалкил, гетероциклалкил или Z1Z2N-алкил-;
m имеет значение 0, 1 или 2;
a имеет значение 0 или 1;
b имеет значение 0, 1 или 2;
c имеет значение 0, 1, 2 или 3; и
d имеет значение 0, 1, 2, 3 или 4.
Также обеспечиваются фармацевтически приемлемые композиции, включающие терапевтически эффективное количество соединения формулы (I) в сочетании с фармацевтически приемлемым носителем.
Целью настоящего изобретения является обеспечение соединений, которые являются полезными для профилактики или лечения заболеваний, вызванных аномальной активностью протеинкиназы. Кроме того, изобретение также обеспечивает фармацевтически эффективные композиции соединений по настоящему изобретению, которые являются полезными для профилактики или лечения указанных заболеваний.
Настоящее изобретение также относится к фармацевтической композиции, которая включает, по меньшей мере, одно 5-замещенное индазольное соединение формулы (I), которое может существовать в виде его фармацевтически приемлемой соли или пролекарства, в присутствии или в отсутствие фармацевтически приемлемых носителей, драже, адъювантов или других вспомогательных веществ.
Соединения по настоящему изобретению обладают ингибируещей активностью в отношении GSK-3, ROCK-1, ROCK-2, JAK2, а также других киназ и являются полезными для ингибирования таких киназ. Некоторые соединения по настоящему изобретению являются селективными в отношении одной или нескольких киназ и могут быть полезными для селективного ингибирования таких киназ. Следовательно, соединения по настоящему изобретению являются полезными в качестве активного ингредиента для получения композиции, которая обеспечивает возможность профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK-3, и, более конкретно, нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Кроме того, соединения по настоящему изобретению также являются полезными в качестве активного ингредиента для получения композиции для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, таупатии (например, лобно-височно-теменная деменция, кортикобазальная дегенерация, болезнь Пика, прогрессирующей супрануклеарный паралич) и других деменций, включая сосудистую деменцию; острый удар и другие травматические поражения; цереброваскулярные расстройства (например, возрастная дегенерация желтого пятна); травма головного и спинного мозга; периферические невропатии; ретинопатия и глаукома; и других заболеваний, таких как инсулин-независимый диабет (такой как диабет типа II) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; раковые заболевания, такие как рак молочной железы, немелкоклеточная карцинома легкого, рак щитовидной железы, T или B-клеточный лейкоз и некоторые вирус-индуцированные опухоли.
Подробное описание изобретения
Соединения по настоящему изобретению имеют формулу (I), описанную выше. Более конкретно, соединения формулы (I) могут включать, но не ограничиваются этим, соединения, где A представляет собой (ii), (iii), (iv), (vii), (x), (xiv), (xv), (xvi), (xvii), (xviii), (xix), (xx), (xxi), (xxii) или (xxiii).
В другом варианте воплощения настоящего изобретения раскрывается соединение формулы (I), где A представляет собой (ii),
R1 представляет собой водород, арил, гетероарил, гетероцикл, RaRbN- или RcRdN-C(O)-; R2 представляет собой водород, алкоксикарбонил, гетероциклкарбонил, алкилкарбонил или ReRfN-алкил-C(O)-; R4 представляет собой алкил, алкоксиалкил, арил, циклоалкил, гетероцикл, гетероциклалкил, RjRkN- или RjRkN-алкил-; R5 представляет собой алкил, арил или гетероарил; Ra и Rb, каждый независимо, представляют собой водород, арилалкил, циклоалкилалкил, R4-C(О)- или R5-S(O)2-; Rc и Rd, каждый независимо, представляют собой водород или гетероарил, Re и Rf, каждый независимо, представляют собой водород или алкил, Rj и Rk, каждый независимо, представляют собой водород, алкил, арил, циклоалкил или гетероцикл; Rii представляет собой алкил, алкоксиалкил, алкоксикарбонил, арил, арилалкил, арил(гидрокси)алкил, арилоксиалкил, арилкарбонил, алкоксикарбонилалкил, арилтиоалкил, карбокси, карбоксиалкил, циклоалкил, циклоалкилалкил, циклоалкилкарбонил, галоген, гетероарил, гетероарилалкил, гетероцикл, гетероциклалкил, гетероциклкарбонил, гидроксиалкил, триалкилсилилалкил, ZaZbN-, ZaZbNалкил- или ZcZdNC(О)-; Za и Zb, каждый независимо, представляют собой водород, алкил или H2NалкилC(O)-; Zc и Zd, каждый независимо, представляют собой водород, алкил, алкоксиалкил, арил, арилалкил, циклоалкил, циклоалкилалкил, гетероарилалкил, гетероциклалкил, гидроксиалкил или диалкилN-алкил-; m имеет значение 0; и b имеет значение 0, 1 или 2.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (iii),
R1 представляет собой водород или RaRbN-; R2 представляет собой водород; R4 представляет собой RjRkN-алкил-; Ra и Rb, каждый независимо, представляют собой водород или R4-C(O)-; Rj и Rk, каждый, представляют собой алкил; Riii представляет собой алкоксикарбонилалкил, алкил, арилалкил, цианоалкил, гетероциклалкил или H2NC(O)-алкил-; c имеет значение 0, 1 или 2; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (iv),
R1 представляет собой водород или R3RbN-; R2 представляет собой водород; R3 и Rb, каждый, представляют собой водород; RiV представляет собой арил, арилалкил, гетероцикл, гетероциклалкил, ZaZbNалкил или ZcZdNS(O)2-; Za и Zb, каждый независимо, представляют собой водород или алкил; Zc и Zd, каждый, представляют собой алкил; c имеет значение 0, 1 или 2; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (vii),
R1 представляет собой водород, алкил или RaRbN; R2 представляет собой водород; Ra и Rb, каждый, представляют собой водород; RVii представляет собой алкил, алкоксикарбонил, арил, арилалкил, циклоалкил, гетероциклалкил, гетероциклкарбонил, гидроксиалкил или ZcZdNC(O)-; Zc и Zd, каждый независимо, представляют собой водород, алкил, алкоксиалкил, арил, арилалкил, арил(гидрокси)алкил, циклоалкил, циклоалкилалкил, гетероарилалкил, гетероцикл, гетероциклалкил, гидроксиалкил или CHZeZf, Ze представляет собой арил или гетероарил, Zf представляет собой гетероарилалкил, гетероциклалкил или Z1Z2N-алкил-; b имеет значение 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (x),
R1 представляет собой водород; R2 представляет собой водород; Rx представляет собой алкил, арил или ZaZbN-; Za и Zb, каждый независимо, представляют собой водород, алкил, арил или арилалкил; b имеет значение 1 или 2; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xiv),
R1 представляет собой водород; R2 представляет собой водород; RXiV представляет собой ZaZbN-; Za и Zb, каждый независимо, представляют собой водород или циклоалкил; c имеет значение 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xv),
(xv)
R1 представляет собой водород или R3RbN-; R2 представляет собой водород; R3 и Rb, каждый, представляют собой водород; Rxv представляет собой ZaZbN-; Za и Zb, каждый независимо, представляют собой водород, алкоксикарбонилалкил, арил, арилалкил или циклоалкил; d имеет значение 0 или 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xvi)
R1 представляет собой водород; R2 представляет собой водород; RXVi представляет собой ZaZbN-; Za и Zb, каждый независимо, представляют собой водород или циклоалкил; d имеет значение 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xvii)
R1 представляет собой водород; R2 представляет собой водород; RXVii представляет собой арил или ZaZbN-; Za и Zb, каждый независимо, представляют собой водород, алкил, алкоксикарбонилалкил, арил, арилалкил, циклоалкил или H2NC(O)-алкил-; d имеет значение 0 или 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xviii)
R1 представляет собой RaRbN-; R2 представляет собой водород; Ra и Rb, каждый, представляют собой водород; c имеет значение 0; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xix)
R1 представляет собой RaRbN-; R2 представляет собой водород; Ra и Rb, каждый независимо, представляют собой водород; c имеет значение 0; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xx)
R1 представляет собой RaRbN-; R2 представляет собой водород; R4 представляет собой RjRkN-алкил-; Ra и Rb, каждый, представляют собой водород или R4-C(O)-; Rj и Rk независимо представляют собой алкил; Rxx представляет собой ZaZbN- или гетероцикл; Za и Zb независимо представляют собой водород или алкил; c имеет значение 0 или 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xxi)
R1 представляет собой RaRbN-; R2 представляет собой водород; Ra и Rb, каждый, представляют собой водород; RXXi представляет собой алкокси; d имеет значение 1; и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xxii)
R1 представляет собой RaRbN-; R2 представляет собой водород; R4 представляет собой RjRkN-алкил-; Ra и Rb, каждый независимо, представляют собой водород или R4-C(O)-; Rj и Rk, каждый, представляют собой алкил; c имеет значение 0 и m имеет значение 0.
В другом варианте воплощения настоящего изобретения, раскрывается соединение формулы (I), где A представляет собой (xxiii)
R1 представляет собой RaRbN-; R2 представляет собой водород; Ra и Rb, каждый, представляют собой водород; c имеет значение 0; и m имеет значение 0.
Конкретные варианты воплощения, рассматриваемые как часть настоящего изобретения, включают, но не ограничиваются этим, соединения формулы (I), например:
5-(1-бензил-1H-1,2,3-триазол-5-ил)-1H-индазольное соединение с 5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазолом;
5-(1H-1,2,3-триазол-5-ил)-1H-индазол;
5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол;
5-[1-(2-метилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3-метилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(4-метилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3-метоксибензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2-фторбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3-фторбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(4-фторбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2-хлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3-хлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(4-хлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2-бромбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2-нитробензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3-нитробензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(4-нитробензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
2-{[4-(1H-индазол-5-ил)-1H-1,2,3-триазол-1-ил]метил}бензонитрил;
3-{[4-(1H-индазол-5-ил)-1H-1,2,3-триазол-1-ил]метил}бензонитрил;
4-{[4-(1H-индазол-5-ил)-1H-1,2,3-триазол-1-ил]метил}бензонитрил;
5-{1-[2-(трифторметил)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
5-{1-[3-(трифторметил)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
5-{1-[4-(трифторметил)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
5-{1-[3-(трифторметокси)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
5-{1-[4-(трифторметокси)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
5-[1-(4-трет-бутилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
метил 3-{[4-(1H-индазол-5-ил)-1H-1,2,3-триазол-1-ил]метил} бензоат;
метил 4-{[4-(1H-индазол-5-ил)-1H-1,2,3-триазол-1-ил]метил}бензоат;
5-[1-(2,4-диметилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3,5-диметилбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2,3-дихлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2,4-дихлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(2,5-дихлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[1-(3,5-дихлорбензил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-{1-[2,4-бис(трифторметил)бензил]-1H-1,2,3-триазол-4-ил}-1H-индазол;
N-циклогексил-6-(1H-индазол-5-ил)имидазо[2,1-b][1,3]тиазол-5-амин;
N-циклогексил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиридин-3-амин;
N-циклогексил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиразин-3-амин;
5-[1-бензил-4-(4-фторфенил)-1H-индазол-5-ил]-1H-индазол;
N-{3-[4-(4-фторфенил)-5-(1H-индазол-5-ил)-1H-индазол-1-ил]пропил}-N,N-диметиламин;
N-циклогексил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиримидин-3-амин;
5-[4-(4-фторфенил)-1-(1-фенилэтил)-1H-индазол-5-ил]-1H-индазол;
2-(1H-индазол-5-ил)-N-изопропилимидазо[1,2-a]пиримидин-3-амин;
4-(1H-индазол-5-ил)-N-фенил-1,3-тиазол-2-амин;
5-(2-метил-1,3-тиазол-4-ил)-1H-индазол;
N-этил-4-(1H-индазол-5-ил)-1,3-тиазол-2-амин;
N-бензил-4-(1H-индазол-5-ил)-1,3-тиазол-2-амин;
4-(1H-индазол-5-ил)-1,3-тиазол-2-амин;
4-(1H-индазол-5-ил)-N-(2-фенилэтил)-1,3-тиазол-2-амин;
N-бензил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиримидин-3-амин;
N-бутил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиримидин-3-амин;
N-(4-хлорфенил)-2-(1H-индазол-5-ил)имидазо[1,2-a]пиримидин-3-амин;
2-(1H-индазол-5-ил)-N-(4-метоксифенил)имидазо[1,2-a]пиримидин-3-амин;
2-(1H-индазол-5-ил)имидазо[1,2-a]пиримидин;
метил N-[2-(1H-индазол-5-ил)имидазо[1,2-a]пиридин-3-ил]глицинат;
N-бензил-2-(1H-индазол-5-ил)имидазо[1,2-a]пиридин-3-амин;
N-(4-хлорфенил)-2-(1H-индазол-5-ил)имидазо[1,2-a]пиридин-3-амин;
2-(1H-индазол-5-ил)-N-(4-метоксифенил)имидазо[1,2-a]пиридин-3-амин;
трет-бутил 4-[4-(4-фторфенил)-5-(1H-индазол-5-ил)-1H-индазол-1-ил}пиперидин-1-карбоксилат;
3,5-бис(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол;
5-(1-бензил-1H-1,2,3-триазол-4-ил)-3-фенил-1H-индазол;
5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-амин;
5-(1-бензил-1H-1,2,3-триазол-4-ил)-1-[(1-метилпиперидин-4-ил)карбонил]-1H-индазол-3-амин;
N-[5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-ил]-2-метоксиацетамид;
N1-[5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-ил]-N2,N2-диметилглицинамид;
Ν-[5-(1-бензил-lΗ-1,2,3-триазол-4-ил)-lΗ-индазол-3-ил]бутанамид;
5-[4-(4-фторфенил)-1-пиперидин-4-ил-1H-индазол-5-ил]-1H-индазол;
5-{4-(4-фторфенил)-1-[2-(1-метилпирролидин-2-ил)этил]-1H-индазол-5-ил}-1H-индазол;
5-{4-(4-фторфенил)-1-[3-(4-метилпиперазин-1-ил)пропил]-1H-индазол-5-ил}-1H-индазол;
этил 5-(1H-индазол-5-ил)изоксазол-3-карбоксилат;
5-(1H-индазол-5-ил)-N-метилизоксазол-3-карбоксамид;
5-(3-бензилизоксазол-5-ил)-1H-индазол;
N-[5-(1-бензил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-ил]бензамид;
5-(3-пропилизоксазол-5-ил)-1H-индазол;
N-бензил-4-(1H-индазол-5-ил)-5-фенил-1,3-тиазол-2-амин;
4-(1H-индазол-5-ил)-N,5-дифенил-1,3-тиазол-2-амин;
5-(1-бензил-5-циклопропил-1H-1,2,3-триазол-4-ил)-1H-индазол;
5-(1-бензил-4-циклопропил-1H-1,2,3-триазол-5-ил)-1H-индазол;
2-(1H-индазол-5-ил)-3-фенилимидазо[1,2-a]пиримидин;
5-[1-(тетрагидро-2H-пиран-4-илметил)-1H-1,2,3-триазол-4-ил]-1H-индазол;
5-[3-(пиперидин-1-илкарбонил)изоксазол-5-ил]-1H-индазол;
5-(1H-индазол-5-ил)-N-фенилизоксазол-3-карбоксамид;
N-циклогексил-5-(1H-индазол-5-ил)изоксазол-3-карбоксамид;
5-[3-(пиперидин-1-илметил)изоксазол-5-ил]-1H-индазол;
[5-(1H-индазол-5-ил)изоксазол-3-ил]метанол;
5-(1H-индазол-5-ил)-N-(2-метоксиэтил)изоксазол-3-карбоксамид;
5-(1-бензил-5-фенил-1H-1,2,3-триазол-4-ил)-1H-индазол;
5-(4-бензил-1H-1,2,3-триазол-1-ил)-1H-индазол;
5-(1-бензил-5-циклопропил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-амин;
5-(1-бензил-4-циклопропил-1H-1,2,3-триазол-5-ил)-1H-индазол-3-амин;
5-(3-изобутилизоксазол-5-ил)-1H-индазол-3-амин;
5-(3-бензилизоксазол-5-ил)-1H-индазол-3-амин;
N-{2-[4-(4-фторфенил)-5-(1H-индазол-5-ил)-1H-имидазол-1-ил]этил}-N,N-диметиламин;
5-[4-(4-фторфенил)-1-(3-морфолин-4-илпропил)-1H-индазол-5-ил]-1H-индазол;
5-[4-(4-фторфенил)-1-(3-пирролидин-1-илпропил)-1H-индазол-5-ил]-1H-индазол;
5-{4-(4-фторфенил)-1-[2-(4-метилпиперидин-1-ил)этил]-1H-имидазол-5-ил}-1H-индазол;
5-[1-(1-бензилпиперидин-4-ил)-4-(4-фторфенил)-1H-имидазол-5-ил]-1H-индазол;
5-[4-(4-фторфенил)-1-(2-морфолин-4-илэтил)-1H-имидазол-5-ил]-1H-индазол;
5-[1-(1-бензилпирролидин-3-ил)-4-(4-фторфенил)-1H-имидазол-5-ил]-1H-индазол;
2-{4-[4-(4-фторфенил)-5-(1H-индазол-5-ил)-1H-имидазол-1-ил]пиперидин-1-ил}-2-оксоэтанол;
5-(1-бензил-5-фенил-1H-1,2,3-триазол-4-ил)-1H-индазол-3-амин;
2-[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]пропан-2-ол;
5-[4-(метоксиметил)-1H-1,2,3-триазол-1-ил]-1H-индазол;
1-[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]-1-фенилэтанол;
5-(4-пропил-1H-1,2,3-триазол-1-ил)-1H-индазол;
1-[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]пропан-2-ол;
3-[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]пропан-1-ол;
1-{[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]метил}-1H-1,2,3-бензотриазол;
5-{4-[(фенилтио)метил]-1H-1,2,3-триазол-1-ил}-1H-индазол;
5-(4-циклопропил-1H-1,2,3-триазол-1-ил)-1H-индазол;
5-[4-(2-фенилэтил)-1H-1,2,3-триазол-1-ил]-1H-индазол;
5-[4-(циклогексилметил)-1H-1,2,3-триазол-1-ил]-1H-индазол;
5-(4-циклопентил-1H-1,2,3-триазол-1-ил)-1H-индазол;
1-[1-(1H-индазол-5-ил)-1H-1,2,3-триазол-4-ил]циклогексанол;
5-[4-(феноксиметил)-1H-1,2,3-триазол-1-ил]-1H-индазол;
5-{4-[(1,1-диоксидотиоморфолин-4-ил)метил]-1H-1,2,3-триазол-1-ил}-1H-индаз