Одноцепочечные мультивалентные связывающие белки с эффекторной функцией
Иллюстрации
Показать всеИзобретение относится к иммунологии. Предложен одноцепочечный мультиспецифический связывающий белок для связывания или модулирования активности одной или нескольких молекул-партнеров связывания. Он содержит от N-конца к С-концу: первый связывающий домен, полученный из вариабельных областей легкой и тяжелой цепей иммуноглобулина; константную субобласть, полученную из иммуноглобулина, содержащую шарнирный или шарнир-подобный домен, CH2-домен и CH3-домен; пептид линкера-скорпиона, где указанный пептид содержит аминокислотную последовательность из шарнира иммуноглобулина или области «стебля» («stalk») белка лектина С типа II; и второй связывающий домен, полученный из вариабельных областей легкой и тяжелой цепей иммуноглобулина. Описаны: кодирующая нуклеиновая кислота, а также экспрессирующий вектор на ее основе и клетка-хозяин для экспрессии белка на основе вектора. Предложены: фармацевтическая композиция для лечения нарушения пролиферации клеток на основе одноцепочечного белка и белковый димер для связывания или модулирования активности одной или нескольких молекул-партнеров связывания - на основе двух одноцепочечных связывающих белков. Изобретение обеспечивает мультиспецифические молекулы, сохраняющие эффекторные функции, нечувствительные к протеолитическому расщеплению, и может найти применение в терапии различных заболеваний. 7 н. и 24 з.п. ф-лы, 61 ил., 16 табл., 19 пр.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится главным образом к области мультивалентных связывающих молекул и их терапевтическим применениям.
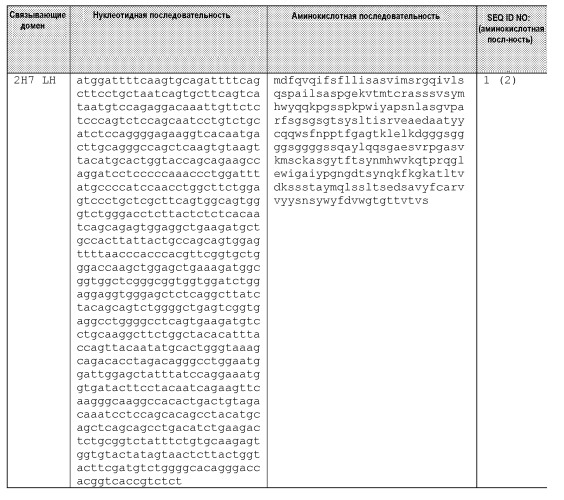
Список последовательностей представлен в виде текстового файла и в виде PDF-файла в соответствии с предъявляемыми требованиями для электронной подачи. Список последовательностей создан 12 июня 2007 года. Список последовательностей включен здесь в качестве ссылки в его полном виде.
Уровень техники
У здорового млекопитающего иммунная система защищает организм от повреждения чужеродными веществами и патогенами. Однако, в некоторых случаях иммунная система дает сбой, продуцируя травматический инсульт и/или заболевание. Например, В-клетки могут продуцировать антитела, которые узнают собственные белки, а не чужеродные белки, приводя к продуцированию аутоантител, характерных для аутоиммунных заболеваний, таких как системная красная волчанка, ревматоидный артрит и т.п. В других случаях, обычно благоприятное действие иммунной системы в борьбе с чужеродными веществами приводит к обратным результатам, например, после трансплантации органов. Эта способность иммунной системы млекопитающих и, в частности, иммунной системы человека, была обнаружена, и были предприняты попытки регуляции этой системы во избежание или для облегчения пагубных последствий для здоровья, которые происходят либо в результате нормального функционирования иммунной системы в аномальных обстоятельствах (например, при трансплантации органов), либо в результате функционирования иммунной системы в явно нормальных в остальном обстоятельствах (например, при прогрессировании аутоиммунного заболевания). Кроме того, были предприняты попытки использования иммунной системы для обеспечения ряда мишень-специфических диагностических и терапевтических методологий, основывающихся на способности антител специфически узнавать и специфически связывать антигенные мишени.
Одним путем, в котором иммунная система защищает организм, является продуцирование специализированных клеток, называемых В-лимфоцитами или В-клетками. В-клетки продуцируют антитела, которые связываются с чужеродным веществом или патогеном и в некоторых случаях опосредуют их деструкцию. Однако, в некоторых случаях иммунная система человека и, в частности, В-лимфоциты иммунной системы человека дают сбой, и возникает заболевание. Существуют многочисленные типы раков, которые вызывают неконтролируемую пролиферацию В-клеток. Существуют также многочисленные аутоиммунные заболевания, которые вызывают продуцирование В-клетками антител, которые, вместо связывания с чужеродными веществами и патогенами, связываются с частями организма. Кроме того, существуют многочисленные аутоиммунные и воспалительные заболевания, которые вызывают В-клетки в их патологии, например, через некорректную презентацию антигенов В-клеток Т-клеткам или через другие пути, в которых участвуют В-клетки. Например, мыши, предрасположенные к аутоиммунным нарушениям, дефицитные по В-клеткам, не развивают аутоиммунное заболевание почек, васкулит или аутоантитела (Shlomchik et al., J Exp. Med. 1994, 180:1295-306). Интересно, что те же самые предрасположенные к аутоиммунному заболеванию мыши, у которых имеются В-клетки, но которые являются недостаточными в отношении продуцирования иммуноглобулина, действительно развивают аутоиммунные заболевания при экспериментальной индукции (Chan et al., J Exp. Med. 1999, 189:1639-48), что указывает на то, что В-клетки играют существенную роль в развитии аутоиммунного заболевания.
В-клетки могут быть идентифицированы по молекулам на их клеточной поверхности. CD20 был первой поверхностной молекулой, специфической для В-клеточного направления дифференцировки клеток человека, идентифицированной моноклональным антителом. Он является негликозилированным, гидрофобным В-клеточным трансмембранным фосфопротеином 35 кДа, которые имеет как амино-, так и карбокси-концы, расположенные внутри клетки (Einfeld et al., EMBO J. 1988, 7:711-17). CD20 экспрессируется всеми нормальными зрелыми В-клетками, но не экспрессируется предшественниками В-клеток или плазматическими клетками. Природные лиганды для CD20 не были идентифицированы, и функция CD20 в биологии В-клеток все еще не выяснена полностью.
Другой поверхностной молекулой, специфической для В-клеточного направления дифференцировки, является CD37. CD37 является сильно гликозилированным белком 40-52 кДа, который принадлежит к трансмембранному семейству тетраспанинов антигенов поверхности клеток. Он пронизывает клеточную мембрану четыре раза, образуя две внеклеточные петли и обращая его амино- и карбокси-концы в цитоплазму. CD37 экспрессируется в высокой степени на нормальных продуцирующих антитела (sIg+)В-клетках, но не экспрессируется на пре-В-клетках или плазматических клетках. Экспрессия CD37 на покоящихся и активированных Т-клетках, моноцитах и гранулоцитах является низкой, и детектируемая экспрессия CD37 отсутствует на NK-клетках, тромбоцитах или эритроцитах. См., Belov et al., Cancer Res., 61(11):4483-4480 (2001); Schwartz-Albiez et al., J. Immunol., 140(3): 905-914 (1988) и Link et al., J. Immunol., 137(9): 3013-3018 (1988). Наряду с нормальными В-клетками, почти все злокачественные опухоли В-клеточного происхождения являются положительными по экспрессии CD37, в том числе CLL, NHL и злокачественный (гистиоцитарный) лейкоз (гистиолимфоцитоз Бернарда) (Moore et al., 1987; Merson and Brochier 1988; Faure, et al., 1900). CD37 участвует в регуляции В-клеточной функции, так как было обнаружено, что мыши, лишенные CD37, имеют низкие уровни сывороточного IgG1 и являются неполноценными в их гуморальной реакции на вирусные антигены и модельные антигены. Он действует, по-видимому, как неклассическая костимулирующая молекула или посредством прямого влияния на презентацию антигена через образование комплекса с молекулами МНС класса II. См. Knobeloch et al., Mol. Cell. Biol., 20(15):5363-5369 (2000).
Развитие исследований и лекарственных средств происходило на основе концепции, что молекулы клеточной поверхности, специфические для В-клеточного направления дифференцировки, такие как CD37 и CD20, могут сами быть мишенями для антител, которые могли бы связываться с раковыми и вызывающими аутоиммунное заболевание В-клетками, которые имеют CD37 и CD20 на их поверхностях, и опосредовать их разрушение. Названные «иммунотерапией», антитела, образованные у животного, не являющегося человеком, которые связываются с CD37 или CD20 (или полученные на основе образованных антителах), назначают пациенту для истощения раковых или вызывающих аутоиммунное заболевание В-клеток.
Технология моноклональных антител и способы генной инженерии способствовали развитию молекул иммуноглобулинов для диагностики и лечения заболеваний человека. Доменная структура иммуноглобулинов поддается конструированию, в том смысле, что антигенсвязывающие домены и домены, придающие эффекторные функции, могут быть обменены между классами и подклассами иммуноглобулинов. Структура и функция иммуноглобулинов обсуждается, например, в Harlow et al, Eds., Antibodies: A Laboratory Manual, Chapter 14, Cold Spring Harbor Laboratory, Cold Sprig Harbor (1988). Обширное введение, а также подробная информация относительно всех аспектов технологии рекомбинантных антител может быть найдена в справочнике “Recombinant Antibodies” (John Wiley & Sons, NY, 1999). Исчерпывающая коллекция подробных лабораторных протоколов конструирования антител может быть найдена в R. Kontermann and S. Dubel (eds.), “The Antibody Engineering Lab Manual” (Springer Verlag, Heidelberg/New York, 2000).
Молекула иммуноглобулина (обозначаемая как Ig) является мультимерным белком, обычно состоящим из двух идентичных полипептидов легкой цепи и двух идентичных полипептидов тяжелой цепи (Н2L2), которые соединены в макромолекулярный комплекс межцепочечными дисульфидными связями, т.е. ковалентными связями между сульфгидрильными группами соседних остатков цистеина. Пять классов иммуноглобулинов человека определены на основе состава их тяжелой цепи и названы IgG, IgМ, IgА, IgЕ и IgD. Антитела IgG-класса и IgA-класса дополнительно подразделены на подклассы, а именно, IgG1, IgG2, IgG3 и IgG4 и IgA1 и IgA2, соответственно. Внутрицепочечные дисульфидные связи соединяют разные участки одной и той же полипептидной цепи, что приводит к образованию петель, которые, вместе со смежными аминокислотами, составляют домены иммуноглобулина. В аминоконцевой части каждая легкая цепь и каждая тяжелая цепь имеет единственную вариабельную область, которая обнаруживает значительную вариацию в аминокислотном составе от одного антитела к другому. Вариабельная область легкой цепи, VL, имеет единственный антигенсвязывающий домен и связывается с вариабельной областью тяжелой цепи, VH (также содержащей единственный антигенсвязывающий домен), с образованием антигенсвязывающего сайта иммуноглобулина, Fv.
Кроме вариабельных областей, каждая из цепей полноразмерного антитела имеет константную область, содержащую один или несколько доменов. Легкие цепи имеют константную область, содержащую единственный домен. Таким образом, легкие цепи имеют один вариабельный домен и один константный домен. Тяжелые цепи имеют константную область, содержащую несколько доменов. Тяжелые цепи в антителах IgG, IgА и IgD, имеют три домена, которые названы CH1, CH2 и CH3; тяжелые цепи в антителах IgM и IgE имеют четыре домена, CН1, CH2, CН3 и CН4. Таким образом, тяжелые цепи имеют один вариабельный домен и три или четыре константных домена. Примечательной является инвариантная организация этих доменов во всех известных видах, причем константные области, содержащие один или несколько доменов, расположены при С-конце или вблизи С-конца как легкой, так и тяжелой цепей молекул иммуноглобулина, а вариабельные домены расположены в направлении N-концов легкой и тяжелой цепей. Структура и функция иммуноглобулинов рассматривается, например, в Harlow et al., Eds., Antibodies: A Laboratory Manual, Chapter 14, Cold Spring Harbor Laboratory, Cold Spring Harbor (1988).
Тяжелые цепи иммуноглобулинов могут быть также подразделены на три функциональных области: Fd-область (фрагмент, содержащий VH и CH1, т.е. два N-концевых домена тяжелой цепи), шарнирную область и Fc-область (область «кристаллизуемого фрагмента»). Fc-область содержит домены, которые взаимодействуют с рецепторами иммуноглобулинов на клетках и с начальными элементами каскада комплемента. Таким образом, Fc-область или фрагмент обычно считается ответственным за эффекторные функции иммуноглобулина, такие как ADCC (антителозависимая клеточно-опосредованная цитотоксичность), CDC (комплементзависимая цитотоксичность) и связывание (фиксация) комплемента, связывание с Fc-рецепторами, больший период полужизни in vivo относительно полипептида, лишенного Fc-области, связывание белка А и, возможно, даже переход (лекарственного средства) через плаценту (Capon et al, Nature, 337: 525-531, (1989)). Далее, полипептид, содержащий Fc-область, делает возможной димеризацию/мультимеризацию полипептида. Эти термины используются также для аналогичных областей других иммуноглобулинов.
Хотя все изотипы иммуноглобулинов человека содержат узнаваемую общую структуру, каждый изотип проявляет отличающуюся картину эффекторной функции. IgG, в качестве неисчерпывающего примера, нейтрализует токсины и вирусы, опсонизирует, фиксирует комплемент (CDC) и участвует в ADCC. IgM, в противоположность этому, нейтрализует переносимые кровью патогены и участвует в опсонизации. IgA, при ассоциации с его секреторным участком, секретируется и обеспечивает первичную защиту от микробной инфекции через слизистую оболочку; он также нейтрализует токсины и поддерживает опсонизацию. IgE опосредует воспалительные реакции, участвуя централизованно в рекрутинге других клеток, необходимых для установления полной реакции. Известно, что IgD обеспечивает иммунорегуляторную функцию, контролирующую активацию В-клеток. Эти характеристики эффекторных функций изотипов обеспечивают неисчерпывающую иллюстрацию различий, которые могут быть обнаружены среди изотипов человека.
Шарнирная область, обнаруживаемая в классах IgG, IgA, IgD, и IgE антител, действует как гибкий спейсер, позволяя Fab-части свободно перемещаться в пространстве. В противоположность константным областям, шарнирные домены являются структурно разнообразными, варьирующими как по последовательности, так и по длине, среди классов и подклассов иммуноглобулинов. Например, длина и гибкость шарнирной области варьирует среди подклассов IgG. Шарнирная область IgG1 включает аминокислоты 216-231 и, поскольку она является свободно гибкой, Fab-фрагменты могут вращаться вокруг их осей симметрии и перемещаться в сфере с центром при первом из двух дисульфидных мостиков между тяжелыми цепями. IgG2 имеет более короткий шарнир, чем IgG1, с 12 аминокислотными остатками и четырьмя дисульфидными мостиками. Шарнирная область IgG2 лишена остатка глицина, является относительно короткой и содержит негибкую полипролиновую двойную спираль, стабилизированную дополнительными дисульфидными мостиками между тяжелыми цепями. Эти свойства ограничивают гибкость молекулы IgG2. IgG3 отличается от других подклассов ее уникальной удлиненной шарнирной областью (примерно в 4 раза более длинной, чем шарнир IgG1), содержащей 62 аминокислоты (в том числе 21 пролин и 11 цистеинов), образующие негибкую полипролиновую двойную спираль. В IgG3, Fab-фрагменты находятся относительно далеко от Fc-фрагмента, что придает этой молекуле бóльшую гибкость. Удлиненный шарнир в IgG3 ответствен также за его более высокую молекулярную массу в сравнении с другими подклассами. Шарнирная область IgG4 является более короткой, чем шарнирная область IgG1, и ее гибкость является промежуточной между гибкостью IgG1 и IgG2. Сообщалось, что гибкость шарнирных областей уменьшается в следующем порядке: IgG3>IgG1>IgG4>IgG2. Эти четыре подкласса IgG отличаются также друг от друга в отношении их эффекторных функций. Это различие относится к различиям в структуре, в том числе различиям в отношении взаимодействия между вариабельными областями, Fab-фрагментами и константным Fc-фрагментом.
Согласно кристаллографическим исследованиям, шарнирная область иммуноглобулинов может быть дополнительно подразделена функционально на три области: верхнюю шарнирную область, центральную (коровую) область и нижнюю шарнирную область. Shin et at., 1992 Immunological Reviews 130:87. Верхняя шарнирная область включает аминокислоты от карбоксильного конца CH1 до первого остатка в шарнире, который ограничивает движение, обычно первого остатка цистеина, который образует межцепочечную дисульфидную связь между двумя тяжелыми цепями. Длина верхней шарнирной области коррелирует с сегментной гибкостью антитела. Центральная шарнирная область содержит дисульфидные мостики между тяжелыми цепями, а нижняя шарнирная область соединяет аминоконец CH2-домена и включает остатки в CH2·Id. Центральная (коровая) шарнирная область IgG1 человека содержит последовательность Cys-Pro-Pro-Cys, которая, при димеризации образованием дисульфидной связи, приводит к циклическому октапептиду, который, как считается, действует в качестве точки вращения, придавая таким образом гибкость. Шарнирная область может содержать также один или несколько сайтов гликозилирования, которые включают ряд структурно отличающихся типов сайтов для присоединения углеводов. Например, IgА1 содержит пять сайтов гликозилирования в состоящем из 17 аминокислот сегменте шарнирной области, придавая устойчивость полипептиду шарнирной области к кишечным протеазам, что считается предпочтительным свойством для секреторного иммуноглобулина.
Конформационные изменения, допускаемые структурой и гибкостью полипептидной последовательности шарнирной области иммуноглобулина, могут также влиять на эффекторные функции Fc-части антитела. Три основные категории эффекторных функций, ассоциированных с Fc-областью, включают (1) активацию классического каскада комплемента, (2) взаимодействие с эффекторными клетками и (3) компартментализацию иммуноглобулинов. Разные подклассы IgG человека варьируют по относительным эффективностям, с которыми они фиксируют (связывают) комплемент или активируют и усиливают стадии каскада комплемента. См., например, Kirschfink, 2001 Immunol. Rev. 180:177; Chakraborti et al., 2000 Cell Signal 12:607; Kohl et al., 1999 Mol. Immunol. 36:893; Marsh et al., 1999 Curr. Opin. Nephrol. Hypertens. 8:557; Speth et al, 1999 Wien Klin. Wochenschr. 111:378.
Исключения в отношении H2L2-структуры обычных антител встречаются в некоторых изотипах иммуноглобулинов, обнаруженных в семействе верблюдовых (верблюдах, дромедарах (одногорбых верблюдах) и ламах; Hamers-Casterman et al., 1993 Nature 363:446; Nguyen et al., 1998 J. Mol. Biol 275:413), усатых акулах-няньках (Roux et al., 1998 Proc. Nat. Acad. Sci. USA 95: 11804) и пятнистой химере (Nguyen, et al., 2002 Immunogenetics 54(l):39-47). Эти антитела могут, очевидно, образовывать антигенсвязывающие области с использованием только вариабельной области тяжелой цепи, т.е. эти функциональные антитела являются гомодимерами только тяжелых цепей (называемые «антителами тяжелой цепи» или “HCAb"). Несмотря на преимущества технологии антител в диагностике и лечении заболеваний, существуют некоторые невыгодные аспекты развития технологий полноразмерных антител в качестве диагностических и/или терапевтических реагентов. Полноразмерные антитела являются большими белковыми структурами, примером которых является гетеротетрамерная структура IgG-изотипа, содержащая две легкие и две тяжелые цепи. Такие большие молекулы являются стерически затрудненными в некоторых применениях. Например, в лечении солидных опухолей, полноразмерные антитела не могут легко проникать во внутреннюю часть опухоли. Кроме того, относительно большой размер полноразмерных антител представляет проблему для гарантии того, что введение in vivo таких молекул не индуцирует иммунную реакцию. Кроме того, генерирование активных молекул антител обычно включает культивирование рекомбинантных эукариотических клеток, способных обеспечивать подходящий посттрансляционный процессинг возникающих молекул антител, и такие клетки могут быть трудоемкими для культивирования и индукции таким образом, который обеспечивает коммерчески применимые выходы активного антитела.
Недавно, были сконструированы меньшие молекулы иммуноглобулинов для преодоления проблем, ассоциированных с методологиями полноразмерных иммуноглобулинов. Одноцепочечный вариабельный фрагмент антитела (scFv) содержит вариабельный домен тяжелой цепи антитела, соединенный через короткий пептид с вариабельным доменом легкой цепи антитела (Huston et al., Proc. Natl. Acad. Sci. USA, 1988, 85: 5879-83). Вследствие малого размера молекул scFv, они проявляют более эффективное проникновение в ткани, чем полноразмерный иммуноглобулин. Противоопухолевые scFv обнаруживали более быстрое проникновение в опухоль и более равномерное распределение по массе опухоли, чем соответствующее химерное антитело (Yokota et al, Cancer Res. 1992, 52:3402-08).
Несмотря на преимущества, которые вносят молекулы scFv в серотерапию, существуют несколько недостатков в отношении этого терапевтического подхода. scFv быстро выводится из кровотока, что может уменьшать токсические действия в нормальных клетках, но такой быстрый клиренс препятствует доставке минимальной эффективной дозы к ткани-мишени. Приготовление адекватных количеств scFv для введения пациентам было проблемой вследствие трудностей экспрессии и выделения scFv, которые неблагоприятно влияли на выход. Во время экспрессии молекулы scFv лишены стабильности и часто агрегируют вследствие спаривания вариабельных областей из разных молекул. Кроме того, уровни получения молекул scFv в экспрессионных системах млекопитающих являются низкими, что ограничивает потенциал эффективного получения молекул scFv для терапии (Davis et al, J Biol. Chem. 1990, 265:10410-18); Traunecker et al., EMBO J 1991, 10: 3655-59). Исследовались стратегии для улучшения получения, включающие добавление сайтов гликозилирования в вариабельные области (Jost, C. R. U.S. Pat. No. 5888773, Jost et al, J. Biol. Chem. 1994, 69: 26267-73).
Другим недостатком использования scFv для терапии является отсутствие эффекторной функции. scFv без цитолитической функции, такой как антителозависимая клеточно-опосредованная цитотоксичность (ADCC) и комплементзависимая цитотоксичность (CDC), ассоциированные с константной областью иммуноглобулина, могут быть неэффективными для лечения заболевания. Даже хотя развитие технологии scFv началось более 12 лет назад, в настоящее время scFv-продукты не одобрены для терапии.
Альтернативно, было сделано предположение, что слияние scFv с другой молекулой, такой как токсин, могло бы использовать преимущество специфической антигенсвязывающей активности и малого размера scFv для доставки этого токсина к ткани-мишени. Chaudary et al., Nature 1989, 339:394; Batra et al., Mol. Cell. Biol. 1991, 11:2200. Таким образом, конъюгация или слияние токсинов с scFv были предложены в качестве альтернативной стратегии для обеспечения эффективных, антиген-специфических молекул, но введение доз с такими конъюгатами или химерами может быть ограничено избыточной и/или неспецифической токсичностью вследствие присутствия токсиновой части таких препаратов. Токсические эффекты могут включать надфизиологическое повышение ферментов печени и синдром сосудистого просачивания и другие нежелательные эффекты. Кроме того, иммунотоксины сами являются высокоиммуногенными после введения хозяину, и антитела хозяина, генерированные против этого иммунотоксина, ограничивают потенциальную применимость повторяемых терапевтических курсов лечения индивидуума.
Нехирургическая противораковая терапия, такая как наружное облучение и химиотерапия, могут страдать от ограниченной эффективности вследствие токсических действий на нормальные ткани и клетки, вследствие отсутствия специфичности, которое проявляют эти способы лечения в отношении раковых клеток. Для преодоления этого недостатка, были разработаны методологии нацеленного лечения для увеличения специфичности лечения в отношении клеток и тканей, нуждающихся в лечении. Примером такой нацеленной методологии для применения in vivo является введение конъюгатов антител, с антителом, сконструированным для специфического узнавания маркера, ассоциированного с клеткой или тканью, нуждающимися в лечении, и это антитело конъюгировано с терапевтическим агентом, таким как токсин, в случае лечения рака. Антитела, в виде системных агентов, циркулируют к чувствительным и нежелательным компартментам тела, таким как костный мозг. В остром радиационном повреждении, деструкция лимфоидного и гемопоэтического компартментов является основным фактором в развитии септицемии и последующей смерти. Кроме того, антитела являются большими глобулярными белками, которые могут проявлять слабое проникновение в ткани, нуждающиеся в лечении.
Пациенты-люди и субъекты, не являющиеся людьми, страдающие от различных процессов конечной стадии заболевания, часто требуют трансплантации органов. Однако, трансплантация органов должна преодолевать неблагоприятную иммунную реакцию реципиента и сдерживать иммунологическое отторжение трансплантированного органа подавлением клеточной иммунной реакции реципиента на чужеродный орган цитотоксическими агентами, которые влияют на лимфоидную ткань и другие части гемопоэтической системы. Принятие трансплантата ограничивается толерантностью реципиента к этим цитотоксическим химикалиям, многие из которых являются сходными с противораковыми (антипролиферативными) агентами. Подобным образом, при применении цитотоксических противомикробных агентов, в частности, антивирусных лекарственных средств, или при применении цитотоксических лекарственных средств для терапии аутоиммунных заболеваний, например, в лечении системной красной волчанки, серьезным недостатком являются токсические действия терапевтических агентов на костный мозг и гемопоэтические клетки тела.
Применение нацеленных терапий, таких как нацеленная терапия конъюгатами антител, предназначено для локализации максимального количества терапевтического агента по возможности в желаемом участке действия, и успех таких терапий обнаруживают по относительно высокому отношению сигнала к фону терапевтического агента. Примеры нацеленных антител включают конъюгаты с диагностическим или терапевтическим агентом антитела или фрагментов антитела, клетко- или тканеспецифических пептидов и гормонов и других рецепторсвязывающих молекул. Например, антитела против различных детерминант, ассоциированных с патологическими и нормальными клетками, а также ассоциированных с патогенными микроорганизмами, были использованы для детектирования и лечения большого разнообразия патологических состояний или повреждений. В этих способах, нацеливающее антитело непосредственно конъюгируют с подходящим детектирующим или терапевтическим агентом, как описано, например, в Hansen et al, Патенте США № 3927193, и Goldenberg, Патентах США с номерами 4331647, 4348376, 4361544, 4468457, 4444744, 4460459, 4460561, 4624846 и 4818709.
Одной проблемой, встречающейся в способах прямого нацеливания, т.е. в способах, в которых диагностический или терапевтический агент («активный агент») конъюгирован непосредственно с нацеливающей частью молекулы, является то, что относительно малая фракция этого конъюгата действительно связывается с участком-мишенью, в то время как большинство конъюгата остается в кровотоке и ухудшает одним или другим путем функцию нацеленного конъюгата. Для гарантии максимальной локализации активного агента, вводят обычно избыток нацеленного конъюгата, гарантируя, что некоторая часть конъюгата будет оставаться несвязанной и вносить вклад в уровни фона этого активного агента. Диагностический конъюгат, например, конъюгат радиоиммуносцинтиграфической визуализации или визуализации с использованием магнитного резонанса, который не связывается с его мишенью, может оставаться в кровотоке, увеличивая посредством этого фон и уменьшая разрешение этого диагностического способа. В случае терапевтического конъюгата, имеющего токсин в качестве активного агента (например, радиоизотопа, лекарственного средства или токсического соединения), присоединенный к долгоциркулирующей нацеливающей части, такой как антитело, этот циркулирующий конъюгат может приводить к неприемлемой токсичности в хозяине, например, токсичности для костного мозга или системным вредным побочным действиям.
Патент США № 4782840 описывает способ уменьшения эффекта повышенных уровней фоновой радиации во время хирургии. Этот способ предусматривает инъекцию пациенту антител, специфических для неопластической ткани, причем эти антитела помечены радиоизотопами, имеющими подходящий период полужизни в организме, такими как 125I. После инъекции радиоактивно меченого антитела операцию откладывают по меньшей мере на 7-10 дней, предпочтительно 14 дней - 21 день, чтобы любое несвязанное радиоактивно меченое антитело было выведено до низкого уровня фона.
Патент США № 4932412 описывает способы уменьшения или коррекции неспецифической фоновой радиации во время интраоперационного детектирования. Эти способы включают введение пациенту, который получил радиоактивно меченое первичное антитело, контрастного агента, субтракционного агента или вторичного антитела, которое связывает первичное антитело.
Кроме продуцирования антител, описанного выше, иммунная система включает различные типы клеток, которые имеют мощные биологические действия. Во время гемопоэза, происходящие из костного мозга стволовые клетки дифференцируются в любые зрелые клетки иммунной системы (“В”-клетки») или в предшественники клеток, которые мигрируют из костного мозга для созревания в вилочковой железе (тимусе) (“T”-клетки).
В-клетки являются центральными относительно гуморального компонента иммунной реакции. В-клетки активируются посредством соответствующей презентации антигена, чтобы стать антитело-секретирующими плазматическими клетками; презентация антигена приводит также к клональной экспансии активированной В-клетки. В-клетки являются первично ответственными за гуморальный компонент иммунной реакции. Плазматическая клетка обычно обнаруживает приблизительно 105 молекул антител (IgD и IgM) на ее поверхности.
T-лимфоциты могут быть подразделены на две категории. Цитотоксические Т-клетки, Тс-лимфоциты или CTL (CD8+ T-клетки), уничтожают клетки, несущие чужеродный поверхностный антиген, в ассоциации с МНС Класса I, и могут уничтожать клетки, которые захватывают внутриклеточных паразитов (бактерии или вирусы), пока инфицированная клетка имеет микробный антиген на ее поверхности. Tc-клетки уничтожают опухолевые клетки и ответственны за отторжение трансплантированных клеток. Tc-клетки узнают комплексы антиген-МНС Класса I на клетках-мишенях, контактируют с ними и высвобождают содержимое гранул непосредственно на мембрану клеток-мишеней, которое лизирует эту клетку.
Второй категорией T-клеток является хелперная Т-клетка или Тh-лимфоцит (CD4+ T-клетки), которая продуцирует лимфокины, являющиеся «хелперными» факторами в созревании В-клеток в секретирующие антитело плазматические клетки. Тh-клетки также продуцируют определенные лимфокины, которые стимулируют дифференцировку эффекторных Т-лимфоцитов и активность макрофагов. Тh1-клетки узнают антиген на макрофагах в ассоциации с МНС Класса II и становятся активированными (посредством IL-1) для продуцирования лимфокинов, в том числе IFN-γ, который активирует макрофаги и NK-клетки. Эти клетки опосредуют различные аспекты клеточноопосредованной иммунной реакции, в том числе реакций гиперчувствительности замедленного типа. Th2-клетки узнают антиген в ассоциации с МНС Класса II на антигенпрезентирующей клетки или APC (например, мигрирующие макрофаги и дендритные клетки) и затем продуцируют интерлейкины и другие вещества, которые стимулируют специфическую В-клеточную и Т-клеточную пролиферацию и активность.
Кроме функционирования в качестве APC, которые инициируют Т-клеточные взаимодействия, развитие и пролиферацию, макрофаги участвуют в экспрессии клеточно-опосредованного иммунитета, так как они становятся активированными IFN-γ, продуцируемым клеточно-опосредованной иммунной реакцией. Активированные макрофаги имеют увеличенный фагоцитарный потенциал и высвобождают растворимые вещества, которые вызывают воспаление и разрушают многие бактерии и другие клетки. Природные клетки-убийцы (клетки-киллеры) являются цитотоксическими клетками, которые лизируют клетки, несущие новый антиген, независимо от типа их МНС и даже лизируют клетки, которые не несут белков МНС. Природные Т-клетки-киллеры, или NK-клетки, определяют по их способности уничтожать клетки, обнаруживающие чужеродный антиген (например, опухолевые клетки), независимо от типа МНС и независимо от предыдущей сенсибилизации (подвергания действию) этого антигена. NK-клетки могут активироваться IL-2 и IFN-γ и лизируют клетки таким же образом, что и цитотоксические Т-лимфоциты. Некоторые NK-клетки имеют рецепторы для Fc-домена антитела IgG (например, CD16 или FcγRIII) и, следовательно, способны связываться с Fc-частью IgG на поверхности клетки-мишени и высвобождать цитолитические компоненты, которые уничтожают эту клетку-мишень посредством антителозависимой клеточно-опосредованной цитотоксичности.
Другой группой клеток являются гранулоциты или полиморфно-ядерные лейкоциты (PMN). Нейтрофилы, один тип PMN, уничтожают проникшие бактерии, а фагоцитоз остальное. Эозинофилы являются другим типом PMN и содержат гранулы, которые являются цитотоксическими при высвобождении на другой клетке, такой как чужеродная клетка. Базофилы, другой тип PMN, являются важными медиаторами сильных физиологических реакций (например, воспаления), которые проявляют их действия посредством высвобождения различных биологически активных соединений, таких как гистамин, серотонин, простагландины и лейкотриены. Общей для всех этих типов клеток является способность проявлять физиологическое действие в организме, часто посредством уничтожения, и необязательно утилизации, ядовитых (вредных) композиций, таких как чужеродные клетки.
Хотя различные клетки млекопитающих, в том числе клетки иммунной системы, способны проявлять непосредственно физиологическое действие (например, уничтожение клеток, примером чего служат Tc, NK, некоторые PMN, макрофаг и т.п.), другие клетки опосредованно способствуют физиологическому действию. Например, первоначальная презентация антигена необученной Т-клетке иммунной системы требует МНС-презентации, которая дает разрешение на контакт клетка-клетка. Далее, часто требуется контакт между активированной Т-клеткой и антиген-специфической В-клеткой для получения конкретной иммуногенной реакции. Третьей формой контакта клетка-клетка, часто наблюдаемой в иммунных реакциях, является контакт между активированной В-клеткой и фолликулярными дендритными клетками. Каждое из этих требований контакта клетка-клетка усложняет нацеливание биологически активного агента на конкретную мишень.
Считается, что комплементзависимая цитотоксичность (CDC) является важным механизмом клиренса конкретных клеток-мишеней, таких как опухолевые клетки. CDC является серией событий, которая состоит из совокупности ферментов, которые становятся активированными друг другом в виде каскада. Комплемент играет важную роль в клиренсе антигена, выполняемом его четырьмя основными функциями: (1) локальной вазодилатацией; (2) аттракцией иммунных клеток, особенно фагоцитов (хемотаксисом); (3) маркированием чужеродных организмов для фагоцитоза (опсонизацией) и (4) деструкцией внедрившихся организмов атакующим комплексом мембраны (MAC-атакой). Центральной молекулой является белок С3. Он является ферментом, который расщепляется на два фрагмента компонентами либо классического пути, либо альтернативного пути. Классический путь индуцируется антителами, главным образом IgG и IgМ, тогда как альтернативный путь стимулируется бактериальными продуктами, такими как липополисахарид (LPS). Вкратце, продукты расщепления С3 включают малый пептид С3а, который является хемотаксическим для фагоцитарных иммунных клеток и приводит к локальной вазодилатации, вызывая высвобождение С5а-фрагмента из С5. Другая часть С3, C3b, покрывает антигены на поверхности чужеродных организмов и осуществляет опсонизацию этого организма для деструкции. C3b реагирует также с другими компонентами системы комплемента с образованием MAC, состоящего из C5b, C6, C7, C8 и C9.
Существуют проблемы, связанные с применением антител в терапии человека, так как реакция иммунной системы на любой антиген, даже самый простой, является «поликлональной», т.е. эта система производит антитела большого диапазона структур как в их связывающих областях, так и в их эффекторных областях.
Два подхода использовали в попытке уменьшения проблемы иммуногенных антител. Первым является получение химерных антител, в которых антигенсвязывающая часть (вариабельные области) моноклонального антитела мыши слита с эффекторной частью (константной областью) антитела человека. Во втором подходе, антитела изменяли посредством способа, известного как трансплантация определяющего комплементарность области (CDR) или «гуманизация». Этот процесс был дополнительно усовершенствован для включения изменений, называемого «реконструированием» молекулы антитела (Verhoeyen, et al, 1988 Science 239:1534-1536; Riechmann, et al, 1988 Nature 332:323-337; Tempest, et al, Bio/Technol 1991 9:266-271), "гиперхимеризацией" (Queen, et al, 1989 Proc Natl Acad Sci USA 86:10029-10033; Co, et al, 1991 Proc Natl Acad Sci USA 88:2869-2873; Co, et al, 1992 J Immunol 148:1149-1154) и “облицовкой" (Mark, et al, In: Metcalf BW, Dalton BJ, eds. Cellular adhesion: molecular definition to therapeutic potential. New York: Plenum Press, 1994:291-312).
В среднем менее одного терапевтического антитела в год вводили на рынок начиная с 1986 года, спустя одиннадцать лет после публикации моноклональных антител. Пять мышиных моноклональных антител были введены в медицину человека на протяжении десятилетнего периода 1986-1995, в том числе "муромонаб-CD3" (OrthoClone OKT3®) для острого отторжения трансплантатов органов; "эдреколомаб" (Panorex®) для колоректального рака; "одулимомаб" (Antilfa®) для отторжения трансплантата; и "ибритумомаб" (Zevalin® yiuxetan) для не-ходжкинской лимфомы. Дополнительно был введен на рынок моноклональный Fab, "абциксимаб" (ReoPro®) для предотвращения рецидива окклюзии коронарной артерии. Были запущены также три химерных моноклональных антитела: "ритуксимаб" (Rituxan®) для лечения В-клеточных лимфом; "базиликсимаб" (Simulect®) для отторжения трансплантата и "инфликсимаб" (Remicad