Соединения, имеющие арилсульфонамидную структуру, применимые в качестве ингибиторов металлопротеаз
Иллюстрации
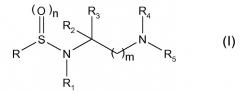
Показать всеИзобретение относится к арилсульфонамидным соединениям, имеющим приведенную ниже формулу (I), где R представляет собой группу формулы -Ar-Х-Ar' (II), где Ar представляет собой фениленовую группу и Ar' является фенильной группой; причем указанные фениленовая и фенильная группы необязательно замещены одной группой, выбранной из неразветвленных или разветвленных С1-4алкоксигрупп; Х представляет собой одинарную связь или -O-; R1 представляет собой группу -ORa, где Ra выбран из неразветвленных или разветвленных С1-С4алкильных групп; или Ra представляет собой группу формулы , где в формуле (III) p равно целому числу 1 или 2; Z представляет собой одинарную связь или двухвалентный линкер, выбранный из -O-; r равно 0, 1 или 2, и W представляет собой фенил или пиперазин, каждый из которых необязательно замещен одной или более группами, выбранными из -COR', где R' представляет собой неразветвленный или разветвленный С1-4алкил; R2 и R3 являются одинаковыми или разными и каждый независимо представляет собой Н или связывающую цинк группу, выбранную из группы, состоящей из -СООН, и -CONHOH; R4 представляет собой группу, выбранную из -CORc, -COORc и -S(O)2Rc, где Rc представляет собой группу, выбранную из неразветвленного или разветвленного алкила, фенила, фенилалкила, имеющего от 1 до 4 атомов углерода в алкильной цепи; R5 представляет собой Н или R4 и R5 вместе с атомом N, к которому они присоединены, образуют N-фталоимидо группу (а), n равно 2; m равно целому числу от 1 до 6; или их фармацевтически приемлемым солям. Изобретение относится также к способу получения арилсульфонамидных соединений, содержащим их фармацевтическим композициям и их применению в качестве терапевтических агентов, для лечения дегенеративных нарушений, вовлекающих металлопротеазы ММР-2, ММР-13, ММР-14. Технический результат - арилсульфонамидные соединения, обладающие ингибирующей активностью в отношении металлопротеаз ММР-2, ММР-13, ММР-14. 5 н. и 10 з.п. ф-лы, 1 табл., 17 пр.
Реферат
Область изобретения, к которой относится изобретение
Настоящее изобретение находит применение в области терапии, и, более конкретно, оно относится к арилсульфонамидосоединениям, способу их получения, содержащим их фармацевтическим композициям и их применению в качестве терапевтических агентов, особенно при лечении дегенеративных нарушений.
Уровень техники
Известно, что многие физиологические и патологические процессы характеризуются как значительной гиперпролиферацией, так и подвижностью клеток. Среди них имеются физиологические процессы, подобные, например, эмбриогенезу или развитию и дифференциации ткани, а также патологические процессы, среди которых имеются опухоли или, более обычно, нарушения, поражающие различные участки или органы тела: легкие, мышцы, кости, кожу, а также нервную, лимфатическую, желудочно-кишечную, почечную, макуло-глазную, сердечно-сосудистую систему и тому подобное.
При патологических или непатологических условиях высокая клеточная пролиферация и подвижность в основном зависит от активности металлопротеаз цинка, класса каталитических протеаз, присутствующих в организме людей (называемых также протеиназами), которые, как известно, координируют ионы цинка в их каталитическом сайте и которые способны гидролизовать амидные связи в пептидной цепи белков.
Среди металлопротеаз цинка имеются металлопротеазы внеклеточного матрикса (далее обозначаемые ММР), ADAMS (дизинтегрин и металлопротеазы) и ADAMT (дизинтегрин и металлопротеаза с повторами тромбоспондина типа I).
После продуцирования эти протеазы остаются прикрепленными на клеточных мембранах или экскретируются во внеклеточный матрикс (ЕСМ), важную физиологическую структуру, содержащую организованную трехмерную сетчатую структуру клеток окружающих тканей, которые электрически, химически и физически соединяются друг с другом.
Как таковые, они могут играть ключевую роль в некоторых внеклеточных процессах, включающих взаимодействия клетка-клетка и клетка-ЕСМ, а также в физиологических внутриклеточных процессах, например, росте, развитии и ремоделировании тканей, трансдукции внутри- и внеклеточных сигналов и феномене адгезии.
Протеолитическая активность этих металлопротеаз цинка в физиологических условиях значительно и тонко регулируется эндогенными ингибиторами, известными как тканевые ингибиторы металлопротеаз (TIMP), которые, как было обнаружено, играют фундаментальную роль также в регуляции активности ADAM и ADAMT.
Так, тонкое равновесие между ММР и их ингибиторами делает возможным надлежащее функционирование всех из физиологических процессов, в которых принимает участие ММР, таких как, например, эмбрионный рост и развитие, морфогенез тканей, миграция клеток и ремоделирование матриксов, репродуктивные процессы, т.е. менструальный цикл и овуляция, образование костей, адипогенез, заживление ран и ангиогенез или даже высвобождение и процессинг биоактивных молекул, как например, внутри- или межклеточные сигналы пептидов.
Вследствие их диффузии в теле человека и их роли в оказании усилия, таким образом очевидно, что любое изменение в регуляции даже одного из указанных выше процессов, например, из-за патологий, подобных опухолям, развитие которых может определить либо сверхэкспрессию, либо недостаточную экспрессию ММР, может привести, почти неизбежно, к возникновению дегенеративных процессов, приводящих к аномальному изменению и/или развитию тканей.
Примеры указанных выше патологий, в которых могут участвовать сверхэкспрессия или недостаточная экспрессия ММР, таким образом приводящая к измененной тканевой морфологии с нерегулируемой пролиферацией клеток, могут включать артрит и нарушения соединительных тканей; нейродегенеративные нарушения, такие как рассеянный склероз, болезнь Альцгеймера, удар и ALS (боковой амиотрофический склероз); сердечно-сосудистые нарушения, такие как атеросклероз, аневризма, сердечная недостаточность, застойная кардиомиопатия; легочные заболевания, такие как эмфизема или муковисцидоз; язвы желудка; сепсис и аутоиммунные нарушения.
Помимо этого, во время тканевой дегенерации измененная экспрессия этих протеаз цинка может также зависеть, например, от типа клеток, активации их проферментативных форм, путей генной транскрипции, а также механизмов экскреции и эндоцитоза. Внеклеточная и внутриклеточная пороговая величина активных металлопротеаз цинка часто регулируется на поверхности клеточной мембраны посредством устранения их каталитической активности другими металлопротеазами, подобными ММР, закрепленными на клеточной мембране, известными как ММР мембранного типа, альфа-конвертазой фактора некроза опухоли, более известной как ТАСЕ (и соответствующей ADAM-17), или даже другими ADAM или ADAMT.
Поэтому для терапевтических целей, когда имеют место патологические нарушения, характеризующиеся значительной активностью металлопротеаз на клеточной поверхности инвазивных и гиперпролиферирующих клеток, может быть желательным ингибирование этих МТ-ММР или некоторых других ADAM или ADAMT.
До сих пор по меньшей мере 23 разных фермента, которые, как известно, принадлежат к семейству ММР, были классифицированы на подклассы согласно их специфичности к субстратам. Известно, что среди них, например, ММР-1, ММР-8 и ММР-13 действуют на коллагеназу; с другой стороны, известно, что ММР-2 и ММР-9 действуют на желатиназу как на мишень, и известно, что ММР-3, ММР-10 и ММР-11 действуют на стромелизин как на мишень.
Помимо этого, к настоящему времени идентифицирована и характеризована четвертая подгруппа мембранного типа ММР, названная МТ-ММР, а именно, МТ1-ММР (ММР-14), МТ2-ММР (ММР-15), МТ3-ММР (ММР-16), МТ4-ММР (ММР-17), МТ5-ММР (ММР-24) и МТ6-ММР (ММР-26); оказываемое действие, однако, было выяснено только для некоторых из них (см. для ссылки HG Munshi et al., Cancer Metastasis Rev., 2006, 25, 45-56; и VS Golubkov et al., J. Biol. Chem, 2005, 280, 25079-25086).
Известно, например, что ММР-14 является ответственной за активацию про-ММР-2 на наружной поверхности некоторых типов клеток, например, клеток гладких мышц васкулярной ткани в ангиогенетических процессах (см. для ссылки N. Koshikawa et al., J. Cell. Biol. 2000, 148, 615-624; и Y. Itoh, H. Nagase, Essays in Biochemistry, 2002, 38, 21-36). Кроме того, известно, что ММР-14 гиперэкспрессируется на мембранах некоторых типов опухолевых клеток, таких как в меланомах (см. в качестве ссылки NE Sounni et al., Int. J. Cancer, 2002, 98, 23-28), аденокарциноме молочной железы (см. в качестве ссылки NE Sounni, et al., FASEB J 2002, 16, 555-564) и в глиомах (AT Belien, et al., J. Cell Biol 1999, 144, 373-384; и EI Deryugina, et al., Cancer Res, 2002; 62: 580-588).
ММР-14 может также активировать другие про-ММР, подобные про-ММР-13, гиперэкспрессия которых, как известно, коррелирует в некоторых типах клеток с опухолями, воспалением или сердечно-сосудистыми и нейродегенеративными нарушениями (см., например, AR Folgueras et al., Int. J. Dev. Biol., 2004, 48, 411-424; и JO Degushi, et al., Circulation, 2005, 2708-2715).
Известно, что даже другие ММР способствуют активации про-ММР-2, и/или про-ММР-13, и/или про-ММР-9. Известно, что, например, ММР-15, ММР-16, ММР-17 и ММР-24 активируют про-ММР-2 и про-ММР-13; ММР-17 действует только для активации про-ММР-2, тогда как ММР-26 активирует про-ММР-2 и про-ММР-9; см. в качестве ссылки AR Folgueras et al. (Int. J. Dev. Biol., 2004, 48, 411-424).
Кроме того, ММР-2 и ММР-13 продуцируются из пролиферирующих и инвазивных клеток и активируются или так или иначе становятся активируемыми в ЕСМ каталитической активностью ММ-ММР мембранной поверхности; поэтому они представляют собой предварительное средство для движения клеток через дигестивную проницаемую поверхность ЕСМ.
На основании предыдущих исследований по так называемым “деградомикам” (см. в качестве ссылки C Lopez-Otin et al., Nature Rev. 2002, 3, 509-519; и CM Overall et al., Nature Review Cancer, 2006, 6, 227-239) возможность нацеливания на некоторые ММР в качестве кандидатов для доставки лекарственного средства при раковых и других патологиях, но при исключении препятствий физиологическим функциям, вызываемых некоторыми другими ММР, в настоящее время широко подтверждается.
По существу исследования продолжают проводить для разработки ингибиторов ММР, которые можно применять в терапии и которые способны селективно воздействовать на патологические поражения без указанных выше недостатков.
Следовательно, когда активность некоторых ММР должна быть ингибирована, чтобы ограничить имеющий место дегенеративный процесс и противодействовать ему, активность некоторых других типов ММР, регулирующих физиологические процессы развития и морфогенеза, не должна быть ослаблена, что, как указано выше, может привести к нежелательным побочным действиям.
Известно, что среди них, например, мышечно-скелетный синдром с фибропролиферативными действиями в суставной капсуле колена имеет место при недостаточности нормальной активности ремоделирования ткани, вызванной ММР-1. Таким же образом, ингибирование некоторых ММР, принимающих участие в регуляции онкогенеза, таких как, например, ММР-3, может вызвать увеличение клеточной пролиферации и инвазии.
Поэтому в терапии отсутствие ингибирования ММР-1 и ММР-3, рассматриваемых как не являющихся мишенями ММР, представляется очень желательным.
В противоположность этому, обнаружено, что при явной селективности по отношению к ММР-2 и ММР-9 имеют место проапоптические действия на опухолевые клеточные культуры без проявления значительных побочных эффектов.
Следовательно, поиск молекул, способных специфически регулировать активность определенных ММР, когда утрачены нормальные механизмы, может обеспечить пригодные соединения для лечения некоторых заболеваний.
В данной области известны различные ингибиторы металлопротеаз, некоторые из которых относятся к сульфонамидопроизводным.
Среди них имеются, например, содержащие карбоциклическую боковую цепь N-замещенные ингибиторы металлопротеаз, описанные в WO 01/70720, и их фармацевтические композиции.
В US 6686355 описаны производные бифенила, содержащие циклическую азотсодержащую сульфонамидогруппу, в качестве ингибиторов ММР.
В WO 2004/069365 описаны диагностические агенты для получения изображения, содержащие ингибиторы металлопротеаз матрикса, имеющие сульфонамидогруппы, замещенные N,N-диалкильной цепью и должным образом меченные γ-испускающим радионуклидом.
В WO 98/39329 описаны производные сульфонамидогидроксамовой кислоты, специфически поражающие как мишени ММР-2, ММР-9 и ММР-13; приведенные в ней в качестве примеров несколько соединений содержат сульфонамидогруппы, замещенные боковой N,N-диалкильной цепью.
В US 7067670 описаны производные алкилсульфонамидогидроксамовых кислот, обладающие ингибирующей активностью в отношении ММР-2 и ММР-13.
В US 6500948 описаны пиридилокси- и пиридилтиоарилсульфонамидопроизводные, обладающие ингибирующей ММР активностью, у которых N-атом сульфонамидогруппы является частью шестичленного гетероцикла, содержащего атомы углерода, соседние с указанным выше N-атомом.
В US 6495568 описаны производные алкил- или циклоалкилсульфонамидогидроксамовых кислот в качестве ингибиторов металлопротеаз матрикса.
В US 5985900 описаны сульфонамидопроизводные, характеризующиеся фенил- или фенилен-SO2NH-частью, обладающие ингибирующий ММР активностью.
В US 99/42443 описаны производные сульфониламиногидроксамовой кислоты, содержащие группу арил-SO2NH-, которые охарактеризованы как разрушающие матрикс металлопротеиназы.
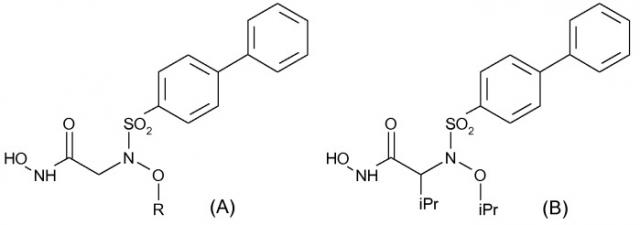
В данной области известны другие сульфонамидоингибиторы ММР. Среди них имеются селективные ингибиторы желатиназы А (ММР-2), описанные Rossello et al. в Bioorg. & Med. Chem. 12 (2004) 2441-2450 и имеющие указанную ниже формулу (А), где R представляет собой группу, выбранную из изопропила, аллила или п-(бензилокси)бензила.
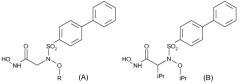
Кроме того, ингибиторы ММР-2, проявляющие хорошую селективность в отношении ММР-2/ММР-1, были также описаны Tuccinardi et al. (Bioorg. & Med. Chem. 14 (2006) 4260-4276); среди описанных в этой публикации в качестве примеров соединений имеется производное указанной ниже формулы (В)
Помимо указанных выше публикаций, в предыдущих работах в данной области указывается, что применение селективных ингибиторов ММР-2, которые не действуют на некоторые ММР, такие как ММР-1 и ММР-3, позволяет блокировать прорастание (инвазию) клеток НТ1080 (очень инвазивной фибросаркомы) и клеток HUVEC (эндотелия вены пупка человека) на моделях хемоинвазии и ангиогенеза (A. Rossello, et al., Bioorg & Med. Chem., 2004, 12, 2441-2450; и A. Rossello, et al., Bioorg & Med. Chem. Lett., 2005, 15, 1321-1326).
Как указывалось в вышеупомянутой публикации Bioorg & Med. Chem. Lett., (2005), была разработана возможная модель антиангиогенеза и были синтезированы определенные соединения, обозначаемые в ней (5b) и (5с), формулы которых представлены ниже
На основании результатов, полученных на выделенных ферментах и согласно способу, описанному CG Knight et al. (см. в качестве ссылки FEBS Lett. 1992, 296, 263; и Methods Enzymol. 1995, 248, 470), причем указанный способ включает применение флуорогенного субстрата FS-1 (например, Mca-Pro-Leu-Gly-Leu-Dpa-Ala-Arg-NH2), как указывается Rossello et al., in Bioorg. Med. Chem. Lett. 12 (2004), 2441-2450, показано, что соединение (5b) является двойным ингибитором ММР-2 (величина IC50, соответствующая 0,41 нМ) и ММР-14 (величина IC50, соответствующая 7,7 нМ).
В этом отношении, если не оговорено особо, в нижеследующих фармакологических и экспериментальных разделах, вышеуказанное соединение (5b) известного уровня техники, здесь называется “ссылочным соединением (5b)”.
Кроме того, в вышеуказанных публикациях Bioorg. Med. Chem. Lett. 15 (2005), 1321-1326, и Bioorg. Med. Chem. Lett. 15 (2005), 2311-2314 описаны химические синтетические промежуточные продукты следующей формулы
Авторами изобретения теперь обнаружен новый класс ингибиторов металлопротеазы Zn, имеющих арилсульфонамидную структуру, которые на основании испытаний на ингибирование имеют IC50 в молярном диапазоне нано/субнановеличин и в результате являются особенно эффективными в отношении мишеней-ферментов, в частности ММР-2, ММР-13 и ММР-14.
Задача изобретения
Таким образом, первой задачей настоящего изобретения является соединение, имеющее следующую общую формулу (I)
где
R представляет собой группу формулы -Ar-X-Ar' (II), где Ar представляет собой ариленовую, гетероариленовую, арильную или гетероарильную группу и Ar' является таким же или другим и независимо от Ar представляет собой арильную или гетероарильную группу или Н; причем указанные Ar и Ar' необязательно замещены одной или более группами, выбранными из
(i) неразветвленного или разветвленного алкила, алкокси, гидроксиалкила, алкоксиалкила, аминоалкила, алкиламино, аминоацила, ациламино или перфторированного алкила, каждый из которых имеет от 1 до 4 атомов углерода в алкильной цепи;
(ii) неразветвленной или разветвленной С2-С6алкенильной или алкинильной группы;
(iii) галогена или цианогруппы (-CN);
Х представляет собой одинарную связь или представляет собой двухвалентный линкер (соединяющую группу), выбранный из неразветвленной или разветвленной С1-С4алкиленовой цепи, -О-, -S-, -S(O)2-, -CO-, -NR'-, -NR'CO- или -CONR'-, где R' представляет собой Н или неразветвленную или разветвленную С1-С4алкильную группу;
R1 представляет собой -ОН или группу -ORa, где Ra выбран из неразветвленных или разветвленных С1-С4алкильных или С2-С4алкенильных групп; или Ra представляет собой группу формулы (III)
-(CH2)p-Z-(CH2)r-W (III)
где р равно нулю или целому числу от 1 до 4; Z представляет собой одинарную связь или двухвалентный линкер, выбранный из -О-, -NR'-, -NR'CO- или -CONR'-, где R' имеет значения, указанные выше; r равно нулю или целому числу от 1 до 4 и W представляет собой фенил или 5- или 6-членный гетероцикл, каждый из которых необязательно замещен одной или более группами, выбранными из -NH2, -COR', -CONHR', -COOR' или -SO2NHR', где R' имеет значения, указанные выше, арилом или гетероарилом, или одной или более вышеуказанными группами от (i) до (ii);
R2 и R3 являются одинаковыми или разными и каждый независимо представляет собой Н, неразветвленную или разветвленную С1-С4алкильную группу, необязательно замещенную гидроксилом или С1-С4алкоксигруппами, или связывающую цинк группу, выбранную из -COOH, -COORb, -CONHOH, -CONHORb, -CONRbOH, -CONHS(O)2Rb, -CONH2, -CONHRb или -Р(О)(ОН)2, где Rb представляет собой неразветвленную или разветвленную алкильную, арилалкильную или гетероарилалкильную группу, имеющую от 1 до 4 атомов углерода в алкильной цепи; или любая из вышеуказанных групп R2 или R3 связывается с R1 так, что образовывалось 5-7-членное гетероциклическое кольцо, содержащее по меньшей мере два соседних гетероатома N-O, необязательно замещенных одной или более оксогруппами (=О);
R4 представляет собой Н или группу, выбранную из -CORc, -COORc, -S(O)2Rc, -CONHRc или -S(O)2NHRc, где Rc представляет собой группу, выбранную из С3-С6циклоалкила, неразветвленного или разветвленного алкила, арила, гетероарила, арилалкила, гетероарилалкила, алкиларила, алкилгетероарила, 5- или 6-членного гетероциклила, алкилгетероциклила или гетероциклоалкила, имеющего от 1 до 4 атомов углерода в алкильной цепи;
R5 представляет собой Н или R4 и R5 вместе с атомом N, к которому они присоединены, образуют необязательно бензоконденсированный 4-6-членный гетероцикл, необязательно замещенный группой Ra, которая имеет значения, указанные выше, и/или одной или более оксогруппами (=О);
n равно 1 или 2;
m равно целому числу от 1 до 6;
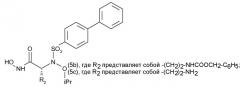
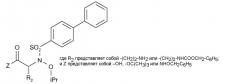
при условии, что, когда R представляет собой бифенил-4-ил, R1 представляет собой изопропокси, m и n, оба, равны 2, R5 представляет собой Н, один из R2 или R3 представляет собой -COOH, -COOC(CH3)3, -CONHOH или -CONHOCH2C6H5 и другой из R2 или R3 представляет собой Н, то R4 не является Н или бензилоксикарбонилом;
и его фармацевтически приемлемые соли.
Соединения формулы (I) могут иметь один или более асимметричных атомов углерода, иначе называемых хиральными атомами углерода, и поэтому могут существовать в форме индивидуальных энантиомеров, рацематов, диастереоизомеров и любой их смеси, предполагается, что все они включены в объем настоящего изобретения.
Как указано выше, в соединениях формулы (I) изобретения R представляет собой группу формулы -Ar-X-Ar' (II), где Ar представляет собой ариленовую или гетероариленовую группу, связанную с -Х-Ar', или когда Х представляет собой одинарную связь и Ar' представляет собой Н, арильную или гетероарильную группу.
В данном контексте, несмотря на тот факт, что в настоящее время предполагается, что арилен и гетероарилен обозначают двухвалентную группу (например, фенилен-С6Н4-), оба термина «арил» и «арилен» (и, таким образом, «гетероарил» и «гетероарилен») используют в описании взаимозаменяемым образом, если не оговорено особо.
В настоящем описании, если не оговорено иначе, авторы изобретения предполагают, что термин «арильная группа» (и, таким образом, «ариленовая группа») означает карбоциклическую ароматическую группу.
Авторы изобретения предполагают, что термин «гетероарил» (и, таким образом, «гетероарилен») означает 5- или 6-членный ароматический гетероцикл с 1-3 гетероатомами или гетероатомными группами, выбранными из N, NH, O или S.
Подходящие примеры арильных или гетероарильных групп, относящихся к Ar и Ar', а также к любой другой арильной или гетероарильной группе, присутствующей в соединениях формулы (I), могут таким образом включать фенил, пирролил, фурил, тиенил, пиразолил, имидазолил, оксазолил, изоксазолил, пиридил, пиримидинил, тиазолил и тому подобное.
Что касается формулы (II), специалисту в данной области ясно, что как Ar, так и Ar', могут быть непосредственно соединены друг с другом, когда Х представляет собой одинарную связь, так что образуется группа -Ar-Ar'-, или в альтернативном случае они могут быть связаны друг с другом через любой подходящий двухвалентный линкер среди линкеров, указанных выше, таким образом образуя, например группы R, соответствующие -Ar-O-Ar'-, Ar-S-Ar', -Ar-CONR'-Ar' и тому подобное.
Помимо этого, при указании на Ar', как соответствующую атому водорода Н, любую из вышеуказанных групп R можно идентифицировать соответственно самим -Ar (когда Х представляет собой связь) или группой -Ar-OH, -Ar-SH, -Ar-CONR'H и тому подобное.
Как ранее указывалось, любая из вышеуказанных групп Ar и/или Ar' может быть необязательно дополнительно замещена в любом свободном положении одной или более группами, указываемыми в пунктах от (i) до (iii).
Среди необязательных заместителей, если не оговорено особо, авторы изобретения предполагают, что неразветвленным или разветвленным алкилом с 1-4 атомами углерода в цепи является любая из С1-С4алкильных групп, таким образом включающая метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил.
Таким же образом, при указании на алкокси авторы изобретения предполагают любые соответствующие алкилоксигруппы, такие как метокси, этокси, н-пропокси, изопропокси и тому подобное.
Как указано выше, алкильные группы могут быть дополнительно замещены гидроксилом (-ОН), амино (-NH2) или даже указанными выше алкоксигруппами (-OAlk), так что образуется гидроксиалкил (НО-Alk-), аминоалкил (H2N-Alk-) или алкоксиалкильные группы (Alk-O-Alk-), соответственно.
По аналогии, термины «алкиламино» авторы изобретения относят к аминогруппе, которая дополнительно замещена любой из вышеуказанных алкильных групп, так что образуются группы Alk-NH-.
При применении термина «ацил», если не оговорено особо, авторы изобретения предполагают любую из групп, обычно идентифицируемых как группы Alk(CO)-, где остаток Alk представляет собой только любую неразветвленную или разветвленную С1-С4алкильную группу.
Подходящие примеры ацильных групп могут таким образом включать ацетил (CH3CO-), пропионил (CH3CH2CO-), бутирил [СН3(СН2)2СО-], изобутирил [(CH3)2CHCO-], валерил [CH3(CH2)3CO-] и тому подобное.
На основании вышеуказанного, аминоацильные группы могут таким образом включать H2NCO-, а также любую из вышеуказанных ацильных групп, у которых алкильная цепь должным образом замещена амино, таких как, например, аминоацетил (H2NCH2CO-), аминопропионил [H2NCH2CH2CO- или CH3CH(NH2)CO-] и тому подобное.
По аналогии, если не оговорено особо, ациламиногруппы могут быть подходящим образом представлены карбоксамидогруппами, в которых любая из вышеуказанных ацильных групп связана с -NH-, такими как, например, ацетамидо (CH3CONH-), пропионамидо (CH3CH2CONH-), бутирамидо [CH3(CH2)2CONH-] и тому подобное.
При применении термина «перфторированный алкил» авторы изобретения предполагают любые из вышеуказанных алкильных групп, у которых все атомы водорода заменены атомами фтора, подобные, например, группам трифторметил, -C2F5, C3F7 или C4F9.
При применении термина «неразветвленная или разветвленная С2-С6алкенильная или алкинильная группа», авторы изобретения предполагают любые из С2-С6углеводородных цепей, содержащих по меньшей мере одну двойную связь или тройную связь, соответственно.
Подходящие примеры алкенильных или алкинильных групп согласно изобретению таким образом включают винил, аллил, пропенил, изопропенил, бутенил, изобутенил, гексенил, этинил, пропинил, бутинил и тому подобное.
Наконец, при применении термина «атом галогена» авторы изобретения предполагают любой из атомов фтора, хлора, брома или йода.
Согласно первому варианту осуществления в соединениях формулы (I) R представляет собой группу формулы (II), где Ar представляет собой необязательно замещенную фениленовую группу, Х представляет собой одинарную связь или двухвалентный линкер, выбранный из -О-, -S- или -NH-, и Ar' представляет собой Н или необязательно замещенную фенильную группу.
Предпочтительными заместителями в этом классе являются неразветвленные или разветвленные С1-С4алкильные группы или алкоксигруппы или атомы галогена.
Еще более предпочтительно, в соединениях формулы (I) R представляет собой группу формулы (II), в которой Ar представляет собой фениленовую группу, Х представляет собой одинарную связь или -О- и Ar' представляет собой Н или фенильную группу, причем фениленовая и фенильная группы необязательно замещены неразветвленными или разветвленными С1-С4алкильными группами или алкоксигруппами или атомами галогена.
Еще более предпочтительными в этом классе являются соединения формулы (I), в которой R представляет собой группу, выбранную из бифенил-4-ила, 4-бромфенила, 4-(4'-метоксифенил)фенила, 4-(4'-этоксифенил)фенила, 4-феноксифенила, 4-(4'-метоксифенокси)фенила и 4-(4'-этоксифенокси)фенила.
Согласно другому аспекту изобретения, в соединениях формулы (I) R1 представляет собой группу -ОН или -ORa, где Ra представляет собой алкил или алкенил, или R1 представляет собой группу формулы (III), где p, Z и r имеют значения, указанные выше, и W представляет собой фенил или 5- или 6-членный гетероцикл, каждый из которых необязательно дополнительно замещен, как указано выше.
В настоящем изобретении, если не оговорено особо, при применении термина «5- или 6-членный гетероцикл» или «гетероциклическая группа» авторы изобретения предполагают любой 5- или 6-членный ароматический или неароматический гетероцикл, потому включающий насыщенные, частично ненасыщенные или даже полностью ненасыщенные кольца с 1-3 гетероатомами или гетероатомными группами, выбранными из N, NH, O или S.
Из вышеуказанного специалисту в данной области ясно, что указанное выше определение гетероцикла или гетероциклической группы включает также любой полностью ненасыщенный гетероцикл, известный также как гетероарильная группа.
Подходящие примеры гетероциклических групп, не включающие гетероциклические группы, уже указанные как находящиеся в пределах определения гетероарила, могут таким образом содержать тетрагидрофуран, пирролин, пирролидин, морфолин, тиоморфолин, пиперидин, пиперазин и тому подобное.
Согласно предпочтительному варианту осуществления изобретения, в соединениях формулы (I) R1 представляет собой группу -ORa, где Ra представляет собой алкильную или алкенильную группу, указываемую выше, или R1 представляет собой группу формулы (III), где р равно 1 или 2, Z представляет собой одинарную связь или двухвалентную группу, выбранную из -О- или -NH-, r равно 0, 1 или 2 и W представляет собой необязательно замещенную фенильную или гетероциклическую группу, которая имеет указанные выше значения.
Еще более предпочтительными в данном классе являются соединения формулы (I), в которой R1 выбран из изопропокси, бензилокси, 4-фенилбензилокси, аллилокси, 2-[2-(пиперазинил-1-ил)этокси]этокси или 2-[2-(4-(этилкарбонил)пиперазинил-1-ил)этокси]этокси.
Что касается R2 и R3 в формуле (I), они независимо представляют собой Н, необязательно замещенную алкильную группу или связывающую цинк группу среди групп, указанных ранее.
Альтернативно, R2 или R3 может быть связан с R1 так, чтобы образовывать 5-7-членное гетероциклическое кольцо, содержащее по меньшей мере два соседних гетероатома N-O, причем, например, N-атом связан с S в формуле (I) и атом О является частью самого R1.
В качестве неограничивающего примера подходящие соединения формулы (I), в которой один из R2 или R3 (например, R2) связан с R1 так, чтобы образовывать вышеуказанные гетероциклические структуры, могут таким образом содержать
где вышеуказанные соседние гетероатомы N-O представлены отчетливо.
Согласно предпочтительному варианту осуществления, R2 и R3, каждый независимо, выбраны из Н, неразветвленного или разветвленного С1-С4алкила, -СООН, -COORb, -CONHOH или -CONHORb, где Rb представляет собой неразветвленную или разветвленную алкильную, арилалкильную или гетероарилалкильную группу, имеющую от 1 до 4 атомов углерода в алкильной цепи.
Еще более предпочтительно, в этом классе соединений R2 и R3 представляют собой, оба, атомы Н или один из них представляют собой Н и другой из R2 или R3 представляет собой -СООН или -CONHOH.
Что касается значений R4, указанная группа может представлять собой атом водорода Н или карбонил, карбоксил, сульфонил, карбоксамидо- или сульфонамидогруппу, дополнительно превращенную в производное посредством вышеуказанных групп Rc.
Что касается значений Rc, если не указано особо, при применении термина «С3-С6циклоалкил» авторы изобретения предполагают любое 3-6-членное циклоалифатическое кольцо, такое как циклопропил, циклобутил, циклопентил и циклогексил.
Из указанных выше определений значений алкила, арила, гетероарила и гетероцикла (или гетероциклила) любая группа с комбинированным названием, такая как арилалкил, алкиларил, гетероарилалкил, алкилгетероарил, алкилгетероциклил или гетероциклилалкил, должна быть понятна специалисту в данной области.
Просто в качестве примера, если не оговорено особо, при применении термина «алкиларил» авторы изобретения предполагают любую арильную группу, дополнительно замещенную алкилом, например, п-этилфенил (пС2Н5-C6H4-); термин «арилалкил» авторы изобретения вместо этого относят к алкильной группе, дополнительно замещенной арилом, например, 2-фенилэтил (С6Н5-СН2-СН2-) и тому подобное.
Из всего указанного выше специалисту в данной области должно быть понятно, что аналогичное рассмотрение можно применять для гетероарилалкильных, алкилгетероарильных, гетероциклоалкильных или алкилгетероциклических групп.
Что касается R5 в формуле (I), он представляет собой Н, или, альтернативно, R4 и R5 вместе с атомом N, с которым они связаны, образуют необязательно бензоконденсированный 4-6-членный гетероцикл, который имеет указанные выше значения.
Подходящие примеры указанных гетероциклов, например, замещенных Ra и оксогруппами, могут таким образом включать
Согласно дополнительному предпочтительному варианту осуществления изобретения, R4 выбран из -CORc, -COORc или -S(O)2Rc, где Rc представляет собой арильную, неразветвленную или разветвленную алкильную или арилалкильную группу, имеющую от 1 до 4 атомов углерода в алкильной цепи, и R5 представляет собой Н.
Еще более предпочтительными в данном классе являются соединения формулы (I), в которой R4 выбран из ацетила, бензоила, фенацетила, 4-фенилбутаноила, бензилоксикарбонила, метансульфонила, фенилсульфонила или бензилсульфонила и R5 представляет собой Н.
Согласно еще одному другому варианту осуществления изобретения, R4 и R5 вместе с атомом N, к которому они присоединены, образуют N-фталимидогруппу.
Наконец, согласно дополнительному предпочтительному варианту осуществления изобретения, в соединениях формулы (I) n и m, оба, равны 2.
Как указывалось ранее, соединения формулы (I) изобретения могут также присутствовать в форме фармацевтически приемлемой соли.
Термин “фармацевтически приемлемая соль”, применяемый в настоящем описании, относится к производным соединений изобретения, у которых исходное соединение подходящим образом модифицировано превращением любой из свободных кислотных или основных групп, если она присутствует, в соответствующую аддитивную соль с любым основанием или кислотой, которая обычно предполагается как фармацевтически приемлемая.
Не говоря о том, что соответствующие соли соединений формулы (I) изобретения являются нетоксичными, они характеризуются также высокой стабильностью, включающей физиологическую стабильность при применении и введении.
Подходящие примеры упомянутых солей могут таким образом включать минеральные или органические кислотно-аддитивные соли основных остатков, таких как аминогруппы, а также минеральные или органические основно-аддитивные соли кислотных остатков, таких как карбоксильные, фосфоновые или серные группы.
Предпочтительные катионы неорганических оснований, которые можно подходящим образом применять для получения солей в изобретении, содержат ионы щелочных или щелочноземельных металлов, таких как калий, натрий, кальций или магний. Предпочтительные катионы органических оснований включают, среди прочих, катионы первичных, вторичных и третичных аминов, таких как этаноламин, диэтаноламин, морфолин, глюкамин, N-метилглюкамин, N,N-диметилглюкамин.
Предпочтительные анионы неорганических кислот, которые можно подходящим образом применять для получения солей соединений изобретения, включают ионы галогенов, такие как хлориды, бромиды, иодиды или другие подходящие ионы, такие как сульфаты.
Предпочтительные анионы органических кислот включают анионы, обычно применяемые в фармацевтических технологиях для получения солей основных веществ, таких как, например, ацетат, трифторацетат, сукцинат, цитрат, фумарат, малеат или оксалат.
Предпочтительные аминокислоты, которые можно подходящим образом применять для получения солей соединений изобретения, могут включать также, например, таурин, глицин, лизин, аргинин, орнитин, аспарагиновую и глутаминовую кислоты.
Определенные примеры соединений формулы (I) изобретения вместе со способом их получения описаны в нижеследующем экспериментальном разделе. Способ получения соединений изобретения можно проводить согласно общепринятым способам, хорошо известным специалистам в области методик синтетической органической химии.
Следовательно, дополнительной задачей изобретения является способ получения соединений формулы (I), который включает
а) реакцию соединения формулы (IV) с соединением формулы (V)
где R, R1, R2, R3, R4, R5, n и m имеют значения, указанные выше, так чтобы получить соединение формулы (I) изобретения, и необязательно
b) превращение соединения формулы (I), полученного на стадии (а), в другое соединение формулы (I) и/или в его фармацевтически приемлемую соль.
Указанный выше способ является особенно подходящим, когда он является восприимчивым к модуляции должным образом посредством любого подходящего варианта, так чтобы получить любые требуемые соединения формулы (I).
На стадии (а) способа реакцию между соединениями формулы (IV) и (V) проводят согласно общепринятым способам для образования сульфонамидо- или сульфинамидогрупп с n, равным 2 или 1, соответственно.
Реакцию обычно проводят в известных рабочих условиях конденсации Мицунобу, в присутствии подходящих растворителей, включающих, среди других растворителей, тетрагидрофуран, дихлорметан, ацетонитрил, N-метилпирролидон, бензол, толуол, м-ксилол и их смеси.
В этом отношении указанную выше реакцию можно проводить в присутствии подходящего агента конденсации, либо как такового, либо подходящим образом нанесенного на полимерные смолы, включающего, например, диэтилазодикарбоксилат (DEAD), диизопропилазодикарбоксилат (DIAD), 1,1'-азодикарбонилдипиперидин (ADDP), N,N,N',N'-тетраметилазодикарбоксамид (TMAD), трифенилфосфин (PPh3), трибутилфосфин (PBu3) и тому подобное.
Из всего указанного выше специалисту в данной области должно быть ясно, что на стадии (а) способа любая из групп R, R1, R2, R3, R4 и R5, в дальнейшем коротко обозначаемых группами “R”, может присутствовать как таковая или же может присутствовать в любой нужным образом защищенной форме.
Более конкретно, функциональные группы, которые присутствуют в любом из соединений формулы (IV) или (V) и которые могут вызывать нежелательные побочные реакции и образование побочных продуктов, необходимо нужным образом защитить перед проведением реакции конденсации. Кроме того, после завершения упомянутых реакций может следовать последующее удаление тех же защитных групп.
В настоящем изобретении, если не оговорено особо, термин “защитная группа” означает защитную группу, адаптированную для защиты функциональной группы, с которой она