Реагенты и способы для бета-кетоамидного синтеза синтетического предшественника иммунологического адъюванта е6020
Иллюстрации
Показать всеИзобретение относится к соединениям формулы , которые могут использоваться в способе синтеза предшественников иммунологического адъюванта Е6020. В формуле (3) R1, R2, R3 представляют собой C5-C15 алкильную группу, C5-C15 алкенильную группу или C5-C15 алкинильную группу. Кроме того, изобретение относится к соединениям формулы (4), которые также могут использоваться в синтезе предшественников указанного адъюванта. В формуле R4 представляет собой C1-С6 алкильную группу, С3-С5 алкенильную группу, С3-С5 алкинильную группу, циклоалкильную группу, этильную группу, замещенную в положении 2, галогенэтильную группу, арильную группу, бензильную группу или силильную группу; R5, R6 независимо представляют собой C1-С6 алкильную группу, С3-С6 алкенильную группу или С3-С6 алкинильную группу; или же R5 и R6 совместно с атомом азота, к которому они присоединены, образуют 5- или 6-членный гетероцикл. Изобретение относится также к способам синтеза соединений формул (3) и (4) и к кристаллическим формам их конкретных представителей. 7 н. и 27 з.п. ф-лы, 8 ил., 2 табл., 6 пр.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка согласно 35 U.S.C. § 119 претендует на приоритет предварительной заявки на патент США №61/014648, поданной 18 декабря 2007, которая включена в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способу синтеза предшественников иммунологического адъюванта E6020 через β-кетоамидный интермедиат. Кроме того, настоящее изобретение относится к промежуточным соединениям в указанном способе синтеза и, для двух соединений, к их кристаллическим формам.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Было доказано, что применение вакцин является успешным способом профилактики инфекционных заболеваний. Как правило, применение вакцин является экономически эффективным и не вызывает устойчивости к антибиотикам у целевого патогена или не влияет на нормальную микрофлору, присутствующую в организме-хозяине. Во многих случаях, например, при стимулировании противовирусного иммунитета, вакцины могут предотвратить заболевания, для которых отсутствуют реальные способы лечения или облегчения.
Вакцины действуют за счет инициирования реакции иммунной системы на тот или иной агент или антиген, как правило, инфекционный микроорганизм или его часть, которые вводятся в организм в не инфекционной или не патогенной форме. Если иммунная система однажды была «обучена» или настроена на микроорганизм, последующий контакт иммунной системы с этим микроорганизмом в форме инфекционного патогена приводит к быстрому и надежному иммунному ответу, который разрушит патоген, прежде чем он сможет размножится и инфицировать в организме-хозяине достаточное для проявления симптомов заболевания количество клеток. Агент или антиген, применяемый для обучения иммунной системы, может представлять собой целый микроорганизм с меньшей инфекционностью, известный как ослабленный микроорганизм, или, в некоторых случаях, компоненты этого микроорганизма, например, углеводы, белки или пептиды, представляющие собой различные структурные компоненты этого микроорганизма.
Во многих случаях необходимо улучшить иммунную реакцию на антигены, присутствующие в вакцине, чтобы в достаточной степени стимулировать иммунную систему с целью сделать вакцину эффективной, т.е. вызвать появление иммунитета. Многие антигены, представляющие собой белки и, в наибольшей степени, пептиды и углеводы, введенные сами по себе, не вызывают достаточного для появления иммунитета образования антител. Эти антигены необходимо представить иммунной системе таким образом, чтобы они были распознаны, как инородные объекты и вызвали иммунный ответ. С этой целью были разработаны добавки (адъюванты), которые стимулируют, усиливают и/или направляют иммунный ответ на выбранный антиген.
Лучший из известных адъювантов - полный адъювант Фрейнда - состоит из смеси микобактерий в эмульсии масло/вода. Адъювант Фрейнда действует по двум направлениям: во-первых, за счет усиления клеточно- и гуморально-опосредованного иммунитета и, во-вторых, путем блокирования быстрого распространения провоцирующего антигена («эффект депо»). Однако, вследствие часто встречающихся токсических физиологических и иммунологических реакций на этот препарат, адъювант Фрейнда не следует применять к людям.
Другой молекулой, которая, как было показано, обладает иммуностимулирующей или адъювантной активностью является эндотоксин, известный также как липополисахарид (LPS). LPS стимулирует иммунную систему путем инициирования «природной» иммунной реакции, т.е. реакции, которая способствует тому, чтобы организм распознал эндотоксин (и проникающую в организм бактерию, компонентом которой он является), причем нет необходимости в том, чтобы организм ранее подвергался его действию. В то время как LPS является слишком токсичным, чтобы реально применяться в качестве адъюванта, молекулы, структурно родственные этому эндотоксину, например, монофосфориллипид A (“MPL”), проходили тестирование в качестве адъювантов в клинических исследованиях. Было показано, что как LPS, так и MPL являются агонистами человеческого toll-подобного рецептора 4 (TLR-4). Тем не менее, в настоящее время единственным адъювантом, одобренным FDA для применения в отношении человека, является персульфат алюминия, именуемый также Alum, который используют для «депонирования» антигенов путем их осаждения. Кроме того, Alum стимулирует иммунный ответ на антигены.
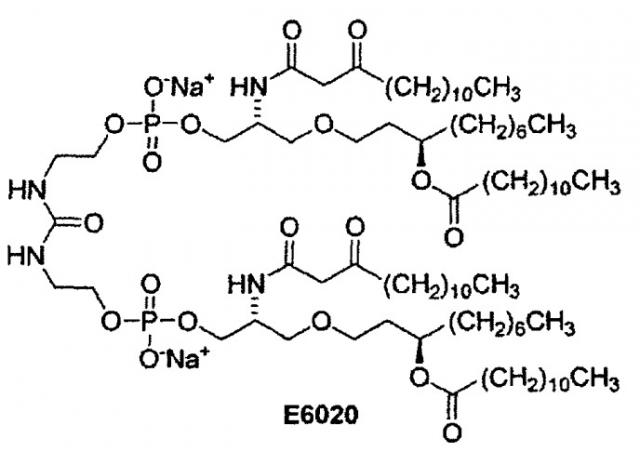
E6020 является мощным агонистом рецептора TLR-4 и, следовательно, применим в качестве иммунологического адъюванта, вводимого совместно с антигенами, например, вакцинами против бактериальных и вирусных заболеваний. Например, E6020 может применяться в комбинации с любым подходящим антигеном или компонентом вакцины, например, антигенным агентом, выбранным из группы, состоящей из антигенов из патогенных и не патогенных микроорганизмов, вирусов и грибков. В качестве еще одного примера, E6020 может применяться в комбинации с белками, пептидами, антигенами и вакцинами, которые проявляют фармакологическую активность в отношении таких заболеваний и состояний, как натуральная оспа, желтая лихорадка, рак, собачья чума, холера, птичья оспа, скарлатина, дифтерия, столбняк, коклюш, грипп, бешенство, свинка, корь, заболевания ступней ног и рта, и полиомиелит, а также вирусных заболеваний, таких как герпес и родственные ему заболевания, а также гепатит и родственные ему заболевания. При применении в качестве вакцины, E6020 и антиген присутствуют в количествах, эффективных для стимулирования иммунного ответа, в случае введения в организм животного-хозяина, эмбрион или яйцеклетку, которые вакцинируют указанным составом.
Благодаря способности стимулировать более надежный иммунный ответ по сравнению с антигеном в чистом виде, такие соединения как E6020 являются важными в иммунологическом отношении. Существует потребность в разработке способов синтеза, предназначенных для получения таких соединений, как E6020 и их синтетических предшественников, которые могут вводиться вместе с антигенами в составе вакцин. Новые способы синтеза включают новые соединения в качестве интермедиатов, и новые реакции в качестве стадий способа. В изобретении разработан улучшенный способ синтеза интермедиатов и предшественников агонистов рецептора TLR-4, например, E6020.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым способам синтеза, интермедиатам и синтетическим предшественникам, ведущим к соединению 26, которое является предшественником E6020, через β-кетоамидный интермедиат, а именно, соединение 22. Способы синтеза по настоящему изобретению начинаются с соединения 14, которое служит для получения соединения 22, которое затем вводят во взаимодействие с соединением 25 для получения соединения 26 - непосредственного предшественника иммунологического адъюванта E6020. Соединение 22 и соединение 25, а также их кристаллические формы представляют собой отдельные варианты осуществления настоящего изобретения.
В другом варианте осуществления изобретение относится к соединению формулы (3):
где R1,R2 и R3 в каждом случае независимо представляют собой C5-C15 алкильную группу, C5-C15 алкенильную группу или C5-C15 алкинильную группу. Кроме того изобретение относится к способу получения соединений формулы (3). β-кетоамидный интермедиат, т.е. соединение 22, принадлежит к числу соединений формулы (3).
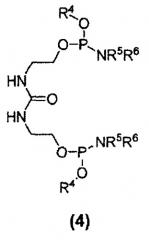
Другим вариантом осуществления изобретения является соединение формулы (4):
где R4 в каждом случае независимо представляет собой защитную группу, например, C1-C6 алкильную группу, C3-C5 алкенильную группу, арильную группу, бензильную группу или другую подходящую защитную группу; и каждый из заместителей R5 и R6 в каждом случае независимо представляет собой C1-C6 алкильную группу или же эти заместители, совместно с атомом азота, к которому они присоединены, образуют 5- или 6-членный гетероцикл. Кроме того, настоящее изобретение относится к способу получения соединений формулы (4). Соединение 25 является соединением формулы (4).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 в общих чертах изображен β-кетоамидный синтез соединения E6020 по настоящему изобретению.
На фиг.2 показана картина дифракции рентгеновских лучей на кристаллическом порошке соединения 22.
На фиг.3 изображена DSC-термограмма кристаллического соединения 22.
На фиг.4 показана картина дифракции рентгеновских лучей на кристаллическом порошке соединения 25.
На фиг.5 показана DSC-термограмма кристаллического соединения 25.
На фиг.6 показано ORTEP-изображение кристаллического соединения 25, на котором отмечены различные атомы.
На фиг.7 показана диаграмма кристаллической упаковки кристаллического соединения 25 вдоль оси c.
На фиг.8 показана смоделированная картина дифракции рентгеновских лучей на порошке для кристаллического соединения 25.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
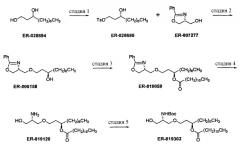
В заявке на патент США №11/477936 “Compounds for preparing Immunological Adjuvant”, поданной 30 июня 2006 (опубликована 12 апреля 2007 под номером US 2007-0082875 A1) описан синтез соединения E6020, и эта заявка включена в настоящую заявку посредством ссылки. Описанный синтез проходит через стадию получения уреидо димера эфира фосфорной кислоты, а именно соединения 19. На схемах 1-3 заявки US 2007-0082875 A1 показан синтез E6020 через соединение 19. Исходными веществами, показанными на схеме 1, являются ER-028694 (1,3-декандиол, коммерчески доступный от продавца Mitsui & Co. (US), New York, NY; производитель Nippon Fine Chemicals) и ER-807277 (4-оксазолметанол, 4,5-дигидро-2-фенил-,(4R)-пропандиол, коммерчески доступный от Catalytica Pharmaceuticals, Boonton, NJ). Непосредственным предшественником соединения E6020 является соединение 26.
Настоящее изобретение относится к новому способу синтеза, интермедиатам и предшественникам, ведущим к соединению 26, являющемуся предшественником соединения E6020, через β-кетоамидный интермедиат, т.е. соединение 22. Синтез по настоящему изобретению начинается с соединения 14, которое используют для получения соединения 22, которое затем вводят в реакцию с соединением 25 с получением соединения 26, т.е. синтетического предшественника иммунологического адъюванта E6020. Эти стадии синтеза по настоящему изобретению, т.е. получение β-кетоамидного интермедиата (3), с последующей конденсацией β-кетоамида (3) и дифосфорамидита мочевины (4), показаны на схеме 4 и затем подробно описаны. Соединения 22 и 25 и их кристаллические формы являются отдельными вариантами осуществления настоящего изобретения.
Получение кристаллической формы соединения, например, соединения 22 или 25 является чрезвычайно полезным при разработке лекарственных средств. Твердые формы соединения (кристаллические или аморфные) могут иметь различные физические и химические свойства, например, растворимость, стабильность или различаться возможностью воспроизведения. Эти свойства часто делают возможным оптимизацию производственных процессов, особенно, когда образуется кристаллический интермедиат. В многостадийном синтезе, например, синтезе, описанном в настоящем изобретении, получают интермедиаты, причем нежелательные побочные продукты или загрязнения могут переходить в продукт из более ранних стадий. В синтез вводят частые стадии фильтрования, разделения и/или очистки для удаления нежелательных побочных продуктов или загрязнений. Введение этих стадий не только может увеличить затраты на производство, но также способно уменьшить итоговый выход продукта синтеза. Присутствие в многостадийном синтезе кристаллического интермедиата дает возможность решить эти проблемы. Кристаллический интермедиат обеспечивает определенные преимущества - интермедиат высокой степени чистоты может уменьшить необходимость очистки на других стадиях и снизить себестоимость способа синтеза.
Схема 1
Стадия 1: TsCl, Et3N, ТГФ.
Стадия 2: NaHMDS, ТГФ, хроматография, кристаллизация.
Стадия 3: лауриновая кислота, EDC, DMAP, CH2Cl2, хроматография.
Стадия 4: H2, 10% Pd/C, хроматография.
Стадия 5: Boc2O, ТГФ, хроматография.
Схема 2
Стадия 6: a. диизопропиламин; Py·TFA, ((i-Pr)2N)2P(OAllyl), CH2Cl2.
b. HOAc, Py·TFA, FmocNH(CH2)2OH
c. H2O2, хроматография.
Стадия 7: диметиламин, ТГФ.
Стадия 8: 20% фосген в толуоле, насыщенный водный NaHCO3,
хроматография
Схема 3
Стадия 9: TFA, CH2Cl2.
Стадия 10: 3-оксотетрадекановая кислота, EDC, ДМФА, хроматография.
Стадия 11: Pd(PPh3)4, PPh3, PhSiH3, ТГФ, хроматография.
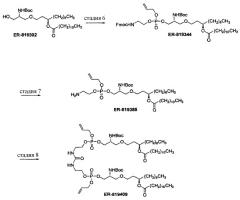
Схема 4
Стадия 1: H2, Pd/C, IPA.
Стадия 2: 3-оксотетрадекановая кислота, CDI, ACN, кристаллизация.
Стадия 3: Py·TFA, ACN, кристаллизация.
Стадия 4: ACN, гептан, HOAc, H2O2, Na2S2O3, хроматография.
Получение β-кетоамидоспиртового интермедиата (3)
Синтез соединения 26 и аналогичных соединений включает на первом этапе взаимодействие α-гидроксиамина формулы (1) с соединением формулы (2) с получением β-кетоамида формулы (3) в подходящих условиях проведения реакции. Реакция показана на схеме 5.
Схема 5
а
Получение соединения (3) согласно схеме 5 может быть осуществлено с применением различных способов. Группы R1, R2 и R3 соответствуют данным ниже определениям. Поскольку заместители R1, R2 и R3 могут меняться независимо друг от друга, соединение (3) может включать симметричные или асимметричные группы, обозначенные как R1, R2 и R3. В соединении (2) X представляет собой подходящую уходящую группу, как, например, OH, Cl, F, имидазолидил, карбонат и сложноэфирный фрагмент. Предпочтительные уходящие группы включают OH, Cl, F, имидазолидил, триметилацетокси, этилкарбонат, метилкарбонат, изобутилкарбонат или группу формулы Z:
где группа R7 и группа R3 в формуле (2) являются одинаковыми, так что соединение формулы (2) представляет собой симметричный ангидрид бета-кетоэфира. Такие ангидриды могут быть получены путем конденсации двух идентичных молекул бета-кетокислоты.
В одном из способов получения, соединение (3) могло бы быть получено путем конденсации соединения (1) с соединением (2), в котором X представляет собой имидазолид. Последнее соединение получают при активации соединения (2), в котором X представляет собой OH (карбоновой кислоты) действием реагента CDI (карбонилдиимидазола) в полярном апротонном растворителе, например, ацетонитриле.
Во втором способе получении, соединение 3 могло бы также быть получено при конденсации соединения (1) с соединением (2), в котором X представляет собой OH (карбоновой кислотой) в присутствии реагента, способствующего образованию амидной связи, например, HBTU (гексафторфосфата O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония) или другого сшивающего реагента того же семейства и третичного амина (например, основания Хюнига, N,N-диизопропилэтиламина), в таком растворителе, как ДМФА или CH2Cl2. Кроме того, для активации соединения (2), в котором X представляет собой OH (карбоновой кислоты), могут применяться карбодимидные реагенты, например, EDC (гидрохлорид N-(3-диметиламинопропил)-N-этил карбодиимида).
Третий способ получения соединения (3) представляет собой конденсацию соединения (1) с соединением (2), в котором X означает F (ацилфторидом), в присутствии третичного амина (например, основания Хюнига) в таком растворителе, как CH2Cl2. Соединение (2), в котором X означает F (ацилфторид) может быть получено при активации соединения (2), в котором X означает OH (карбоновой кислоты) действием реагента TFFH (гексафторфосфата фтор-N,N,N',N'-тетраметилформамидиния) в таком растворителе, как CH2Cl2.
Соединение (3) могло бы быть получено также согласно четвертому способу синтеза, путем конденсации соединения (1) с соединением (2), в котором X представляет собой Cl (ацилхлоридом) в присутствии третичного амина (например, основания Хюнига) в таком растворителе, как CH2Cl2. Соединение (2), в котором X представляет собой Cl (ацилхлорид) может быть получено при активации соединения (2), в котором X означает OH (карбоновой кислоты) действием оксалилхлорида в таком растворителе, как CH2Cl2.
Пятый способ позволяет получить соединение (3) путем конденсации соединения (1) с соединением (2) в форме ангидрида карбоновой кислоты, в котором X представляет собой карбонат, в присутствии третичного амина (например, основания Хюнига) в таком растворителе, как CH2Cl2. Указанный ангидрид получают путем активации соединения (2), в котором X представляет собой OH (карбоновой кислоты) этилхлорформиатом в присутствии третичного амина (например, триэтиламина) в таком растворителе, как CH2Cl2.
Согласно шестому способу, соединение (3) можно получить конденсацией соединения (1) со смешанным ангидридом (2), в котором X означает сложноэфирную группу, в присутствии третичного амина (например, основания Хюнига) в таком растворителе, как CH2Cl2. Указанный смешанный ангидрид получают путем активации соединения (2), в котором X означает OH (карбоновой кислоты) пивалоилхлоридом в присутствии третичного амина (например, триэтиламина) в таком растворителе, как CH2Cl2.
Соединение (3) также можно было бы получить по седьмому способу, в котором соединение (2), где X означает OH (карбоновую кислоту), во-первых, превращают в симметричный ангидрид действием оксалилхлорида и третичного амина (например, триэтиламина) в таком растворителе, как CH2Cl2. Полученный ангидрид конденсируют с соединением (1) в присутствии третичного основания (например, триэтиламина) в таком растворителе, как CH2Cl2.
Как показано ниже в примере 1, соединение формулы (1) может быть получено гидрированием соединения формулы Y:
где заместители R1 и R2 соответствуют данным выше определениям. Гидрирование можно осуществлять в любом подходящем растворителе, например, этаноле, изопропаноле и других растворителях, известных в технике, но предпочтительно проводить его в изопропаноле.
В формулах (1), (2) и (3) каждый из заместителей R1, R2 и R3 независимо в каждом случае может представлять собой C5-C15 алкильную группу, C5-C15 алкенильную группу или C5-C15 алкинильную группу. Эта алкильная группа, алкенильная группа и алкинильная группа могут быть замещенными или незамещенными, линейными или разветвленными и предпочтительно имеют линейную цепь. В предпочтительном варианте осуществления R1 представляет собой C5-C12 алкильную группу, C5-C12 алкенильную группу или C5-C12 алкинильную группу и, наиболее предпочтительно, C5-C9 алкильную группу, C5-C9 алкенильную группу или C5-C9 алкинильную группу, в то время как каждый из заместителей R2 и R3 независимо в каждом случае представляет собой C7-C14 алкильную группу или C7-C14 алкенильную группу и более предпочтительно C9-C13 алкильную группу или C9-C13 алкенильную группу. Предпочтительно R1 является C7 алкильной группой, наиболее предпочтительно незамещенной н-гептильной группой, и обе группы R2 и R3 являются C11 алкильными группами, наиболее предпочтительно незамещенной н-ундецильными группами.
Алкильные, алкенильные и алкинильные группы, упомянутые в качестве конкретных вариантов осуществления различных групп R1,R2 и R3, и рассмотренные выше с точки зрения настоящего изобретения, могут быть замещенными или незамещенными. Примеры заместителей включают, не ограничиваясь этим, галогены (например, F, Cl, Br и I); C1-C6 алкоксигруппы (например, -OCH3, -OCH2CH3, -OCH(CH3)2 и т.п.); C1-C6 галогеналкильные группы (например, -CF3, -CH2CF3, -CHCl2 и т.п.); C1-C6 алкилтиогруппы; амиды; -NO2; и -CN. Если не указано иное, алкильные, алкенильные и алкинильные группы могут иметь линейные или разветвленные цепи, причем линейные цепи являются в основном предпочтительными.
β-кетоамидоспирты формулы (3) являются новыми соединениями и они применимы, в том числе, как интермедиаты при получении таких соединений, как E6020. Соединения формулы (3) являются отдельным вариантом осуществления настоящего изобретения. β-кетоамидоспирты, имеющие стереохимию формулы (3a) являются особенно предпочтительными.
В случае синтеза соединения E6020, β-кетоамидоспирт представляет собой соединение 22. Соединение 22 и его кристаллическая форма также являются отдельными вариантами осуществления настоящего изобретения. Синтез соединения 22, исходя из соединения 14, описан ниже в примере 1, и получение характеристик твердой кристаллической формы соединения 22 описано ниже в примере 2.
соединение 22
Получение дифосфорамидита мочевины (4)
Дифосфорамидит мочевины формулы (4) представляет собой другое новое промежуточное соединение в β-кетоамидоспиртовом способе синтеза соединения E6020. Следовательно, соединения формулы (4) являются отдельным вариантом осуществления настоящего изобретения. Дифосфорамидиты мочевины формулы (4) могут быть получены взаимодействием 1,3-бис(2-гидроксиэтил)мочевины с двумя молекулами фосфордиамидита формулы (7), как показано на схеме 6, где заместители R4, R5 и R6 соответствуют данному ниже описанию.
Схема 6
В некоторых вариантах осуществления взаимодействие 1,3-бис(2-гидроксиэтил)мочевины с фосфордиамидитом осуществляют взаимодействием бис-гидроксисоединения с подходящим активирующим агентом, например, известным специалисту в данной области техники, и затем добавляют фосфордиамидит к полученной реакционной смеси. В некоторых вариантах осуществления упомянутый активирующий агент выбран из группы, состоящей из (1H)-тетразола и трифторацетата пиридиния. В некоторых вариантах осуществления активирующий агент представляет собой трифторацетат пиридиния. В некоторых вариантах осуществления взаимодействие по схеме 6 проводят в растворителе, выбранном из группы, состоящей из ацетонитрила, дихлорметана, дихлорэтана и трет-бутилметилового эфира. В некоторых вариантах осуществления для проведения реакции по схеме 6 в качестве растворителя применяют ацетонитрил.
Конденсация β-кетоамидоспирта (3) с дифосфорамидитом мочевины (4)
Как показано выше на схеме 4, синтез соединения 26 включает реакцию конденсации β-кетоамидоспирта формулы (3) с дифосфорамидитом мочевины формулы (4) с образованием фосфита β-кетоамидомочевины формулы (5), который может быть окислен до фосфата β-кетоамидомочевины формулы (6). Это показано ниже на схеме 7.
Схема 7
В формулах (4), (5) и (6) заместители R1, R2 и R3 соответствуют приведенному выше описанию, включая предпочтительные варианты их осуществления, и независимы друг от друга. В каждом случае заместители R1, R2 и R3 могут быть одинаковыми или различными. Другими словами, соединение формулы (6) может включать одинаковые или различные алкильные, алкенильные и/или алкинильные группы, в каждом из положений, где находятся заместители R1, R2 и R3. Каждая из групп R4 может независимо являться защитной группой, включая, но не ограничиваясь этим, такие группы, как: алкильная группа или замещенная алкильная группа, например, метил, этил, изопропил, трет-бутил и т.п., предпочтительно C1-C6 алкильная группа; алкенильная группа или замещенная алкенильная группа, например, аллил, 2-метилпропенил, бутенил и т.п., предпочтительно C3-C5 алкенильная группа; алкинильная группа, предпочтительно C3-C5 алкинильная группа; циклоалкильная группа, например, циклогексил; этильная группа, замещенная в положение 2, например, 2-цианоэтил, 2-циано-1,1-диметилэтил, 2-(триметилсилил)этил и т.п.; галогенэтильная группа, например, 2,2,2-трихлорэтил, 2,2,2-трихлор-1,1-диметилэтил, 2,2,2-трибромэтил и т.п.; бензильная или замещенная бензильная группа, например, бензил, 4-нитробензил, 4-хлорбензил и т.п.; арильная или замещенная арильная группа, например, фенил, 4-нитрофенил, 4-хлорфенил, 2-хлорфенил, 2-метилфенил, 2,6-диметилфенил, 2-бромфенил и т.п.; и силильная группа, например, триметилсилил и т.п. Особенно предпочтительными защитными группами, обозначенными символом R4, являются метил, этил, трет-бутил, аллил, 2-метилпропенил, бутенил, 2-цианоэтил (NCCH2CH2-), 2-(триметилсилил)этил ((CH3)3SiCH2CH2-) и 2,2,2-трихлорэтил (Cl3CCH2-). Как и для заместителей R1, R2 и R3, в каждом случае заместители R4 могут отличаться друг от друга, в рамках определения заместителя R4.
Заместители R5 и R6 в каждом случае независимо представляют собой C1-C6 алкильную группу, С3-С6 алкенильную группу или C3-C6 алкинильную группу, где указанные алкильная, алкенильная и алкинильная группы могут являться замещенными или незамещенными, или же совместно с атомом азота, к которому они присоединены, заместители R5 и R6 могут образовывать 5- или 6-членный гетероцикл. Этот гетероцикл может включать дополнительные гетероатомы, например, N, O и/или S; может быть насыщенным или ненасыщенным, а также может быть замещенным или незамещенным. Примеры заместителей включают, не ограничиваясь перечисленными, галогены (например F, Cl, Br и I); С1-С6 алкоксигруппы (например, -OCH3, -OCH2CH3, -OCH(CH3)2 и т.п.); С1-С6 галогеналкильные группы (например, -CF3, -CH2CF3, -CHCl2 и т.п.); С1-С6 алкилтиогруппы; группу -NO2; и группу -CN. Подходящие гетероциклические группы включают, но не ограничиваются этим, пиперидил, морфолинил, тиоморфолинил, пирролидил и т.п. Алкильные, алкенильные и алкинильные группы, обозначаемые символами R4, R5 и R6, могут быть замещенными или незамещенными, линейными или разветвленными. Примеры заместителей включают, не ограничиваясь перечисленными галогены (например F, Cl, Br и I); С1-С6 алкоксигруппы (например, -OCH3, -OCH2CH3, -OCH(CH3)2 и т.п.); С1-С6 галогеналкильные группы (например, -CF3, -CH2CF3, -CHCl2 и т.п.); С1-С6 алкилтиогруппы; группу -NO2; и группу -CN. В предпочтительном варианте осуществления заместитель R4 представляет собой C3-C5 алкенильную группу, и каждый из заместителей R5 и R6 независимо представляют собой разветвленную C1-C6 алкильную группу. Предпочтительно, R4 является аллильной группой, и R5 и R6 являются изопропильными группами.
В некоторых вариантах осуществления соединение формулы (3) вводят в реакцию с соединением формулы (4), добавляя растворитель к смеси соединения формулы (3) и соединения формулы (4), осуществляя перемешивание до полного растворения всех твердых веществ и добавляя к полученной смеси уксусную кислоту. В некоторых вариантах осуществления растворитель является безводным и может представлять собой смесь сорастворителей. В некоторых вариантах осуществления эта смесь сорастворителей включает ацетонитрил и углеводородный растворитель и в предпочтительном варианте осуществления растворитель может представлять собой, например, смесь безводного ацетонитрила и безводного гептана. В некоторых вариантах осуществления смесь сорастворителей включает гептан и ацетонитрил. В некоторых вариантах осуществления масса гептана в смеси сорастворителей в 4-6 раз превышает массу соединения формулы (3). В некоторых вариантах осуществления масса гептана в смеси сорастворителей в 4,5-5,5 раз превышает массу соединения формулы (3). В некоторых вариантах осуществления масса ацетонитрила в смеси сорастворителей в 1-2 раза превышает массу соединения формулы (3). В некоторых вариантах осуществления масса ацетонитрила в смеси сорастворителей в 1,2-1,5 раза превышает массу соединения формулы (3). В некоторых вариантах осуществления масса использованной в реакции уксусной кислоты составляет от 1 до 2 мольных эквивалентов количества соединения формулы (3). В некоторых вариантах осуществления масса использованной в реакции уксусной кислоты составляет от 1 до 2 мольных эквивалентов количества соединения формулы (3). В некоторых вариантах осуществления количество использованной в реакции уксусной кислоты составляет от 1,2 до 5 мольных эквивалентов количества соединения формулы (3). В некоторых вариантах осуществления температуру реакционной смеси во время добавления уксусной кислоты поддерживают около примерно 20-25°C.
В некоторых вариантах осуществления соединение формулы (5), полученное по способу схемы 7, окисляют до соединения формулы (6) действием окисляющего агента. В некоторых вариантах осуществления этим окисляющим агентом является пероксид водорода, окислитель Oxone®, mCPBA (мета-хлорпербензойная кислота) и т.п. В некоторых вариантах осуществления пероксид водорода применяют в виде 30% раствора (масс.) H2O2 в воде. В некоторых вариантах осуществления реакционную смесь, содержащую образовавшееся соединение формулы (5), разбавляют перед стадией окисления дополнительным количеством гептана. В некоторых вариантах осуществления масса этого дополнительно добавленного гептана составляет от 5 до 10 масс использованного соединения формулы (3). В некоторых вариантах осуществления масса этого дополнительно добавленного гептана примерно в 8 раз превышает массу использованного соединения формулы (3). В некоторых вариантах осуществления реакционную смесь, содержащую образовавшееся соединение формулы (5), охлаждают до примерно -5-10°C после добавления дополнительного гептана и перед добавлением окисляющего агента. В некоторых вариантах осуществления реакционную смесь, содержащую образовавшееся соединение формулы (5), охлаждают до примерно 0-5°C после добавления дополнительного гептана и перед добавлением окисляющего агента. В некоторых вариантах осуществления температуру реакционной смеси после добавления окисляющего агента поддерживают около примерно -5-10°C. В некоторых вариантах осуществления температуру реакционной смеси после добавления окисляющего агента поддерживают около примерно 0-2°C. В некоторых вариантах осуществления реакционную смесь после добавления окисляющего агента перемешивают при температуре примерно -5-10°C до завершения реакции. В некоторых вариантах осуществления реакционную смесь после добавления окисляющего агента перемешивают при температуре примерно -1-2°C до завершения реакции. В некоторых вариантах осуществления за ходом реакции наблюдают с помощью ВЭЖХ, чтобы определить момент ее завершения. В некоторых вариантах осуществления реакционную смесь после завершения реакции гасят пентагидратом тиосульфата натрия для разрушения избытка пероксида.
В случае синтеза соединения 26, соединение формулы (4) представляет собой соединение 25. Соединение 25 и его кристаллическая форма также являются отдельными вариантами осуществления настоящего изобретения. Синтез соединения 25, начиная с дигидроксимочевины 24, описан ниже в примере 4, и получение характеристик твердой формы кристаллического соединения 25 описано ниже в примере 5.
В примере 6 ниже описано получение синтетического предшественника E6020 - соединения 26 (варианта соединения формулы (6), где R1 представляет собой гептил, оба заместителя R2 и R3 являются н-ундецилами и R4 представляет собой аллил) путем взаимодействия соединения 22 и соединения 25.
Описанный в настоящем описании способ синтеза может быть адаптирован для получения любого из всех возможных стереоизомеров соединения 26 и, соответственно E6020, например, показанных ниже соединений (A) и (B) соответственно, имеющих следующие структуры:
Хотя приведенные ниже примеры раскрывают получение конкретного стереоизомера, считается, что способы получения других стереоизомеров соединения 26 входят в объем настоящего изобретения. Способы синтеза по настоящему изобретению хорошо подходят для получения чистых стереоизомеров, для которых определена начальная стереохимия исходного соединения (3) и используется 2-кратный избыток соединения (3) по отношению к дифосфорамидиту мочевины (4), как показано на схеме 7 (выше). Этот способ мог бы дать возможность получения четырех чистых стереоизомеров, в т.ч. E6020 с конфигурацией (R,R,R,R) в положениях 1,6,22,27; ER-824156 (S,S,S,S); ER-804053 (R,S,S,R); и ER-824095 (S,R,R,S). Для получения других стереоизомеров (ER-826685 (R,R,S,R); ER-824887 (R,R,R,S); ER-826682 (R,R,S,S); ER-827905 (R,S,R,S); ER-826683 (R,S,S,S); ER-804097 (S,S,R,S)), можно было бы приготовить смесь исходных продуктов, в которой использовался бы 1 эквивалент исходного соединения (3) с определенной конфигурацией в положениях 2 и 7, тогда как второй эквивалент исходного соединения (3) мог бы иметь другую конфигурацию в положениях 2 и 7. В итоге реакция (по схеме 7) могла бы привести к 3 различным стереоизомерам соединения (6), которые можно разделить колоночной хроматографией и определить структуру с помощью сравнения данных 1H-ЯМР и ВЭЖХ с достоверными данными для стереоизомеров, полученных ранее по первому способу синтеза, описанному выше, и отдельному способу, описанному в патенте США №6290973. Патенты США №№6551600; 6290973 и 6521776, в которых раскрыты другие пути синтеза E6020 и родственных соединений, предоставляют полезную дополнительную информацию относительно получения некоторых реагентов и исходных соединений и включены в настоящую заявку посредством ссылки.
ПРИМЕРЫ
В приведенных ниже примерах, в случаях, когда для описания реактора (например, реакционного сосуда, колбы, стеклянного реактора и т.п.) используется термин «создана инертная атмосфера», подразумевается, что воздух в реакторе был заменен в основном свободным от влаги или сухим инертным газом (например, азотом, аргоном и т.п.). Термин «эквивалент» (сокращение: экв.) в настоящей заявке описывает стехиометрию (мольное отношение) реагента или вступающего в реакцию соединения путем сравнения с количеством предварительно выбранного исходного соединения. Термин «массовая единица» (сокращение: масс.ед.) в настоящей заявке соответствует отношению массы вещества или группы веществ к массе конкретного химического компонента реакции или методики очистки, конкретно указанного в приведенных ниже примерах. Это отношение рассчитывают как г/г или кг/кг. Термин «объемная единица» (сокращение: объемн.ед.) в настоящей заявке соответствует отношению объема данного вещества или группы веществ к массе или объему предварительно выбранного химического компонента реакции или методики очистки. Единицы, используемые в уравнении для расчета этого параметра, должны соответствовать друг другу по порядку величины. Например, соотношение рассчитывают как: мл/мл, мл/г, л/л или л/кг. В настоящей заявке используются следующие сокращения:
| Сокращение | Химическое соединение |
| ACN | ацетонитрил |
| Boc | трет-бутоксикарбонил |
| CDI | карбонилдиимидазол |
| DMAP | 4-(диметиламино)пиридин |
| DMF (ДМФА) | диметилформамид |
| EDC | гидрохлорид N-(3-диметиламинопропил)-N-этил карбодиимида |
| EtOH | этанол |
| Et3N | триэтиламин |
| Fmoc | 9-флуоренилметоксикарбонил |
| NaHMDS | гексаметилдисилазид натрия |
| HOAc | уксусная кислота |
| IPA | изопропиловый спирт |
| iPr | изопропил |
| Pd/C | палладий на угле |
| Pd(PPh3)4 | тетракис(трифенилфосфин)палладий (0) |