Биологически активные вещества, подавляющие патогенные бактерии, и способ ингибирования секреции iii типа у патогенных бактерий
Иллюстрации
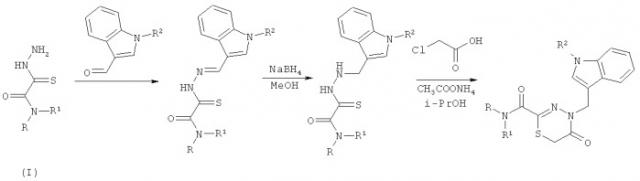
Показать всеИзобретение относится к индолил-замещенным производным тиадиазинонов, полученным на основе тиогидразидов оксаминовых кислот, общей формулы
где R представляет собой Н; R1 представляет собой пиридинил; фенил, замещенный алкилом С1-C5, Hal, CF3; R2 представляет собой H; алкил C1-С5; -CH2COOR4; бензил, замещенный Hal, OR4; бензоил, замещенный Hal, OR4, а R4 представляет собой незамещенный алкил C1-С4. Технический результат: получены новые соединения, которые могут найти применение в медицине для создания лекарственных средств, обладающих ингибирующей активностью в отношении патогенных бактерий. 2 н.п. ф-лы, 2 ил., 2 табл., 13 пр.
Реферат
Область техники
Изобретение относится к индолил-замещенным производным тиадиазинонов, полученным на основе тиогидразидов оксаминовых кислот общей формулы
которые могут быть использованы для подавления патогенных бактерий, в частности воздействовать на систему секреции III типа у патогенов.
Предшествующий уровень техники
По данным ВОЗ почти 60% случаев смертности связаны с хроническими заболеваниями, в основе которых лежит хроническое воспаление, индуцированное патогенными микроорганизмами. Общей тенденцией является существенное снижение эффективности используемых в клинической практике антибиотиков в отношении хронических инфекций. На данный момент эффективных антибиотиков, оказывающих выраженный терапевтический эффект на хроническую инфекцию, на рынке лекарственных препаратов не существует. Это обусловлено тем, что при хронической инфекции имеет место эволюционно выработанная адаптация патогена, направленная на длительное выживание в макроорганизме, в том числе изменение метаболической активности. Это приводит к снижению чувствительности микроорганизма к антибактериальным препаратам, эффективным на острой стадии инфекционного процесса.
Не менее остро стоит проблема развития антибиотикорезистентности к используемым антибактериальным препаратам. Формирование микроорганизмами устойчивости к антибиотикам сопряжено с рядом негативных последствий как для отдельных пациентов, так и для общества в целом. При устойчивости возбудителя инфекционной болезни к основным антибиотикам резко возрастает вероятность неудачи эмпирического лечения конкретного пациента. В то же время вполне очевидно, что каждое конкретное заболевание, вызываемое резистентным микроорганизмом, является проявлением процесса формирования и распространения устойчивости в микробной популяции. Ситуация осложняется еще и тем, что крупные фармацевтические компании существенно снизили разработку антибиотиков, т.к. рост антибиотикорезистентности ограничивает со временем возможности применения препарата и, соответственно, снижает прибыли от продаж.
Если оценивать экономическую сторону рассматриваемой проблемы, то основным мотивирующим фактором разработки новых антибактериальных препаратов в настоящее время является множественная лекарственная устойчивость. Однако потребность в препаратах для лечения хронических и рецидивирующих инфекций охватывает значительно больший контингент больных, недополучающих необходимое эффективное лечение, что и определяет широкие перспективы в области разработки и внедрения новых лекарственных препаратов.
В связи с вышесказанным совершенно очевидна необходимость выбора иной стратегии поиска лекарственных средств, основанной на выявлении принципиально новых мишеней у бактериальных патогенов.
Детальное изучение и понимание механизмов взаимодействия патогенов с организмом хозяина и выявление наиболее уязвимых звеньев в цепи динамичных событий проявления патогенетического потенциала могут явиться основой для эффективного выбора мишеней для действия препаратов нового поколения, направленных на подавление вирулентности, т.н. антивирулентных лекарственных средств. Такие препараты должны иметь ряд преимуществ по сравнению с используемыми ныне антибиотиками. Во-первых, действие на вирулентные свойства патогена, которые важны при взаимодействии в системе патоген-хозяин без подавления жизнеспособности, дает основание прогнозировать отсутствие селективного давления и отбор резистентных штаммов бактерий. Во-вторых, препараты, действующие на специфические мишени патогенных бактерий, не будут токсичными для эукариотических клеток и для нормальной микрофлоры человека, что представляет собой серьезнейшую проблему при использовании антибиотиков. Действительно, микробные клетки, образующие микробиоту здорового человека, превосходят по количеству человеческие клетки в десятки раз, колонизируя различные органы и способствуя реализации многих жизненно важных процессов, роль микробиоты в которых только начинает осознаваться. Микробиота представляет собой динамичное состояние, и нарушение ее популяционного состава при действии антибиотиков приводит к утрате симбиотической выгоды и развитию инфекций, обусловленных оппортунистическими патогенами.
Ведущая роль в реализации вирулентных свойств патогенных бактерий принадлежит системе секреции III типа, посредством которой осуществляется транспорт белковых факторов вирулентности в клетку макроорганизма. Процесс осуществляется путем секреции и экспорта эффекторных молекул через мембраны в межклеточное пространство или непосредственно в цитоплазму клетки-хозяина, что приводит к изменению ее нормального физиологического состояния и способствует адгезии, инвазии и внутриклеточному размножению патогена. Кроме того, через систему секреции реализуются спектр адаптационных механизмов, направленных на длительное выживание в организме хозяина, связанное с их способностью инактивировать защитные реакции организма.
В уровне техники известны соединения, воздействующие на вирулентные свойства патогенных бактерий. Эти соединения подавляют секреторные функции некоторых грамотрицательных бактерий, таких как Yersinia pseudotuberculosis, Salmonella enterica, Pseudomonas aeruginosa, патогенных штаммов E.coli, Chlamydia spp, и не вызывают развитие устойчивости к препаратам на их основе. К таким соединениям можно отнести гидразоны, полученные на основе гидразидов бензойных и пиридинкарбоновых кислот
(«Small molecule inhibitors of type III secretion in Yersinia block the Chlamydia pneumoniae infection cycle» FEBS Letters, 581 (2007), 587-595 / Низкомолекулярные ингибиторы системы секреции III типа иерсиний блокируют инфекционный цикл Chlamydia pneumoniae;
«Small-Molecule Inhibitors Specifically Targeting Type III Secretion» Infection and Immunity, 2005, p.3104-3114, Vol.73, No.5 / Низкомолекулярные ингибиторы, специфически действующие на систему секреции III типа;
«А small-molecule inhibitor of type III secretion inhibits different stages of the infectious cycle of Chlamydia trachomatis» PNAS, 26, 2006, vol.103, No. 39, 14566-14571 / Низкомолекулярные ингибиторы системы секреции III типа подавляют различные стадии внутриклеточного цикла развития Chlamydia trachomatis).
Однако недостатком этих соединений является их значительная токсичность для эукариотических клеток, что принципиально ограничивает возможность их для дальнейшей разработки в качестве лекарственных препаратов.
Раскрытие изобретения
Задачей изобретения является создание соединений, подавляющих секреторную функцию патогенных бактерий, не являющихся токсичными для нормальной микрофлоры и клеток хозяина, снижающих риск развития резистентности.
Технический результат достигается получением биологически активных соединений, обладающих высокой избирательной ингибирующей активностью в отношении патогенных бактерий, в том числе вызывающих хронические болезни. При этом полученные соединения нетоксичны для клеток человека и животных, они хорошо растворимы в органических растворителях, а также характеризуются специфической активностью в условиях биологических систем воздействия на патогенные бактерии и снижают риск развития резистентности патогенных бактерий.
Технический результат обеспечивается за счет того, что заявленные биологически активные соединения, подавляющие патогенные бактерии, представляют собой индолил-замещенные производные тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот общей формулы
где
R представляет собой Н;
R1 представляет собой пиридинил, фенил, замещенный алкилом С1-С5, Hal, CF3;
R2 представляет собой H, алкил C1-С5, -CH2COOR4, бензил, замещенный Hal, OR4, бензоил, замещенный Hal, OR4, а
R4 представляет собой незамещенный алкил C1-С4.
Способ ингибирования секреции III типа у патогенных бактерий заключается в воздействии на бактерии эффективным количеством соединения заявленного соединения.
Система секреции выявлена у таксономически далеких микроорганизмов (патогенных бактерий) - возбудителей особо опасных инфекций, таких как Yersinia, Brucella, и возбудителей социально-значимых инфекций, таких как Chlamydia, Salmonella, Shigella и др. Получившая название система секреции III типа является консервативной, абсолютно необходимой для развития острого инфекционного процесса, а хронизация инфекции принципиально зависит от ее функционирования. Следовательно, ингибиторы секреции III типа у патогенов будут оказывать направленное воздействие на механизмы, обуславливающие процесс хронизации инфекции, не влияя на жизнеспособность бактерий, фактически «обезоруживая» патоген. В отличие от антибиотиков действие таких специфических ингибиторов не будет приводить к развитию генетически детерминированной устойчивости. Кроме того, система III секреции присутствует только у патогенных бактерий, следовательно, ее ингибиторы не токсичны для нормальной микрофлоры человека и клеток хозяина, т.е. характеризуются избирательностью.
Примеры синтеза соединений
Замещенные тиадиазины получаются на основе тиогидразидов оксаминовых кислот общей формулы (I), которые получают взаимодействием соответствующих хлорацетамидов с предварительно приготовленным раствором элементной серы с морфолином и последующее взаимодействием монотиооксамидов с гидразин-гидратом. Полученные таким образом тиогидразиды конденсируют с соответствующими индолкарбальдегидами, восстанавливают боргидридом натрия в метаноле и циклизуют с монохлоруксусной кислотой в условиях щелочного катализа с образованием соответствующего тиадиазина. Замещенные тиадиазины на основе производных тиогидразидов оксаминовых кислот могут быть синтезированы по следующей схеме:
Общая методика получения хлорацетамидов
К раствору (0,1 моль) соответствующего анилина в 100 мл ДМФА добавляли при охлаждении 8,75 мл (0,11 моль) хлорацетилхлорида, следя за тем, чтобы температура не превышала 20°С. После окончания прибавления перемешивали при комнатной температуре раствор еще 2 часа. Затем выливали реакционную смесь в 600 мл холодной воды и отфильтровывали осадок. Промывали его на фильтре водой и сушили на воздухе.
Общая методика получения тиогидразидов
Готовили раствор 0,15 моль элементной серы в 50 мл ДМФА и добавляли 0,06 моль морфолина. Полученную смесь перемешивали 20-30 минут и добавляли к ней раствор 0,05 моль соответствующего хлорацетамида в минимальном количестве ДМФА при охлаждении, следя за тем, чтобы температура не превышала 15°С. Полученную смесь перемешивали 3-6 часов (контроль по ТСХ). После окончания реакции реакционную смесь выливали в воду, экстрагировали вещество этилацетатом, пропускали органический слой через колонку с силикагелем, упаривали на роторном испарителе, затем полученный остаток растворяли в небольшом количестве (5-6 мл) ДМФА и добавляли 6 мл (0,12 моль) гидразин-гидрата и перемешивали при комнатной температуре 2 часа. Затем выливали в воду и подкисляли разбавленной соляной кислотой до рН 7. Отфильтровывали осадок и сушили его на воздухе.
Общая методика получения N-индолил-замещенных тиогидразидов
К 10 ммоль соответствующего тиогидразида оксаминовой кислоты в 5 мл метанола добавляли 11 ммоль соответствующего альдегида и кипятили при перемешивании в течение 5 минут. Охлаждали реакционную смесь. При охлаждении льдом (0-5°С) и перемешивании добавили 55 мг (1,5 ммоль) боргидрида натрия, небольшими порциями. Реакционную смесь оставили на 2 часа при охлаждении и перемешивании, затем добавили 25 мл воды и нейтрализовали разбавленной соляной кислотой до нейтральной среды. Выпавший осадок отфильтровали и при необходимости перекристаллизовывали из изопропанола.
Общая методика получения индолил-замещенных тиадиазинонов
1 ммоль соответствующего N'-индолил-замещенного тиогидразида оксаминовой кислоты добавляли к раствору 1,2 ммоль хлоруксусной (или бромуксусной) кислоты в 5 мл изопропанола. Добавляли к реакционной смеси каталитическое количество ацетат аммония и кипятили 2-5 часов (контроль по тонкослойной хроматограмме). После окончания реакции выливали реакционную смесь в 50 мл воды и экстрагировали вещество этилацетатом, промывали органический слой водой 2×50 мл. Затем отделяли органический слой, сушили его над сульфатом натрия и удаляли растворитель на роторном испарителе. Остаток перекристаллизовывали из минимального количества этанола.
Получение исходных тиогидразидов
N-хлорацетил-2-аминопиридин (1)
Выход: N-хлорацетил-2-аминопиридина (1) 11,9 г (70%). Т.пл. 140-141°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 4,20 (с, 2Н, CH2Cl); 7,41-7,45 (м, 2Н, Ar); 8,07-8,11 (м, 2Н, аром); 10,31 (с, 1Н, NH). Найдено (%): С 49.20, Н 4.03, N 16.21. Вычислено (%): С 49.28, Н 4.14, N 16.42. Масс-спектр, m/z: 170.
2-Гидразино-N-пиридин-2-ил-2-тиоксо-ацетамид (2)
Выход: 2-гидразино-N-пиридин-2-ил-2-тиоксо-ацетамида (2) 1,2 г (60%). Т.пл. 164-165°С. ЯМР 1H DMSOd6 (δ, м.д., J, Гц): 7,40-7,43 (м, 2Н, Ar); 8,07-8,10 (м, 2Н, аром); 10,59 (с, 1Н, NH). Найдено (%): С 42.76, Н 4.01, N 28.44. Вычислено (%): С 42.85, Н 4.11, N 28.55. Масс-спектр, m/z: 196.
N-хлорацетил-4-(трифторметил)-анилин (3)
Выход хлорацетамида (3) 19 г, 80%. Т.пл. 115-116°С. ЯМР 1H DMSOd6 (δ, м.д., J, Гц): 4,20 (с, 2Н, Ar-CH2-Cl); 7,07 (д, 2Н, аром); 7,21 (д, 2Н, аром). Найдено (%): С 45.38, Н 2.81, N 5.96. Вычислено (%): С 45.49, Н 2.97, N 5.89. Масс-спектр, m/z: 237.
2-Гидразино-2-тиоксо-N-[4-(трифторметил)фенил]ацетамид (4)
Выход тиогидразида (4) 6,4 г, 60%. Т.пл. 154-155°С. ЯМР 1H DMSOd6 (δ, м.д., J, Гц): 7,08 (д, 2Н, аром); 7,24 (д, 2Н, аром); 10,59 (с, 1Н, NH). Найдено (%): С 41.16, Н 3.13, N 15.83. Вычислено (%): С 41.06, Н 3.06, N 15.96. Масс-спектр, m/z: 263.
N-хлорацетил-2,4-дифторанилин (5)
Выход хлорацетамида (5) 87%. Т.пл. 101-102°С. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 4,20 (с, 2Н, ArCH2Cl); 7,10-7,25 (м, 2Н, Ar); 7,53 (м, 1Н, Ar); 10,25 (с, 1H, Ar-NH-CO). Найдено (%): С 46.62, Н 2.99, N 6.84. Вычислено (%): С 46.74, Н 2.94, N 6.81. Масс-спектр, m/z: 205.
2-[Гидразино-(тиоксо)-ацетиламино]-2,4-дифторанилин (6)
Выход: (6) 8,1 г, 70%. Т.пл. 154-156°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 7,10-7,26 (м, 2Н, Ar); 7,50 (м, 1Н, Ar); 10,30 (с, 1Н, Ar-NH-CO). Найдено (%): С 41.40, Н 3.18, N 18.25. Вычислено (%): С 41.56, Н 3.05, N 18.17. Масс-спектр, m/z: 231.
N-хлорацетил-2-метиланилин (7)
Выход хлорацетамида (7) 15,5 г, 85%. Т.пл. 124-126°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 1,74 (с, 3H, ArCH3); 4,20 (с, 2Н, CH2Cl); 7,07 (м, 1H, Ar); 7,21 (м, 1Н, Ar); 7,41 (м, 1H, Ar); 7,63 (м, 1Н, Ar); 10,57 (с, 1Н, Ar-NH-CH2Cl). Найдено (%): С 58.86, Н 5.47, N 7.64. Вычислено (%): С 58.87, Н 5.49, N 7.63. Масс-спектр, m/z: 183.
2-[Гидразино-(тиоксо)-ацетиламино]-2-метиланилин (8)
Выход тиогидразида (8) 10,4 г, 60%. Т.пл. 154-157°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 1,74 (с, 3H, ArCH 3); 7,07-7,61 (м, 4Н, Ar); 10,32 (с, 1Н, Ar-NH-CO). Найдено: С 51.41, Н 5.53, N 20,40. Вычислено: С 51.66, Н 5.30, N 20.08. Масс-спектр, m/z: 209.
N-хлорацетил-4-фторанилин (9)
Выход (9) 80%. Т.пл. 110-112°С. ЯМР 1H DMSOd6 (δ, м.д., J, Гц): 4,20 (с, 2Н, ArCH2Cl); 7,21 (м, 2Н, Ar); 7,61 (м, 2Н, Ar); 10,21 (с, 1H, Ar-NH-CO). Найдено (%): С 51.17, Н 3.73, N 7.44. Вычислено (%): С 51.22, Н 3.76, N 7.47. Масс-спектр, m/z: 187.
2-[Гидразино-(тиоксо)-ацетиламино]-4-фторанилин (10)
Выход: (10) 6,4 г, 60%. Т.пл. 154-155°С. ЯМР 1H DMSOd6 (δ, м.д., J, Гц): 7,22 (м, 2Н, Ar); 7,63 (м, 2Н, Ar); 10,17 (с, 1Н, Ar-NH-CO). Найдено (%): С 45.01, Н 3.85, N 19.80. Вычислено (%): С 45.06, Н 3.78, N 19.71. Масс-спектр, m/z: 213.
Краткое описание фигур
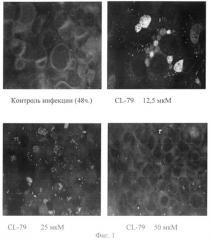
На фиг.1 показаны наиболее характерные морфологические изменения внутриклеточного развития хламидийной инфекции в условиях in vitro под влиянием изучаемых соединений на примере соединения CL-79.
На фиг.2. показан анализ специфической активности выбранных соединений в отношении III транспортной системы хламидий.
Примеры исполнения заявленного способа
Пример 1
(CL-79)
2-[2-(1Н-индол-3-илметил)гидразино]-2-тиоксо-N-[2-(трифторметил) фенил] ацетамид (11)
В качестве исходных соединений использовали тиогидразид 4 и индол-3-карбальдегид.
Выход гидразида (9) 255 мг, 75%. Т.пл. 238-239°С. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 5,32 (с, 1H, -NH-CH2-Indole); 7,07-7,77 (м, 8Н, Ar); 7,92 (с, 1Н, (С-Н) Indole); 10,12 (с, 1Н, Ar-NH-CO); 10,92 (с, 1Н, (N-H) Indole). Найдено (%): С 59.54, Н 4.31, N 16.22. Вычислено (%): С 59.64, Н 4.42, N 16.36. Масс-спектр, m/z: 341.
4-(1Н-индол-3-илметил)-5-оксо-N-[2-(трифторметил) фенил]-5,6-дигидро-4Н-1,3,4-тиодиазин-2-карбоксамид (CL-79)
Выход (CL-79) 250 мг, 75%. Т.пл. >250°С с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 4,02 (с, 2Н, -S-CH2); 5,36 (с, 1Н, -NH-CH2-Indole); 7,07-7,79 (м, 8Н, Ar); 7,90 (с, 1H, (С-Н) Indole); 10,10 (с, 1H, Ar-NH-СО); 10,94 (с, 1Н, (N-H) Indole). Найдено (%): С 59.60, Н 4.02, N 14.60. Вычислено (%): С 59.68, Н 3.95, N 14.65. Масс-спектр, m/z: 387.
Пример 2
(CL-80)
2-(2-{[1-(4-Фторбензил)-1Н-индол-3-ил]метил}гидразино)-2-тиоксо-N-[2-(трифторметил)фенил]ацетамид (13)
В качестве исходных соединений использовали тиогидразид 4 и N-(4-фторбензил)-индол-3-карбальдегид.
Выход гидразида (13) 269 мг, 60%. Т.пл. 279-280°С. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 4,32 (д, 2Н, -NH-CH2-Indole); 4,98 (с, 2Н, -NHIndole-CH2-Ar); 5,32 (с, 1H, NH); 6,77-8,18 (м, 13Н, Ar); 10,14 (с, 1H, Ar-NH-СО); 10,92 (с, 1H, CS-NH). Найдено (%): С 63.92, Н 4.57, N 12.38. Вычислено (%): С 63.99, Н 4.47, N 12.44. Масс-спектр, m/z: 449.
4-{[1-(4-Фторбензил)-1H-индол-3-ил]метил}-5-оксо-N-[2-(трифторметил)фенил]-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид (CL-80)
Выход (CL-80) 367 мг, 75%. Т.пл. >250°С с разл. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 4,05 (с, 2Н, -S-CH2); 4,98 (с, 2Н, -NHIndole-CH2-Ar); 5,36 (с, 1Н, -NH-CH2-Indole); 7,07-7,79 (м, 8Н, Ar); 7,90 (с, 1Н, (С-Н) Indole); 10,10 (с, 1Н, Ar-NH-CO); 10,94 (с, 1H, (N-H) Indole). Найдено (%): С 63.60, Н 4.19, N 11.37. Вычислено (%): С 63.66, Н 4.11, N 11.42. Масс-спектр, m/z: 489.
Пример 3
(CL-81)
2-{2-[(1-Метил-1Н-индол-3-ил)метил]гидразино}-2-тиоксо-N-[2-(трифторметил) фенил] ацетамид (15)
В качестве исходных соединений использовали тиогидразид 4 и N-метил-индол-3-карбальдегид.
Выход гидразида (15) 220 мг, 62%. Т.пл. 253-254°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 3,61 (с, 3H, СН3); 4,35 (д, 2Н, -NH-CH2-Indole); 4,90 (с, 2Н, -NHIndole-CH2-Ar); 5,33 (с, 1Н, NH); 6,79-8,10 (м, 9Н, Ar); 10,12 (с, 1Н, Ar-NH-CO); 10,89 (с, 1Н, CS-NH). Найдено (%): С 60.61, Н 4.85, N 15.66. Вычислено (%): С 60.66, Н 4.81, N 15.72. Масс-спектр, m/z: 355.
4-[(1-Метил-1H-индол-3-ил)метил]-5-оксо-N-[2-(трифторметил) фенил]-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид (CL-81)
Выход (CL-81) 316 мг, 75%. Т.пл. >250°С с разл. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 3,62 (с, 3H, СН3); 4,02 (с, 2Н, -S-CH2); 5,31 (с, 1H, -NH-CH2-Indole); 6,89-7,71 (м, 8Н, Ar); 7,92 (с, 1H, (С-Н) Indole); 10,11 (с, 1H, Ar-NH-CO). Найдено (%): С 60.52, Н 4.36, N 14.10. Вычислено (%): С 60.59, Н 4.32, N 14.13. Масс-спектр, m/z: 395.
Пример 4
(CL-82)
2-[2-(1Н-индол-3-илметил)гидразино]-N-(2-метилфенил)-2-тиоксоацетамид (17)
В качестве исходных соединений использовали тиогидразид 8 и индол-3-карбальдегид.
Выход гидразида (17) 179 мг, 52%. Т.пл. 251-252°С. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 2,23(с, 3H, СН3) 4,34 (д, 2Н, -NH-CH2-Indole); 5,32 (с, 1Н, NH) 6,79-8,11 (м, 9Н, Ar); 10,11 (с, 1Н, Ar-NH-СО); 10,87 (с, 1Н, CS-NH). Найдено (%): С 63.74, Н 5.39, N 16.50. Вычислено (%): С 63.88, Н 5.36, N 16.55. Масс-спектр, m/z: 337.
4-(1Н-индол-3-илметил)-N-(2-метилфенил)-5-оксо-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид (CL-82)
Выход (CL-82) 324 мг, 86%. Т.пл. >250°С с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 2,23 (с, 3H, СН3); 4,08 (с, 2Н, -S-CH2); 5,33 (с, 1Н, NH); 5,38 (с, 1H, -NH-CH2-Indole); 6,77-8,09 (м, 9Н, Ar); 10,11 (с, 1Н, Ar-NH-СО). Найдено (%): С 63.32, Н 4.81, N 14.72. Вычислено (%): С 63.47, Н 4.79, N 14.80. Масс-спектр, m/z: 377.
Пример 5
(CL-83)
2-(2-{[1-(4-Метоксибензил)-1Н-индол-3-ил]метил}гидразино)-2-тиоксо-N-[2,4-дифторфенил]ацетамид (19)
В качестве исходных соединений использовался тиогидразид 6 и N-(4-метоксибензил-индол-3-карбальдегид.
Выход гидразида (19) 388 мг, 81%. Т.пл. 281-282°С. ЯМР 1Н CDCl3 (6, м.д., J, Гц): 3,87 (с, 3H, СН3); 4,36 (д, 2Н, -NH-CH2-Indole); 4,87 (с, 2Н, -NHIndole-CH2-Ar); 5,30 (с, 1Н, NH); 6,82-8,23 (м, 12Н, Ar); 10,05 (с, 1Н, Ar-NH-CO); 10,84 (с, 1Н, CS-NH). Найдено (%): С 62.42, Н 4.69, N 11.52. Вычислено (%): С 62.49, Н 4.61, N 11.66. Масс-спектр, m/z: 479.
4-{[1-(4-Метоксибензил)-1Н-индол-3-ил]метил}-5-оксо-N-[2,4-дифторфенил]-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид
Выход (CL-83) 436 мг, 86%. Т.пл. >300°С с разл. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 3,87 (с, 3H, СН3); 4,05 (с, 2Н, -S-CH2); 4,86 (с, 2Н, -NHIndole-CH2-Ar); 5,31 (с, 1Н, -NH-CH2-Indole); 6,82-8,24 (м, 12Н, Ar); 10,06 (с, 1Н, Ar-M/-CO). Найдено (%): С 62.20, H 4.32, N 10.61. Вычислено (%): С 62.30, Н 4.26, N 10.76. Масс-спектр, m/z: 519.
Пример 6
(CL-84)
2-(2-{[1-(4-Фторбензил)-1Н-индол-3-ил]метил}гидразино)-2-тиоксо-N-[4-фторфенил]ацетамид
В качестве исходных соединений использовали тиогидразид 10 и N-(4-фторбензил)-индол-3-карбальдегид.
Выход гидразида (21) 328 мг, 72%. Т.пл. 254-255°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 4,32 (д, 2Н, -NH-CH2-Indole); 4,98 (с, 2Н, -NHIndole-CH2-Ar); 5,32 (с, 1Н, NH); 7,13-8,20 (м, 13Н, Ar); 10,11 (с, 1Н, Ar-NH-СО); 10,82 (с, 1Н, CS-NH). Найдено (%): С 63.90, Н 4.53, N 12.40. Вычислено (%): С 63.99, Н 4.47, N 12.44. Масс-спектр, m/z: 449.
4-{[1-(4-Фторбензил)-1Н-индол-3-ил]метил}-5-оксо-N-[4-фторфенил]-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид
Выход (CL-84) 316 мг, 75%. Т.пл. >250°С с разл. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 4,05 (с, 2Н, -S-CH2); 4,32 (д, 2Н, -NH-CH2-Indole); 4,97 (с, 2Н, -NHIndole-CH2-Ar); 7,13-8,22 (м, 13Н, Ar); 10,13 (с, 1Н, Ar-NH-CO). Найдено (%): С 63.56, Н 4.18, N 11.34. Вычислено (%): С 63.66, Н 4.11, N 11.42. Масс-спектр, m/z: 489.
Пример 7
(CL-85)
N-(2,4-Дифторфенил)-2-(2-{[1-(4-фторбензоил)-1Н-индол-3-ил]метил}гидразино)-2-тиоксоацетамид
В качестве исходных соединений использовали тиогидразид 6 и N-(4-фторбензил)-индол-3-карбальдегид.
Выход гидразида (23) 414 мг, 86%. Т.пл. >300°С с разл. ЯМР 1Н CDCl3 (5, м.д., J, Гц): 4,12 (д, 2Н, -NH-CH2-Indole); 5,38 (с, 1Н, NH); 6,92-8,32 (м, 12Н, Ar); 10,11 (с, 1H, Ar-NH-CO); 10,98 (с, 1Н, CS-NH). Найдено (%): С 59.61, Н 3.59, N 11.52. Вычислено (%): С 59.75, Н 3.55, N 11.61. Масс-спектр, m/z: 481.
N-(2,4-дифторфенил)-4-{[1-(4-фторбензоил)-1Н-индол-3-ил]метил}-5-оксо-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид
Выход (CL-85) 316 мг, 75%. Т.пл. >300°С с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 4,02 (с, 2Н, -S-CH2); 4,45 (д, 2Н, -NH-CH2-Indole); 5,38 (с, 1Н, NH); 6,92-8,32 (м, 12Н, Ar); 10,11 (с, 1H, Ar-NH-CO). Найдено (%): С 59.70, Н 3.31, N 10.68. Вычислено (%): С 59.77, Н 3.28, N 10.72. Масс-спектр, m/z: 521.
Пример 8
(CL-86)
N-(2,4-дифторфенил)-2-(2-{[1-(4-метоксибензоил)-1Н-индол-3-ил]метил}гидразино)-2-тиоксоацетамид
В качестве исходных соединений использовали тиогидразид 6 и N-(4-фторбензоил)-индол-3-карбальдегид.
Выход гидразида (25) 409 мг, 83%. Т.пл. >300°С с разл. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 4,03 (д, 2Н, -NH-CH2-Indole); 5,30 (с, 1Н, NH); 6,98-8,21 (м, 12Н, Ar); 10,09 (с, 1Н, Ar-NH-CO); 10,92 (с, 1Н, CS-NH). Найдено (%): С 60.61, Н 4.14, N 11.23. Вычислено (%): С 60.72, Н 4.08, N 11.33. Масс-спектр, m/z: 493.
N-(2,4-дифторфенил)-4-{[1-(4-метоксибензоил)-1Н-индол-3-ил]метил}-5-оксо-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид
Выход (CL-86) 442 мг, 83%. Т.пл. >300°C с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 3,87 (с, 3H, СН3); 4,05 (с, 2Н, -S-CH2); 4,03 (д, 2Н, -NH-CH2-Indole); 5,30 (с, 1Н, NH); 6,98-8,21 (м, 12Н, Ar); 10,09 (с, 1Н, Ar-NH-CO); 10,92. Найдено (%): С 60.52, Н 3.81, N 10.31. Вычислено (%): С 60.67, Н 3.77, N 10.48. Масс-спектр, m/z: 533.
Пример 9
(CL-87)
Метил{3-[(2-{2-[(2,4-дифторфенил)амино]-2-оксоэтантиоил}гидразино)метил]-1Н-индол-1-ил}ацетат
В качестве исходных соединений использовали тиогидразид 6 и метил-(3-формил-1Н-индол-1-ил)-ацетат.
Выход гидразида (27) 336 мг, 78%. Т.пл. 247- 248°С. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 3,61 (с, 3H, СН3); 4,28 (д, 2Н, -NH-CH2-Indole); 4,45 (с, 2Н, -NHIndole-CH2-COOMe); 5,36 (с, 1Н, NH); 6,82-7,96 (м, 8Н, Ar); 10,12 (с, 1H, Ar-NH-СО); 10,78 (с, 1Н, CS-NH). Найдено (%): С 55.42, Н 4.25, N 12.85. Вычислено (%): С 55.55, Н 4.20, N 12.96. Масс-спектр, m/z: 431.
Метил{3-[(2-{[(2,4-дифторфенил)амино]карбонил}-5-оксо-5,6-дигидро-4Н-1,3,4-тиадиазин-4-ил)метил]-1 Н-индол-1-ил}ацетат (CL-87)
Выход (CL-87) 316 мг, 75%. Т.пл. >250°С с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 3,62 (с, 3H, СН3); 4,04 (с, 2Н, -S-CH2); 4,27 (д, 2Н, -NH-CH2-Indole); 4,46 (с, 2Н, -NHIndole-CH2-COOMe); 6,80-7,92 (м, 8Н, Ar); 10,14 (с, 1H, Ar-NH-CO). Найдено (%): С 55.85, Н 3.88, N 11.72. Вычислено (%): С 55.93, Н 3.84, N 11.86. Масс-спектр, m/z: 471.
Пример 10
(CL-88)
2-{2-[(1-Метил-1Н-индол-3-ил)метил]гидразино}-N-пиридин-2-ил-2-тиоксоацетамид
В качестве исходных соединений использовали тиогидразид 2 и N-метил-индол-3-карбальдегид.
Выход гидразида (29) 139 мг, 44%. Т.пл. 279-280°С. ЯМР 1Н CDCl3 (δ, м.д., J, Гц): 3,62 (с, 3H, СН3); 4,34 (д, 2Н, -NH-CH2-Indole); 5,37 (с, 1Н, NH); 6,67-8,30 (м, 9Н, Ar); 10,27 (с, 1H, Ar-NH-CO); 10,82 (с, 1H, CS-NH). Найдено (%): С 60.12, Н 5.11, N 20.53. Вычислено (%): С 60.16, Н 5.05, N 20.63. Масс-спектр, m/z: 338.
4-[(1-Метил-1Н-индол-3-ил)метил]-5-оксо-N-пиридин-2-ил-5,6-дигидро-4Н-1,3,4-тиадиазин-2-карбоксамид (CL-88)
Выход (CL-88) 223 мг, 59%. Т.пл. >300°С с разл. ЯМР 1H CDCl3 (δ, м.д., J, Гц): 3,62 (с, 3H, СН3); 4,12 (с, 2Н, -S-CH2); 4,45 (д, 2Н, -1H-СН2-Indole); 6,74-8,32 (м, 9Н, Ar); 10,29 (с, 1H, Ar-NH-CO). Найдено (%): С 60.10, Н 4.58, N 18.41. Вычислено (%): С 60.14, Н 4.52, N 18.46. Масс-спектр, m/z: 378.
Биологические примеры
Для определения токсичности и биологической активности индолил-замещенных производных тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот, были использованы следующие методы.
1. Методы определения цитотоксического эффекта
А) Для определения токсичности в отношении эукариотической клетки использовали метод окрашивания клеток метиленовым синим (стандартная методика) с последующим спектрометрическим учетом результатов. Работу проводили в формате 96-луночных планшетов.
В суточном монослое клеток McCoy (гибридная линия синовиальных клеток человека и мышиных фибробластов) заменяли среду культивирования на свежую среду и вносили разные дозы исследуемых химических соединений. Клетки инкубировали в течение 24 часов в СО2 инкубаторе при 37°С. Спустя 24 часа из лунок отбирали культуральную среду и отмывали клетки 0,1 мМ раствором фосфатно-солевого буфера (ФСБ). Клетки фиксировали охлажденным метанолом (20 мкл) в течение 15 мин при 4°С. К фиксированным клеткам добавляли 40 мкл 0,5% метиленового синего и инкубировали 20 мин при комнатной температуре. После инкубации метиленовый синий отбирали из лунок и отмывали клетки ФСБ 4 раза. В лунки добавляли 100 мкл 5% додецилсульфата натрия (SDS) в ФСБ и инкубировали в течение 1 часа при комнатной температуре до полного лизиса клеток. Количество живых клеток определяли спектрофотометрически при длине волны 540 нм на фотометре MultiscanEX.
Б) Метод, направленный на определение метаболической активности клетки - МТТ-тест (Niks М., Otto М. Towards an optimized МТТ assay. // J Immunol. 1900. V.130, №1, p.149-151), основанный на восстановлении бесцветной соли тетразолия (3-[4,5-диметилтиазол-2-ил]-2,5-дифенил-тетразолия бромид, МТТ) митохондриальными и цитоплазматическими дегидрогеназами живых метаболически активных клеток с образованием голубых кристаллов формазана, количество которого измеряется спектрофотометрически.
Метод проводили в формате 96-луночного культурального планшета. В суточном монослое клеток McCoy заменяли среду культивирования на свежую среду и вносили разные дозы исследуемых химических соединений. Клетки инкубировали в течение 24 часов в CO2 инкубаторе при 37°С. За 4 часа до окончания эксперимента вносили 1:10 от объема культуральной среды 10х раствора МТТ (5 мг/мл). Инкубировали 4 часа при 37°С 5% CO2. Отбирали культуральную среду, отмывали однократно ФСБ. Добавляли в каждую лунку по 100 мкл изопропанола (пропанола-2). Инкубировали при комнатной температуре 30 минут. Оценивали оптическую плотность при длине волны 540 нм на фотометре Multiscan EX. Субстратное поглощение оценивали при 405 нм.
1. Метод суспензионного заражения эукариотических клеток
Метод суспензионного заражения эукариотических клеток хламидиями позволяет стандартизовать проведение биологических экспериментов в скрининговом формате на 96-луночных планшетах. Для получения суспензии клеток использовали суточный монослой клеток McCoy, который обрабатывали раствором трипсина и версена (соотношение 1:3 соответственно) для открепления клеток от поверхности флакона. Флакон помещали в термостат на 5 мин. Затем отбирали раствор трипсина и версена и клетки суспендировали в среде культивирования (RPMI 1640 с 10% фетальной сывороткой).
Для получения монослоя из приготовленной клеточной суспензии производили подсчет клеток в камере Горяева из расчета 1,5x105 кл./мл. Заражение клеток штаммом Bu-434 Chlamydia trachomatis серовар L2 производили в соотношении бактерия : клетка 1:1 в необходимом объеме транспортной среды (среда RPMI с 5% фетальной сывороткой, 25 мМ раствора глюкозы, 5 мкг/мл амфотерицина и 4 мкг/мл гентамицина), что обеспечивает 80-90% инфицирование клеток. Готовую суспензию вносили в лунки 96- или 24-луночных планшетов в объеме 100 мкл или 1000 мкл соответственно. Для осаждения клеток и стимуляции взаимодействия с ними хламидий планшеты центрифугировали при 3000 об/мин 1 час при температуре 25°С. После этого планшет помещали в инкубатор на 48 ч при 37°С.
2. Определение влияния индолил-замещенных производных тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот, на жизнеспособность хламидий
Исследуемые химические соединения в разных концентрациях вносили в культуру клеток одновременно с патогеном для оценки их влияния на внутриклеточное размножение хламидий. Эффект оценивали методом прямой иммунофлюоресценции.
Методы иммунофлюоресценции направлены на выявление объектов, содержащих некоторый антиген, и основаны на обработке препаратов соответствующими антителами, меченными флюорохромом, с последующей микроскопией в ультрафиолетовом луче.
В данной работе использован метод прямой иммунофлюоресценции (стандартная методика), позволяющий проводить полуколичественный учет развития хламидийной инфекции при использовании моноклональных антител к видоспецифическому белковому антигену С.trachomatis.
Работу проводили на клеточных линиях McCoy, инфицированных методом суспензионного заражения Ви-434 С.trachomatis серовар L2 в формате 96-луночных планшетов или 24-луночных со стеклами. Исследуемые химические соединения добавляли в разных дозах непосредственно при заражении клеток. Через 48 ч из лунок отбирали надосадок и фиксировали клетки. При работе с 96-луночными планшетами фиксацию осуществляли ледяным 72° этанолом с последующим помещением планшета на 30-40 мин на -20°С. При работе с 24-луночными планшетами стекла промывали в 0,1 мМ растворе ФСБ и высушивали. После этого клетки фиксировали ацетоном в течение 15 мин при комнатной температуре. На фиксированные клетки наносили 30-50 мкл моноклональных меченных ФИТЦ антител к белковому антигену С.trachomatis (ХлаМоноСкрин-2, ООО «НИАРМЕДИК ПЛЮС») и инкубировали в течение 30 мин во влажной камере при 37°С. После инкубации клетки промывались 2 раза раствором ФСБ. Препарат полностью высушивали. В формате 24-луночных планшетов подготовленные таким образом стекла монтировали на предметное стекло при помощи монтирующей жидкости (глицерин в ФСБ). Готовые препараты исследовали в люминесцентном микроскопе.
3. Определение влияния индолил-замещенных производных тиадиазинонов и полученных на основе тиогидразидов оксаминовых кислот на III транспортную систему хламидий
Оценку влияния исследуемых соединений на III транспортную систему (ТСС) хламидий проводили на основе детекции транслокации эффекторного белка IncA С.trachomatis на мембрану внутриклеточного хламидийного включения. Белок IncA детектировали с помощью метода непрямой иммунофлюоресценции (стандартная методика) с использованием коммерческих антител к эффекторному белку ТТС IncA С.trachomatis (поликлональная кроличья сыворотка, специфическая к IncA, «Innovagen», Швеция) с последующей детекцией антикроличьими антителами, меченными ФИТЦ.
Для этого суточный монослой заражали для получения 80-90% инфицированных клеток, центрифугировали при 3000 об/мин 30 мин при 25°С. Через 8 ч после заражения (время начала транслокации эффекторного белка в мембрану включения) добавляли разные дозы исследуемых химических соединений. Через 24 ч из лунок отбирали культуральную среду, стекла промывали в 0,1 мМ растворе ФСБ и высушивали. После этого клетки фиксировали ацетоном в течение 15 мин при комнатной температуре. На фиксированные клетки наносили 50 мкл первичных анти IncA антител и инкубировали в течение 30 мин при 37°С. Затем стекла промывали указанным раствором ФСБ и наносили антитела, меченные ФИТЦ. Инкубировали в течение 30 мин во влажной камере при 37°С. После инкубации стекла с клетками промывались 2 раза раствором ФСБ. Препарат полностью высушивали. Подготовленные таким образом стекла монтировали на предметное стекло при помощи монтирующей жидкости. Готовые препараты исследовали в люминесцентном микроскопе. Одновременно проводилась окраска моноклональными антителами к белку МОМР наружной мембраны клеточной стенки, что позволяло оценивать развитие хламидийной инфекции.
Пример 11
Влияние соединений класса индолил-замещенных производных тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот, на жизнеспособность эукариотических клеток
Соединения характеризуются высокой степенью растворимости в диметилформамиде (ДМФ), не образуют осадка в процессе хранения и при переведении в транспортную среду.
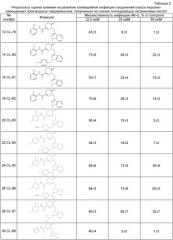
Анализ токсичности 10 исследуемых соединений и 1 соединения, являющегося прототипом и относящегося к гидразонам, полученным на основе гидразидов бензойных (INP0400), в условиях in vitro при добавлении в среду культивирования эукариотических клеток в дозах 12.5, 25 и 50 мкМ и последующем инкубировании в течение 24 часов при 37°С, проведенный методами 1.А и Б, выявил отсутствие негативного влияния на жизнеспособность эукариотических клеток соединений класса индолил-замещенных производных тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот. Результаты представлены в таблице 1.
Наименьший цитотоксический эффект по результатам двух использованных тестов был показан для соединений CL-79 и CL-82. Даже при наибольшей концентрации в 50 мкМ эти соединения вызывали не более 1-5% гибели клеток и снижали метаболическую активность не более чем у 10-14% клеток. Другие 8 соединений также показали удовлетворительные результаты по цитотоксичности, что свидетельствует в пользу того, что выбранные соединения относятся к малотоксичным. Напротив, соединение-прототип LHC-540 показало выраженную токсичность для эукариотических клеток, что ограничивает возможность его дальнейшей разработки в качестве терапевтического средства и указывает на очевидные преимущества заявляемых в данном патенте соединений.
Пример 12
Влияние соединений класса индолил-замещенных производных тиадиазинонов, полученных на основе тиогидразидов оксаминовых кислот, на развитие хламидийной инфекции
Способность десяти представленных в примерах 1-10 соединений подавлять внутриклеточный жизненный цикл хламидий в условиях in vitro оценивали при помощи методов 2-3, результаты которых представлены в таблице 2.
Наилучший эффект оказывали соединения CL-79, CL-83, CL-88, подавляя внутриклеточное накопление хламидий на 98-99% при концентрац