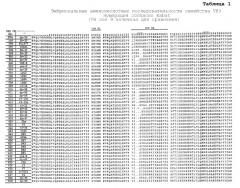
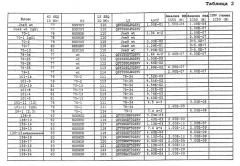
Способ лечения псориаза (варианты)
Иллюстрации
Показать всеИзобретение относится к способу лечения псориаза у субъекта путем введения субъекту антитела или его антигенсвязывающей части, способных связываться с субъединицей p40 IL-12 и/или IL-23, в дозе от приблизительно 0,1 до 5,0 мг/кг по определенной схеме. Антитело или его антигенсвязывающую часть можно вводить раз в две недели, раз в неделю или однократно в различных дозах в зависимости от состояния пациента. Способ предназначен для лечения хронического псориаза. Курс лечения проводят периодами, каждый из которых составляет по меньшей мере 12 недель, т.е. первый длительный период, в течение которого вводят антитело, затем прекращение введения антитела или его фрагмента по меньшей мере на 12 недель и далее второй длительный период из по меньшей мере 12 недель с введением антитела или его фрагмента. Доза антитела или его фрагмента для введения составляет от приблизительно 100 мг до 200 мг. Лечение проводят под контролем индекса площади и тяжести псориаза (PASI). Использование способа позволит увеличить эффективность лечения хронического псориаза. 5 н. и 35 з.п. ф-лы, 51 ил., 14 табл., 8 пр.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет по предварительной заявке США № 61/069840, поданной 18 марта 2008 года; предварительной заявке США № 61/095275, поданной 8 сентября 2008 года; и предварительной заявке США № 61/207904, поданной 18 февраля 2009 года, полное содержание каждой из которых включено в настоящий документ в качестве ссылки.
ПРЕДОСТАВЛЕНИЕ КОМПАКТ-ДИСКА
Данная заявка включает в качестве ссылки текстовый файл ASCII под названием SequenceListing.txt, содержащий 785 KB данных, созданный 10 марта 2009 и представленный в считываемом компьютером формате (CRF).
УРОВЕНЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Псориаз представляет собой опосредуемое T-клетками воспалительное заболевание, которое считается одним из наиболее распространенных аутоиммунных заболеваний, которым страдают приблизительно от 2% до 3% взрослых, хотя его распространенность по всему миру широко варьирует (Stern R.S., et al., J Investig Dermatol Symp Proc 2004, 9: 136-39; Davidson A and Diamond B. N Engl J Med 2001, 345: 340-50; Langley R.G.B., et al., Ann Rheum Dis 2005, 64(Suppl II): ii18-23). Псориаз оказывает значительное влияние на качество жизни (de Korte J, et al., J Investig Dermatol Symp Proc 2004, 9: 140-7; Krueger G, et al., Arch Dermatol 2001, 137: 280-4; Finlay AY and Coles EC, Br J Dermatol 1995, 132: 236-44), и он ассоциирован с рядом психологических и психосоциальных проблем (Kimball AB, et al., Am J Clin Dermatol 2005, 6: 383-92; Russo PA, et al., Australas J Dermatol 2004, 45: 155-9). Многие традиционные способы лечения псориаза имеют побочные действия; таким образом, их продолжительное применение ограничено (Lebwohl M. and Ali S., J Am Acad Dermatol 2001, 45: 487-98; Lebwohl M. и Ali S., J Am Acad Dermatol 2001, 45: 649-61). Кроме того, многих пациентов с псориазом не удовлетворяют традиционные способы лечения (Stern RS, et al., J Investig Dermatol Symp Proc 2004, 9: 136-39; Finlay AY and Ortonne JP, J Cutan Med Surg 2004, 8: 310-20); таким образом, существует очевидная потребность в способах лечения, которые являются более безопасными и более простыми в применении и которые могут быть предписаны на длительное время.
Интерлейкин-12 (IL-12) и родственный ему цитокин IL-23 являются членами суперсемейства IL-12 цитокинов, которые имеют общую субъединицу p40 (Anderson EJR, et al., Springer Semin Immunopathol 2006, 27: 425-42). Оба цитокина участвуют в развитии иммунного ответа T-хелперов 1 типа (Th1) при псориазе, однако каждый из них играет уникальную роль (Rosmarin D and Strober BE, J Drugs Dermatol 2005, 4: 318-25; Hong K, et al., J Immunol 1999, 162: 7480-91; Yawalkar N, et al., J Invest Dermatol 1998, 111: 1053-57). IL-12, главным образом, стимулирует дифференцировку Th1-клеток и последующую секрецию интерферона-гамма, в то время как IL-23 предпочтительно стимулирует дифференцировку наивных T-клеток в эффекторные T-хелперные клетки (Th17), которые стимулируют IL-17, провоспалительный медиатор (Rosmarin D and Strober BE, J Drugs Dermatol 2005, 4: 318-25; Harrington Le, et al., Nature Immunol 2005, 6: 1123-32; Park H, et al. Nature Immunol 2005, 6: 1132-41). Сверхэкспрессия матричной РНК p40 IL-12 и p40 IL-23 в псориатических очагах повреждения кожи указывает на то, что ингибирование IL-12 и IL-23 нейтрализующим антителом к субъединице p40 белка IL-12/23 может обеспечить эффективный терапевтический подход для лечения псориаза (Yawalkar N, et al., J Invest Dermatol 1998, 111: 1053-57; Lee E, et al., J Exp Med 2004, 199: 125-30; Shaker OG, et al., Clin Biochem 2006, 39: 119-25; Piskin G, et al., J Immunol 2006, 176: 1908-15). Очевидно, что в данной области необходимы такие терапевтические подходы для лечения псориаза.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения псориаза, например, хронического псориаза, с использованием антитела или его антигенсвязывающей части, которые связываются с IL-12 человека и/или IL-23 человека.
В одном аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта сохраняется по меньшей мере ответ PASI 75 в течение первого длительного периода после начального введения антитела или его антигенсвязывающей части, где у субъекта обнаруживается снижение ответа после прекращения введения антитела или его антигенсвязывающей части, и где у субъекта сохраняется по меньшей мере ответ PASI 75 в течение второго длительного периода после повторного введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В одном варианте осуществления первый длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления введение антитела прекращают по меньшей мере приблизительно на 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно на 12 недель.
В одном варианте осуществления второй длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в две недели. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в неделю. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в однократной дозе.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 или 220 мг.
В одном варианте осуществления псориаз представляет собой хронический псориаз. В одном варианте осуществления псориаз представляет собой бляшечный псориаз, например, хронический бляшечный псориаз. В другом варианте осуществления псориаз представляет собой хронический псориаз, например, хронический бляшечный псориаз. В другом варианте осуществления псориаз представляет собой псориаз от умеренного до тяжелого, например, бляшечный псориаз от умеренного до тяжелого, хронический псориаз от умеренного до тяжелого или хронический бляшечный псориаз от умеренного до тяжелого. В одном варианте осуществления субъект имеет клинический диагноз псориаза в течение по меньшей мере 6 месяцев. В другом варианте осуществления субъект имеет стабильный бляшечный псориаз в течение по меньшей мере 2 месяцев.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту однократной дозы антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где после введения антитела или его антигенсвязывающей части достигают по меньшей мере одного фармакокинетического свойства, выбранного из группы, состоящей из времени полужизни, составляющего по меньшей мере приблизительно 3 суток, Tmax, меньшего или равного 4 суткам, и биодоступности, составляющей по меньшей мере приблизительно 40%.
В различных вариантах осуществления достигают времени полужизни по меньшей мере приблизительно 2 суток, 3 суток, 4 суток, 5 суток, 6 суток, 7 суток, 8 суток, 9 суток или 10 суток.
В различных вариантах осуществления достигают Tmax, меньшего или равного приблизительно 1 суткам, 2 суткам, 3 суткам, 4 суткам, 5 суткам, 6 суткам или более.
В различных вариантах осуществления достигают биодоступности по меньшей мере приблизительно 0,1%, 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или более.
В одном варианте осуществления антитело вводят путем внутривенной инъекции.
В одном варианте осуществления антитело вводят путем подкожной инъекции.
В одном варианте осуществления однократная доза составляет от приблизительно 0,1 до приблизительно 5,0 мг/кг (например, от приблизительно 0,1 до приблизительно 1,0 мг/кг, от приблизительно 0,1 до приблизительно 2,0 мг/кг, от приблизительно 0,1 до приблизительно 3,0 мг/кг, от приблизительно 0,1 до приблизительно 4,0 мг/кг, от приблизительно 1,0 до приблизительно 2,0 мг/кг, от приблизительно 1,0 до приблизительно 3,0 мг/кг, от приблизительно 1,0 до приблизительно 4,0 мг/кг или от приблизительно 1,0 до приблизительно 5,0 мг/кг) антитела или его антигенсвязывающей части.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта сохраняется по меньшей мере ответ PASI 75 в течение первого длительного периода после начального введения антитела или его антигенсвязывающей части, где у субъекта обнаруживается снижение ответа после прекращения введения антитела или его антигенсвязывающей части, и где у субъекта сохраняется по меньшей мере ответ PASI 50 в течение второго длительного периода после повторного введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В одном варианте осуществления первый длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления введение антитела прекращают по меньшей мере приблизительно на 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления второй длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в две недели. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в неделю.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в однократной дозе. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг или 200 мг.
В одном варианте осуществления псориаз представляет собой хронический псориаз.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта сохраняется по меньшей мере ответ PASI 75 в течение первого длительного периода после начального введения антитела или его антигенсвязывающей части, где у субъекта обнаруживается снижение ответа после прекращения введения антитела или его антигенсвязывающей части, и где у субъекта сохраняется показатель PGA "отсутствие признаков" или "минимальные признаки" в течение второго длительного периода после повторного введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В одном варианте осуществления первый длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления введение антитела прекращают по меньшей мере приблизительно на 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления второй длительный период составляет по меньшей мере приблизительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 недель и предпочтительно 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в две недели. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в неделю.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в однократной дозе. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг или 200 мг.
В одном варианте осуществления псориаз представляет собой хронический псориаз.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту однократной дозы антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где после введения антитела или его антигенсвязывающей части достигают по меньшей мере одного фармакокинетического свойства, выбранного из группы, состоящей из максимальной концентрации в сыворотке (Cmax) в диапазоне от приблизительно 0,15 до приблизительно 150 мкг/мл (например, от приблизительно 0,2 до приблизительно 140 мкг/мл, от приблизительно 0,5 до приблизительно 125 мкг/мл, от приблизительно 1,0 до приблизительно 100 мкг/мл, от приблизительно 10 до приблизительно 90 мкг/мл, в диапазоне от приблизительно 25 до приблизительно 75 мкг/мл, от приблизительно 35 до приблизительно 60 мкг/мл и от приблизительно 40 до приблизительно 50 мкг/мл) и значения площади под кривой концентрация в сыворотке-время (AUC) от приблизительно 80 до приблизительно 13000 мкг × ч/мл (например, от приблизительно 100 до приблизительно 12000 мкг × ч/мл, от приблизительно 150 до приблизительно 10000 мкг × ч/мл, от приблизительно 200 до приблизительно 8000 мкг × ч/мл, от приблизительно 400 до приблизительно 6000 мкг × ч/мл, от приблизительно 800 до приблизительно 4000 мкг × ч/мл, от приблизительно 1000 до приблизительно 2000 мкг × ч/мл, от приблизительно 145 до приблизительно 13000 мкг × ч/мл и от приблизительно 80 до приблизительно 5000 мкг × ч/мл).
В одном варианте осуществления антитело вводят путем внутривенной инъекции.
В предпочтительном варианте осуществления Cmax составляет от приблизительно 1 до приблизительно 150 мкг/мл (например, от приблизительно 2 до приблизительно 125 мкг × ч/мл, от приблизительно 5 до приблизительно 100 мкг × ч/мл, от приблизительно 10 до приблизительно 80 мкг × ч/мл, от приблизительно 20 до приблизительно 60 мкг × ч/мл, от приблизительно 30 до приблизительно 50 мкг × ч/мл, от приблизительно 1 до приблизительно 20 мкг × ч/мл, от приблизительно 20 до приблизительно 300 мкг × ч/мл и от приблизительно 140 до приблизительно 150 мкг × ч/мл).
В предпочтительном варианте осуществления AUC составляет от приблизительно 145 до приблизительно 13000 мкг × ч/мл (например, от приблизительно 200 до приблизительно 11000 мкг × ч/мл, от приблизительно 500 до приблизительно 10000 мкг × ч/мл, от приблизительно 1000 до приблизительно 5000 мкг × ч/мл, от приблизительно 2000 до приблизительно 4000 мкг × ч/мл, от приблизительно 145 до приблизительно 165 мкг × ч/мл, от приблизительно 500 до приблизительно 600 мкг × ч/мл, от приблизительно 2000 до приблизительно 3000 мкг × ч/мл и от приблизительно 12000 до приблизительно 13000 мкг × ч/мл).
В одном варианте осуществления антитело вводят путем подкожной инъекции.
В предпочтительном варианте осуществления Cmax составляет от приблизительно 0,15 до приблизительно 20 мкг/мл (например, от приблизительно 0,25 до приблизительно 15 мкг/мл, от приблизительно 0,5 до приблизительно 13 мкг/мл, от приблизительно 1 до приблизительно 10 мкг/мл, от приблизительно 2 до приблизительно 8 мкг/мл, от приблизительно 0,15 до приблизительно 0,3 мкг/мл, от приблизительно 0,5 до приблизительно 2 мкг/мл, от приблизительно 2 до приблизительно 4 мкг/мл и от приблизительно 10 до приблизительно 15 мкг/мл).
В предпочтительном варианте осуществления AUC составляет от приблизительно 80 до приблизительно 5000 мкг × ч/мл (например, от приблизительно 200 до 3000 мкг × ч/мл, от приблизительно 400 до 2000 мкг × ч/мл, от приблизительно 500 до 1500 мкг × ч/мл, от приблизительно 4000 до 5000 мкг × ч/мл, от приблизительно 80 до 90 мкг × ч/мл и от приблизительно 200 до 300 мкг × ч/мл).
В одном варианте осуществления однократная доза составляет от приблизительно 0,1 до приблизительно 5,0 мг/кг (например, от приблизительно 0,1 до приблизительно 1,0 мг/кг, от приблизительно 0,1 до приблизительно 2,0 мг/кг, от приблизительно 0,1 до приблизительно 3,0 мг/кг, от приблизительно 0,1 до приблизительно 4,0 мг/кг, от приблизительно 1,0 до приблизительно 2,0 мг/кг, от приблизительно 1,0 до приблизительно 3,0 мг/кг, от приблизительно 1,0 до приблизительно 4,0 мг/кг или от приблизительно 1,0 до приблизительно 5,0 мг/кг) антитела или его антигенсвязывающей части.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту однократной дозы антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где после внутривенного введения антитела или его антигенсвязывающей части достигают по меньшей мере одного фармакокинетического свойства, выбранного из группы, состоящей из клиренса (CL) в диапазоне от приблизительно 30 до приблизительно 600 мл/ч (например, от приблизительно 50 до приблизительно 500 мл/ч, от приблизительно 75 до приблизительно 400 мл/ч, от приблизительно 100 до приблизительно 300 мл/ч, от приблизительно 150 до приблизительно 250 мл/ч, от приблизительно 30 до приблизительно 40 мл/ч, от приблизительно 40 до приблизительно 60 мл/ч и от приблизительно 500 до приблизительно 600 мл/ч) и объема распределения (Vz) в диапазоне от приблизительно 8 до приблизительно 11 л (например, от приблизительно 8 до приблизительно 10 л, от приблизительно 8 до приблизительно 9 л, от приблизительно 9 до приблизительно 10 л, от приблизительно 10 до приблизительно 11 л и от приблизительно 8,5 до 9,5 л).
В родственном аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту однократной дозы антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где после подкожного введения антитела или его антигенсвязывающей части достигают по меньшей мере одного фармакокинетического свойства, выбранного из группы, состоящей из кажущегося клиренса (CL/F) в диапазоне от приблизительно 90 до приблизительно 250 мл/ч (например, от приблизительно 100 до приблизительно 225 мл/ч, от приблизительно 125 до приблизительно 200 мл/ч, от приблизительно 140 до приблизительно 180 мл/ч, от приблизительно 90 до приблизительно 100 мл/ч, от приблизительно 150 до приблизительно 200 мл/ч и от приблизительно 200 до приблизительно 250 мл/ч) и кажущегося объема распределения (V/F) в диапазоне от приблизительно 23 до приблизительно 67 л (например, от приблизительно 25 до приблизительно 60 л, от приблизительно 30 до приблизительно 55 л, от приблизительно 35 до приблизительно 50 л, от приблизительно 40 до приблизительно 45 л, от приблизительно 23 до приблизительно 35 л и от приблизительно 60 до приблизительно 70 л).
В одном варианте осуществления однократная доза составляет от приблизительно 0,1 до приблизительно 5,0 мг/кг (например, от приблизительно 0,1 до приблизительно 1,0 мг/кг, от приблизительно 0,1 до приблизительно 2,0 мг/кг, от приблизительно 0,1 до приблизительно 3,0 мг/кг, от приблизительно 0,1 до приблизительно 4,0 мг/кг, от приблизительно 1,0 до приблизительно 2,0 мг/кг, от приблизительно 1,0 до приблизительно 3,0 мг/кг, от приблизительно 1,0 до приблизительно 4,0 мг/кг или от приблизительно 1,0 до приблизительно 5,0 мг/кг) антитела или его антигенсвязывающей части.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта проявляется ответ PASI 75 после начального введения антитела или его антигенсвязывающей части, где у субъекта обнаруживается снижение ответа после прекращения введения антитела или его антигенсвязывающей части, и где у субъекта проявляется по меньшей мере ответ PASI 75 приблизительно через 25 суток после повторного введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В одном варианте осуществления у субъекта проявляется по меньшей мере ответ PASI 75 приблизительно через 50 суток после повторного введения антитела или его антигенсвязывающей части. В одном варианте осуществления у субъекта проявляется по меньшей мере ответ PASI 75 приблизительно через 60 суток после повторного введения антитела или его антигенсвязывающей части. В одном варианте осуществления у субъекта проявляется по меньшей мере ответ PASI 75 приблизительно через 30, 35, 40, 45, 50, 60, 65, 70, 75, 80, 85, 90 или более суток после повторного введения антитела или его антигенсвязывающей части.
В одном варианте осуществления начальное введение антитела проводят в течение по меньшей мере приблизительно 12 недель.
В одном варианте осуществления введение антитела прекращают по меньшей мере приблизительно на 4, 5, 6, 7, 8, 9, 10, 11 или 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в две недели. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в неделю. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в однократной дозе.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг или 200 мг.
В одном варианте осуществления псориаз представляет собой хронический псориаз.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта проявляется ответ PASI 75 после начального введения антитела или его антигенсвязывающей части, где у субъекта обнаруживается снижение ответа приблизительно через 60 суток после прекращения введения антитела или его антигенсвязывающей части, и где у субъекта достигается ответ PASI 75 после повторного введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В одном варианте осуществления у субъекта обнаруживается снижение ответа приблизительно через 120 суток после прекращения введения антитела или его антигенсвязывающей части. В одном варианте осуществления у субъекта обнаруживается снижение ответа приблизительно через 180 суток после прекращения введения антитела или его антигенсвязывающей части. В одном варианте осуществления у субъекта обнаруживается снижение ответа приблизительно через 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200 или более суток после прекращения введения антитела или его антигенсвязывающей части.
В одном варианте осуществления начальное введение антитела проводят в течение по меньшей мере приблизительно 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в две недели. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят раз в неделю. В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в однократной дозе.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг или 200 мг.
В одном варианте осуществления псориаз представляет собой хронический псориаз.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту раз в две недели, раз в неделю или однократной дозы антитела или его антигенсвязывающей части, направленных против IL-12 человека и/или IL-23 человека. В родственном аспекте изобретение относится к способу лечения псориаза у субъекта, включающему стадии: (i) выбора субъекта, который страдает хроническим псориазом; и (ii) введения субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23; тем самым осуществляя лечение хронического псориаза у субъекта.
В другом родственном аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта сохраняется по меньшей мере ответ PASI 50, по меньшей мере ответ PASI 75 или по меньшей мере ответ PASI 90 в течение длительного периода после прекращения введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта сохраняется показатель PGA "отсутствие признаков" или "минимальные признаки" в течение длительного периода после начального введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антигенсвязывающей части, которые способны связываться с эпитопом субъединицы p40 IL-12 и/или IL-23, где у субъекта обнаруживается улучшенный показатель PASI приблизительно через 8 недель после начального введения антитела или его антигенсвязывающей части, тем самым осуществляя лечение псориаза у субъекта. В одном варианте осуществления у субъекта обнаруживается улучшенный показатель PASI приблизительно через 7 недель, приблизительно через 6 недель, приблизительно через 5 недель, приблизительно через 4 недели, приблизительно через 3 недели, приблизительно через 2 недели или приблизительно через 1 неделю после начального введения антитела или его антигенсвязывающей части.
В одном варианте осуществления длительный период после прекращения введения антитела составляет по меньшей мере приблизительно 12 недель. В одном варианте осуществления длительный период составляет по меньшей мере приблизительно 12, 13, 14, 15, 16, 17, 18, 19, 20 недель, 21 неделю, 22, 23 или 24 недели. В одном варианте осуществления антитело вводят в течение по меньшей мере приблизительно 12 недель.
В одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, способны связываться с эпитопом субъединицы p40 IL-12.
В другом варианте осуществления антитело или его антигенсвязывающая часть способны связываться с эпитопом субъединицы p40, когда субъединица p40 связана с субъединицей p35 IL-12. В другом варианте осуществления антитело или его антигенсвязывающая часть способны связываться с эпитопом субъединицы p40, когда субъединица p40 связана с субъединицей p19. В одном варианте осуществления антитело или его антигенсвязывающая часть способны связываться с эпитопом субъединицы p40, когда субъединица p40 связана с субъединицей p35 IL-12 и когда субъединица p40 связана с субъединицей p19.
В одном варианте осуществления антитело или его антигенсвязывающая часть связываются с эпитопом субъединицы p40 IL-12, с которым связывается антитело, выбранное из группы, состоящей из Y61 и J695.
В другом варианте осуществления антитело, кроме того, способно связываться с первым гетеродимером, а также оно способно связываться со вторым гетеродимером, где первый гетеродимер содержит субъединицу p40 IL-12 и субъединицу p35 IL-12, и где второй гетеродимер содержит субъединицу p40 IL-12 и субъединицу p19.
В еще одном варианте осуществления антитело нейтрализует активность первого гетеродимера. В другом варианте осуществления антитело нейтрализует активность второго гетеродимера. В другом варианте осуществления антитело нейтрализует активность первого гетеродимера и второго гетеродимера.
В еще одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе PHA in vitro с IC50 1×10-9 M или менее, или ингибируют продукцию IFNγ человека с IC50 1×10-10 M или менее.
В одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, диссоциируют от субъединицы p40 IL-12 с Kd 1×10-10 M или менее или константой скорости koff 1×10-3 с-1 или менее, как определено поверхностным плазмонным резонансом.
В одном варианте осуществления выделенное антитело или его антигенсвязывающая часть, используемые в способах по изобретению, представляют собой химерное антитело, гуманизированное антитело или антитело человека.
В другом варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, имеют CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:25, и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:26.
В еще одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, имеют CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:27, и CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:28.
В одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, имеют CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:29, и CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:30.
В другом варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, способны связываться с интерлейкином, содержащим субъединицу p40. В одном варианте осуществления интерлейкин содержит субъединицу p40 и субъединицу p35, например, интерлейкин представляет собой IL-12. В другом варианте осуществления интерлейкин содержит субъединицу p40 и субъединицу p19. В другом варианте осуществления антитело или его антигенсвязывающая часть нейтрализуют активность интерлейкина.
В одном варианте осуществления антитело или его антигенсвязывающая часть связываются с эпитопом субъединицы p40.
В одном варианте осуществления антитело или его антигенсвязывающую часть вводят субъекту в фармацевтической композиции, содержащей антитело или его антигенсвязывающую часть и фармацевтически приемлемый носитель. Фармацевтическая композиция также может содержать дополнительное средство, такое как лекарственное средство, например, буденозид, эпидермальный фактор роста, кортикостероиды, циклоспорин, сульфасалазин, аминосалицилаты, 6-меркаптопурин, азатиоприн, метронидазол, ингибиторы липоксигеназы, месаламин, олсалазин, балсалазид, антиоксиданты, ингибиторы тромбоксана, антагонисты рецептора IL-1, моноклональные антитела против IL-1β, моноклональные антитела против IL-6, факторы роста, ингибиторы эластазы, пиридинил-имидазольные соединения, антитела к TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-15, IL-16, IL-18, EMAP-II, GM-CSF, FGF и PDGF или их агонисты, антитела к CD2, CD3, CD4, CD8, CD25, CD28, CD30, CD40, CD45, CD69, CD90 или их лиганды, метотрексат, циклоспорин, FK506, рапамицин, микофенолата мофетил, лефлуномид, NSAID (НПВС), ибупрофен, кортикостероиды, преднизолон, ингибиторы фосфодиэстеразы, агонисты аденозина, антитромботические средства, ингибиторы комплемента, адренергические средства, IRAK, NIK, IKK, p38, ингибиторы MAP-киназы, ингибиторы IL-1β-превращающего фермента, ингибиторы TNFα-превращающего фермента, ингибиторы T-клеточной передачи сигнала, ингибиторы металлопротеиназы, сульфасалазин, азатиоприн, 6-меркаптопурины, ингибиторы ангиотензинпревращающего фермента, растворимые рецепторы цитокинов, растворимый рецептор p55 TNF, растворимый рецептор p75 TNF, sIL-1RI, sIL-1RII, sIL-6R, противовоспалительные цитокины, IL-4, IL-10, IL-11, IL-13 и TGFβ.
В другом варианте осуществления лекарственное средство в фармацевтической композиции, вводимое субъекту, может быть выбрано из группы, состоящей из антител против TNF и фрагментов этих антител, конструкций TNFR-Ig, ингибиторов TACE, ингибиторов PDE4, кортикостероидов, буденозида, дексаметазона, сульфасалазина, 5-аминосалициловой кислоты, олсалазина, ингибиторов IL-1β-превращающего фермента, IL-1ra, ингибиторов тирозинкиназы, 6-меркаптопуринов и IL-11.
В другом варианте осуществления лекарственное средство может быть выбрано из группы, состоящей из кортикостероидов, преднизолона, метилпреднизолона, азатиоприна, циклофосфамида, циклоспорина, метотрексата, 4-аминопиридина, тизанидина, интерферона-β1a, интерферона-β1b, сополимера 1, гипербарического кислорода, внутривенного иммуноглобулина, клабрибина, антител к TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-15, IL-16, IL-18, EMAP-II, GM-CSF, FGF, PDGF или их агонистов, антител к CD2, CD3, CD4, CD8, CD25, CD28, CD30, CD40, CD45, CD69, CD80, CD86, CD90 или их лигандов, метотрексата, циклоспорина, FK506, рапамицина, микофенолата мофетила, лефлуномида, NSAID (НПВС), ибупрофена, кортикостероидов, преднизолона, ингибиторов фосфодиэстеразы, агонистов аденозина, антитромботических средств, ингибиторов комплемента, адренергических средств, IRAK, NIK, IKK, p38 или ингибиторов MAP-киназы, ингибиторов IL-1β-превращающего фермента, ингибиторов TACE, ингибиторов T-клеточной передачи сигнала, ингибиторов киназы, ингибиторов металлопротеиназы, сульфасалазина, азатиоприна, 6-меркаптопуринов, ингибиторов ангиотензинпревращающего фермента, растворимых рецепторов цитокинов, растворимых рецепторов p55 TNF, растворимых рецепторов p75 TNF, sIL-1RI, sIL-1RII, sIL-6R, sIL-13R, антитела против P7s, гликопротеинового лиганда p-селектина (PSGL), противовоспалительных цитокинов, IL-4, IL-10, IL-13 и TGFβ.
В одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, связываются с IL-12 человека и/или IL-23 человека и диссоциируют от IL-12 человека и/или IL-23 человека, соответственно, с Kd 1×10-10 M или менее и константой скорости koff 1×10-3с-1 или менее, как определено поверхностным плазмонным резонансом. В одном варианте осуществления антитело или его антигенсвязывающая часть диссоциируют от IL-12 человека и/или IL-23 человека с константой скорости koff 1×10-4с-1 или менее. В другом варианте осуществления антитело или его антигенсвязывающая часть диссоциируют от IL-12 человека и/или IL-23 человека с константой скорости koff 1×10-5с-1 или менее.
В другом варианте осуществления антитело или его антигенсвязывающая часть связываются с IL-12 человека и/или IL-23 человека и диссоциируют от IL-12 человека и/или IL-23 человека, соответственно, с константой скорости koff 1×10-2с-1 или менее, как определено поверхностным плазмонным резонансом. В другом варианте осуществления антитело или его антигенсвязывающая часть диссоциируют от IL-12 человека и/или IL-23 человека с константой скорости koff 1×10-3с-1 или менее. В другом варианте осуществления антитело или его антигенсвязывающая часть диссоциируют от IL-12 человека и/или IL-23 человека с константой скорости koff 1×10-4с-1 или менее. В другом варианте осуществления антитело или его антигенсвязывающая часть диссоциируют от IL-12 человека и/или IL-23 человека с константой скорости koff 1×10-5с-1 или менее.
В другом варианте осуществления антитело или его антигенсвязывающая часть связываются с IL-12 человека и/или IL-23 человека и диссоциируют от IL-12 человека и/или IL-23 человека, соответственно, с Kd 1,34×10-10 M или менее. В другом варианте осуществления антитело или его антигенсвязывающая часть связываются с IL-12 человека и/или IL-23 человека и диссоциируют от IL-12 человека и/или IL-23 человека, соответственно, с Kd 9,74×10-11 M или менее. В одном варианте осуществления антитело или его антигенсвязывающая часть представляют собой рекомбинантное антитело или его антигенсвязывающую часть.
В одном варианте осуществления антитело или его антигенсвязывающая часть, используемые в способах по изобретению, представляют собой нейтрализующее антитело, например, они нейтрализуют активность IL-12 человека и/или IL-23 человека. В одном варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе PHA in vitro с IC50 1×10-9 M или менее. В другом варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе PHA in vitro с IC50 1×10-10 M или менее. В другом варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе PHA in vitro с IC50 1×10-11 M или менее. В другом варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе пролиферации бластных клеток при стимуляции фитогемагглютинином in vitro (анализе PHA) с IC50 1×10-7 M или менее. В другом варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют пролиферацию бластных клеток при стимуляции фитогемагглютинином в анализе PHA in vitro с IC50 1×10-8 M или менее. В одном варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют продукцию IFNγ человека с IC50 1×10-10 M или менее. В другом варианте осуществления нейтрализующее антитело или его антигенсвязывающая часть ингибируют продукцию IFNγ человека с IC50