Пептиды с большим числом мостиковых связей, выделяемые из actinomadura namibiensis
Иллюстрации
Показать всеГруппа изобретений относится к биохимии. Предложены соединения лабиринтопептинов А1, А2, или А3 формулы (I), где {A}, {B}, {C}, R1-R6, m и n имеют значения, указанные в формуле изобретения. Соединения получают при ферментации штамма Actinomadura namibiensis DSM 6313 в приемлемых условиях в культуральной среде до образования одного или нескольких соединений формулы (I). Предложены ДНК, кодирующая препролабиринтопептин А2, и ДНК, кодирующая препролабиринтопептин А1, а также препролабиринтопептины А1 и А2, пролабиринтопептины А1 и А2. Лабиринтопептины формулы (I) применяют для лечения инфекций, вызываемых грамположительными бактериями, вирусных инфекций и/или невропатической боли, вызываемой воспалением. 11 н. и 13 з. п. ф-лы, 4 табл., 20 пр.
Реферат
В научной литературе описано несколько пептидов с большим числом мостиковых связей, таких как, например, конопептиды, выделяемые из брюхоногих моллюсков с колпачковидной раковиной (см., например, публикацию Terlau & Olivera, Physiol. Rev. 2004, 84, 41-68), или так называемые лантибиотики (Chatterjee et al., Chem. Rev. 2005, 105, 633-683), выделяемые из грамположительных бактерий. Указанные пептиды имеют разные применения. Лантибиотик низин, например, в течение многих лет используется в качестве консерванта для пищевых продуктов.
Конопептиды могут быть использованы для лечения боли, диабета, рассеянного склероза и сердечно-сосудистых заболеваний и в настоящее время проходят преклинические или клинические испытания. Примерами конопептидов являются α-GI (последовательность: ECCNPACGRHYSC*, *амидированная, связность: 1-3, 2-4) и α-GID (последовательность: IRγCCSNPACRVNNOHVC, связность: 1-3, 2-4), где О/Hyp означает гидроксипролин, и связность определяет положение цистеина в конкретных дисульфидных связях, например первый - третий и второй - четвертый, как в α-GID:
(α-GI),
(α-GID).
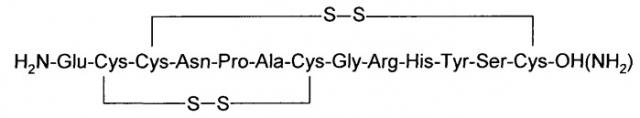
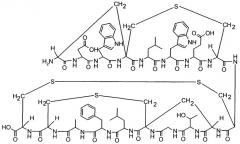
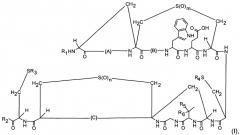
Недавно была обнаружена новая группа пептидов с большим числом мостиковых связей, получивших название лабиринтопептины (заявка на европейский патент ЕР06020980.6). Так называемые лабиринтопептины содержат уникальный мостиковый фрагмент в пептидной цепи, иллюстрируемый соединением нижеследующей формулы:
В настоящее время установлено, что другие пептиды с большим числом мостиковых связей, относящиеся к классу лабиринтопептинов, могут быть выделены из штамма микроорганизмов Actinomadura namibiensis (DSM 6313). Указанные соединения существенно отличаются от производных лабиринтопептинов, описанных в заявке на патент ЕР 06020980.6.
Объектом настоящего изобретения является соединение формулы (I)
где
{A} означает группу, выбираемую из
{B} означает группу, выбираемую из
{C} означает группу, выбираемую из
R1 означает группу R1' или группу
где R1' означает Н, С (О)-(С1-С6)алкил или С(О)-О-(С1-С6)алкил;
R2 означает ОН, NH2, NH-(C1-C6)алкил, NH-(C1-C4)алкиленфенил или NH-(C1-C4)алкиленпиридил;
R3 и R4 независимо означают Н, (C1-C6)алкил, (C1-C6)алкилен-С(О)NH2, (С1-С6)алкилен-С(О)NH(С1-С4)алкил или (С1-С6)алкилен-С(О)N[(C1-C4)алкил]2, либо R3 и R4 вместе с атомами S, к которым они присоединены, образуют дисульфидную группу S-S;
R5 и R6 независимо означают Н или ОН, либо R5 и R6 вместе означают = О;
m и n независимо равны 0, 1 или 2;
при условии, что если
{A} означает
{B} означает
{C} означает
R3 и R4 не могут образовывать дисульфидную группу S-S вместе с атомами S, к которым они присоединены;
которое имеет любую стереохимическую форму или представляет собой смесь любых стереохимических форм в любом соотношении либо является его физиологически приемлемой солью.
В предпочтительном варианте осуществления изобретения
{A} означает
{B} означает
{C} означает
В другом предпочтительном варианте осуществления изобретения
{A} означает
{B} означает
{C} означает
R1 предпочтительно означает группу R1'.
R1' предпочтительно означает Н.
R2 предпочтительно означает ОН.
R3 и R4 предпочтительно независимо означают Н, (С1-С6)алкил, (С1-С6)алкилен-С (О)NH2 или образуют дисульфидную группу S-S вместе с атомами S, к которым они присоединены. Более предпочтительно R3 и R4 означают Н или образуют дисульфидную группу S-S вместе с атомами S, к которым они присоединены. Наиболее предпочтительно R3 и R4 образуют дисульфидную группу S-S вместе с атомами S, к которым они присоединены.
R5 и R6 предпочтительно означают Н или ОН, при этом если R5 означает ОН, тогда R6 означает Н, и если R5 означает Н, тогда R6 означает ОН, или R5 и R6 вместе означают =О. Более предпочтительно R5 означает ОН и R6 означает Н или R5 означает Н и R6 означает ОН.
В предпочтительном варианте осуществления изобретения соединение (I) является соединением формулы (II)
в котором R1 означает R1' или группу
где R1' означает Н, С (О) - (С1-С6)алкил или С (О)- О- (С1-С6)алкил, предпочтительно Н.
В другом предпочтительном варианте осуществления изобретения соединение (I) является соединением формулы (III)
в котором R1 означает R1' или группу
где R1' означает Н, С (О) - (С1-С6)алкил или С(О)-О-(С1-С6)алкил, предпочтительно Н;
R2 означает ОН, NH2, NH-(C1-C6)алкил, N[(C1-C6)алкил]2, NH-(C1-C4)алкиленфенил или NH-(C1-C4)алкиленпиридил, R2 предпочтительно означает Н; и
R3 и R4 независимо означают Н, (С1-С6)алкил или (С1-С4)алкилен-С(О)NH2.
Соединения формул (II) и (III), где R1 означает R1', далее именуются лабиринтопептинами А1 .
Соединения формул (II) и (III), где R1 означает группу
далее именуются лабиринтопептинами А3.
В другом предпочтительном варианте осуществления изобретения соединение (I) является соединением формулы (IV)
в котором R1 означает Н, С (О) - (С1-С6)алкил или С (О) - О -(С1-С6)алкил;
R2 означает ОН, NH2, NH-(C1-C6)алкил, N[(C1-C6)алкил]2, NH-(C1-C4)алкиленфенил или NH-(C1-C4)алкиленпиридил; и
R3 и R4 независимо означают Н, (С1-С6)алкил или (С1-С4)алкилен-С(О)NH2.
Соединения формулы (IV) именуются лабиринтопептинами А 2.
В соединениях формулы (I) предпочтительно m и n оба равны 0, или m и n оба равны 2, или m равно 0 и n равно 2, или m равно 2 и n равно 0. Наиболее предпочтительно m и n оба равны 0.
Настоящее изобретение далее относится ко всем очевидным химическим эквивалентам соединений формулы (I) по настоящему изобретению. Такие эквиваленты являются соединениями, которые имеют лишь незначительные отличия в химической структуре и оказывают такое же фармакологическое действие или могут быть превращены в соединения по настоящему изобретению в мягких условиях. Указанные эквиваленты включают также, например, соли, продукты восстановления, продукты окисления, сложные эфиры, полученные в результате частичного гидролиза, простые эфиры, ацетали или амиды соединений формулы (I), а также эквиваленты, которые специалист может получить стандартными методами, и, помимо этого, все оптические изомеры, диастереомеры и все стереоизомерные формы.
За исключением особо оговоренных случаев хиральные центры в соединениях формулы (I) могут находиться в R-конфигурации или S-конфигурации. Настоящее изобретение относится как к оптически чистым соединениям, так и к смесям стереоизомеров, таким как смеси энантиомеров и смеси диастереомеров.
Физиологически переносимые соли соединений формулы (I) являются их органическими и неорганическими солями, описанными в публикации Remington's Pharmaceutical Sciences (17th edition, page 1418 (1985)). Благодаря их физической и химической стойкости и растворимости предпочтительными являются, среди прочего, соли натрия, калия, кальция и аммония, при наличии кислотных групп; соли хлористоводородной кислоты, серной кислоты или фосфорной кислоты, карбоновых или сульфоновых кислот, таких как уксусная кислота, лимонная кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, винная кислота и паратолуолсульфоновая кислота, среди прочего, являются предпочтительными при наличии основных групп.
Более предпочтительно соединения формул (I)-(IV) характеризуются стереохимией, показанной для соединения формулы (V), которое является соединением формулы (I), в котором
{A} означает
{B} означает
{C} означает
R1 означает
где R1' означает Н;
R2 означает Н;
R3 и R4 вместе с атомами S, к которым они присоединены, образуют дисульфидную группу S-S;
R5 означает Н;
R6 означает ОН; и
m и n равны 0:
наиболее предпочтительно стереохимией, представленной в формуле (VI)
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), имеющему формулу (VII),
предпочтительно формулу (VIII)
при этом формулы (V) и (VI) относятся к лабиринтопептину А3, и формулы (VII) и (VIII) относятся к лабиринтопептину А1.
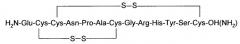
Для дальнейшего исследования соединений по настоящему изобретению пептидные остатки были превращены в их вероятные предшественники, получаемые в результате синтеза пептидов на рибосомах. В научной литературе отсутствует описание альфа, альфа-дизамещенных аминокислот в положении остатков 4 и 13. Указанные аминокислоты могут быть описаны на основании остатка Ser, в котором замещена гидроксильная группа в бета-положении, как показано ниже для соединений формул (II) и (III):
(SEQ ID NO:1).
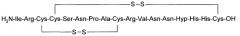
В предшествующей заявке на европейский патент, относящейся к лабиринтопептину А2 (ЕР06020980.6), при отсутствии знаний о биосинтезе была представлена следующая последовательность предшественника, синтезируемого на рибосомах:
(SEQ ID NO:2).
С учетом новых знаний о биосинтезе лабиринтопептинов (см. ниже) биосинтетический предшественник соединений формулы (IV) представлен следующим образом:
(SEQ ID NO:3).
Настоящее изобретение относится также к способу получения соединения формулы (I) по пункту 1, который включает:
а) ферментацию штамма Actinomadura namibiensis (DSM 6313) или одного из его вариантов и/или мутантов в приемлемых условиях в культуральной среде до образования одного или нескольких соединений формулы (I) в указанной культуральной среде;
b) выделение соединения формулы (I) из культуральной среды;
с) модификацию, при необходимости, соединения, выделенного на стадии b), и/или превращение, при необходимости, соединения, выделенного на стадии b), или производного соединения, выделенного на стадии b), в физиологически переносимую соль.
Соединение, выделенное на стадии b), предпочтительно имеет формулу (II), где m и n оба равны 0,
R1 означает R1' или группу
где R1' означает Н, и
R2 означает ОН.
Соединение, выделенное на стадии b), более предпочтительно является лабиринтопептином А2, который затем превращают на стадии с) в соединение формулы (IV), где m и n оба равны 0,
R1 означает Н,
R2 означает ОН, и
R3 и R4 независимо означают Н, (С1-С6)алкил, (С1-С6)алкилен-С (О)NH2, (С1-С6)алкилен-С (О)NH(C1-C4)алкил или (С1-С6)алкилен-С(О)N[(C1-C4)алкил]2.
Культуральная среда является питательным раствором или плотной средой, содержащей по меньшей мере один обычный источник углерода и по меньшей мере один источник азота, а также одну или несколько обычных неорганических солей.
Способ по настоящему изобретению может быть использован для ферментации в лабораторных условиях (в диапазоне от миллилитров до литров) и для ферментации в промышленном масштабе (в диапазоне кубических метров).
Приемлемыми источниками углерода для ферментации являются ассимилируемые углеводы и сахарные спирты, такие как глюкоза, лактоза, сахароза или D-маннит, а также углеводсодержащие природные продукты, такие как солодовый экстракт или дрожжевой экстракт. Примерами азотсодержащих питательных веществ являются аминокислоты; пептиды и белки, а также их продукты распада, например казеин, пептоны или триптоны; мясные экстракты; дрожжевые экстракты; глютен; семена, например, кукурузы, пшеницы, фасоли, сои или хлопчатника; остатки после дистилляции при получении спирта; мясо; дрожжевые экстракты; соли аммония; нитраты. Предпочтительным является источник азота, представляющий собой один или несколько пептидов, полученных путем синтеза или биосинтеза. Примерами неорганических солей являются хлориды, карбонаты, сульфаты или фосфаты щелочных металлов, щелочноземельных металлов, железа, цинка, кобальта и марганца. Примерами следовых элементов являются кобальт и марганец.
Лабиринтопептины по настоящему изобретению получают в нижеследующих особенно приемлемых условиях: 0,05-5%, предпочтительно 0,1-2,5% дрожжевого экстракта; 0,2-5,0%, предпочтительно 0,1-2% казитона; 0,02-1,0%, предпочтительно 0,05-0,5% CaCl2 × 2H2O; 0,02-1,5%, предпочтительно 0,05-0,7% MgSO4 × 7H2O и 0,00001-0,001% витамина В12. Указанные процентные значения приведены в расчете на массу всего питательного раствора.
Указанный микроорганизм культивируют в аэробных условиях, то есть, например, в состоянии погружения в питательную среду при встряхивании или перемешивании во встряхиваемых колбах или ферментерах либо на плотной среде при подаче воздуха или кислорода. Указанный микроорганизм можно культивировать в температурном интервале от около 18°С до 35°С, предпочтительно от около 20°С до 32°С, в частности от 27°С до 30°С. Показатель рН должен находиться в пределах от 4 до 10, предпочтительно от 6,5 до 7,5. Микроорганизм обычно культивируют в указанных условиях в течение 2-10 дней, предпочтительно от 72 до 168 часов. Микроорганизм предпочтительно культивируют в несколько стадий, то есть сначала получают одну или несколько предварительных культур в жидкой питательной среде, после чего указанные предварительные культуры инокулируют в стандартную производственную питательную среду, то есть основную культуру, например, в объемном отношении от 1:10 до 1:100. Предварительную культуру получают, например, путем инокуляции штамма в виде растительных клеток или спор в питательный раствор и выращивания в течение 20-120 часов, предпочтительно 48-96 часов. Растительные клетки и/или споры можно получить, например, выращивая штамм в течение примерно 1-15 дней, предпочтительно 4-10 дней на плотном или жидком питательном субстрате, таком как агар с дрожжевым экстрактом.
Производные лабиринтопептинов могут быть выделены из культуральной среды и очищены известными методами с учетом химических, физических и биологических свойств природных веществ. Концентрации соответствующих производных лабиринтопептинов в культуральной среде или на отдельных стадиях выделения определяют при помощи ВЭЖХ, при этом количество образованного вещества сравнивают с калибровочным раствором.
Для выделения продукта культуральный бульон или культуру вместе с плотной средой необязательно лиофилизуют и производные лабиринтопептинов экстрагируют из лиофилизата, используя органический растворитель или смесь воды и органического растворителя, предпочтительно содержащую 50-90% органического растворителя. Примерами органических растворителей являются метанол и 2-пропанол. Фазу органического растворителя, содержащую природные вещества по настоящему изобретению, при необходимости концентрируют в вакууме и подвергают дальнейшей очистке.
Последующую очистку одного или нескольких соединений по настоящему изобретению производят при помощи хроматографии на приемлемых материалах, например предпочтительно на молекулярном сите, силикагеле, оксиде алюминия, ионообменных смолах, адсорбирующих смолах или обращенных фазах (RP). Указанную хроматографию используют для выделения производных лабиринтопептинов. Производные лабиринтопептинов хроматографируют, используя буферные, основные или подкисленные водные растворы или смеси водных и органических растворов.
Смеси водных или органических растворов включают все смешивающиеся с водой органические растворители, предпочтительно метанол, 2-пропанол или ацетонитрил, при концентрации органического растворителя от 5 до 99%, предпочтительно от 5 до 50% органического растворителя, или все буферные водные растворы, смешивающиеся с органическими растворителями. Используемые буферы аналогичны указанным выше.
Производные лабиринтопептинов выделяют с учетом их разной полярности при помощи хроматографии с обращенной фазой, например, на MCl (адсорбирующая смола, Mitsubishi, Japan), амберлите XAD (TOSOHAAS) или других гидрофобных материалах, например на фазах RP-8 или RP-18. Кроме того, могут быть выделение можно осуществить при помощи хроматографии с нормальной фазой, например, на силикагеле, оксиде алюминия и подобных веществах.
Буферные, основные или подкисленные водные растворы, например, представляют собой воду, фосфатный буфер, аммоний-ацетатный и цитратный буфер, в концентрации до 0,5 М, а также муравьиную кислоту, уксусную кислоту, трифторуксусную кислоту, аммиак и триэтиламин или все коммерчески доступные кислоты и основания, известные специалисту, предпочтительно в концентрации до 1%. В случае буферных водных растворов особенно предпочтительным является 0,1% ацетат аммония.
Хроматография может быть выполнена в градиенте, начиная со 100% воды и кончая 100% органического растворителя; хроматографию предпочтительно выполняют в линейном градиенте от 5 до 95% ацетонитрила.
Альтернативно может быть выполнена гель-хроматография или хроматография на гидрофобных фазах. Гель-хроматография может быть выполнена, например, на полиакриламидных гелях или сополимерных гелях. Последовательность выполнения вышеуказанных стадий хроматографии может быть изменена.
Лабиринтопептины, присутствующие в виде стереоизомеров, могут быть выделены известными методами, например путем отделения на колонке для хиральной хроматографии.
Группу ОН превращают в сложноэфирное или простое эфирное производное при помощи известных методов (J. March, Advanced Organic Chemistry, John Wiley & Sons, 4th edition, 1992), например, в результате осуществления взаимодействия с ангидридом кислоты, диалкилкарбонатом или диалкилсульфатом. Группу СООН превращают в сложноэфирное или амидное производное известными методами (J. March, Advanced Organic Chemistry, John Wiley & Sons, 4th edition, 1992), например, в результате осуществления взаимодействия с аммиаком с образованием соответствующей группы CONH2, или с необязательно активированным алкильным соединением с образованием соответствующего сложного алкилового эфира. Группы -СН2-S-CH2- можно окислить в группу -СН2-S(O)-CH2- или -СН2-S(O)2-CH2-, подвергая соответствующее производное лабиринтопептина воздействию кислорода или воздуха. Восстановление дисульфидов, необязательно с последующим алкилированием свободных групп SH, выполняют известными методами (A. Henschen, Analysis of cyst(e)ine residues, disulfide bridges, and sulfhydryl groups in proteins, in: B. Wittmann-Liebold, J. Salnikov, V.A. Erdman (Eds.), Advanced Methods in Protein Microsequence Analysis, Springer, Berlin, 1986, pp. 244-255), например, путем восстановления дитиотреитом и алкилирования с использованием алкилиодидов. Восстановление сульфида в соединении формулы (I), где R3 и R4 означают Н, (С1-С6)алкил, (С1-С6)алкилен-С(О)NH2, (C1-C6)алкилен-С(О)NH(C1-C4)алкил или (С1-С6)алкилен-С(О)N[(C1-C4)алкил]2, может быть произведено путем осуществления взаимодействия соединения формулы (I), где R3 и R4 образуют дисульфидную группу S-S вместе с атомами S, к которым они присоединены, с (С1-С6)алкилгалогенидом или галоген(С1-С6)алкилен-С(О)NH2, галоген(С1-С6)алкилен-С(О)NH(C1-C4)алкилом или галоген-(С1-С6)алкилен-С(О)N[(C1-C4)алкил]2 в присутствии дитиотреита (общая литература). Галоген является F, Cl, Br или I.
Штамм микроорганизмов Actinomadura namibiensis был депонирован Hoechst AG., Франкфурт, Германия, под идентифицирующим номером FH-A 1198 в Deutsche Sammlung von Mikroorganismen und Zellkulturen [Германская коллекция микроорганизмов и культур клеток] GmbH (DSMZ), Mascheroder Weg 1B (2008: Inhoffenstr. 7 B), 38124 Braunschweig, Germany, согласно положениям Будапештского соглашения от 23.01.1991 под следующим номером: DSM 6313. Штамм микроорганизмов Actinomadura namibiensis описан в публикации Wink et al. in International Journal of Systematic and Evolutionary Mictobiology 2003, 53, 721-724.
Вместо штамма Actinomadura namibiensis (DSM 6313) можно также использовать его мутанты и/или варианты, синтезирующие одно или несколько соединений по настоящему изобретению.
Мутант является микроорганизмом, в котором изменен один или несколько генов в геноме, при этом ген или гены, определяющие способность организма продуцировать соединение по настоящему изобретению, остаются функциональными и наследуемыми.
Такие мутанты могут быть получены известными методами с использованием физических средств, например облучения ультрафиолетовыми или рентгеновскими лучами, или химических мутагенов, таких как этилметансульфонат (EMS), 2-гидрокси-4-метоксибензофенон (МОВ) или N-метил-N'-нитро-N-нитрозогуанидин (MNNG), или методами, описанными в публикации Brock et al. in “Biology of Microorganisms”, Prentice Hall, pages 238-247 (1984).
Вариант является фенотипом микроорганизма. Микроорганизмы обладают способностью адаптироваться к окружающей среде и поэтому характеризуются высокоразвитой физиологической гибкостью. Все клетки микроорганизма участвуют в фенотипической адаптации, при этом характер изменения генетически не закреплен и может быть обратимым в изменившихся условиях (H. Stolp, Mictobial ecology: organism, habitats, activities. Cambridge University Press, Cambridge, GB, page 180, 1988).
Скрининг мутантов и/или вариантов, синтезирующих одно или несколько соединений по настоящему изобретению, производят путем необязательной лиофилизации ферментационной среды, экстракции лиофилизата или ферментационного бульона органическим растворителем или вышеуказанной смесью воды и органического растворителя и анализа методом ВЭЖХ или ТСХ или исследования биологической активности.
Условия ферментации аналогичны для Actinomadura namibiensis (DSM 6313), его мутантов и/или вариантов.
Другой вариант осуществления настоящего изобретения относится к применению соединения формулы (I) для лечения бактериальных инфекций, в частности бактериальных инфекций, вызываемых грамположительными бактериями, для лечения вирусных инфекций и/или для лечения боли, в частности невропатической боли или боли, вызываемой воспалением.
Вышеописанное лекарственное средство (именуемое также фармацевтическим препаратом или фармацевтической композицией) содержит эффективное количество по меньшей мере одного соединения формулы (I) в любой стереохимической форме или в виде смеси любых стереохимических форм в любом соотношении, его физиологически переносимой соли или химического эквивалента и по меньшей мере один фармацевтически приемлемый носитель, предпочтительно один или несколько фармацевтически приемлемых носителей (или сред) и/или добавок (или наполнителей).
Лекарственное средство можно вводить перорально, например, в форме пилюль, таблеток, глазурованных таблеток, таблеток с покрытием, гранул, твердых и мягких желатиновых капсул, растворов, сиропов, эмульсий, суспензий или аэрозольных смесей. Однако указанное лекарственное средство можно также вводить ректально, например, в форме суппозиториев, или парентерально, например, внутривенно, внутримышечно или подкожно, в виде инъекционных растворов или растворов для вливаний, микрокапсул, имплантов или стержней, чрескожно или местно, например, в форме мазей, растворов или настоек, либо другими способами, например, в виде аэрозолей или растворов, распыляемых в нос.
Лекарственные средства по настоящему изобретению получают методами, хорошо известными специалисту в данной области, при этом помимо соединений формулы (I) в любой стереохимической форме или в виде смеси любых стереохимических форм в любом соотношении, физиологически переносимой соли или химического эквивалента, используют фармацевтически приемлемые инертные неорганические и/или органические носители и/или добавки. Для получения пилюль, таблеток, таблеток с покрытием и твердых желатиновых капсул можно использовать, например, лактозу, кукурузный крахмал или их производные, тальк, стеариновую кислоту или ее соли и т.д. Носителями для мягких желатиновых капсул и суппозиториев являются, например, жиры, воски, полутвердые и жидкие полиолы, природные или отвержденные масла и т.д. Приемлемыми носителями для получения растворов, например инъекционных растворов, эмульсий или сиропов, являются, например, вода, физиологический раствор, спирты, глицерин, полиолы, сахароза, инвертированный сахар, глюкоза, растительные масла и т.д. Приемлемые носители для микрокапсул, имплантов или стержней включают, например, сополимеры гликолевой кислоты и молочной кислоты. Фармацевтические препараты обычно содержат примерно 0,5-90% масс. соединения формулы (I) и/или его физиологически приемлемых солей и/или пролекарств. Количество активного ингредиента формулы (I) в любой стереохимической форме или в виде смеси любых стереохимических форм в любом соотношении, его физиологически переносимой соли или химического эквивалента в лекарственных средствах обычно составляет от около 0,5 до около 1000 мг, предпочтительно от около 1 до около 500 мг.
Помимо активных ингредиентов формулы (I) в любой стереохимической форме или в виде смеси любых стереохимических форм в любом соотношении, физиологически переносимой соли или химического эквивалента и носителей, фармацевтические препараты могут содержать одну или несколько добавок, таких как, например, наполнители, дезинтеграторы, связывающие вещества, смазывающие вещества, смачивающие вещества, стабилизаторы, эмульгаторы, консерванты, подсластители, красители, вкусовые вещества, ароматизаторы, загустители, разбавители, буферы, растворители, солюбилизаторы, вещества для достижения пролонгированного действия, соли для изменения осмотического давления, покрывающие вещества или антиоксиданты. Указанные препараты могут также содержать два или более соединений формулы (I) в любой стереохимической форме или в виде смеси любых стереохимических форм в любом соотношении, физиологически переносимую соль или химический эквивалент. В том случае если фармацевтический препарат содержит два или более соединений формулы (I), выбор отдельных соединений может быть направлен на достижение специфического общего фармакологического профиля фармацевтического препарата. Например, сильнодействующее соединение менее продолжительного действия может быть объединено с менее активным соединением длительного действия. Гибкость, допускаемая при выборе заместителей в соединениях формулы (I), позволяет контролировать в широких пределах биологические и физико-химические свойства указанных соединений и таким образом позволяет выбирать требуемые соединения. Кроме того, помимо по меньшей мере одного соединения формулы (I) фармацевтические препараты могут также содержать один или несколько других терапевтически или профилактически активных ингредиентов.
При использовании соединений формулы (I) доза лекарственного средства, которая может изменяться в широких пределах и в соответствии с обычной практикой, известной лечащему врачу, должна быть определена в зависимости от состояния субъекта в каждом конкретном случае. Например, доза зависит от используемого соединения, характера и тяжести заболевания, подлежащего лечению, способа и схемы введения, острого или хронического заболевания или применения данного лекарственного средства для профилактики. Соответствующая доза может быть определена в результате клинических испытаний, хорошо известных в данной области медицины. Как правило, суточная доза, необходимая для достижения требуемого результата у взрослого с массой тела примерно 75 кг, составляет от около 0,01 до около 100 мг/кг, предпочтительно от около 0,1 до около 50 мг/кг, в частности от около 0,1 до около 10 мг/кг (во всех случаях в мг на кг массы тела). Суточная доза может быть разделена на несколько частей, например на 2, 3 или 4 части, особенно в случае введения относительно больших количеств. Как правило, в зависимости от состояния субъекта суточная доза может быть увеличена или уменьшена по сравнению с указанной дозой.
Пример 1. Получение криокультуры Actinomadura namibiensis (DSM 6313)
Штамм Actinomadura namibiensis (DSM 6313) высевали в 100 мл культуральной среды (10 г крахмала, 2 г дрожжевого экстракта, 10 г глюкозы, 10 г глицерина, 2,5 г порошкообразного кукурузного экстракта, 2 г пептона, 1 г NaCl, 3 г СаСО3 в 1 л водопроводной воды, рН 7,2 до стерилизации) в стерильной 500 мл колбе Эрленмейера и инкубировали в течение 72 часов при 27°С на шейкере со скоростью вращения 120 об/мин. Затем 1 мл культуры смешивали с 1 мл стерильного консервирующего раствора (20 г глицерина, 10 г сахарозы, 70 мл деионизированной воды) и хранили при -80°С. Альтернативно небольшие части хорошо проросшей культуры на агаре переносили в криопробирки® (Vangard International) с 1,5 мл 50% стерильного раствора глицерина и хранили при -196°С в жидком азоте.
Пример 2. Получение лабиринтопептинов
В стерильную 500 мл колбу Эрленмейера, содержащую 100 мл культуральной среды, описанной в примере 1, высевали культуру Actinomadura namibiensis (DSM 6313), которую выращивали на агаровой пластинке и инкубировали при 27°С на шейкере со скоростью вращения 120 об/мин. Через 72 часа в другие колбы Эрленмейера, содержащие такую же культуральную среду в таком же количестве, высевали 2 мл указанной прекультуры и инкубировали в аналогичных условиях в течение 168 часов. Альтернативно культуру Actinomadura namibiensis (DSM 6313) высевали в 300 мл колбу Эрленмейера, содержащую 100 мл культуральной среды, описанной в примере 1, и инкубировали при 25°С со скоростью вращения 180 об/мин. Через 72 часа в другие колбы Эрленмейера, содержащие такую же культуральную среду в таком же количестве, высевали 5 мл прекультуры и инкубировали в аналогичных условиях в течение 168 часов.
Пример 3. Твердофазная экстракция лабиринтопептинов
После окончания ферментации 40 л Actinomadura namibiensis (DSM 6313) культуральный бульон фильтровали. Фильтрат культуры (примерно 30 л) вводили в колонку (размер: 160×200 мм), заполненную примерно 3 л материала СНР-20Р. Соединения элюировали со скоростью потока 250 мл/мин в градиенте от 5% до 95% изопропанола в воде. Фракции собирали через каждые 4 минуты в течение 45 минут. Фракции, содержащие лабиринтопептины, объединяли и лиофилизовали (фракция 8: молекулярная масса = 2190 Да; фракция 9: молекулярная масса = 2190 и 2074 Да; фракции 10-12: молекулярная масса = 2074 Да).
Пример 4. Предварительная очистка лабиринтопептина А1 при помощи хроматографии с обращенной фазой 18
Фракции 10-12 (670 мг), полученные в примере 3, растворяли в 500 мл метанола и вводили в колонку 10 мк С18 (2) Phenomenex Luna® (размер: 50 мм × 250 мм), включающую предварительную колонку 10 мк С18 (2) Phenomenex Luna® (размер: 21,2 мм × 60 мм). Соединения элюировали в градиенте от 5% до 75% ацетонитрила в воде в течение 40 минут со скоростью потока 190 мл/мин (буфер: 0,1% ацетата аммония, рН 9,0, доведенный до требуемого значения 30% водным раствором аммиака). Фракции собирали каждую минуту. Фракции 21-22 содержали требуемый лабиринтопептин (молекулярная масса = 2074 Да). После лиофилизации было получено 322 мг неочищенного продукта.
Пример 5. Конечная очистка лабиринтопептина А1
Фракции 21-22, полученные в примере 4 (60 мг), растворяли в 50 мл метанола и вводили в колонку 5 мк С18 (2) Axia Phenomenex Luna® (размер: 30 мм × 100 мм), включающую предварительную колонку 10 мк С18 Prep MS Waters XTerra® (размер: 19×10 мм). Соединения элюировали в градиенте от 5% до 75% ацетонитрила в воде в течение 40 минут со скоростью потока 70 мл/мин (буфер: 0,1% ацетата аммония, рН 4,6, доведенный до требуемого значения водным раствором уксусной кислоты). Элюенты собирали в виде 10 мл фракций, производя детекцию с помощью УФ-излучения. Фракции, содержащие лабиринтопептин (фракции 9-12), объединяли. После лиофилизации было получено 17 мг лабиринтопептина А1.
Пример 6. Предварительная очистка лабиринтопептина А3 при помощи хроматографии с обращенной фазой 18
Фракцию 8 (~850 мг), полученную в примере 3, растворяли в 500 мл метанола и вводили в колонку 10 мк С18(2) Phenomenex Luna® (размер: 50 мм × 250 мм), включающую предварительную колонку 10 мк С18 (2) Phenomenex Luna® (размер 21,2 мм × 60 мм). Соединения элюировали в градиенте от 5% до 75% ацетонитрила в воде в течение 40 минут (буфер: 0,1% ацетата аммония, рН 7,0) со скоростью потока 190 мл/мин. Фракции собирали каждую минуту. Фракция 19 содержала требуемый лабиринтопептин (молекулярная масса 2190 Да). После лиофилизации было получено 48 мг неочищенного продукта.
Пример 7. Конечная очистка лабиринтопептина А3
Фракцию 19, полученную в примере 6 (48 мг), растворяли в 50 мл метанола и вводили в колонку 5 мк С18 (2) Axia Phenomenex Luna® (размер: 30 мм × 100 мм), включающую предварительную колонку 10 мк С18 Prep MS Waters XTerra® (размер: 19 мм × 10 мм). Соединения элюировали в градиенте от 5% до 75% ацетонитрила в воде в течение 40 минут со скоростью потока 70 мл/мин (буфер: 0,1% ацетата аммония, рН 9,0, доведенный до требуемого значения 30% водным раствором аммиака). Элюенты собирали в виде фракций, производя детекцию с помощью УФ-излучения. Фракции, содержащие лабиринтопептин (фракции 9-12), объединяли. После лиофилизации было получено 12 мг лабиринтопептина А3.
Пример 8. Исследование лабиринтопептинов А1 и А3 методом высокоэффективной жидкостной хроматографии с обнаружением при помощи диодной матрицы и масс-спектрометрии (ВЭЖХ-DAD-MS)
Лабиринтопептины А1 и А3 анализировали в системе UPLC Waters Acquity, оснащенной пробоотборником, бинарным устройством управления растворителем и PDA (детектор на основе фотодиодной матрицы). В качестве колонки для UPLC была использована колонка С18 UPLC BEH Waters Acquity (1,7 мк; 2,1×100 мм), и элюирование производили со скоростью потока 0,6 мл/мин в градиенте вода:ацетонитрил (9:1) в течение 15 минут до 100% ацетонитрила, при этом во все растворители добавляли 6,5 мМ ацетата аммония до рН 4,6. Ультрафиолетовые спектры регистрировали детектором PDA при длинах волн от 200 до 600 нм. Масс-спектры регистрировали при помощи масс-спектрометра для жидкостной хроматографии µTOF Bruker, используя ортогональную электрораспылительную ионизацию, при частоте отбора проб 0,5 Гц и пределе обнаружения 150-1500 атомных единиц массы.
Пример 9. Исследование лабиринтопептинов А1
Лабиринтопептин А1 элюирован в момент времени, равный 5,46 мин (PDA). Ультрафиолетовый спектр выражен в виде λmax при длине волны 218 нм (сдвиг) и 279 нм.
Двухзарядные молекулярные ионы были обнаружены при m/z (I): 1035,87 (4539), 1036,37 (5566), 1036,87 (4086), 1037,37 (2296), 1037,87 (1034) и 1038,37 (280) в отрицательной моде. В положительной моде были обнаружены двухзарядные молекулярные ионы m/z (I): 1037,88 (2925), 1038,38 (3252), 1038,88 (2492), 1039,38 (1396) и 1039,88 (623).
Исследование лабиринтопептина А1 методом масс-спектрометрии с высоким разрешени