Питательная композиция, содержащая смесь олигосахаридов
Иллюстрации
Показать всеИзобретение относится к производству детского питания. Питательная композиция для грудных детей содержит в расчете на сухое вещество от 2,5 до 15,0 масс.% смеси олигосахаридов. Смесь олигосахаридов состоит из N-ацетилированного олигосахарида(ов), галактоолигосахарида(ов) и сиалилированного олигосахарида(ов). При этом композиция содержит, по меньшей мере, 0,02 масс.% N-ацетилированного олигосахарида, по меньшей мере, 2,0 масс.% галактоолигосахарида и, по меньшей мере, 0,04 масс.% сиалилированного олигосахарида. Причем N-апетилированный олигосахарид(ы) составляет от 0,5 до 4,0% смеси олигосахаридов, галактоолигосахарид(ы) составляет от 92,0 до 98,5% смеси олигосахаридов и сиалилированный олигосахарид(ы) составляет от 1,0 до 4,0% смеси олигосахаридов. Изобретение позволяет получить питательную композицию для введения грудным детям в первые шесть месяцев жизни для снижения риска развития ожирения в более позднем периоде жизни, для снижения липогенеза и стимуляции бета-окисления жирных кислот у грудных детей. 4 н. и 13 з.п. ф-лы, 2 ил., 1 табл., 2 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к питательной композиции, такой как смесь для детского питания, обогащенной смесью олигосахаридов.
Уровень техники
В кишечнике человека обитает множество видов бактерий, которые оказывают как положительное, так и отрицательное воздействия на физиологию кишечника, а также другие системные воздействия. Доминирующими группами бактерий, обнаруженными в кишечнике, являются бактероиды, бифидобактерии, эубактерии, клостридии и лактобациллы. Присутствующие бактерии проявляют неустойчивую активность в зависимости от доступности субстрата, окислительно-восстановительного потенциала, pH, давления О2 и локализации в толстом кишечнике. В большинстве случаев кишечные бактерии можно подразделить на виды, которые могут потенциально оказывать либо вредное, либо полезное воздействие на. организм-хозяина. Патогенные воздействия (которые могут вызываться, например, клостридиями или бактероидами) включают диарею, инфекции, поражение печени, канцерогенез и гнилостные процессы в кишечнике. Полезные для здоровья воздействия могут быть обусловлены ингибированием роста вредных бактерий, стимулированием иммунных функций, улучшением пищеварения и абсорбцией необходимых питательных веществ и синтезом витаминов. Желательным является повышение количества и/или активности таких видов бактерий (как Bifidobacterium и Lactobacillus), которые способны оказывать полезное для здоровья действие.
Что касается конкретно грудных детей, то считается, что незадолго до появления ребенка на свет, его желудочно-кишечный тракт является стерильным. В процессе родов он контактирует с бактериями пищеварительного тракта и кожи матери и начинает заселяться ими. Существуют большие различия в составе микробиоты кишечника у грудных детей в зависимости от их кормления. Микрофлора фекалий детей, вскармливаемых материнским молоком, содержит значительные популяции бифидобактерии с некоторым количеством лактобацилл, в то время как у детей, вскармливаемых искусственными смесями, микробиота является более сложной по составу и в ней обычно присутствуют бифидобактерии, бактероиды, клостридии и стрептококки. После отнятия от груди, у детей постепенно устанавливается микробиота кишечника, сходная с микробиотой кишечника взрослого человека.
Один из подходов к стимуляции количества и/или активности полезных бактерий в толстом кишечнике предусматривает добавление в пищевые продукты пребиотиков. Пребиотик представляет собой неусвояемый пищевой ингредиент, который благотворно влияет на организм-хозяин, избирательно стимулируя рост и/или активность одного или ограниченного количества видов бактерий в толстом кишечнике и улучшая, тем самым, здоровье хозяина. Такие ингредиенты являются неусвояемыми в том смысле, что они не расщепляются, а абсорбируются в желудке или тонком кишечнике и проходят в целостном виде в толстый кишечник, где они избирательно сбраживаются полезными бактериями. Примеры пребиотиков включают некоторые олигосахариды, такие как фруктоолигосахариды (FOS) и галактоолигосахариды (GOS).
Известно, что женское молоко содержит повышенное количество неперевариваемых олигосахаридов по сравнению с молоком большинства видов животных. Фактически неперевариваемые олигосахариды представляют собой третий по количеству твердый компонент (после лактозы и липидов) женского молока, причем его концентрация составляет 12-15 г/л в молозиве и 5-8 г/л в зрелом молоке. Олигосахариды женского молока очень устойчивы к ферментативному гидролизу, что указывает на то, что эти олигосахариды могут выполнять жизненно важные функции, не связанные непосредственно с их энергетической ценностью.
Материнское молоко рекомендуется всем грудным детям. Однако в некоторых случаях грудное вскармливание является неадекватным или безуспешным по медицинским причинам или матери отказываются кормить грудью. Для таких ситуаций разработаны детские смеси. По мере досконального изучения состава женского молока было предложено вводить пребиотики в смеси для детского питания. Промышленностью выпускаются различные смеси для детского питания с добавлением пребиотиков, например, смеси фруктоолигосахаридов с галактоолигосахаридами. Однако эти смеси лишь довольно приблизительно имитируют смесь олигосахаридов женского молока. В женском молоке обнаружено свыше 100 различных олигосахаридных компонентов, некоторые из которых не были обнаружены в молоке животных, например, в коровьем молоке указанные компоненты не были обнаружены вообще или были обнаружены только в малых количествах. Примерами тех классов олигосахаридов женского молока, которые присутствуют в коровьем молоке и молозиве только в очень малых количествах или не присутствуют вообще, могут служить сиалилированные и фукозилированные олигосахариды.
Заявка на патент US №2003/0129278 описывает смесь олигосахаридов на основе олигосахаридов, полученных из молока одного или нескольких видов животных, которая характеризуется тем, что она содержит, по меньшей мере, две олигосахаридных фракции, каждая из которых состоит, по меньшей мере, из двух различных олигосахаридов при отсутствии лактозы. Общий спектр олигосахаридов, присутствующих в указанной смеси, отличается от их спектра в молоке одного или нескольких видов животных, из которого указанные олигосахаридные фракции были экстрагированы. Кроме того, (а) если указанные олигосахариды экстрагированы из молока только одного вида животного, то отношение нейтральных олигосахаридов к кислотным (сиалилированным) олигосахаридам составляет 90-60:10-40 масс.%, или (б) если указанные олигосахариды экстрагированы из молока, по меньшей мере, двух видов животных, то олигосахариды, экстрагированные из молока каждого из двух разных видов животных, составляют 10 масс.% общего количества олигосахаридов, присутствующих в смеси олигосахаридов.
WO 2007/090894 описывает смесь олигосахаридов, которая содержит от 5 до 70 масс.%, по меньшей мере, одного N-ацетилированного олигосахарида, от 20 до 90 масс.%, по меньшей мере, одного нейтрального галактоолигосахарида и от 5 до 50 масс.%, по меньшей мере, одного сиалилированного олигосахарида.
Наибольший интерес исследователей сосредоточился на ферментируемости и бифидогенности олигосахаридных пребиотиков. Однако исследования in vitro показали, что ряд олигосахаридных пребиотиков имитирует рецепторы клеточной поверхности эукариот, к которым прикрепляются вирулентные бактерии в ходе патогенетического процесса (Shoaf et al, 2006). Также, обнаружили, что транс-галактоолигосахариды повышают защитную способность Bifidobacterium breve у мышей, инфицированных Salmonella enterica (Asahara et al, 2001). Изучались и другие возможные преимущества пребиотиков у взрослых, включая иммуномодуляторные свойства, минерализацию костей и действие на сердечнососудистую систему. Исследования на новорожденных и грудных детей сосредоточились на способности олигосахаридов повышать популяцию фекальных бифидобактерий. Удивительным образом было установлено, что применение пребиотиков у грудных детей является высокоэффективным при профилактике и лечении заболеваний.
В последние годы во всем мире вызывают беспокойство проблемы относительно повышенного веса и ожирения в популяции взрослых людей, поскольку ожирение является наиболее обременительным и дорогим состоянием, связанным с питанием. В результате, обратили внимание на значимость в младенчестве риска развития ожирения, которое возникает позже во взрослой жизни, особенно принимая во внимание степень роста в течение грудного периода, что может являться прогностическим фактором отдаленного ожирения. Некоторые комментаторы полагают, что прибавление в весе в первые шесть месяцев жизни в первую очередь является увеличением жировых отложений; если прибавление в весе в младенчестве фактически является прогнозом отдаленного ожирения, то отсюда следует, что прибавление в весе у младенцев должно тщательно контролироваться для снижения риска развития ожирения в более позднем периоде жизни (Gilman M.W., "The first months of life: a critical period for development of obesity" Am J Clin Nutr 2008; 87: 1587-9).
Сущность изобретения
Изобретатели настоящего изобретения неожиданно обнаружили, что при введении смеси пребиотических олигосахаридов, содержащей галактоолигосахариды с небольшими количествами более комплексных видов олигосахаридов, таких как сиалилированные олигосахариды и не сиалилированные олигосахариды, включая, по меньшей мере, одну N-ацетиловую группу, стерильным мышам, инокулированным микробиотой ребенка, модулируется липидный метаболизм посредством снижения липогенеза и стимулирования бета-окисления жирных кислот, по сравнению с контрольной группой, не получавшей смеси олигосахаридов.
Соответственно, настоящее изобретение обеспечивает применение N-ацетилированного олигосахарида, галактоолигосахарида и сиалилированного олигосахарида при получении питательной композиции для введения грудным детям в первые шесть месяцев жизни для снижения впоследствии риска развития ожирения.
Изобретение распространяется на питательную композицию для введения грудным детям, причем композиция содержит в пересчете на сухое вещество от 2,5 до 15,0 масс.% смеси олигосахаридов, состоящей из N-ацетилированного олигосахарида(ов), галактоолигосахарида(ов) и сиалилированного олигосахарида(ов). При этом соблюдается условие, что композиция содержит, по меньшей мере, 0,02 масс.% N-ацетилированного олигосахарида, по меньшей мере, 2,0 масс.% галактоолигосахарида и, по меньшей мере, 0,04 масс.% сиалилированного олигосахарида, и что смесь олигосахаридов содержит от 0,5 до 4,0% N-ацетилированного олигосахарида(ов), от 92,0 до 98,5% галактоолигосахарида(ов) и от 1,0 до 4,0% сиалилированного олигосахарида(ов).
Преимущество питательной композиции согласно изобретению распространяется на снижение липогенеза и на более высокое бета-окисление жирных кислот.
В воплощении, смесь олигосахаридов может быть получена из молока животных, например, из коровьего молока, козьего молока или молока буйволиц.
Предпочтительно, питательная композиция представляет собой смесь для грудных детей, но она также может иметь вид любой пищи или напитка, потребляемого грудными детьми в первые несколько месяцев жизни, включая терапевтическую питательную композицию, отвечающую требованиям Европейского Управления по контролю за качеством продуктов питания для специальных медицинских целей (FSMP).
Краткое описание фигур
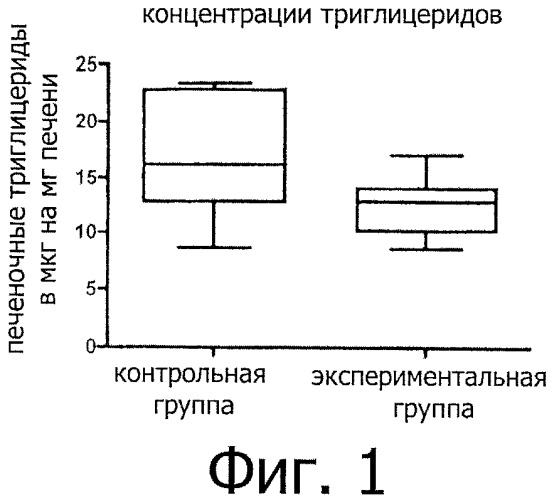
Фигура 1 сравнивает концентрации триглицеридов в печени мышей контрольной группы (n=9) и мышей экспериментальной группы (n=10), при использовании диаграммы вида "ящик с усами"; и
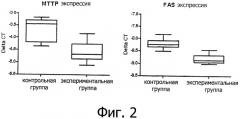
Фигура 2 сравнивает экспрессию микросомального белка, переносящего триглицериды (МТТР), и синтазы жирных кислот (FAS) в печени мышей контрольной группы (n=9) и мышей экспериментальной группы (n=10), при использовании диаграммы вида "ящик с усами".
Раскрытие изобретения
В данном описании следующие термины даются в тех значениях, которые указаны для них ниже:
"галактоолигосахарид" означает олигосахарид, содержащий две или более галактозных молекул, которые не имеют заряда и не содержат N-ацетиловый остаток;
"грудной ребенок" означает ребенка в возрасте до 12 месяцев;
"смесь для детского питания" означает пищевой продукт, предназначенный для полноценного питания грудных детей в течение первых от четырех до шести месяцев жизни (ст.1.2 директивы Комиссии 91/321/EEC от 14 мая 1991, касающаяся смесей для грудных детей и смесей для детей младшего возраста);
"N-ацетилированный олигосахарид" означает олигосахарид, содержащий N-ацетил-остаток;
"олигосахарид" означает углевод, имеющий степень полимеризации (DP) от 2 до 20 включительно, но не включающий лактозу;
"пребиотик" означает избирательно ферментированный ингредиент, который обеспечивает специфичные изменения и в композиции и/или в микробиоте желудочно-кишечного тракта, улучшая здоровье и самочувствие хозяина (Bouhnik et al, 2004);
"сиалилированный олигосахарид" означает олигосахарид, содержащий остаток сиаловой кислоты с ассоциированным зарядом.
Пригодные N-ацетилированные олигосахариды включают GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc. N-ацетилированные олигосахариды могут быть получены действием глюкозаминидазы и/или галактозаминидазы на N-ацетил-глюкозу и/или N-ацетил-галактозу. Равным образом, для этой цели могут использоваться N-ацетил-галактозил-трансферазы и/или N-ацетил-гликозил-трансферазы. N-ацетилированные олигосахариды могут быть получены также технологией ферментации с применением соответствующих ферментов (рекомбинантных или природных) и/или микробной ферментацией. В последнем случае микроорганизмы могут либо экспрессировать свои природные ферменты и субстраты, либо могут быть генетически модифицированы с целью продуцирования ими соответствующих субстратов и ферментов. Могут использоваться культуры одного вида микроорганизмов или смешанные культуры. Образование N-ацетилированных олигосахаридов может инициироваться акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP=1 и выше. Другим вариантом является химическая конверсия кето-гексоз (например, фруктозы), либо свободных, либо связанных с олигосахаридом (например, лактулозой), в N-ацетилгексозамин или в N-ацетилгексозамин-содержащий олигосахарид, как описано у Wrodnigg, T.M.; Stutz, A.E. (1999) в Angew. Chem. Int. Ed. 38: 827-828.
Подходящие галакто-олигосахариды включают Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc, Galβ1,3Galβ1,3Galβ1,4Glc, Galβ1,4Galβ1,4Glc b Galβ1,4Galβ1,4Galβ1,4Glc. Синтезированные галакто-олигосахариды, такие как Galβ 1,6Galβ1, 4Glc Galβ 1,6Galβ1, 6Glc, Galβ1,3Galβ1,4Glc, Galβ l,6Galβ1,6Galβ1, 4Glc, Galβ1,6Galβ1,3Galβ1,4Glc and Galβ 1,3Galβ1,6Galβ1, 4Glc, Galβ 1,4Galβ1, 4Glc and Galβ 1,4Galβ1,4Galβ1, 4Glc и их смеси, реализуются на рынке под торговыми марками Vivinal® и Elix' или ®. Другими поставщиками олигосахаридов являются Dextra Laboratories, Sigma-Aldrich Chemie GmbH и Kyowa Hakko Co., Ltd. Альтернативно для получения нейтральных олигосахаридов могут использоваться специфические гликозилтрансферазы, такие как галактозилтрансферазы.
Подходящие сиалилированные олигосахариды включают NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc. Эти сиалилированные олигосахариды быть выделены хроматографией или технологией фильтрации из природного источника, например, из молока животных. Альтернативно они могут быть получены также биотехнологически с применением специфических сиалилтрансфераз либо технологией ферментации, основанной на применении ферментов (рекомбинантных или природных), либо микробной ферментацией. В последнем случае микроорганизмы могут либо экспрессировать свои природные ферменты и субстраты, либо могут быть генетически модифицированы с целью продуцирования ими соответствующих субстратов и ферментов. Могут использоваться культуры одного вида микроорганизмов или смешанные культуры. Образование сиалил-олигосахаридов может инициироваться акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP=1 и выше.
Предпочтительно, питательная композиция содержит от 3,0 до 12,0% смеси олигосахаридов, более предпочтительно от 4,0 до 7,0% смеси олигосахаридов.
Питательная композиция предпочтительно содержит, по меньшей мере, 0,03 масс.% N-ацетилированного олигосахарида, по меньшей мере, 3,0 масс.% галактоолигосахарида и, по меньшей мере, 0,08 масс.% сиалилированного олигосахарида, более предпочтительно, по меньшей мере, 0,04 масс.% N-ацетилированного олигосахарида, по меньшей мере, 4,0 масс.% галактоолигосахарида и, по меньшей мере, 0,09 масс.% сиалилированного олигосахарида.
Питательная композиция по изобретению также предпочтительно содержит, по меньшей мере, один пробиотический бактериальный штамм. Пробиотик представляет собой препарат из микробной клетки или компоненты микробных клеток с полезным воздействием на здоровье или самочувствие организма-хозяина. Подходящие пробиотические бактериальные штаммы включают Lactobacillus rhamnosus ATCC 53103, поставляемый фирмой Valio Oy, Finland, под торговой маркой LGG, Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus paracasei CNCM 1-2116, Lactobacillus reuteri ATCC 55730 и Lactobacillus reuteri DSM 17938, поставляемый от Biogaia, Lactobacillus fermentum VRI 003, Streptococcus salivarius DSM 13084, реализуемый фирмой BLIS Technologies Limited, New Zealand, под торговой маркой K12, Bifidobacterium lactis CNCM 1-3446, реализуемый среди прочих компанией Christian Hansen, Denmark, под торговой маркой Bb12, Bifidobacterium longum ATCC BAA-999, реализуемый Morinaga Milk Industry Co. Ltd., Japan, под торговой маркой BB536, штамм Bifidobacterium breve, реализуемый Danisco под торговой маркой Bb-03, штамм Bifidobacterium breve, реализуемый Morinaga под торговой маркой M-16V, штамм Bifidobacterium infantis, реализуемый Procter & Gamble Co. под торговой маркой Bifantis и штамм Bifidobacterium breve, реализуемый Institut Rosell (Lallemand) под торговой маркой R0070. Пробиотик можно добавлять в количестве от 103 до 1012 КОЕ/г порошка, более предпочтительно от 107 до 1012 КОЕ/г порошка.
Предпочтительно, питательная композиция по изобретению представляет собой смесь для детского питания. Общая композиция смеси для грудных детей, согласно изобретению, будет описана ниже посредством примера.
Смесь для детского питания содержит источник белков. Вид белка не является критическим в настоящем изобретении при условии, что он удовлетворяет минимальным потребностям по содержанию незаменимых аминокислот и обеспечивает удовлетворительный рост. Так, в смесях могут использоваться источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается белков молочной сыворотки, то основу источника белка могут составлять кислая сыворотка или сладкая сыворотка либо их смеси, и источник белка может включать альфа-лактальбумин и бета-лактоглобулин в требуемых количественных соотношениях.
Белки могут быть нативными или гидролизованными либо представлять собой смесь нативного и гидролизованного белков. В некоторых случаях может быть желательным использование частично гидролизованных белков (степень гидролиза от 2 до 20%), например, для грудных детей, которые предположительно относятся к группе риска развития аллергии на коровье молоко. Если необходимы гидролизованные белки, то процесс гидролиза может проводиться требуемым образом и известным из уровня техники способом. Например, гидролизат белков молочной сыворотки можно получить путем ферментативного гидролиза сывороточной фракции в одну или более стадий. Если сывороточная фракция, используемая в качестве исходного материала, не содержит, в основном, лактозы, то в процессе гидролиза, как было установлено, белок подвержен блокаде лизина в намного меньшей степени. Это позволяет снизить степень блокады лизина примерно с 15 масс.% общего лизина до менее чем 10 масс.% общего лизина; например, степень блокады лизина может составлять около 7 масс.% лизина, что значительно повышает питательную ценность источника белка.
Смесь для грудных детей согласно настоящему изобретению содержит источник углеводов. Может использоваться любой источник углеводов, который традиционно можно обнаружить в смесях для грудных детей, такой как лактоза, сахароза, мальтодекстрин, крахмал и их смеси, хотя предпочтительным источником углеводов является лактоза. Предпочтительно источники углеводов составляют от 35 до 65% общего количества энергии в смеси.
Смесь для грудных детей согласно настоящему изобретению содержит источник липидов. Источник липидов может быть любым липидом или жиром, который пригоден для использования в смесях для грудных детей. Предпочтительные источники жира включают пальмовый олеин, высокоолеиновое подсолнечное масло и высокоолеиновое сафлоровое масло. Незаменимые жирные кислоты - линолевая кислота и α-линоленовая кислота - также могут добавляться, равно как и небольшие количества масел с высоким содержанием арахидоновой и докозагексаеновой кислот, такие как рыбий жир или масла микробного происхождения. В целом содержание жира предпочтительно должно быть таким, чтобы жир поставлял от 30 до 55% общего количества энергии смеси. Источник жира предпочтительно имеет соотношение n-6 жирных кислот к n-3 жирным кислотам примерно от 5:1 до 15:1, например, примерно от 8:1 до 10:1.
Смесь для грудных детей содержит также все витамины и минералы, считающиеся незаменимыми в каждодневном рационе питания, в значительных в питательном отношении количествах. Установлены минимальные потребности для некоторых витаминов и минералов. Примеры минералов, витаминов и других нутриентов, необязательно присутствующих в смеси для грудных детей, включают витамин А, витамин B1, витамин B2, витамин В6, витамин В12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозит, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлорид, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минералы обычно добавляются в форме солей. Присутствие и количества конкретных минералов и других витаминов будет варьировать в зависимости от популяции грудных детей, для которой предназначена данная смесь.
При необходимости смесь для грудных детей может содержать эмульгаторы и стабилизаторы, такие как соевый лецитин, эфиры лимонной кислоты и моно- и диглицеридов и др. Они используются преимущественно в том случае, если указанная смесь изготавливается в жидком виде.
Смесь для грудных детей может необязательно содержать другие вещества, которые могут обладать полезным действием, такие как пищевые волокна, лактоферрин, нуклеотиды, нуклеозиды и т.п.
В конечном итоге, смесь будет содержать от 2,5 до 15,0 масс.% смеси олигосахаридов, состоящей из N-ацетилированного олигосахарида(ов), галактоолигосахарида(ов) и сиалилированного олигосахарида(ов) в следующих количествах: меньшей мере, 0,02 масс.% N-апетилированного олигосахарида, по меньшей мере, 2,0 масс.% галактоолигосахарида и, по меньшей мере, 0,04 масс.% сиалилированного олигосахарида, причем в смеси олигосахаридов содержится от 0,5 до 4,0% N-ацетилированного олигосахарида(ов), от 92,0 до 98,5% галактоолигосахарида(ов) и от 1,0 до 4,0% сиалилированного олигосахарида(ов).
Смесь для детского питания может быть приготовлена путем смешивания источника белка, источника углеводов и источника жира в соответствующих соотношениях. При необходимости могут быть добавлены эмульгаторы. Одновременно можно добавлять витамины и минералы, однако обычно их добавляют позднее во избежание их расщепления при нагреве. Липофильные витамины, эмульгаторы и т.п. можно предварительно растворить в источнике жира перед смешиванием. Затем для получения жидкой смеси можно добавить воду, предпочтительно воду, подвергнутую обработке обратным осмосом.
Затем полученная жидкая смесь может подвергаться тепловой обработке для снижения бактериальной нагрузки. Например, жидкая смесь может подвергаться быстрому нагреву до температуры примерно от 80°C до 110°C в течение примерно от 5 секунд до 5 минут. Это может осуществляться путем прямой инжекции пара или пропусканием через теплообменник, например, пластинчатый теплообменник.
Затем жидкая смесь может охлаждаться до температуры примерно от 60°C до 85°C, например, мгновенным охлаждением. После этого жидкая смесь может подвергаться гомогенизации, например, в две стадии при давлении примерно от 7 МПа до 40 МПа на первой стадии и примерно от 2 МПа до 14 МПа на второй стадии. Гомогенизированная смесь может охлаждаться далее до температуры, при которой можно добавлять чувствительные к нагреву компоненты, такие как витамины и минералы. Именно в этот момент удобно стандартизировать гомогенизированную смесь по pH и содержанию сухих веществ.
Гомогенизированная смесь подается в соответствующую сушильную установку, такую как распылительная сушилка или сублимационная сушилка, и превращается в порошок. Порошок должен иметь влагосодержание ниже примерно 5 масс.%.
Олигосахариды могут быть добавлены непосредственно в смесь для грудных детей путем сухого смешивания.
Предпочтительно, смесь для грудных детей согласно изобретению представляет собой питание для малышей накаждый день.
Изобретение иллюстрируется нижеприведенными примерами.
Пример 1
Пример композиции смеси для грудных детей согласно настоящему изобретению приводится ниже.
| Нутриент | На 100 ккал | На литр |
| Энергетическая ценность (ккал) | 100 | 670 |
| Белок (г) | 1,83 | 12,3 |
| Жир (г) | 5,3 | 35,7 |
| Линолевая кислот (г) | 0,79 | 5,3 |
| α-линоленовая кислотй (мг) | 101 | 675 |
| Лактоза (г) | 11,2 | 74,7 |
| Галактоолигосахариды (г) | 1,1 | 6,8 |
| N-ацетилированные олигосахариды (г) | 0,027 | 0,055 |
| Сиалилированные олигосахариды (г) | 0,027 | ,134 |
| Минералы (г) | 0,37 | 2,5 |
| Na (мг) | 23 | 150 |
| K(мг) | 89 | 590 |
| Cl (мг) | 64 | 430 |
| Ca (мг) | 62 | 410 |
| P (мг) | 31 | 210 |
| Mg (мг) | 7 | 50 |
| Mn (мг) | 8 | 50 |
| Se (мг) | 2 | 13 |
| Витамин А (мкг RE) | 105 | 700 |
| Витамин D (мкг) | 1,5 | 10 |
| Витамин Е (мкг ТЕ) | 0,8 | 5,4 |
| Витамин K1 (мкг) | 8 | 54 |
| Витамин С (мг) | 10 | 67 |
| Витамин В1 (мг) | 0,07 | 0,47 |
| Витамин В2 (мг) | 0,15 | 1,0 |
| Ниацин (мг) | 1 | 6,7 |
| Витамин В6 (мг) | 0,075 | 0,50 |
| Фолиевая кислота (мкг) | 9 | 60 |
| Пантотеновая кислота (мг) | 0,45 | 3 |
| Витамин В 12 (мкг) | 0,3 | 2 |
| Биотин (мкг) | 2,2 | 15 |
| Холин (мг) | 10 | 67 |
| Fe (мг) | 1,2 | 8 |
| I (мкг) | 15 | 100 |
| Cu (мг) | 0,06 | 0,4 |
| Zn (мг) | 0,75 | 5 |
Пример 2
Изучали влияние питательной композиции изобретения на липогенез и окисление жиров у стерильных мышей, инокулированных микробиотой ребенка (НВМ). План эксперимента. Всего 19 стерильных самок-мышей линии С3Н (Charles River, France) поместили в одинаковые условия обитания и кормили стандартным полусинтетическим кормом для грызунов (Reeves et al, 1993). В возрасте 8 недель, стерильные мыши получили однократную дозу смеси бактерий микробиоты ребенка человека (НВМ) и их произвольно разделили на 2 группы, с последующим разным питательным режимом в течение 2-недельного периода. Состав НВМ ранее был определен (Martin et al, 2007). Одну группу выбрали в качестве контроля и кормили ′базовой смесью′, содержащей в составе 2,5% глюкозо-лактозной смеси (1,25% каждой) (контрольная группа, n=9). Корм второй группы мышей содержал 0,11% N-ацетилированных олигосахаридов, 2,7% галактоолигосахаридов и 0,11% сиалилированных олигосахаридов (экспериментальная группа, n=10).
Сбор материала и аналитические измерения. После аутопсии собирали образцы утренней порции мочи, плазмы крови и интактной ткани печени и быстро замораживали перед проведением метаболического анализа. Метабономика, использующая высокочувствительные спектроскопические методы с последующим применением многомерной статистики, является традиционной стратегией для дифференциального определения метаболического пути и оценки действия и эффективности диетического воздействия (Martin et al, 2008; Nicholson et al, 2005; Rezzi et al, 20070b; Rezzi et al, 2007a; Stella et al, 2006). Метаболические профили разрабатываются с применением методов многомерной статистики для извлечения метаболических зондов воздействия олигосахаридов, которые служат в качестве источника для описания и определения групп животных, согласно лечению (Таблица 1).
Результаты
Таблица 1 и Фигура 1 показывают, что применение питательной композиции согласно изобретению снижает концентрацию триглицеридов в печени. Контрольную и экспериментальную группы сравнивали с использованием непарного критерия Стьюдента и разница являлась статистически достоверной при 95% уровне значимости. Таблица 1 и Фигура 2 показывают, что применение питательной композиции согласно изобретению также снижает липогенез и включение триацилглицеринов в липопротеины в печени, при этом показатель Delta CT, нанесенный на у-ось на Фигуре 2, является разницей между пороговым циклом представляющего интерес гена и пороговым циклом эндогенного эталонного гена. Снижение уровней экспрессии у животных в экспериментальной группе являлось достоверным при 99,9% уровне значимости, используя непарный критерий Стьюдента. Более высокая экскреция карнитина и ацетилкарнитина с мочой дополнительно показывает усиление окисления жирных кислот (Таблица 1). Эти результаты совместно с высокой метаболической активностью бетаин-гомоцистеин-метилтрансферазы в печени (Таблица 1) показывают более высокую секрецию новообразующихся липопротеиновых частиц, более мелких по размерам и несущих меньше триацилглицеринов.
Показатели триглицеридов и активности микросомального белка, переносящего триглицериды, (МТТР) и синтазы жирных кислот (FAS) в печени мышей контрольной и экспериментальной групп подтверждают, что мыши в экспериментальной группе имеют пониженный уровень печеночных триглицеридов, пониженную липогенную активность (FAS) и небольшое включение триглицеридов в липопротеины (МТТР) (Фигура 2).
Высокие концентрации карнитина и ацетио-карнитина и низкие уровни L-аминоадипата и α-кето-изокапроата в моче мышей, получавших пребиотик, представляют дополнительное доказательство изменения липидного метаболизма (Kliewer et al, 1997). В частности, карнитин является хорошо известным кофактором, необходимым для превращения свободных длинноцепочечных жирных кислот в ацилкарнитины и их последующий транспорт в матрикс митохондрий, где они подвергаются β-окислению (Bremer, 1983). Следовательно, результаты показывают усиление окисления жирных кислот (Таблица 1).
Эти результаты показывают специфичные для печени изменения активности бетаин-гомоцистеин-метилтрансферазы (ВНМТ), метаболических путей, которые тесно связывают холин, бетаин и образование метионина из гомоцистеина (Niculescu & Zeisel, 2002). Сообщалось, что повышенная экспрессия ВНМТ является возможным механизмом, способствующим более высокой секреции АроВ, требующейся для сборки VLDL (Sparks et al, 2006). Кроме того, предыдущие исследования показали, что определенные диеты с применением сложных углеводов (крахмал) приводят к более высокой секреции образующихся частиц VLDL, имеющих меньший размер и несущих меньше триацилглицеринов, и повышает фракционные скорости катаболизма VLDL и ароВ (Fernandez et al, 1996). Таким образом, повышенный метаболизм ВНМТ и пониженная активность МТТР свидетельствуют о более высоком синтезе апопротеинов ароВ и сниженном превращении липидов в новообразующиеся липопротеины, что предполагает вовлечение аналогичного механизма в ответ на это воздействие.
| Таблица 1 | ||
| Значимые метаболиты, показывающие влияние пребиотиков на метаболические процессы в плазме, печени и моче | ||
| Метаболит | Контрольная группа | Экспериментальная группа |
| Плазма | QY 2=29%, RX 2=86% | |
| Липопротеины | 0,5±0,2 | 0,4±0,1 |
| Печень | OY 2=36%, RX 2=46% | |
| Бетаин | 1,6±0,3 | 2,5±0,2*** |
| Холин | 0,5±0,2 | 1,1±0,2*** |
| DMG | 0,06±0,02 | 0,19±0,05*** |
| Триглицериды | 3,6±1,3 | 2,1±0,4* |
| Фосфохолин | 1,7±0,3 | 2,4±0,3*** |
| Саркозин | 0,14±0,03 | 0,18±0,02* |
| Моча | QY 2=70%, RX 2=49% | |
| Карнитин | 0,3±0,06 | 5,2±1,3*** |
| N-ацетилкарнитин | 0,17±0,02 | 1,3±0,3*** |
| α-кето-изокапроат | 1,3±0,3 | 0,9±0,1* |
| α-аминоадипат | 0,33±0,05 | 0,19±0,02*** |
O-PLS-модели были созданы с 1 прогнозируемым компонентом и 2 ортогональными компонентами для проведения различий между 2 группами мышей. Значение RX 2 показывает, как много вариантов в массиве данных, X объясняется моделью. Значение QY 2 представляет прогнозируемость моделей и относится к ее статистической достоверности. Данные представлены как нормализованные по площади интенсивности (а.u.) представленных метаболических сигналов как средние +- стандартное отклонение (SD). Значения для НВМ мышей, которым вводили пребиотики, сравнивали с НВМ контрольных мышей, * и *** обозначают статистическую достоверность при 95% и 99,9% уровне значимости, соответственно.
1. Применение N-ацетилированного олигосахарида, галактоолигосахарида и сиалилированного олигосахарида для получения питательной композиции для введения грудным детям в первые шесть месяцев жизни для снижения риска развития ожирения в более позднем периоде жизни.
2. Применение N-ацетилированного олигосахарида, галактоолигосахарида и сиалилированного олигосахарида для получения питательной композиции для введения грудным детям в первые шесть месяцев жизни для снижения липогенеза у грудных детей.
3. Применение N-ацетилированного олигосахарида, галактоолигосахарида и сиалилированного олигосахарида для получения питательной композиции для введения грудным детям в первые шесть месяцев жизни для стимуляции бета-окисления жирных кислот у грудных детей.
4. Применение по любому из пп.1-3, где N-ацетилированный олигосахарид представляет собой GalNAcα1,3Galβ1,4Glc, Galβ1,6GalNAcα1,3Galβ1,4Glc или их смесь.
5. Применение по любому из пп.1-3, где галактоолигосахарид представляет собой Galβ1,6Gal, Galβ1,6Galβ1,4Glc, Galβ1, 6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc, Galβ1,3Galβ1,6Galβ1,4Glc, Galβ1,3Galβ1,3Galβ1,4Glc, Galβ1,4Galβ1,4Glc и Galβ1,4Galβ1,4Galβ1,4Glc или их смесь.
6. Применение по любому из пп.1-3, где сиалилированный олигосахарид представляет собой NeuAcα2,3Galβ1,4Glc, NeuAcα2,6Galβ1,4Glc или их смесь.
7. Питательная композиция для введения грудным детям, которая содержит в расчете на сухое вещество от 2,5 до 15,0 мас.% смеси олигосахаридов, состоящей из N-ацетилированного олигосахарида(ов), галактоолигосахарида(ов) и сиалилированного олигосахарида(ов), при условии, что композиция содержит, по меньшей мере, 0,02 мас.% N-ацетилированного олигосахарида, по меньшей мере, 2,0 мас.% галактоолигосахарида и, по меньшей мере, 0,04 мас.% сиалилированного олигосахарида и что N-ацетилированный олигосахарид(ы) составляет от 0,5 до 4,0 мас.% смеси олигосахаридов, галактоолигосахарид(ы) составляет от 92,0 до 98,5 мас.% смеси олигосахаридов и сиалилированный олигосахарид(ы) составляет от 1,0 до 4,0 мас.% смеси олигосахаридов.
8. Композиция по п.7, которая содержит, по меньшей мере, 0,03 мас.% N-ацетилированного олигосахарида, по меньшей мере, 3,0 мас.% галактоолигосахарида и, по меньшей мере, 0,08 мас.% сиалилированного олигосахарида.
9. Композиция по п.7, которая содержит, по меньшей мере, 0,04 мас.% N-ацетилированного олигосахарида, по меньшей мере, 4,0 мас.% галактоолигосахарида и, по меньшей мере, 0,09 мас.% сиалилированного олигосахарида.
10. Композиция по п.7, которая содержит 3,0-12,0 мас.% смеси олигосахаридов.
11. Композиция по п.7, которая содержит 4,0-7,0 мас.% смеси олигосахаридов.
12. Композиция по любому из пп.7-9, в которой N-ацетилированный олигосахарид представляет собой GalNAcα1,3Galβ1,4Glc, Galβ1,6GalNAcα1,3Galβ1,4Glc или их смесь.
13. Композиция по любым пп.7-11, в которой галактоолигосахарид представляет собой Galβ1,6Gal, Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ3,1,3Galβ1,4Glc, Galβ1,3Galβ1,6Galβ1,4Glc, Galβ1,3Galβ1,3Galβ1,4Glc, Galβ1,4Galβ1,4Glc и Galβ1,4Galβ1,4Galβ1,4Glc или их смесь.
14. Композиция по любому из пп.7-11, в которой сиалилированный олигосахарид представляет собой NeuAcα2,3Galβ1,4Glc, NeuAcα2,6Galβ1,4Glc или их смесь.
15. Композиция по любому из пп.7-11, которая дополнительно содержит пробиотический бактериальный штамм.
16. Композиция по п.15, в которой пробиотический бактериальный штамм представляет собой Lactobacillus rhamnosus ATCC 53103, Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus reuteri DSM 17938, Streptococcus salivarius DSM 13084 или Bifidobacterium lactis CNCM 1-3446.
17. Композиция по любому из пп.7-11 или 16, которая представляет собой смесь для детского питания.