Производное селеназола, имеющее лиганд, который активирует рецептор, активируемый пролифератором пероксисом ( ppar ), способ его получения и применение химических соединений
Иллюстрации
Показать всеИзобретение относится к производному селеназола или его фармацевтически приемлемой соли. Соединение представлено формулой I:
где А представляет собой О, NR, S, S(=O), S(=O)2 или Se; В представляет собой водород или ; R1 представляет собой водород, С1-С8 алкил или галоген; R2 представляет собой водород, С1-С8 алкил, или ; Xa и Xb независимо представляют собой CR или N; R представляет собой водород или С1-С8 алкил; R3 представляет собой водород, С1-С8 алкил; R4 и R5 независимо представляют собой водород, галоген или С1-С8 алкил; R6 представляет собой водород, С1-С8 алкил, или фармацевтически приемлемую органическую соль; R21, R22 и R23 независимо представляют собой водород, галоген, NO2, С1-С7 алкил, замещенный или незамещенный галогеном, С3-С12 гетероарил, содержащий один или несколько гетероатом(ов), выбранных из N, О и S; m равно целому числу от 1 до 4; р равно целому числу от 1 до 5; s равно целому числу от 1 до 5; и равно целому числу от 1 до 3; w равно целому числу от 1 до 4; и алкил в R1, R3, R4, R5 и R6 могут быть дополнительно замещены одним или несколькими галогеном, С3-С7 циклоалкилом или С1-С5 алкиламином. Также предложены способы получения производных селеназола, фармацевтическая композиция, композиция функциональной пищевой добавки, функционального напитка, пищевой добавки, корма для животных, функциональная косметическая композиция, композиция активатора рецептора, активируемого пролифератором пероксисом (PPAR). Изобретение позволяет получить производное селеназола, которое активирует рецептор, активируемый пролифератором пероксисом (PPAR). 10 н. и 5 з.п. ф-лы, 1 ил., 6 табл., 298 пр.
Реферат
Область техники
Настоящее изобретение относится к производному селеназола - соединению, представленному химической формулой I, используемому в качестве лиганда, активирующего рецептор, активируемый пролифератором пероксисом (PPAR), которое может применяться для лечения ожирения, гиперлипемии, жировой инфильтрации печени, атеросклероза и диабета, его гидрату, сольвату, стереоизомеру и фармацевтически приемлемой соли, и фармацевтической композиции, косметической композиции, функциональной пищевой композиции, композиции функционального напитка и кормовой композиции для животных, содержащей указанные соединения:
[Химическая формула I]
Уровень техники
Рецепторы, активируемые пролифератором пероксисом (PPAR), являются ядерными рецепторами. Были идентифицированы три подтипа: PPARα, PPARγ и PPARδ (Nature, 1990, 347, p. 645-650, Proc. Natl. Acad. Sci. USA 1994, 91, p. 7335-7359). PPARα, PPARγ и PPARδ имеют различные функции и экспрессированы в различных тканях. PPARα экспрессируется в основном в сердце, почках, скелетных мышцах и тканях толстого кишечника человека (Mol. Pharmacol. 1998, 53, p. 14-22, Toxicol. Lett. 1999, 110, p. 119-127, J. Biol. Chem. 1998, 273, p. 16710-16714) и вовлечен в β-окисление в пероксисомах и митохондриях (Biol. Cell. 1993, 77, p. 67-76, J. Biol. Chem. 1997, 272, p. 27307-27312). PPARγ слабо экспрессируется в тканях скелетных мышц, но экспрессируется в основном в жировой ткани. Как известно, вовлечен в дифференцировку жировых клеток, аккумулирование энергии в виде жира и регуляцию гомеостаза инсулина и глюкозы (Moll. Cell. 1999, 4, p. 585-594, p. 597-609, p. 611-617). PPARδ эволюционно сохраняется у млекопитающих, включая человека, грызунов и асцидий. Он был идентифицирован как PPARβ у Xenopus laevis (Cell 1992, 68, p. 879-887) и у человека как NUCI (Mol. Endocrinol. 1992, 6, p. 1634-1641), PPARδ (Proc. Natl. Acad. Sci. USA 1994, 91, p. 7355-7359), NUCI (Biochem. Biophys. Res. Commun. 1993, 196, p. 671-677) или FAAR (J. Bio. Chem. 1995, 270, p. 2367-2371). В последнее время он получил унифицированное название - PPARδ. У человека, PPARδ, как известно, присутствует в хромосоме 6p21,1-p21,2. У мышей, мРНК PPARδ обнаружена в различных областях, но в меньшем количестве, чем мРНК PPARα или PPARγ (Endocrinology 1996, 137, p. 354-366, J. Bio. Chem. 1995, 270, p. 2367-2371, Endocrinology 1996, 137, p. 354-366). Согласно исследованиям, проведенным до настоящего времени, PPARδ играет очень важную роль в экспрессии гамет (Genes Dev. 1999, 13, p. 1561-1574). Кроме того, он, как известно, вовлечен в дифференцировку нервных клеток в центральной нервной системе (ЦНС) (J. Chem. Neuroanat. 2000, 19, p. 225-232), заживление ран посредством противовоспалительного действия (Genes Dev. 2001, 15, p. 3263-3277, Proc. Natl. Acad. Sci. USA 2003, 100, p. 6295-6296) или тому подобное. Проведенное в последнее время исследование показало, что PPARδ вовлечен в дифференцировку жировых клеток и метаболизм жировых клеток (Proc. Natl. Acad. Sci. USA 2002, 99, p. 303-308, Mol. Cell. Biol. 2000, 20, p. 5119-5128). Было обнаружено, что PPARδ активирует экспрессию критических генов, связанных с β-окислением и расщеплением белков (UCP), связанных с энергетическим метаболизмом, в процессе расщепления жирных кислот, и таким образом улучшает состояние при ожирении и повышает выносливость (Nature 2000, 406, p. 415-418, Cell 2003, 113, p. 159-170, PLoS Biology 2004, 2, e294, Cell, 2008, 134, 405415). Кроме того, активация PPARδ делает возможным повышение уровня ЛВП (липопротеины высокой плотности) и улучшение состояние при диабете 2 типа без изменения веса тела (Proc. Natl. Acad. Sci. USA 2001, 98, p. 5306-5311, 2003, 100, p. 15924-15929, 2006, 103, p. 3444-3449) и способствует лечению атеросклероза, путем ингибирования связанных с атеросклерозом генов (Science, 2003, 302, p. 453-457, PNAS, 2008, 105, 42714276). Соответственно, регулирование обмена жиров посредством PPARδ предоставляет важный инструмент для лечения ожирения, диабета, гиперлипемии и атеросклероза.
Описание
Техническая задача
Задача настоящего изобретения состоит в получении нового соединения, которое селективно активирует PPARδ. Другой задачей настоящего изобретения является получение фармацевтической композиции, косметической композиции, функциональной пищевой композиции, композиции функционального напитка и кормовой композиции для животных, содержащей новое соединение в соответствии с настоящим изобретением.
Решение технической задачи
Настоящее изобретение относится к соединению - производному селеназола, представленного химической формулой I, которое активирует рецептор, активируемый пролифератором пероксисом (PPAR), его сольвату, стереоизомеру и его фармацевтически приемлемой соли, способу получения указанного соединения, и к фармацевтической композиции, косметической композиции, функциональной пищевой композиции, композиции функционального напитка и кормовой композиции для животных, содержащих указанные соединения:
[Химическая формула I]
где A представляет собой O, NR, S, S(=O), S(=O)2 или Se; B представляет собой водород или ; R1 представляет собой водород, C1-C8 алкил или галоген; R2 представляет собой водород, C1-C8 алкил, или ; Xa и Xb независимо представляют собой CR или N; R представляет собой водород или C1-C8 алкил; R3 представляет собой водород, C1-C8 алкил или галоген; R4 и R5 независимо представляют собой водород, галоген или C1-C8 алкил; R6 представляет собой водород, галоген, C1-C8 алкил, C2-C7 алкенил, аллил, щелочной металл, щелочно-земельный металл или фармацевтически приемлемую органическую соль; R21, R22 и R23 независимо представляют собой водород, галоген, CN, NO2, C1-C7 алкил, C6-C12 арил, C3-C12 гетероарил, содержащий один или несколько гетероатом(ов), выбранных из N, O и S, 5-7-членный гетероциклоалкил или C1-C7 алкокси; m представляет собой целое число от 1 до 4; p представляет собой целое число от 1 до 5; s представляет собой целое число от 1 до 5; u представляет собой целое число от 1 до 3; w представляет собой целое число от 1 до 4; и алкил и алкокси в R1, R3, R4, R5, R6, R21, R22 и R23 могут быть дополнительно замещены одним или несколькими галогеном, C3-C7 циклоалкилом или C1-C5 алкиламином.
Особенно предпочтительным производным селеназола, активирующим PPAR, представленным химической формулой I, является производное, в котором: R1 представляет собой водород, C1-C5 алкил, замещенный одним или несколькими фтором, или фтор; R2 представляет собой водород, C1-C8 алкил, или ; Xa и Xb независимо представляют собой CR или N; R представляет собой водород или C1-C8 алкил; R3 представляет собой водород, C1-C5 алкил, замещенный или незамещенный галогеном, или галоген; R4 и R5 независимо представляют собой водород, C1-C5 алкил, замещенный или незамещенный галогеном; R6 представляет собой водород, C1-C8 алкил, галоген, аллил, C2-C7 алкенил, фармацевтически приемлемую органическую соль, щелочной металл или щелочно-земельный металл; и R21, R22 и R23 независимо представляют собой водород, галоген, CN, NO2, C1-C7 алкил, замещенный или незамещенный галогеном, C6-C12 арил, C3-C12 гетероарил, содержащий один или несколько гетероатом(ов), выбранных из N, O и S, 5-7-членный гетероциклоалкил или C1-C5 алкокси, замещенный или незамещенный галогеном.
В химической формуле I, R1 может представлять собой водород, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 2-этилгексил, фторметил, дифторметил, трифторметил, 2-фторэтил, пентафторэтил, фтор, бром, йод или хлор; R2 может представлять собой водород или замещенный или незамещенный бензил, фенилбензил или пиридилбензил, где фенил, пиридил или бензил в R2 может быть дополнительно замещен фтором, хлором, метилом, этилом, н-пропилом, изо-пропилом, трет-бутилом, фторметилом, дифторметилом, трифторметилом, 2-фторэтил, пентафторэтил, метокси, этокси, пропилокси, н-бутокси, трет-бутокси, фторметокси, дифторметокси, трифторметокси, 2-фторэтокси, пентафторэтокси, CN, NO2, C6-C12 арилом или C3-C12 гетероарилом, содержащим один или несколько гетероатом(ов), выбранных из N, O и S; R3 может представлять собой водород, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 2-этилгексил, фторметил, дифторметил, трифторметил, 2-фторэтил, пентафторэтил, фтор, хлор; R4 и R5 могут независимо представлять собой водород, галоген, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 2-этилгексил, фторметил, дифторметил, трифторметил, 2-фторэтил или пентафторэтил; и R6 может представлять собой водород, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 2-этилгексил, фторметил, дифторметил, трифторметил, 2-фторэтил, пентафторэтил, аллил, этенил, 2-пропенил, 2-бутенил, 3-бутенил, фармацевтически приемлемую органическую соль, Li+, Na+, K+, Ca2+ или Mg2+.
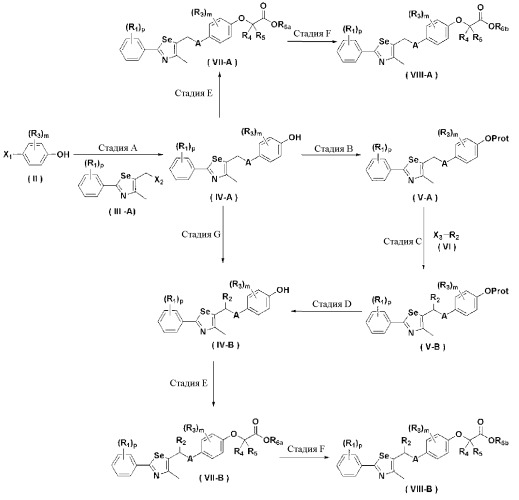
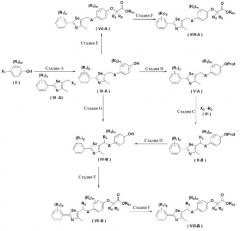
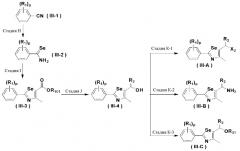
Новые соединения по настоящему изобретению могут быть получены способами, представленными на схемах 1-5. На схеме 1, A представляет собой O, NR, S или Se. На схеме 2, А представляет собой NR. На схеме 3, А представляет собой O.
[Схема 1]
[Схема 2]
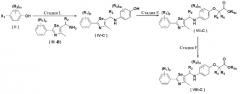
[Схема 3]
На схемах 1-3, A представляет собой O, NR, S или Se; R1, R2, R3, m, p и s являются такими, как определено для химической формулы I; R6a представляет собой C1-C8 алкил или аллил; R6b представляет собой водород, щелочной металл (Li+, Na+, K+), щелочно-земельный металл (Ca2+, Mg2+) или фармацевтически приемлемую органическую соль; Prot представляет собой защитную группу фенола, выбранную из C1-C4 алкила, аллила, алкилсилила, алкиларилсилила или тетрагидропиранила; X1 представляет собой бром или йод; X2 и X3 независимо представляют собой хлор, бром, йод или другую удаляемую группу, подходящую для нуклеофильного замещения.
Соединения химической формулы III-A, III-B и III-C могут быть получены в соответствии со схемой 4.
[Схема4]
На схеме 4, R1, R2 и p являются такими, как определено в химической формуле I; R31 представляет собой C1-C4 алкилсульфонил или C6-C12 арилсульфонил, замещенный или незамещенный C1-C4 алкилом; R101 представляет собой C1-C4 алкил; и X2 представляет собой хлор, бром, йод или другую удаляемую группу, подходящую для нуклеофильного замещения.
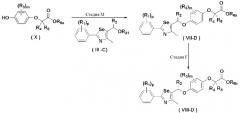
[Схема 5]
Далее способ получения в соответствии с настоящим изобретением описан более подробно.
[Стадия A] Получение соединения, представленного химической формулой (IV-A)
Для получения соединения, представленного химической формулой (IV-A), в фенольную группу соединения, представленного химической формулой (II), вводят защитную группу с помощью реактива Гриньяра без процесса разделения. Затем полученное соединение подвергают взаимодействию с металлоорганическим реагентом и серой (S) или селеном (Se), и далее с соединением, представленным химической формулой (III-A). Эта стадия включает четырехстадийные взаимодействия, которые выполняются сразу.
Подробное описание представлено далее.
[Защита фенольной группы с помощью реактива Гриньяра]
В качестве безводного растворителя используют диэтиловый эфир, тетрагидрофуран, гексан, гептан или смесь двух или более этих веществ. Из них диэтиловый эфир, тетрагидрофуран или смешанный растворитель, состоящий из диэтилового эфира и тетрагидрофурана, являются предпочтительными. Особенно предпочтительным является полярный растворитель. Наиболее предпочтительным является тетрагидрофуран.
Реактивом Гриньяра может быть хлорид метилмагния, хлорид этилмагния, хлорид н-пропилмагния, хлорид изопропилмагния, хлорид н-бутилмагния, хлорид втор-бутилмагния или бромид алкилмагния. Из них наиболее предпочтительным является хлорид изопропилмагния ((CH3)2CHMgCl).
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно реакцию проводят при температуре в пределах от -20 до 40ºC, предпочтительно, при температуре в пределах от 0ºC до комнатной температуры (25ºC). Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно реакцию проводят в течение 10-60 минут, предпочтительно в течение 10-30 минут.
[Галоген-литий замещение и введение серы (S) или селена (Se)]
При галоген-литий замещении может быть использован металлоорганический реагент, такой как н-бутиллитий, втор-бутиллитий, трет-бутиллитий и так далее. Из них, трет-бутиллитий является предпочтительным.
Предпочтительно, сера (S) или селен (Se) представлены в виде тонкодисперсного порошка и добавлялись непосредственно или в виде раствора в безводном тетрагидрофуране.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, взаимодействие осуществляют при температуре от -78 до 25ºC. Предпочтительно, галоген-металл замещение осуществляют при -75ºC, и введение серы (S) или селена (Se) начинают при температуре -75ºC и проводят при комнатной температуре (25ºC). Галоген-металл замещение осуществляют в течение от 10 до 30 минут, и введение серы (S) или селена (Se) осуществляют в течение от 30 до 120 минут.
[Добавление соединения, представленного химической формулой (III-A)]
Соединение, представленное химической формулой (III), синтезируют посредством стадий H и K. Галогеном у соединения, представленного химической формулой (III-A), может быть хлор, бром или йод. Из них хлор является предпочтительным.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, реакцию проводят при температуре от -78 до 25ºC, предпочтительно, при температуре от 0 до 10ºC. Время реакции обычно составляет от 10 до 120 минут, предпочтительно, от 10 до 60 минут.
[Стадия B] Получение соединения, представленного химической формулой (V-A)
Для получения соединения, представленного химической формулой (V-A), соединение, представленное химической формулой (IV-A), может быть подвергнуто взаимодействию с соединением, обычно используемым для введения защитной группы фенола в присутствии основания.
Защитной группой фенола может быть C1-C4 алкил, аллил, алкилсилил, такой как триметилсилил, трет-бутилдифенилсилил, триизопропилсилил, трет-бутилдиметилсилил и так далее, алкиларилсилил, тетрагидропиранил или тому подобное. Из них, трет-бутил, тетрагидропиранил и силил являются предпочтительными.
На этой стадии может быть использован апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, ацетонитрил, ацетон, этилацетат, тетрахлорид углерода, хлороформ, дихлорметан или тому подобное. Также может быть использован простой эфир, такой как тетрагидрофуран, диоксан, диметоксиэтан, диметиловый эфир диэтиленгликоля, диметиловый эфир триэтиленгликоля или тому подобное. Также может быть использован ароматический углеводород, такой как бензол, толуол, ксилол или тому подобное. Из них, апротонный полярный растворитель является предпочтительным. Наиболее предпочтительными являются N,N-диметилформамид, хлороформ и дихлорметан.
Основанием может быть основание на основе амина, такое как пиридин, триэтиламин, имидазол, N,N-диметиламинопиридин или тому подобное. Реакцию образования алкильной или аллильной эфирной защитной группы осуществляют с использованием в качестве основания гидроксида натрия, гидроксида калия, карбоната натрия, карбоната калия или тому подобное. Из них, имидазол и карбонат калия являются предпочтительными.
Тетрагидропиранильную защитную группу получают путем взаимодействия 3,4-дигидро-2H-пирана с алкил или аллил трифенилфосфонийбромидом в присутствии катализатора.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, реакцию проводят при температуре от -10 до 80ºC, предпочтительно, при температуре от 0ºC до комнатной температуры (25ºC). Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно, реакцию проводят в течение от 1 часа до 1 дня, предпочтительно, в течение 4 часов или менее.
[Стадия C] Получение соединения, представленного химической формулой (V-B)
Соединение, представленное химической формулой (V-B), получают путем обработки α-протона тио- или селеноэфирного соединения, представленного химической формулой (V-A), с сильным основанием с получением нуклеофила, и далее взаимодействием с различными электрофилами.
На этой стадии, в качестве безводного растворителя используют диэтиловый эфир, тетрагидрофуран, гексан, гептан или смесь двух или более из них. Из них, диэтиловый эфир, тетрагидрофуран или смесь растворителей диэтилового эфира и тетрагидрофурана являются предпочтительными.
Для экстрагирования α-протона может быть использовано сильное основание, такое как трет-бутоксид калия (трет-BuOK), диизопропиламид лития (LDA), н-бутиллитий, втор-бутиллитий, трет-бутиллитий или тому подобное. Из них, LDA является наиболее предпочтительным.
Электрофил, который взаимодействует с нуклеофилом, может быть известным соединением, которое является легкодоступным, или может быть легко получен в соответствии с известным способом. Он может содержать высоко реакционноспособную группу галогена, альдегида или кетона, и его добавляли напрямую или растворенным в безводном растворителе.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, реакцию проводят при температуре от -78 до 25ºC. Предпочтительно, экстрагирование α-протона с использованием сильного основания осуществляют при температуре от -75ºC. Электрофил добавляли при температуре -75ºC и потом температуру медленно повышают до комнатной температуры (25ºC). Время реакции может изменяться в зависимости от стадий. Экстрагирование α-протона с использованием сильного основания осуществляют в течение от 10 до 30 минут, и взаимодействие с электрофилом осуществляют в течение от 30 до 90 минут.
[Стадия D] Получение соединения, представленного химической формулой (IV-B)
Соединение, представленное химической формулой (IV-B), получают путем удаления защитной группы фенола у соединения, представленного химической формулой (V-B).
На этой стадии может быть использован полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, ацетонитрил, ацетон, этилацетат, тетрахлорид углерода, хлороформ, дихлорметан или тому подобное. В качестве эфира может быть использован тетрагидрофуран, диоксан, диметоксиэтан, диэтиленгликоль диметиловый эфир или тому подобное. В качестве спирта может быть использован метанол, этанол или тому подобное. В качестве ароматического углеводорода может быть использован бензол, толуол, ксилол или тому подобное. Из них полярный растворитель является предпочтительным. Наиболее предпочтительным является тетрагидрофуран.
Для удаления защитной группы фенола используют кислоту Льюиса, такую как триметилсилил йодид, этантиоалкоголят натрия, йодид лития, галогенид алюминия, галогенид бора, трифторуксусную кислоту и так далее, для метильной, этильной, трет-бутильной, бензильной и аллильной эфирной защитных групп, и используют фторид, такой как тетрабутиламмоний фторид (Bu4N+F-), галогенкислоту (например, фтористоводородную кислоту, хлористоводородную кислоту, бромноватую кислоту или йодноватую кислоту), фторид калия и так далее, для силильных защитных групп, таких как триметилсилил, трет-бутилдифенилсилил, триизопропилсилил, трет-бутилдиметилсилил и так далее. Из них, фторид является предпочтительным для удаления силильной защитной группы. Более предпочтительно, может быть использован тетрабутиламмоний фторид.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, реакцию проводят при температуре от 0-120ºC, предпочтительно, при температуре от 10ºC-25ºC. Время реакции может изменяться в зависимости от температуры реакции. Обычно, реакцию проводят в течение от 30 минут до 1 дня, предпочтительно, в течение 2 часов или меньше.
[Стадия E] Получение соединения, представленного химической формулой (VII)
Для получения соединения, представленного химической формулой (VII), соединение, представленное химической формулой (IV), подвергают взаимодействию с алкиловым эфиром галогенуксусной кислоты или алкиловым эфиром алкилгалогенуксусной кислоты в присутствии основания.
Алкиловый эфир галогенуксусной кислоты или алкиловый эфир алкилгалогенуксусной кислоты может быть легко доступным известным соединением. Недоступный алкиловый эфир алкилгалогенуксусной кислоты может быть получен бромированием алкилового эфира алкилуксусной кислоты. Галогеном может быть хлор, бром, йод или тому подобное.
На этой стадии в качестве растворителя может быть использован водорастворимый растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, ацетонитрил, ацетон, этанол и метанол или смесь, содержащая 1-10% воды. Из них ацетон или диметилсульфоксид, содержащий 1-5% воды, является наиболее предпочтительным.
Основанием может быть либо слабое основание, либо сильное основание, без особых ограничений, в той степени, насколько отсутствует отрицательное влияние на реакцию. Сильным основанием может быть гидрид щелочного металла, такой как гидрид натрия, гидрид лития и так далее, гидрид щелочноземельного металла, такой как гидрид калия и так далее, или гидроксид щелочного металла, такой как гидроксид натрия, гидроксид калия и так далее. Кроме того, может быть использован карбонат щелочного металла, такой как карбонат лития, карбонат калия, бикарбонат калия, карбонат цезия и так далее. Предпочтительно, основанием является карбонат щелочного металла, более предпочтительно, карбонат калия.
Температуру реакции особо не ограничивают в той степени, насколько она ниже точки кипения растворителя. Однако реакция при высокой температуре не является предпочтительной, поскольку могут протекать побочные реакции. Обычно, реакцию проводят при температуре от 0 до 90ºC. Время реакции может изменяться в зависимости от температуры реакции. Обычно, реакцию проводят в течение от 30 минут до 1 дня, предпочтительно, в течение 30-120 минут.
[Стадия F-1] Получение соединения, представленного химической формулой (VIII).
Соединение, представленное химической формулой (VIII), получают гидролизом сложного эфира карбоновой кислоты соединения, представленного химической формулой (VII), в растворе водорастворимой неорганической соли и спирта, или гидролизом сложного эфира соединения, представленного химической формулой (VII), в растворе 2,0 M гидроксида лития в ТГФ и воде.
На этой стадии используют смешивающийся с водой спиртовой растворитель, такой как метанол или этанол.
В зависимости от конкретной используемой щелочной соли карбоновой кислоты, в качестве основания используют от 0,1 до 3н водный раствор гидроксида щелочного металла, такого как гидроксид лития, гидроксид натрия, гидроксид калия и так далее. Предпочтительно, кислота, используемая для получения соединения, представленного химической формулой (VIII), в качестве карбоновой кислоты, может быть уксусной кислотой, бисульфатом натрия (NaHSO4) или от 0,1 до 3н HCl. Обычно, для получения соединения, представленного химической формулой (VIII), в качестве карбоновой кислоты, может быть использован 0,5M NaHSO4.
Низкая температура реакции является предпочтительной для предотвращения побочных реакций. Обычно, реакцию проводят при температуре от 0ºC до комнатной температуры. Время реакции может изменяться в зависимости от температуры реакции. Обычно, реакцию проводят в течение от 10 минут до 3 часов, предпочтительно, в течение от 30 минут до 1 часа. В том случае, когда реакцию проводят в растворе 2,0 M гидроксида лития в ТГФ и воде, температура реакции обычно 0ºC, и время реакции, предпочтительно, составляет 1 до 2 часов.
[Стадия F-2] Получение соединения, представленного химической формулой (VIII).
Соединение, представленное химической формулой (VIII), получают замещением соли аллилового эфира соединения, представленного химической формулой (VII), в органическом растворителе с использованием катализатора на основе металла и соли щелочного металла или соли щелочноземельного металла 2-этилгексаноата.
На этой стадии используют безводный органический растворитель, такой как хлороформ, дихлорметан, этилацетат и так далее.
Катализатором на основе металла является тетракис(трифенилфосфин)палладий (Pd(PPh3)4), и катализатор на основе металла может быть использован в количестве от 0,01 до 0,1 эквивалента.
Низкая температура реакции является предпочтительной для предотвращения побочных реакций. Обычно реакцию проводят при температуре от 0ºC до комнатной температуры. Время реакции может изменяться в зависимости от температуры реакции. Обычно, реакцию проводят в течение от 10 минут до 3 часов, предпочтительно, в течение от 30 минут до 1 часа.
Полученную соль соединения отделяют центрифугированием или с использованием ионнообменной смолы. Полученная соль металла соединения, представленного химической формулой (VIII), легче отделяется, чем соль соединения, полученного на стадии F-1 (гидролиз).
[Стадия G] Получение соединения, представленного химической формулой (IV-B)
Соединение, представленное химической формулой (IV-B), получают путем защиты фенольной группы соединения, представленного химической формулой (IV-A), с помощью реактива Гриньяра без процесса разделения, обработкой α-протона полученного тио- или селеноэфира сильным основанием с получением нуклеофила, и последующим взаимодействием с различными электрофилами. Эта стадия включает двух стадийные взаимодействия, которые выполняются сразу.
Далее следует подробное описание.
[Защита фенольной группы с помощью реактива Гриньяра]
На этой стадии в качестве безводного растворителя используют диэтиловый эфир, тетрагидрофуран, гексан, гептан или смесь двух или более этих веществ. Из них наиболее предпочтительным является диэтиловый эфир, тетрагидрофуран или смесь диэтилового эфира и тетрагидрофурана. Особенно предпочтительным является полярный растворитель. Наиболее предпочтительным является тетрагидрофуран.
Реактивом Гриньяра может быть метилмагний хлорид, этилмагний хлорид, н-пропилмагний хлорид, изопропилмагний хлорид, н-бутилмагний хлорид, втор-бутилмагний хлорид или алкилмагний бромид. Из них наиболее предпочтительным является изопропилмагний хлорид ((CH3)2CHMgCl).
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно реакцию проводят при температуре от -20 до 40ºC, предпочтительно, в пределах от 0ºC до комнатной температуры (25ºC). Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно, реакцию проводят в течение 10-60 минут, предпочтительно, в течение 10-30 минут.
[Экстракция α-протона и электрофильное присоединение]
α-Протон тио- или селеноэфира обрабатывали сильным основанием с получением нуклеофила, который затем взаимодействует с различными электрофилами.
На этой стадии в качестве безводного растворителя используют диэтиловый эфир, тетрагидрофуран, гексан, гептан или смесь двух или более этих веществ. Из них, диэтиловый эфир, тетрагидрофуран или смесь диэтилового эфира и тетрагидрофурана являются наиболее предпочтительными.
Реагентом сильного основания, используемым для экстрагирования α-протона, может быть трет-бутоксид калия (трет-BuOK), диизопропиламид лития (LDA), н-бутиллитий, втор-бутиллитий, трет-бутиллитий или тому подобное. Из них LDA является наиболее предпочтительным.
Электрофил, который подвергают взаимодейставию с нуклеофилом тио- или селеноэфиром, может быть легко доступным известным соединением или может быть легко получен известным способом. Он может содержать высоко реакционноспособную группу галогена, альдегида или кетона, и его добавляли напрямую или растворенным в безводном растворителе.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно реакцию проводят при температуре в пределах от -78 до 25ºC. Предпочтительно, экстрагирование α-протона с использованием сильного основания выполняют при -75ºC. Электрофил добавляли при -75ºC и потом температуру медленно повышают до комнатной температуры (25ºC). Время реакции может изменяться в зависимости от стадии. Экстрагирование α-протона с использованием сильного основания проводят в течение 10-30 минут, и взаимодействие с электрофилом проводят в течение 30-90 минут.
[Стадия H] Получение соединения, представленного химической формулой (III-2)
Соединение, представленное химической формулой (III-2), может быть получено восстановлением металлического селена сильным восстанавливающим агентом - боргидридом натрия в спиртовом растворителе с получением гидроселенида натрия, взаимодействия его с арилнитрильным соединением, представленным химической формулой (III-1), в среде сильной кислоты, такой как HCl, при нагревании с обратным холодильником с получением селенокарбамата. На этой стадии в качестве растворителя используют спирт, такой как метанол и этанол, а также большое количество пиридина. Предпочтительно, используют боргидрид натрия и порошок металлического селена в эквивалентных количествах и используют 2-3 M HCl кислоту.
[Стадия I] Получение соединения, представленного химической формулой (III-3)
Соединение, представленное химической формулой (III-3), получают взаимодействием соединения, представленного химической формулой (III-2), с C1-C4 алкил 2-хлорацетоацетатом.
На этой стадии в качестве растворителя могут быть использованы спирт, такой как метанол, этанол, пропанол, бутанол и так далее, или эфир, такой как этиловый эфир, тетрагидрофуран, 1,4-диоксан и так далее. Из них этанол и тетрагидрофуран являются предпочтительными.
Температура реакции может изменяться в зависимости от используемого растворителя. Обычно, реакцию проводят при температуре от 25 до 150ºC, предпочтительно, при 60-120ºC. Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно, реакцию проводят в течение 6 час - 1 день, предпочтительно, в течение 16 часов или меньше.
[Стадия J] Получение соединения, представленного химической формулой (III-4)
Спиртовое соединение, представленное химической формулой (III-4), получают восстановлением сложного эфира соединения, представленного химической формулой (III-3), с использованием восстанавливающего агента.
Восстанавливающий агент, используемый для восстановления эфира, может представлять собой восстанавливающий агент - гидрид алюминия, такой как алюмогидрид лития (LiAlH4), гидрид диизобутилалюминия (DIBAL-H) и так далее, или восстанавливающий агент - боргидрид, такой как боргидрид натрия, боргидрид лития и так далее. Из них восстанавливающий агент - гидрид алюминия является предпочтительным. Наиболее предпочтительными являются LiAlH4 и DIBAL-H.
На этой стадии в качестве безводного растворителя могут быть использованы диэтиловый эфир, тетрагидрофуран, дихлорметан или тому подобное. Дихлорметан является наиболее предпочтительным.
Время реакции может изменяться в зависимости от растворителя и используемого восстанавливающего агента. Обычно, реакцию проводят при температуре от -100 до 60ºC, предпочтительно, при -78ºC - 25ºC. Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно, реакцию проводят в течение от 30 минут до 6 часов, предпочтительно, в течение 2 часов или меньше.
[Стадия K] Получение соединения, представленного химической формулой (III)
Соединение, представленное химической формулой (III-A), может быть получено путем галогенирования спиртовой группы соединения, представленного химической формулой (III-4). Соединение, представленное химической формулой (III-B), может быть получено из соединения, представленного химической формулой (III-4), с использованием NaN3. И, соединение, представленное химической формулой (III-C), может быть получено введением алкил- или арил-замещенного сульфонилхлорида, предпочтительно, метансульфонилхлорида или п-толуолсульфонилхлорида, по гидроксильной группе соединения, представленного химической формулой (III-4).
При галогенировании и введении метансульфонилокси или п-толуолсульфонилокси группы в качестве растворителя может быть использован N,N-диметилформамид, диэтиловый эфир, тетрагидрофуран, тетрахлорид углерода, хлороформ, дихлорметан, пиридин или тому подобное. Из них, дихлорметан является предпочтительным в большинстве случаев при галогенировании, и пиридин является предпочтительным в большинстве случаев при введении метансульфонилокси или п-толуолсульфонилокси группы.
Галогенирование спирта может быть осуществлено с использованием трифенилфосфина (TPP) и N-хлорсукцинимида (NCS), трифенилфосфина и газообразного хлора (Cl2), трифенилфосфина и тетрахлорида углерода (CCl4), пентахлорида фосфора (PCl5), тионилхлорида (SOCl2) или метансульфонил хлорида (MeSO2Cl) или тому подобное для введения хлора, с использованием трифенилфосфина и N-бромсукцинимида (NBS), трифенилфосфина и газообразного брома (BR3), трифенилфосфина и тетрабромида углерода (CBr4), пентабромида фосфора (PBr5) или тионилбромида (SOBr2) или тому подобное для введения брома, и с использованием трифенилфосфина и N-йодсукцинимида, трифенилфосфина и твердого йода, трифенилфосфина и тетрайодида углерода (CI4) или тому подобное для введения йода или путем галоген-йод замещения хлор или бром соединения, представленного химической формулой (IV-A), в ацетоне. Введение метансульфонилокси или п-толуолсульфонилокси группы может быть осуществлено путем взаимодействия с метансульфонилхлоридом или п-толуолсульфонилхлоридом в растворителе пиридине. Наиболее предпочтительной удаляемой группой является хлор или бром, и наиболее предпочтительным способом получения является способ с использованием трифенилфосфина и N-хлорсукцинимида или N-бромсукцинимида.
На этой стадии температура реакции может изменяться в зависимости от способа получения и используемого растворителя. Обычно, реакцию проводят при температуре в пределах от -10 до 40ºC, предпочтительно, при 10-25ºC. Время реакции может изменяться в зависимости от температуры реакции и используемого растворителя. Обычно реакцию проводят в течение от 30 минут до 1 дня, предпочтительно в течение 2 часов или меньше.
[Стадия L] Получение соединения, представленного химической формулой (L-1) или (L-2)
Соединение, представленное химической формулой (L-1), может быть получено путем растворения соединения, представленного химической формулой (VII), полученного на стадии E, в метиленхлориде (CH2Cl2) и добавления 1 эквивалента м-хлорпербензойной кислоты (м-CPBA), поддерживая температуру реакции при от 0 до 5ºC. И, соединение, представленное химической формулой (L-2), может быть получено добавлением 2 эквивалентов м-CPBA.
Полученное таким образом соединение, представленное химической формулой I, является важным лигандом белка PPAR. Поскольку соединение имеет хиральный углерод, существуют его стереоизомеры. Настоящее изобретение включает соединение производное селеназола химической формулы I, его стереоизомер, его сольват и его соль.
Производное селеназола - соединение, представленное химической формулой I, по настоящему изобретению или фармацевтически приемлемую соль соединения используют в качестве активатора PPAR. Кроме того, производное селеназола, представленное химической формулой I, по настоящему изобретению, его гидрат, сольват, стереоизомер и его фармацевтически приемлемую соль используют для фармацевтической композиции, композиции функциональной пищевой добавки, композиции функционального напитка, композиции пищевой добавки, функциональной косметической композиции или композиции корма для животных для профилактики или лечения атеросклероза, жировой инфильтрации печени или гиперлипемии, профилактики или лечения гиперхолестеримении, профилактики или лечения диабета, профилактики или лечения ожире