Меченные радиоактивной меткой ингибиторы переносчика глицина 1
Иллюстрации
Показать всеИзобретение относится к новым меченным радиоактивным изотопом соединения формулы I
в котором R1 представляет собой изопропокси или 2,2,2-трифтор-1-метил-этокси; и R2 представляет собой меченную радиоактивным изотопом группу СН3, где радионуклид представляет собой 3H или 11С. Изобретение также относится к фармацевтической композиции для диагностической визуализации переносчика GlyT1 (переносчика глицина 1 типа). Технический результат: получены новые меченные радиоактивным изотопом соединения, которые могут найти применение в медицине в качестве радиоактивного индикатора в PET (позитронной эмиссионной томографии) для мечения и диагностической молекулярной визуализации функциональности переносчика глицина 1 типа. 5 н. и 8 з.п. ф-лы, 4 пр.
Реферат
Настоящее изобретение относится к новым меченным радиоактивным изотопом ингибиторам, имеющим общую формулу I, переносчика глицина 1 типа (GlyT1), полезным для мечения и диагностической визуализации функциональности переносчика глицина 1 типа
где
R1 представляет собой изопропокси или 2,2,2-трифтор-1-метил-этокси; и
R2 представляет собой меченную радиоактивным изотопом группу СН3, где радионуклид представляет собой 3Н или 11С.
Обнаружено, что меченные радиоактивным изотопом соединения формулы I могут быть использованы в качестве радиоактивного индикатора в PET (позитронной эмиссионной томографии) для мечения и диагностической молекулярной визуализации функциональности переносчика глицина 1 типа. Молекулярная визуализация основана на селективном и специфическом взаимодействии молекулярного зонда (например, радиоактивного индикатора) с биологической мишенью (например, рецептором, ферментом, ионным каналом или любым другим клеточным компонентом, который способен связываться с молекулярным зондом или удерживать молекулярный зонд), который визуализируется посредством PET, ядерного магнитного резонанса, спектроскопии в ближней инфракрасной области или других методов. PET, средство визуализации методами ядерной медицины, идеально подходит для получения трехмерных изображений, которые дают важную информацию о распределении биологической мишени в заданном органе, или о метаболической активности такого органа или клетки, или о способности лекарственного средства проникать в такой орган, связываться с биологической мишенью и/или модифицировать биологические процессы. Поскольку PET является неинвазивным методом визуализации, его можно использовать для изучения патофизиологии заболевания и действия лекарственного средства на заданную молекулярную мишень или клеточные процессы у людей и у животных. Доступность радиоактивного индикатора для использования в PET, специфичного к заданной молекулярной мишени, может способствовать разработке лекарственного препарата и пониманию механизма действия лекарственного средства. К тому же, радиоактивный индикатор для PET может способствовать постановке диагноза заболевания посредством демонстрации патофизиологических изменений, имеющих место вследствие заболевания.
Ингибиторы переносчика глицина подходят для лечения неврологических и психоневрологических расстройств. Большинство непосредственно вовлеченных болезненных состояний представляют собой психозы, шизофрению (Armer RE and Miller DJ, Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001), психотические расстройства настроения, такие как тяжелое главное депрессивное расстройство, расстройства настроения, ассоциированные с психотическими заболеваниями, такими как острый маниакальный синдром или депрессия, ассоциированные с биполярными расстройствами, и расстройства настроения, ассоциированные с шизофренией (Pralong ЕТ et al., Prog. Neurobioi, 67: 173-202, 2002), аутистические расстройства (Carlsson ML, J. Neural Trans. 105: 525-535, 1998), когнитивные расстройства, такие как деменции, включая возрастную деменцию и сенильную деменцию альцгеймерова типа, расстройства памяти у млекопитающего, в том числе человека, синдромы дефицита внимания и боль (Armer RE and Miller DJ, Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001).
Человеческий головной мозг представляет собой сложный орган, состоящий из миллионов нейронов, осуществляющих внутренние связи. Понимание нарушений, относящихся к заболеваниям, является ключом к будущей разработке эффективных диагностических и новых терапевтических средств. Исследование биохимических нарушений у человека стремительно становится существенным и неотделимым компонентом изобретения лекарственных средств и процесса их разработки. Традиционно, изобретение и разработку новых лекарственных средств осуществляли с особым акцентом на методы in vitro с целью отбора перспективных лучших кандидатов, которые потом тестировали на живых животных перед введением людям. Вследствие того, что системы in vitro отражают только часть разнообразия живых систем, а животные модели in vivo заболевания человека зачастую представляют собой только некое приближение к патологии человека, все более растет осознание того, что ясное понимание взаимодействия лекарственного средства с рецептором у живого человека на ранней стадии этого процесса будет представлять собой главную движущую силу в придании дополнительного импульса для эффективного и своевременного изобретения и разработки новых терапевтических средств. В течение последних лет возрастает количество случаев применения диагностической визуализации на людях для оценки патологий, болезненных процессов и действия лекарственных средств. Эти средства визуализации включают PET, MRI (магнитно-резонансную визуализацию), СТ (компьютерную томографию), ультразвуковое исследование, EEG (электроэнцефалографию), SPECT (однофотонную эмиссионную компьютерную томографию) и другие (British Medical Bulletin, 2003, 65, 169-177). Следовательно, использование неинвазивных средств визуализации, например PET, является бесценным инструментом для разработки лекарственных средств в будущем. Неинвазивные методы ядерной визуализации можно использовать для получения основной и диагностической информации о физиологии и биохимии разнообразных живых субъектов. Эти методы опираются на применение утонченной визуализирующей аппаратуры, которая способна детектировать излучение, испускаемое радиоактивными индикаторами, введенными таким живым субъектам. Полученную информацию можно преобразовать с получением плоскостных и томографических изображений, которые показывают распределение радиоактивного индикатора как функцию от времени. Результатом использования радиоактивных индикаторов может быть получение изображений, которые содержат информацию о структуре, функции и, что наиболее важно, физиологии и биохимии субъекта. Большую часть этой информации невозможно получить другими методами. Радиоактивные индикаторы, используемые в этих исследованиях, разработаны с возможностью определения поведения in vivo, что дает возможность определить специфическую информацию, касающуюся физиологии или биохимии субъекта. В настоящее время радиоактивные индикаторы доступны для получения полезной информации, касающейся сердечной деятельности, кровотока в миокарде, легочной перфузии, функции печени, кровотока в головном мозге, регионального метаболизма глюкозы и кислорода в головном мозге (WO 2007/041025). Кроме того,
- РЕТ-визуализация позволяет провести неинвазивный и количественный анализ нормальной и аномальной нейрохимии у человека на ранней стадии разработки лекарственных средств с целью придания дополнительного импульса для продуктивного и эффективного изобретения терапевтических средств;
- использование индикаторных доз меченых соединений позволяет осуществить начальную оценку новых лекарственных средств: исследования биологического распределения; исследования степени занятости рецепторов для оптимизации режима дозирования лекарственных средств и характеристику последующих ответов на действие лекарственного средства;
- понимание механизмов заболевания у человека с использованием неинвазивных методов непосредственно связано с будущими разработками в диагностике и лечении заболеваний и разработками новых терапевтических средств.
Обычно используемые в PET радионуклиды включают 11C, 13N, 15O или 18F. В принципе, существует возможность ввести метку в любые лекарственные средства с получением аналога исходного соединения, однако обнаружено, что только некоторые их них пригодны в качестве визуализирующих агентов in vivo для людей. Периоды полураспада радиоактивных элементов 11С, 13N, 15O и 18F составляют 20, 10, 2 и 110 мин соответственно. Такие короткие периоды полураспада предоставляют ряд преимуществ в отношении их применения в качестве радиоизотопных индикаторов для исследования биологических процессов in vivo посредством PET. Возможно проведение повторных исследований того же субъекта в тот же день. PET все чаще используется в качестве инструмента для определения взаимосвязи между дозой лекарственного средства и степенью занятости ферментов/рецепторов для строго определенных соединений. Применение радиоактивный индикаторов для PET, которые специфически связываются с целевым рецептором или ферментом, может дать информацию о
- способности лекарственного средства проникать в головной мозг и связываться с сайтом-мишенью,
- степени занятости сайта-мишени, обуславливаемой действием заданной дозы лекарственного средства,
- зависимости занятости от времени и
- относительной кинетике в плазме и ткани рассматриваемого лекарственного средства.
Исследования занятости выполняют с использованием радиоактивных индикаторов для PET, которые обычно не идентичны исследуемому лекарственному средству-кандидату (British Medical Bulletin, 2003, 65, 169-177).
Задача настоящего изобретения заключалась в нахождении новых радиоактивных индикаторов для in vivo PET-визуализации переносчика глицина 1 типа. Обнаружено, что полученные меченные радиоактивным изотопом соединения формулы I могут быть использованы в качестве визуализирующего агента для визуализации переносчика глицина 1 типа у людей. Настоящим изобретением охвачены следующие далее меченные радиоактивным изотопом соединения:
меченное радиоактивным изотопом соединение формулы
меченное радиоактивным изотопом соединение формулы
меченное радиоактивным изотопом соединение формулы
и
меченное радиоактивным изотопом соединение формулы
Другими воплощениями данного изобретения являются соединения формулы I для применения в качестве лиганда GlyT1, для применения в исследовании связывания с GlyT1 и для применения в качестве радиоактивных индикаторов для PET.
Кроме того, соединения по настоящему изобертению могут быть использованы для диагностической визуализации GlyT1 в головном мозге млекопитающего.
Данное изобретение включает способ диагностической визуализации переносчика GlyT1, включающий введение млекопитающему эффективного количества соединения формулы I, и включает способ определения функциональности GlyT1 в ткани млекопитающего, включающий введение млекопитающему, для которого желательно такое определение, эффективного количества соединения формулы I.
Задача настоящего изобретения заключается в применении соединения формулы I для изготовления лекарственного средства для диагностической визуализации GlyT1 в головном мозге млекопитающего и фармацевтической композиции, содержащей такое соединение и фармацевтически приемлемый эксципиент.
Ингибиторы переносчиков GlyT1 полезны для лечения болезней, которые представляют собой психозы, боль, расстройство функции памяти и обучения, шизофрению, деменцию и другие заболевания, при которых нарушены когнитивные процессы, такие как синдромы дефицита внимания или болезнь Альцгеймера. Предпочтительным показанием является шизофрения.
Шизофрения представляет собой прогрессирующее и вызывающее помрачение рассудка неврологическое заболевание, характеризующееся эпизодическими позитивными симптомами, такими как бредовые идеи, галлюцинации, нарушения мышления и психоз, и устойчивыми негативными симптомами, такими как эмоциональная тупость, ослабленное внимание и социальная самоизоляция, и когнитивными нарушениями.
Немеченные радиоактивным изотопом соединения известны в предшествующем уровне техники и описаны в WO 2006/082001 в качестве ингибиторов переносчиков GlyT1.
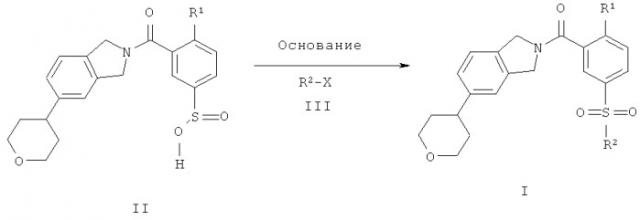
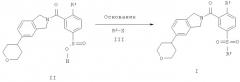
Схема 1 представляет собой путь синтеза соединений формулы (I), где R2 представляет собой меченную радиоактивным изотопом группу
Схема 1
Соединение формулы II приводят во взаимодействие с основанием, таким как карбонат цезия, и с реагентом формулы III, где R2 представляет собой группу, содержащую радионуклид, выбранный из 3Н или 11C и X представляет собой уходящую группу, такую как йод. Реагенты формулы III, такие как [3Н]метилйодид и [11С]метилйодид, известны, и их получают согласно Larsen P., Ulin J., Dahlstrom К. J. Label. Compds. Radiopharm. 37, 73-75, 1995.
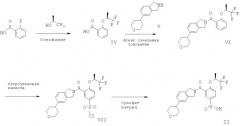
Схема 2 представляет собой путь синтеза соединения формулы (II), где R1 представляет собой (8)-2,2,2-трифтор-1-метил-этокси.
Схема 2
Промежуточная кислота IV может быть получена в результате взаимодействия имеющейся в продаже орто-фторбензойной кислоты с (S)-1,1,1-трифтор-пропан-2-олом (CAS (Chemical abstract cervice): 3539-97-7) в присутствии основания, такого как гидрид натрия, в растворителе, таком как диоксан. Сочетание кислоты IV с известным изоиндолином V (WO 2006082001) с получением амида VI может быть достигнуто в присутствии реагента сочетания, такого как TBTU, и основания, такого как диизопропилэтиламин, в растворителе, таком как DMF. Хлорсульфонилирование соединения VI с получением промежуточного сульфонилхлорида VII может быть выполнено в присутствии хлорсульфоновой кислоты в растворителе, таком как дихлорэтан. Восстановление соединения VII до сульфиновой кислоты II может быть достигнуто путем использования сульфита натрия в качестве восстанавливающего агента в растворителе типа DMF и воды.
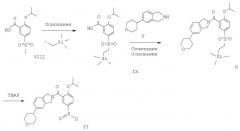
На Схеме 3 представлен путь синтеза соединения формулы (II), где R1 представляет собой изопропокси.
Схема 3
Промежуточное соединение IX может быть получено в результате взаимодействия кислоты VIII (WO 2005014563) с имеющимся в продаже алкилирующим агентом: (йодметил)триметилсиланом, в присутствии основания, такого как диизопропиламид лития, и вспомогательного вещества типа TMEDA в растворителе, таком как THF. Сочетание кислоты IX с известным изоиндолином V (WO 2006082001) с получением амида X может быть достигнуто в присутствии реагента сочетания, такого как TBTU, и основания, такого как диизопропил-этиламин в растворителе, таком как DMF. Превращение соединения X в сульфиновую кислоту II может быть достигнуто в присутствии TBAF в растворителе типа THF.
Сокращения
| TBTU | О-Бензотриазолил-тетраметилизоурония тетрафторборат |
| DMF | Диметилформамид |
| TBAF | Тетрабутиламмонийфторид |
| THF | Тетрагидрофуран |
| TMEDA | Тетраметилэтилендиамин |
| МТВЕ | Простой метил-трет-бутиловый эфир |
| LDA | Диизопропиламид лития |
Как описано выше, обнаружено, что меченные радиоактивным изотопом соединения формулы I могут быть использованы в качестве РЕТ-лигандов для мечения и диагностической молекулярной визуализации функциональности переносчика глицина 1 типа.
Соответствующие немеченные соединения [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон и (2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон активны в отношении переносчика GlyT1 in vitro и имеют величину IC50 (мкМ) 0,028 и 0,014 соответственно. Метод тестирования описан в WO 2006/082001.
Авторадиографические исследования на головном мозге крыс
Распределение сайтов связывания [3Н][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и [3Н](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона исследовали на головном мозге крыс.
Для этих экспериментов использовали самцов крыс Wistar. Крыс умерщвляли; головной мозг крыс быстро извлекали, замораживали в порошке сухого льда. По десять сагиттальных срезов толщиной один мкм нарезали на криостате и размещали с размораживанием на предметных стеклах с адгезивным покрытием. Срезы головного мозга сначала инкубировали в течение 10 мин в растворе Рингера (NaCl 120 мМ, KCl 5 мМ, CaC2 2 мМ, MgCl21 мМ, Трис-HCl 50 мМ pH 7,4) при 37°C и затем в течение 60 мин в растворе Рингера при 37°C, содержащем либо [3Н][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон, либо [3Н](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон в концентрации 1 нМ. Для оценки неспецифического связывания (NSB) радиоактивного индикатора дополнительную группу срезов инкубировали с раствором Рингера, содержащим радиоактивный индикатор и эталонный ингибитор GlyT1, Org 24598, в концентрации 10 мкМ (60 мин при 37°С). По окончании инкубации срезы промывали 2×5 мин и 1×15 мин в охлажденном на льду (4°С) растворе Рингера и затем трижды быстро окунали в дистиллированную воду при 4ºC. Срезы головного мозга, размещенные на предметных стеклах, сушили в потоке холодного воздуха и экспонировали вместе с [3Н]-стандартом ([3H]-microscale) на визуализирующую пластину Fuji в течение 5 суток. Затем визуализирующую пластину сканировали на сканере с высоким разрешением для пластин от FujiFilm. Общее количество радиоактивного индикатора, связавшегося с представляющими интерес участками головного мозга (ТВ (totally bound)), измеряли, используя программу MCID для анализа изображений, и выражали в фмоль связавшегося радиоактивного индикатора/мг белка. Количество [3Н][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона, специфически связавшегося с GlyT1-носителем (SB (specifically bound)), рассчитывали согласно формуле
SB=TB-NSB.
Полученные результаты показали, что распределение сайтов связывания [3Н][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и [3Н](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона соответствовало известному распределению для переносчика GlyT1 (Cubelos В., Gimenez C., Zafra F., Cereb Cortex 15, 448-459, 2005; Zafra F., Aragon C., Olivares L., Danbolt NC, Gimenez C., Storm-Mathisen J., J Neuroscience. 15, 3952-69, 1995). Высокие плотности расположения сайтов связывания наблюдали в таламусе, мозговом стволе, варолиевом мосту и продолговатом мозге и мозжечке. Низкие плотности наблюдали в стриатуме, корковом веществе и гиппокампе. Совместная инкубация радиоактивных индикаторов со специфическим ингибитором GlyT1, Org 24598 или другими специфическими ингибиторами GlyT1 в высоких концентрациях полностью аннулировала связывание как [3Н][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона, так и [3Н](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона со срезами головного мозга крысы, подтверждая, что эти оба радиоактивных индикатора связываются с переносчиком GlyT1.
РЕТ-исследования in vivo на павианах
1) РЕТ-визуализация с использованием [11C](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и [11С][5-метансульфонил-2-((S)-2.2.2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона
Эксперименты, описанные ниже, проводили на самцах павианов (Papio anubis). Животных не кормили в течение 12 часов перед проведением РЕТ-исследования. Сначала на павианов воздействовали седативным средством, используя внутримышечно кетамина гидрохлорид в "сдерживающих" дозировках (restraint dosages) 5-7 мг/кг, для достижения легкой стадии анестезии и затем выдерживали при непрерывной внутривенной инфузии пропофола в режиме 0,3-0,4 мг/кг/ч (эмульсия для инъекции DIPRIVAN®). Объем кровообращения поддерживали путем инфузии изотонического раствора. Для отбора образцов крови вводили катетер в бедренную артерию. В продолжении всего исследования проводили постоянный мониторинг основных физиологических показателей, включая частоту сердечных сокращений, ECG (электрокардиограмму), кровяное давление (Spacelabs Monitor, Issaquah, WA, USA) и насыщение кислородом (пульсовой оксиметр OxiMax® N-600™ от Nellcor, Pleasanton, CA, USA). Животное помещали в РЕТ-сканер для изучения головного мозга HRRT® (от англ. high resolution research tomography) от ECAT (томограф с высоким разрешением для научных исследований, CPS Innovations, Inc., Knoxville, TN). К голове животного прилаживали маску из термопластического материала, которую присоединяли к фиксатору головы для воспроизводимости фиксации. Сначала в течение 6 мин проводили трансмиссионное сканирование, используя точечный источник Cs-137 активностью 1 мКu, для коррекции экранирования. [11С](2-Изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон] и [11С][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон вводили внутривенно в виде болюс-инъекции длительностью 1 минута. РЕТ-сканирование и отбор образцов артериальной крови инициировали после начала введения радиоактивного индикатора и РЕТ-изображения фиксировали в течение от 0 до 90 минут после введения радиоактивного индикатора.
Результаты этих исследований с использованием визуализации показали, что оба радиоактивных индикатора [11С](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон и [11С][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон быстро захватывались многими участками головного мозга в соответствии с кривыми зависимости активности от времени, которые демонстрировали максимальный захват через 20-30 мин после введения и медленное уменьшение в течение остального времени исследования. Региональное распределение обоих радиоактивных индикаторов отражало известное распределение переносчика глицина 1 типа (GlyT1) с более высокой аккумуляцией в участках варолиевого моста, ствола головного мозга, мозжечка и таламуса по сравнению с участками коры головного мозга (Cubelos В., Gimenez C., Zafra F., Cereb. Cortex, 15, 448-459, 2005).
2) РЕТ-визуализация в условиях фармакологической нагрузки в этих экспериментах тестировали способность немеченых ингибиторов GlyT1 блокировать захват [11С](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и [11С][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона в участках головного мозга, известных как содержащие GlyTl. Поскольку и [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон, и (2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон являются селективными ингибиторами GlyT1, то для описанных ниже экспериментов отбирали одно из этих соединений, [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон.
Каждое животное получало два последовательных введения радиоактивного индикатора в один и тот же день. Первое введение радиоактивного индикатора использовали для определения базового захвата радиоактивного индикатора. После сканирования базовой линии павиан получал внутривенное введение немеченого [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона (блокатора). Инфузию блокатора начинали за 20 мин до (второй) инъекции радиоактивного индикатора. Сначала блокатор вводили инфузией в дозе 0,2 мг/кг. Через 10 мин скорость потока изменяли, чтобы в течение оставшихся 100 мин исследования доставлять 0,5 мг/кг. Предварительные фармакокинетические эксперименты и моделирование данных указывали на то, что такие скорости инфузии дают постоянные уровни в плазме [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона в продолжение данного временного интервала РЕТ-сканирования.
Предварительная обработка нерадиоактивным [5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метаноном (селективным ингибитором GlyTl) полностью блокировала специфический захват обоих радиоактивных индикаторов [11С-](2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и [11С][5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона и приводила к гомогенному распределению радиоактивного вещества по всему головному мозгу. Эти результаты подтверждали специфичность обоих радиоактивных индикаторов в отношении переносчика GlyT1 и ясно показывали, что связывание их с переносчиком GlyT-1 может ослабляться наличием немеченых лекарственных средств, которые связываются с переносчиком GlyT1.
Соединения по настоящему изобретению представляют собой диагностические инструменты, которые могут быть полезны в диагностике расстройств центральной нервной системы, например, для шизофрении, когнитивного нарушения и болезни Альцгеймера.
Соединения формулы I могут быть использованы вместе с фармацевтически инертными неорганическими или органическими носителями в процессе изготовления фармацевтических композиций.
Дозировки могут варьировать в широких пределах и, несомненно, в каждом конкретном случае их необходимо будет скорректировать в соответствии с индивидуальными требованиями.
Меченные радиоактивным изотопом ингибиторы предпочтительно вводят внутривенно.
Инъекционный раствор может иметь следующий состав:
| соединение формулы (I) | 1 мг |
| 1 н. HCl | 20 мкл |
| уксусная кислота | 0,5 мг |
| NaCl | 8 мг |
| фенол | 10 мг |
| 1 н. NaOH | сколько необходимо до pH 5 |
| H2О | сколько необходимо до 1 мл |
Следующие далее примеры иллюстрируют изобретение, но не предназначаются для ограничения его объема.
Пример 1
[3Н-Метил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
a) Стадия 1
2-((S)-2.2.2-Трифтор-1-метил-этокси)-бензойная кислота
36,0 г (316 ммоль) (3)-1,1,1-трифтор-пропан-2-ола (CAS: 3539-97-7) добавляли к холодной (0-5°C) суспензии 17,0 г (425 ммоль) NaH (практ., 60%) в 200 мл диоксана. Суспензию перемешивали при комнатной температуре в течение 0,5 ч, затем охлаждали (0-5°C) и добавляли раствор 20,0 г (143 ммоль) 2-фтор-бензойной кислоты в 100 мл диоксана. Смесь перемешивали в течение 0,5 ч при комнатной температуре и в течение 140 ч при кипячении с обратным холодильником. Смесь выливали в 800 мл воды, промывали 300 мл МТВЕ, затем покисляли до рН 2 соляной кислотой и продукт экстрагировали, используя МТВЕ. Растворитель концентрировали в вакууме и остаток кристаллизовали из смеси этанол/вода, получая 27,3 г (82%) указанного в заголовке соединения в виде белого твердого вещества. MS (масс-спектрометрия) (m/e]: 234,1 [M]+.
b) Стадия 2
[5-(Тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил)-[2-((S)-2.2,2-трифтор-1-метил-этокси)-фенил]-метанон
К раствору 0,9 г (3,8 ммоль) 2-((8)-2,2,2-трифтор-1-метил-этокси)-бензойной кислоты в 9 мл DMF в атмосфере аргона при комнатной температуре добавляли 1,4 г (4,2 ммоль) TBTU, 3,3 мл (19,2 ммоль) N-этилдиизопропиламина и в конце 0,8 г (3,8 ммоль) 5-(тетрагидро-пиран-4-ил)-2,3-дигидро-1Н-изоиндола (CAS: 905274-50-2). Смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли в вакууме. Остаток растворяли в этилацетате. Раствор дважды промывали водой и дважды насыщенным раствором NaHCO3, сушили над Na2SO4, фильтровали и концентрировали в вакууме. Неочищенное масло очищали колоночной флэш-хроматографией на диоксиде кремния с элюированием градиентом, образованным из гептана и этилацетата, получая 1,5 г (93%) указанного в заголовке соединения в виде желтого масла. MS (m/e): 420,2 [М+Н]+.
c) Стадия 3
3-[5-(Тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-4-((S)-2,2,2-трифтор-1-метил-этокси)-бензолсульфонилхлорид
Раствор 0,2 г (0,47 ммоль) [5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-[2-((5)-2,2,2-трифтор-1-метил-этокси)-фенил]-метанона в 2 мл 1,2-дихлорэтана добавляли по каплям к 0,32 мл (4,7 ммоль) хлорсульфоновой кислоты при охлаждении в ледяной бане. Смесь перемешивали при комнатной температуре в течение 30 минут и затем при 55°C в течение 30 минут. Смесь охлаждали в ледяной бане и гасили, добавляя по каплям 2 мл воды. Смесь разбавляли дихлорметаном. Органический слой отделяли и водный слой дважды экстрагировали дихлорметаном. Объединенные дихлорметановые экстракты сушили над Na2SO4) фильтровали и концентрировали в вакууме. Полученную пену перемешивали с этилацетатом. Твердое вещество отфильтровывали. Фильтрат дважды промывали насыщенным раствором NaHCO3, сушили над Na2SO4, фильтровали и концентрировали в вакууме, получая 0,12 г (51%) указанного в заголовке соединения в виде светло-желтой пены. MS (m/e): 517,1 [M]+.
d) Стадия 4
3-[5-(Тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-4-((S)-2,2,2-трифтор-1-метил-этокси)-бензолсульфината натриевая соль
1,15 г (8,94 ммоль) Na2SO3 и 1,70 г (9,60 ммоль) Na2HPO4 гидрата растворяли в 13 мл воды. Добавляли этанольный раствор 2,40 г (4,63 ммоль) 3-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-4-((3)-2,2,2-трифтор-1-метил-этокси)-бензолсульфонилхлорида. Реакционную смесь перемешивали при 35-40°C в течение 1 часа и затем в течение ночи при комнатной температуре. Добавляли 1,3 г спидекса (Speedex), реакционную смесь фильтровали и фильтрат упаривали. Неочищенный продукт обрабатывали водным раствором лимонной кислоты/NaCl, затем экстрагировали смесью 1:1 MTBE/THF. Органический растворитель выпаривали, остаток растворяли в смеси МеОН/вода (2:1) и обрабатывали, используя 800 мг (9,52 ммоль) NaHCO3. Добавляли 1 г спидекса и реакционную смесь фильтровали и концентрировали в вакууме. Остаток очищали хроматографическим путем с использованием обращенно-фазовой колонки (RP-18, вода/метанол), получая 1,12 г (48%) указанного в заголовке соединения в виде белой пены. MS (m/e): 484,3 [М+Н]+.
e) Стадия 5
[3Н-Метил]-[5-метансульсфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
0,16 мг (1,2 мкмоль) Lil добавляли к раствору 50 мКu (0,15 мг; 0,6 мкмоль) [3Н]метилнозилата в 0,2 мл DMF. После перемешивания реакционной смеси в течение 3 ч при 20°C в закрытом флаконе добавляли 0,6 мг (1,4 мкмоль) 3-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-4-((S)-2,2,2-трифтор-1-метил-этокси)-бензолсульфината натриевой соли и 1,0 мг (3,1 мкмоль) карбоната цезия и перемешивание продолжали в течение 2 ч при 20°C. Реакционную смесь обрабатывали водой и рассолом и затем экстрагировали этилацетатом. После выпаривания органического растворителя полученный неочищенный продукт очищали колоночной хроматографией (диоксид кремния, этилацетат/гептан 4:1), получая 23,9 мКu (48%) меченного тритием указанного в заголовке соединения с удельной активностью 74 Кu/ммоль (согласно MS-анализу). HPLC-анализ радиоактивного соединения показал радиохимическую чистоту >99%.
Пример 2
[11C-Метил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метил-этокси)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
3-[5-(Тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-4-((S)-2,2,2-трифтор-1-метил-этокси)-бензолсульфината натриевую соль (1 мг; 2 мкмоль) растворяли в 100 мкл диметилформамида. Флакон герметично закрывали; раствор встряхивали в течение одной минуты, вводили в систему Bioscan AutoLoop и продували аргоном (30 мл/мин) в течение 5 секунд. [11C]Метилйодид (полученный согласно Larsen P., Ulin J., Dahlstrom К. J. Label. Compds. Radiopharm. 37, 73-75, 1995) вносили в Bioscan Autoloop (Bioscan Inc, Washington, DC) в потоке гелия (30 мл/мин). Захват [11C]метилйодида в AutoLoop выполняли в течение 3,5 минуты, после чего поток останавливали. Через 4,5 минуты реакционную смесь автоматически направляли на полупрепаративную HPLC и обрабатывали, как указано ниже. Продукт собирали в выдерживающий давление резервуар, где он разбавлялся 50 мл воды, затем наносили на C-18 SepPak Plus от Waters (ниже см. условия аналитической и препаративной HPLC). SepPak, содержащий очищенное указанное в заголовке соединение, промывали 10 мл изотонического раствора, после чего продукт элюировали 1 мл абсолютного этанола, затем 10 мл изотонического раствора через фильтр с порами 0,22 микрона для стерилизации в стерильный апирогенный флакон, содержащий 4 мл изотонического раствора.
Условия HPLC: аналитической: Onyx С18, 4,6×100 мм; 35:65 MeCN:H2O; TEA (триэтиламин) рН 7,2 при 3 мл/мин; препаративной: XTerra C18, 5 мкм, 19×100 мм; 40:60 MeCN:H2O; 0,1М NH4-формиат при 18 мл/мин.
Пример 3
[3H-Метил]-(2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
a) Стадия 1
2-Изопропокси-5-(2-триметилсиланил-этансульфонил)бензойная кислота
К перемешиваемой (-70°С) суспензии 0,26 г (1 ммоль) 2-изопропокси-5-метансульфонил-бензойной кислоты (CAS: 845616-02-6) и 0,75 мл (5 ммоль) TMEDA в 2,6 мл THF добавляли по каплям раствор LDA (приготовленный из 1,3 мл (2,1 ммоль) 1,6 М раствор н-бутиллития в гексане и 0,3 мл (2,1 ммоль) диизопропиламина в 2,5 мл THF при 0°С). Светло-желтую суспензию перемешивали при -70°С в течение 30 минут. По каплям в течение периода времени 5 минут добавляли раствор 0,19 мл (1,3 ммоль) (йодметил)триметил-силана в 0,5 мл THF. Желтую суспензию перемешивали при -70°С в течение 15 минут и затем оставляли нагреваться до комнатной температуры. Светло-желтый раствор перемешивали при комнатной температуре в течение 1 часа и затем гасили, используя 5 мл рассола. Смесь разбавляли 5 мл воды. Смесь концентрировали в вакууме. Водный слой осторожно подкисляли, используя 1 н. HCl, и экстрагировали 3 раза дихлорметаном. Объединенные экстракты сушили над Na2SO4, фильтровали и концентрировали в вакууме. Неочищенное вещество очищали колоночной флэш-хроматографией на диоксиде кремния с элюированием градиентом, образованным из гептана и этилацетата, получая 0,21 г (63%) указанного в заголовке соединения в виде желтого масла. MS (m/e): 343,0 [M-H]+.
b) Стадия 2
[2-Изопропокси-5-(2-триметилсиланил-этансульфонил)-фенил1-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
По аналогии с методикой, описанной для синтеза соединения из примера 1, стадия 2, указанное в заголовке соединение получали из 5-(тетрагидро-пиран-4-ил)-2,3-дигидро-1Н-изоиндола (CAS: 905274-50-2) и 2-изопропокси-5-(2-триметилсиланил-этансульфонил)-бензойной кислоты. MS (m/e): 529,3 [M]+.
c) Стадия 3
4-Изопропокси-3-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-бензолсульФината натриевая соль
1,40 г (2,64 ммоль) [2-изопропокси-5-(2-триметилсиланил-этансульфонил)-фенил]-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанона растворяли в 14 мл THF и обрабатывали 4,0 мл (4,0 ммоль) 1 M раствора TBAF в THF при 60°C в течение 3,5 часа. Реакционную смесь выливали на водный раствор лимонной кислоты/NaCl, затем экстрагировали смесью MTBE/THF 1:1. Органический растворитель выпаривали, остаток растворяли в смеси МеОН/вода (3:1) и обрабатывали 600 мг NaHCO3. После выпаривания остаток очищали хроматографическим путем на обращенно-фазовой колонке (RP-18, вода/метанол), получая 0,66 г (55%) указанного в заголовке соединения в виде белой пены. MS (m/e): 430,2 [М+Н]+.
d) Стадия 4
[3H-Метил]-(2-изопропокси-5-метансульфонил-фенил)-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-ил]-метанон
0,16 мг (1,2 мкмоль) Lil добавляли к раствору 50 мКu (0,15 мг; 0,6 мкмоль) [3H]метилнозилата в 0,2 мл DMF. После перемешивания реакционной смеси в течение 3 ч при 20°C в закрытом флаконе добавляли 0,6 мг (1,3 мкмоль) 4-изопропокси-3-[5-(тетрагидро-пиран-4-ил)-1,3-дигидро-изоиндол-2-карбонил]-бензолсульфината натриевой соли и 1,0 мг (3,1 мкмоль) карбоната цезия и перемешивание продолжали в те