Ускоренный способ очистки для получения капсульных полисахаридов streptococcus pneumoniae
Иллюстрации
Показать всеГруппа изобретений относится к биотехнологии. Предложены варианты способа получения раствора, содержащего очищенные капсульные полисахариды, из лизата клеток выбранного серотипа Streptococcus pneumoniae. Проводят лизис клеток выбранного серотипа S. pneumoniae. Осветляют полученный лизат центрифугированием или фильтрованием. Затем проводят ультрафильтрацию и диафильтрацию осветленного лизата в бессолевой среде с получением ретентата. Понижают pH ретентата до значения менее чем 4,5. Выдерживают подкисленный раствор ретентата для осаждения преципитата. Далее фильтруют или центрифугируют раствор ретентата с получением осветленного раствора капсульного полисахарида. Далее осветленный раствор полисахарида фильтруют через фильтр с активированным углем. Полученный фильтрованный раствор ультрафильтруют и диафильтруют. Полученный концентрированный очищенный раствор капсульного полисахарида фильтруют через стерильный фильтр. При этом серотипы S. pneumoniae выбирают из группы, состоящей из серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18C, 19A, 19F и 23F. Также предложена модификация этого способа для серотипа 19А. Эта модификация включает проведение ультрафильтрации и диафильтрации перед подкислением при 4ºС при рН 6 в натриево-фосфатном буфере, выдерживание подкисленного раствора ретентата в течение по меньшей мере 2 часов при 4ºС и подведение рН осветленного раствора полисахарида до значения 6 перед этапом фильтрации активированным углем. Также предложены растворы, содержащие очищенные капсульные полисахариды выбранного серотипа S. pneumoniae, полученные указанными способами, и их применение в производстве пневмококковой вакцины. Также предложены выделенные из указанных растворов очищенные капсульные полисахариды S. pneumoniae серотипа 6А с мол. весом 640000-670000 Да и 19А с мол. весом 488000-525000 Да. Ускоренный способ позволяет на этапах подкисления и адсорбции активированным углем преципитировать более чем 98% и 90% белка соответственно, сильно не влияя на выход полисахарида. 10 н. и 37 з.п. ф-лы, 14 ил., 19 табл., 4 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам удаления избытка растворимого белка и других примесей из лизатов клеток серотипов Streptococcus pneumoniae (S. pneumoniae), используемых для получения очищенных полисахаридов пневмококков.
УРОВЕНЬ ТЕХНИКИ
Бактерии Streptococcus pneumoniae относятся к грамположительным ланцетовидным коккам, которые обычно объединяются в пары (диплококки), но также могут существовать в виде коротких цепей или в виде отдельных клеток. Они легко растут на чашках с кровяным агаром, образуя блестящие колонии, и способны к альфа-гемолизу, если только их не выращивают в анаэробных условиях, в которых они проявляют бета-гемолиз. Они чувствительны к солям желчных кислот, которые могут разрушить клеточную стенку с помощью присутствующего в самих клетках фермента - аутолизина. Указанный микроорганизм представляет собой аэротолерантный анаэроб, и он прихотлив в том отношении, что он имеет комплексную потребность в питательных веществах.
Клетки большинства серотипов пневмококков имеют капсулу, которая представляет собой слой полисахарида, окружающий каждую клетку. Эта капсула является определяющей для вирулентности в отношении человека, поскольку она препятствует фагоцитозу путем предотвращения присоединения антител к бактериальным клеткам. На сегодняшний день идентифицировано 90 капсульных серотипов, при этом 23 серотипа ответственны за приблизительно 90% инвазивных заболеваний. В виде вакцины указанный полисахарид может придать приемлемую степень иммунитета к S. pneumoniae индивидуумам с развитыми или неослабленными иммунными системами. Тем не менее, если полисахарид конъюгирован с высокомолекулярным белком, таким как CRM197, и входит в состав вакцины, содержащей конъюгаты множества серотипов, такие конъюгатные вакцины позволяют вызывать иммунный ответ у детей и людей преклонного возраста, которые также имеют наибольший риск пневмококковых инфекций.
Капсульный полисахарид для каждого серотипа S. pneumoniae, применяемого для получения продуктов вакцины, получают путем выращивания микроорганизма в жидкой среде. Размер популяции организма часто увеличивают от посевных пробирок до посевных колб и пропускают через один или более посевных ферментеров с возрастающим объемом до тех пор, пока не будут достигнуты промышленные масштабы объемов ферментации. Окончание цикла роста можно определить с помощью нескольких средств, на этом этапе клетки лизируют посредством добавления детергента или другого реагента, который способствует разрушению клеточной стенки и высвобождению аутолизина, который вызывает лизис клеток по достижении клетками стационарной фазы. Бульон затем собирают для последующей переработки (очистки). Основными примесями являются клеточные белки, нуклеиновые кислоты, С-полисахарид и компоненты среды.
Способы получения очищенных индивидуальных полисахаридов из растворов известны из уровня техники, в частности из документов US 5847112 и US 4242501.
Для большинства серотипов, для реализуемой на сегодняшний день на рынке 7-валентной пневмококковой конъюгатной (7vPnC) вакцины (Prevnar®), а также для недавно разработанной 13-валентной пневмококковой конъюгатной (13vPnC) вакцины, известный из уровня техники способ очистки требует шестнадцать этапов, включающих множество дорогостоящих, трудоемких и технологически сложных операций, таких как хроматография и множество разделений на мембранах. Предшествующие попытки улучшить способы очистки полисахаридов S. Pneumoniae включали, например, изменение рН во время ферментации и выделения (см. заявку на патент США, номер публикации 2006/0228381), а также осаждение растворителем и детергентом. Тем не менее удаление примесей в этих способах все еще требует многих трудоемких и дорогостоящих этапов. Уровень содержания белка является наиболее проблематичным техническим требованием, которое нужно удовлетворить, вследствие физических и химических свойств растворимых белков.
Таким образом, существует потребность в упрощенном способе очистки для уменьшения уровней растворимого белка в лизатах S. pneumoniae и устранения неэффективности известного из уровня техники способа очистки для получения по существу очищенных капсульных полисахаридов, подходящих для включения в пневмококковые конъюгатные вакцины.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу получения раствора, содержащего очищенные капсульные полисахариды из лизата клеток Streptococcus pneumoniae. Указанный способ включает следующие стадии:
(a) обеспечение ферментативного бульона, который содержит бактериальные клетки, которые продуцируют выбранный серотип Streptococcus pneumoniae;
(b) лизирование бактериальных клеток, полученных на стадии (а) литическим агентом, с получением лизата клеток, который содержит остатки клеток, растворимые белки, нуклеиновые кислоты и полисахариды;
(c) осветление лизата клеток, полученного на стадии (b), посредством центрифугирования или фильтрования для удаления остатков клеток с получением осветленного лизата клеток;
(d) ультрафильтрование и диафильтрование осветленного лизата клеток, полученного на стадии (с), для удаления низкомолекулярных примесей и повышения концентрации полисахарида с получением ретентата;
(e) понижение рН ретентата, полученного на стадии (d), до значения менее чем 4.5 для преципитации белка и нуклеиновых кислот с получением подкисленного раствора ретентата;
(f) выдерживание подкисленного раствора ретентата, полученного на стадии (е), в течение времени, достаточного для осаждения преципитата, а затем фильтрование или центрифугирование подкисленного раствора ретентата с получением осветленного раствора полисахарида;
(g) фильтрование осветленного раствора полисахарида, полученного на стадии (f) через фильтр с активированным углем;
(h) ультрафильтрование и диафильтрование указанного фильтрованного раствора, полученного на стадии (g), с получением концентрированного очищенного раствора полисахарида; и
(i) фильтрование концентрированного очищенного раствора полисахарида, полученного на стадии (h), с применением стерильного фильтра;
в результате чего получают очищенные капсульные полисахариды в виде раствора. Типичные неограничивающие примеры серотипов S. pneumoniae, выбранные для этого варианта реализации настоящего изобретения, представляют собой 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, 19F, и 23F. В конкретном варианте реализации, рН на стадии (е) понижают до значения приблизительно 3.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 5.5 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 7.0 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения приблизительно 7.4. В еще одном варианте реализации, на стадии (е) удаляют по меньшей мере 98% белка из ретентата, полученного на стадии (d). В следующем варианте реализации, на стадии (g) удаляют по меньшей мере 90% белка из осветленного раствора полисахарида, полученного на стадии (f). В следующем варианте реализации, фильтр с активированным углем, который применяют на стадии (g), включает древесный уголь, активированный фосфорной кислотой. В следующем варианте реализации, стадия (f) включает выдерживание подкисленного раствора ретентата, полученного на стадии (е), в течение по меньшей мере 2 часов. В еще одном варианте реализации, литический агент, который применяют на стадии (b), представляет собой дезоксихолат натрия (DOC). В следующем варианте реализации, литический агент на стадии (b), представляет собой литический агент неживотного происхождения. В еще одном варианте реализации, литический агент, который применяют на стадии (b) представляет собой литический агент неживотного происхождения - N-лаурилсаркозинат натрия (NLS).
Указанный очищенный капсульный полисахарид, полученный с помощью способа согласно настоящему изобретению из лизата клеток Streptococcus pneumoniae, можно применять для производства пневмококковой вакцины, предпочтительно пневмококковой вакцины, содержащей полисахарид, конъюгированный с белковым носителем.
Настоящее изобретение также относится к способу получения раствора, содержащего очищенные капсульные полисахариды из лизата клеток Streptococcus pneumoniae, включающего серотип 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F или 23F. Этот способ включает следующие стадии:
(a) обеспечение ферментативного бульона, который содержит бактериальные клетки, которые продуцируют серотип Streptococcus pneumoniae 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F или 23F;
(b) лизирование бактериальных клеток, полученных на стадии (а), литическим агентом, с получением лизата клеток, который содержит остатки клеток, растворимые белки, нуклеиновые кислоты и полисахариды;
(c) осветление лизата клеток, полученного на стадии (b), посредством центрифугирования или фильтрования для удаления остатков клеток с получением осветленного лизата клеток;
(d) ультрафильтрование и диафильтрование осветленного клеточного лизата, полученного на стадии (с), при комнатной температуре при нейтральном рН в бессолевых средах для удаления низкомолекулярных примесей и повышения концентрации полисахарида с получением бессолевого ретентата;
(e) понижение рН бессолевого ретентата, полученного на стадии (d), до значения менее чем 4.5 для преципитации белка и нуклеиновых кислот с получением подкисленного раствора ретентата;
(f) выдерживание подкисленного раствора ретентата, полученного на стадии (е), в течение по меньшей мере 2 часов при комнатной температуре для осаждения преципитата, а затем фильтрование или центрифугирование подкисленного раствора ретентата с получением осветленного раствора полисахарида;
(g) фильтрование осветленного раствора полисахарида, полученного на стадии (f), через фильтр с активированным углем;
(h) ультрафильтрование и диафильтрование указанного фильтрованного раствора, полученного на стадии (g), с получением концентрированного очищенного раствора полисахарида; и
(i) фильтрование концентрированного очищенного раствора полисахарида, полученного на стадии (h), с применением стерильного фильтра;
в результате чего получают очищенные капсульные полисахариды, включая серотип 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F или 23F в виде раствора. В конкретном варианте реализации, рН на стадии (е) понижают до значения приблизительно 3.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 5.5 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 7.0 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения приблизительно 7.4. В еще одном варианте реализации, на стадии (е) удаляют по меньшей мере 98% белка из бессолевого ретентата, полученного на стадии (d). В следующем варианте реализации, на стадии (g) удаляют по меньшей мере 90% белка из осветленного раствора полисахарида, полученного на стадии (f). В следующем варианте реализации, фильтр с активированным углем, который применяют на стадии (g) включает древесный уголь, активированный фосфорной кислотой. В еще одном варианте реализации, литический агент, который применяют на стадии (b), представляет собой дезоксихолат натрия (DOC). В следующем варианте реализации, литический агент, который применяют на стадии (b), представляет собой литический агент неживотного происхождения. В еще одном варианте реализации, литический агент на стадии (b) представляет собой литический агент неживотного происхождения - N-лаурилсаркозинат натрия (NLS).
Настоящее изобретение также относится к способу получения раствора, содержащего очищенные капсульные полисахариде из лизата клеток Streptococcus pneumoniae, включающего серотип 19А. Этот способ включает следующие стадии:
(a) обеспечение ферментативного бульона, который содержит бактериальные клетки, которые продуцируют серотип Streptococcus pneumoniae 19А;
(b) лизирование бактериальных клеток, полученных на стадии стадии (а), литическим агентом, с получением лизата клеток, который содержит остатки клеток, растворимые белки, нуклеиновые кислоты и полисахариды;
(c) осветление лизата клеток, полученного на стадии (b), посредством центрифугирования или фильтрования для удаления остатков клеток с получением осветленного лизата клеток;
(d) ультрафильтрование и диафильтрование осветленного лизата клеток, полученного на стадии (с), при приблизительно 4°С при рН, равном приблизительно 6, в натриево-фосфатном буфере для удаления низкомолекулярных примесей и повышения концентрации полисахарида с получением ретентата;
(e) понижение рН ретентата, полученного на стадии (d), до значения менее чем 4.5 для преципитации белка и нуклеиновых кислот с получением подкисленного раствора ретентата;
(f) выдерживание подкисленного раствора ретентата, полученного на стадии (е), в течение по меньшей мере 2 часов при приблизительно 4°С для осаждения преципитата, а затем фильтрование или центрифугирование подкисленного раствора ретентата с получением осветленного раствора полисахарида;
(g) подведение рН осветленного раствора полисахарида, полученного на стадии (f), до значения приблизительно 6 с получением осветленного раствора полисахарида с подведенным рН;
(h) фильтрование осветленного раствора полисахарида с подведенным рН, полученного на стадии (g), через фильтр с активированным углем;
(i) ультрафильтрование и диафильтрование указанного фильтрованного раствора, полученного на стадии (h), с получением концентрированного очищенного раствора полисахарида; и
(j) фильтрование концентрированного очищенного раствора полисахарида, полученного на стадии (i), с применением стерильного фильтра;
в результате чего получают очищенные капсульные полисахариды, включая серотип 19А, в виде раствора. В конкретном варианте реализации, рН на стадии (е) понижают до значения приблизительно 3.5. В следующем варианте реализации, диафильтрация на стадии (i) включает подведение рН до значения между приблизительно 5.5 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (i) включает подведение рН до значения между приблизительно 7.0 и приблизительно 7.5. В следующем варианте реализации, диафильтрация на стадии (i) включает подведение рН до значения приблизительно 7.4. В еще одном варианте реализации, на стадии (е) из ретентата, полученного на стадии (d), удаляют по меньшей мере 98% белка. В следующем варианте реализации, на стадии (h) удаляют по меньшей мере 90% белка из осветленного раствора полисахарида с подведенным рН, полученного на стадии (g). В следующем варианте реализации, фильтр с активированным углем, который применяют на стадии (h) включает древесный уголь, активированный фосфорной кислотой. В следующем варианте реализации, натриево-фосфатный буфер, который применяют на стадии (d) представляет собой 25 мМ фосфат натрия. В еще одном варианте реализации, литический агент, который применяют на стадии (b), представляет собой дезоксихолат натрия (DOC). В следующем варианте реализации, литический агент на стадии (b) представляет собой литический агент неживотного происхождения. В еще одном варианте реализации, литический агент, который применяют на стадии (b), представляет собой литический агент неживотного происхождения - N-лаурилсаркозинат натрия (NLS).
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
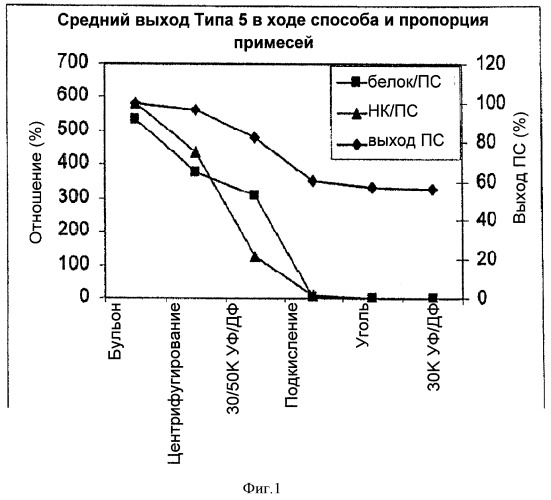
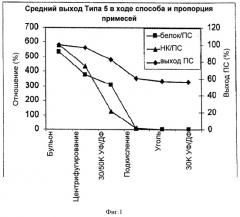
На Фигуре 1 показан средний выход полисахарида (ПС) для способа согласно настоящему изобретению, отношение белок/ПС и отношение нуклеиновая кислота (НК)/ПС для серотипа 5, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты приведены для каждого этапа очистки.
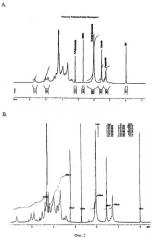
На Фигуре 2 показаны ЯМР-спектры для ПС серотипа 4 из известного способа очистки (А) по сравнению с ПС серотипа 4 из ускоренного способа очистки (В). Не наблюдалось значительных отличий между указанными двумя спектрами. Вторым пиком справа в обоих спектрах был пируват, и высота пика пируватной группы была сравнимой в обоих спектрах.
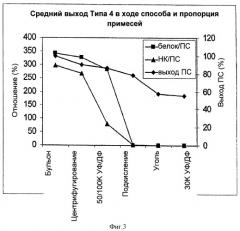
На Фигуре 3 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС, и отношение НК/ПС для серотипа 4, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
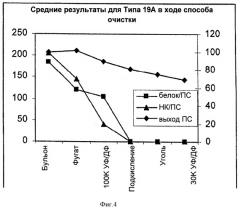
На Фигуре 4 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС, и отношение НК/ПС для серотипа 19А, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 5 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС и отношение НК/ПС для серотипа 7F, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 6 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС и отношение НК/ПС для серотипа 6В, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 7 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС и отношение НК/ПС для серотипа 6А, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 8 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС и отношение НК/ПС для серотипа 1, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 9 показан средний выход ПС для способа согласно настоящему изобретению, отношение белок/ПС и отношение НК/ПС для серотипа 14, с применением ускоренного способа очистки согласно настоящему изобретению. Результаты показаны для каждого этапа очистки.
На Фигуре 10 показано сравнение выходов ПС для способа согласно настоящему изобретению для серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, и 19F, очищенных с применением ускоренного способа очистки согласно настоящему изобретению.
На Фигуре 11 показано сравнение отношений белок/ПС для серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, и 19F, очищенных с применением ускоренного способа очистки согласно настоящему изобретению. Результаты сравнивали для каждого этапа очистки.
На Фигуре 12 показано сравнение отношений НК/ПС для серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, и 19F, очищенных с применением ускоренного способа очистки согласно настоящему изобретению. Результаты сравнивали для каждого этапа очистки.
На Фигуре 13 показана эффективность удаления белка благодаря этапу подкисления при ускоренном способе очистки согласно настоящему изобретению. Различие в концентрации белка (ПААГ-ДСН) перед и после подкисления наносили на график в зависимости от исходной концентрации белка перед подкислением для загрузок серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А и 19F. Различие в концентрации белка, поделенное на исходную концентрацию белка, отражало уровень удаления белка на стадии подкисления.
На Фигуре 14 показана эффективность удаления белка на этапе адсорбции активированным углем для ускоренного способа очистки согласно настоящему изобретению. Количество удаленного белка (адсорбированного на активированный уголь) наносили на график в зависимости от исходных количеств загрузки белка для загрузок серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А и 19F. Количество удаленного белка, поделенное на исходные количества загрузки белка, отражало уровень удаления белка на стадии адсорбции активированным углем.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к ускоренному способу очистки для уменьшения уровней растворимого белка в лизатах клеток Streptococcus pneumoniae для получения по существу очищенных капсульных полисахаридов, подходящих для включения в пневмококковые конъюгатные вакцины. Для большинства серотипов для реализуемой на сегодняшний день на рынке 7-валентной пневмококковой конъюгатной (7vPnC) вакцины (Prevnar®), а также недавно разработанной 13-валентной пневмококковой конъюгатной (13vPnC) вакцины, известный из уровня техники способ очистки полисахаридов требует до шестнадцати этапов. Эти этапы включают множество дорогостоящих, трудоемких и технологически сложных операций, таких как хроматография и множество мембранных разделений. Способ согласно настоящему изобретению освобождает от осуществления вплоть до восьми из этих этапов, при этом позволяет достичь аналогичной степени очистки и освобождает от потребности в хроматографии. Таким образом, настоящее изобретение относится к более эффективному способу очистки, который является менее дорогостоящим, занимает меньше времени и включает меньше этапов.
Ускоренный способ очистки согласно настоящему изобретению основан на обнаружении того, что ультрафильтрование и диафильтрование осветленного раствора лизата клеток S. pneumoniae, а затем подкисление концентрированного раствора лизата клеток до значения рН менее чем 4.5, предпочтительно приблизительно 3.5, позволяет преципитировать по меньшей мере 98% белка из раствора без значительного влияния на выход полисахарида. С помощью ультрафильтрования и диафильтрования лизированного и осветленного ферментативного бульона перед подкислением до значения рН менее чем 4.5, предпочтительно около 3.5, эффекты «удерживания» белков устранены и фракция белка, который "высаливается", повышается. Термин "удерживание" относится к повышенной растворимости белков, тогда как "высаливание" относится к преципитации белков из раствора, как только они достигают своих изоэлектрических точек. Этап ультрафильтрации и диафильтрации также предотвращает пенообразование, наблюдаемое, когда обработанный карбонатом натрия бульон подкисляют даже до значения рН 5.0 (см. заявку на патент США, номер публикации 2006/0228381). Таким образом, ультрафильтрация и диафильтрация осветленного лизатного бульона делают возможным применение любого низкомолекулярного рН-титранта, такого как карбонат натрия, в способе ферментации серотипа S. pneumoniae и предотвращает пенообразование осветленного лизатного бульона, когда он подкислен до рН менее чем 4.5.
Термин "осветленный лизатный бульон/раствор" относится к лизатному бульону, который подвергли центрифугированию или фильтрованию для удаления остатков клеток.
Термин "диафильтрование", "диафильтрация", "ДФ" и тому подобные термины относятся, например, к применению полупроницаемых мембран с подходящими физическими и химическими свойствами для удаления малых молекул из раствора.
Термин "ультрафильтрование", "ультрафильтрация", "УФ" и тому подобные термины относятся, например, к применению полупроницаемых мембран с подходящими физическими и химическими свойствами, позволяющими различать молекулы в растворе и концентрировать одинаковые молекулы в меньший объем раствора.
В рамках способов согласно настоящему изобретению, ультрафильтрация и диафильтрация обычно включают проточную фильтрацию "в перекрестном потоке" или "вдоль потока", чтобы избежать забивания фильтровальной мембраны. При фильтрации "в перекрестном потоке", фильтруемый раствор пропускают через поверхность мембраны. Материалы, которые проходят через мембрану, называют фильтратом. Материалы, которые не проходят через мембрану, называют ретентатом. Ретентат возвращают в подающий резервуар для повторной фильтрации.
В данной заявке, можно использовать любую кислоту для понижения значения рН ультрафильтрованного и диафильтрованного лизатного бульона до тех пор, пока не будет достигнуто значение рН менее чем 4.5, особенно приблизительно 3.5. Соответственно, в способах согласно настоящему изобретению можно применять, как органические, так и минеральные кислоты. В данной заявке термин "минеральная кислота" относится к кислоте, полученной из неорганического минерала с помощью химической реакции, в противоположность органическим кислотам. Например, неограничивающие примеры минеральных кислот, которые можно применять в способах согласно настоящему изобретению, включают соляную кислоту, азотную кислоту, фосфорную кислоту и серную кислоту. В конкретных вариантах реализации, рН концентрированного лизатного бульона понижают до значения менее чем 4.4, 4.3, 4.2, 4.1, 4.0, 3.9, 3.8, 3.7, 3.6, 3.5, 3.4, 3.3, 3.2, 3.1 или 3.0. В других вариантах реализации, рН концентрированного лизатного бульона понижают до значения приблизительно 4.4, приблизительно 4.3, приблизительно 4.2, приблизительно 4.1, приблизительно 4.0, приблизительно 3.9, приблизительно 3.8, приблизительно 3.7, приблизительно 3.6, приблизительно 3.5, приблизительно 3.4, приблизительно 3.3, приблизительно 3.2, приблизительно 3.1, приблизительно 3.0, приблизительно 2.9, приблизительно 2.8, приблизительно 2.7, приблизительно 2.6, приблизительно 2.5, приблизительно 2.4, приблизительно 2.3, приблизительно 2.2, приблизительно 2.1 или приблизительно 2.0.
Ускоренный способ очистки согласно настоящему изобретению также основан на обнаружении того, что в комбинации с этапами концентрирования и понижения рН, описанными выше, фильтрация с применением активированного угля позволяет преципитировать по меньшей мере 90% оставшегося белка, сильно не влияя на выход полисахарида. В конкретных вариантах реализации, было обнаружено, что угольная фильтрация с применением угля, полученного из древесных опилок или других древесных продуктов и активированного фосфорной кислотой, является более эффективной для уменьшения или удаления примесей белков, чем уголь, применяемый в известных из уровня техники способах угольной фильтрации.
Соответственно, настоящее изобретение относится к способу получения по существу очищенных капсульных полисахаридов из лизата клеток Streptococcus pneumoniae, включающему следующие стадии:
(a) обеспечение ферментативного бульона, который содержит бактериальные клетки, которые продуцируют выбранный серотип Streptococcus pneumoniae;
(b) лизирование бактериальных клеток, полученных на стадии (а), литическим агентом с получением лизата клеток, который содержит остатки клеток, растворимые белки, нуклеиновые кислоты и полисахариды;
(c) осветление лизата клеток, полученного на стадии (b), посредством центрифугирования или фильтрования для удаления остатков клеток с получением осветленного лизата клеток;
(d) ультрафильтрование и диафильтрование осветленного лизата клеток, полученного на стадии (с), для удаления низкомолекулярных примесей и повышения концентрации полисахарида с получением ретентата;
(e) понижение рН ретентата, полученного на стадии (d), до значения менее чем 4.5, особенно приблизительно 3.5, для преципитации белка и нуклеиновых кислот с получением подкисленного раствора ретентата;
(f) выдерживание подкисленного раствора ретентата, полученного на стадии (е), в течение промежутка времени, достаточного для осаждения преципитата, особенно в течение по меньшей мере 2 часов, со встряхиванием или без, а затем фильтрование или центрифугирование подкисленного раствора ретентата с получением осветленного раствора полисахарида;
(g) фильтрование осветленного раствора полисахарида, полученного на стадии (f), через фильтр с активированным углем, в частности через фильтр с активированным углем, который содержит древесный уголь, активированный фосфорной кислотой;
(h) ультрафильтрование и диафильтрование указанного фильтрованного раствора, полученного на стадии (g), с получением концентрированного очищенного раствора полисахарида; и
(i) фильтрование концентрированного очищенного раствора полисахарида, полученного на стадии (h), с применением стерильного фильтра;
в результате чего получают по существу очищенные капсульные полисахариды в виде раствора. Стерильная фильтрация на стадии (i) полезна для удаления бактерий и твердых включений из концентрированного очищенного раствора полисахарида. Например, неограничивающие серотипы S. pneumoniae, выбранные для этого варианта реализации настоящего изобретения, представляют собой 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, 19F и 23F. В конкретном варианте реализации, на стадии (е) удаляют по меньшей мере 98% белка из ретентата, полученного на стадии (d). В следующем варианте реализации, на стадии (g) удаляют по меньшей мере 90% белка из осветленного раствора полисахарида, полученного на стадии (f). В следующем варианте реализации, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 5.5 и приблизительно 7.5. Однако, для улучшения стабильности по существу очищенного капсульного полисахарида во время длительного хранения, диафильтрация на стадии (h) включает подведение рН до значения между приблизительно 7.0 и приблизительно 7.5, особенно до приблизительно 7.4.
В данной заявке термин "по существу очищенный лизат, содержащий капсульный полисахарид", или "раствор, содержащий по существу очищенный капсульный полисахарид", относится к лизату клеток Streptococcus pneumoniae или раствору, из которых белок удалили таким образом, что процентное отношение белка к полисахариду (белок/ПС) составляет менее чем 10%, менее чем 9%, менее чем 8%, менее чем 7%, менее чем 6%, менее чем 5%, менее чем 4%, менее чем 3%, менее чем 2%, или менее чем 1% и процентное отношение нуклеиновой кислоты к полисахариду (НК/ПС) составляет менее чем 5%, менее чем 4%, менее чем 3%, менее чем 2% или менее чем 1%. В конкретных вариантах реализации, процентные отношения белок/ПС и НК/ПС для по существу очищенных лизатов или растворов, содержащих капсульные полисахариды, включающие определенные серотипы, представляют собой такие, как перечислено далее: для серотипа 1 отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 2%, для серотипа 4 отношение белок/ПС составляет менее чем 3% и отношение НК/ПС составляет менее чем 2%, для серотипа 5 отношение белок/ПС составляет менее чем или равно 7.5% и отношение НК/ПС составляет менее чем или равно 2%, для серотипа 6А отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 2%, для серотипа 6В отношение белок/ПС составляет менее чем 4% и отношение НК/ПС составляет менее чем 1%, для серотипа 7F отношение белок/ПС составляет менее чем 5% и отношение НК/ПС составляет менее чем 2%, для серотипа 9V отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 1%, для серотипа 14 отношение белок/ПС составляет менее чем 3% и отношение НК/ПС составляет менее чем 2%, для серотипа 18С отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 2%, для серотипа 19А отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 2%, для серотипа 19F отношение белок/ПС составляет менее чем 3% и отношение НК/ПС составляет менее чем 2% и для серотипа 23F отношение белок/ПС составляет менее чем 2% и отношение НК/ПС составляет менее чем 2%. Способы количественного анализа концентраций белка, полисахарида и нуклеиновой кислоты в клеточном лизате или растворе хорошо известны в данной области и включают, например, анализ методом ПААГ-ДСН (электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия), ВЭЖХ (высокоэффективную жидкостную хроматографию) и SEC (эксклюзионную хроматографию), модифицированные методы Лоури, спектрофотометрию, SEC-MALLS (эксклюзионную хроматографию/многоугловое рассеяние лазерного излучения) и ЯМР (ядерный магнитный резонанс).
В способах согласно настоящему изобретению, бактериальные клетки можно лизировать, применяя любой литический агент. "Литический агент" представляет собой любой агент, который способствует разрушению клеточной стенки и высвобождению аутолизина, который вызывает лизис клеток, включая, например, детергенты. В данной заявке термин "детергент" относится к любому анионному или катионному детергенту, способному вызывать лизис бактериальных клеток. Типичные примеры таких детергентов для применения в способах согласно настоящему изобретению включают дезоксихолат натрия (DOC), N-лаурилсаркозинат (NLS), натриевую соль хенодезоксихолевой кислоты и сапонины.
В одном варианте реализации настоящего изобретения, литический агент, применяемый для лизирования бактериальных клеток, представляет собой DOC. DOC представляет собой натриевую соль желчной кислоты - дезоксихолевой кислоты, которую обычно получают из биологических источников, таких как коровы или быки. DOC активирует белок LytA, который представляет собой аутолизин, который участвует в росте клеточной стенки и делении Streptococcus pneumoniae. Белок LytA имеет холин-связывающие домены в С-концевом участке, и известно, что мутации гена lytA дают мутантов LytA, которые устойчивы к лизису DOC.
Хотя нет доказательств того, что применение DOC в способе очистки полисахаридов Streptococcus pneumoniae представляет риск для здоровья, применение подобных реагентов биологического происхождения может вызывать потенциальные проблемы связанные с (официальным) регулированием их применения. Соответственно, в одном варианте реализации настоящего изобретения, литический агент, применяемый для лизирования бактериальных клеток, представляет собой литический агент неживотного происхождения. Литические агенты неживотного происхождения для применения в способах согласно настоящему изобретению включают агенты из неживотных источников со способами действия, аналогичными действию DOC (т.е., которые влияют на функцию LytA и приводят к лизису клеток Streptococcus pneumoniae). Такие литические агенты неживотного происхождения включают, но не ограничены перечисленными: аналоги DOC, поверхностно-активные вещества, детергенты и структурные аналоги холина, и их можно определить, применяя процедуры, описанные ниже в Экспериментальном разделе данной заявки. В одном варианте реализации, литический агент неживотного происхождения выбирают из группы, состоящей из декансульфоновой кислоты, трет-октилфеноксиполи(оксиэтилен)этанолов (например, Igepal® СА-630, CAS #: 9002-93-1, доступных от Sigma Aldrich, Сент-Луис, Миссури), конденсатов оксида октилфенол-этилена (например, Triton® Х-100, доступный от Sigma Aldrich, Сент-Луис, Миссури), N-лаурилсаркозината натрия (NLS), лаурилиминодипропионата, додецилсульфата натрия, хенодезоксихолата, гиодезоксихолата, гликодезоксихолата, тауродезоксихолата, таурохенодезоксихолата и холата. В следующем варианте реализации, литический агент неживотного происхождения представляет собой NLS.
Настоящее изобретение также относится к модификациям способа, описанного выше, специфичным для конкретного серотипа. Например, поскольку полисахарид серотипа 19А нестабилен и его молекулярная масса изменяется в ходе очистки, обнаружили, что модификации описанного способа были полезны для стабилизации полисахарида 19А. Эти модификации включали проведение этапа ультрафильтрации и диафильтрации перед подкислением при приблизительно 4°С при рН, равном приблизительно 6, в натриево-фосфатном буфере, выдерживание подкисленного раствора ретентата в течение по меньшей мере 2 часов при приблизительно 4°С, чтобы обеспечить осаждение преципитата, и подведение рН осветленного раствора полисахарида до значения 6 перед этапом фильтрации активированным углем. Напротив, обнаружили, что для серотипов 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F, и 23F меньшая потеря полисахарида и лучшее удаление белка достигается, когда этап ультрафильтрации и диафильтрации перед подкислением осуществляют в бессолевых средах, таких как вода, и этот этап можно осуществить при комнатной температуре при нейтральном значении рН.
Соответственно, настоящее изобретение также относится к способу получения по существу очищенных капсульных полисахаридов из лизата клеток Streptococcus pneumoniae, включая серотип 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F или 23F, включающему следующие стадии:
(a) обеспечение ферментативного бульона, который содержит бактериальные клетки, которые продуцируют серотип Streptococcus pneumoniae 1, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19F или 23F;
(b) лизирование бактериальных клеток, полученных на стадии (а), детергентом с получением лизата клеток, который содержит остатки клеток, растворимые белки, нуклеиновые кислоты и полисахариды;
(c) осветление клеточного лизата, полученного на стадии (b), посредством центрифугирования или фильтрования для удаления остатков клеток с получением осветленного лизата клеток;
(d) ультрафильтрование