Способ обработки упаковки с однократной дозой лекартвенного препарата
Иллюстрации
Показать всеИзобретение относится к области фармацевтики. Способ деагломерации содержимого упаковки с по меньшей мере одной однократной дозой лекарственного препарата на ленте с множеством упаковок с однократной дозой лекарственного препарата включает осуществление контакта между ультразвуковым зондом и лентой с обеспечением вибрации, посредством чего содержимое упаковки с по меньшей мере одной однократной дозой лекарственного препарата может быть по меньшей мере частично деагломерировано, причем в состав упаковки с одной однократной дозой лекарственного препарата входит термоформованная коробочка, а ультразвуковой зонд контактирует с лентой так, что при этом он не контактирует с термоформованной коробочкой. Способ выполняется до завершающих операций при производстве упаковки. Способ обеспечивает облегчение извлечения лекарственных препаратов из упаковочной тары, причем транспортировка препарата не оказывает влияния на выпущенные дозы. 10 з.п. ф-лы, 8 ил.
Реферат
Ссылка на родственные заявки
Для настоящей заявки испрашивается приоритет по предварительной заявке US 61/000627, поданной 25 октября 2007 г., которая включена в настоящую заявку в полном объеме посредством ссылки.
Область техники
Настоящее изобретение, в частности, относится к обработке (доведению до требуемого состояния) порошковых составов в блистерных упаковках или упаковках других конфигураций, для повышения степени дисперсности порошка. Настоящее изобретение также относится к различным аппаратам для достижения вышеуказанной цели.
Уровень техники
Необходимость эффективного терапевтического лечения пациентов привела к разработке разнообразных способов приема фармацевтических составов пациентами. Один из традиционных способов предполагает пероральное введение фармацевтических составов в форме таблеток, капсул и др. Другой способ, также зарекомендовавший себя в качестве эффективного способа введения лекарственных препаратов, предполагает их введение ингаляцией, при котором пациент вдыхает аэрозольный фармацевтический состав через рот или через нос, для его попадания в дыхательные пути. Согласно одной из техник способа ингаляции фармацевтический состав вводят глубоко в легкие пациента, где указанный состав может абсорбироваться в кровоток. Согласно другой технике фармацевтический состав вводят в конкретную область дыхательных путей для локального лечения этой конкретной области. Существует множество типов устройств для ингаляции, включая устройства, которые переводят фармацевтический состав в виде сухого порошка в аэрозольный состав.
Фармацевтический состав часто имеет такую упаковку, в которой он может быть легко доступен для приема пациентом. Например, доза или часть дозы может располагаться между слоями многослойной упаковки, которую традиционно называют блистером или блистерной упаковкой. В таких упаковках, как правило, нижний слой имеет углубление, в которое помещают лекарственный препарат, а верхний слой герметически наносят на нижний слой способом термосклеивания и(или) прессования слоев, для гарантии нахождения лекарственного препарата внутри указанного углубления. В качестве альтернативного варианта, доза лекарственного препарата может быть заключена в капсулу, предназначенную либо для проглатывания, либо из которой лекарственный препарат может быть переведен в аэрозольный состав. Кроме того, для хранения лекарственных препаратов могут использоваться также и другие упаковочные средства, такие как бутылки, пузырьки и т.д. В публикации международной заявки WO 01/43802 раскрыты системы и способы обращения с упакованными порошковыми лекарственными средствами в момент ингаляции.
Часто эффективное заполнение упаковочных средств лекарственными препаратами связано с определенными трудностями. Например, в процессе заполнения упаковочных средств некоторыми порошковыми препаратами достаточно трудно придать порошку требуемую текучесть и(или) поддерживать текучесть такого порошка постоянной. С другой стороны, иногда порошки могут быть спрессованы в шайбообразные таблетки для их заполнения в штампованные блистерные упаковки. В зависимости от характерных особенностей порошка в насыпном виде, для гарантии требуемого контроля заполняемой массы, специально регулируют степень вакуумирования и амплитуду ультразвукового зонда в расфасовочной машине, формирующей указанные таблетки. Такая таблетка может рассыпаться в порошок во время последующих операций на расфасовочной/упаковочной машине или во время транспортировки. Однако в тех случаях, когда таблетка является относительно "жесткой", она может не полностью диспергироваться с образованием однородного порошка, как это требуется для надлежащего приема пациентом. Механические вибрации, имеющие место во время последующей транспортировки конечного продукта, также могут оказывать влияние на свойства порошка в блистерной упаковке. Такие вибрации могут привести к различию в дозах препарата, предлагаемого пациенту, поскольку результаты выпущенных доз лекарственного препарата на время окончания производственных испытаний могут отличаться от результатов выпущенных доз этого же препарата на момент приема. Следовательно, полезно "обработать" или разбить таблетку порошкового лекарственного препарата после заполнения и герметичного запечатывания блистера для гарантии постоянных характеристик продукта, начиная со времени его производства, до момента его приема. Соответственно имеются в разработке новые механизмы доведения до требуемого состояния упомянутых порошковых препаратов.
Раскрытие изобретения
Настоящее изобретение предлагает способы обработки до требуемого состояния порошковых препаратов (лекарственных средств) после их упаковки для более легкого их извлечения из упаковочных средств. Эти и другие предметы, аспекты, варианты и особенности настоящего изобретения станут еще более очевидными из следующего подробного описания.
Краткое описание чертежей
Далее настоящее изобретение раскрыто в приведенном ниже описании и проиллюстрировано на прилагаемых чертежах, на которых:
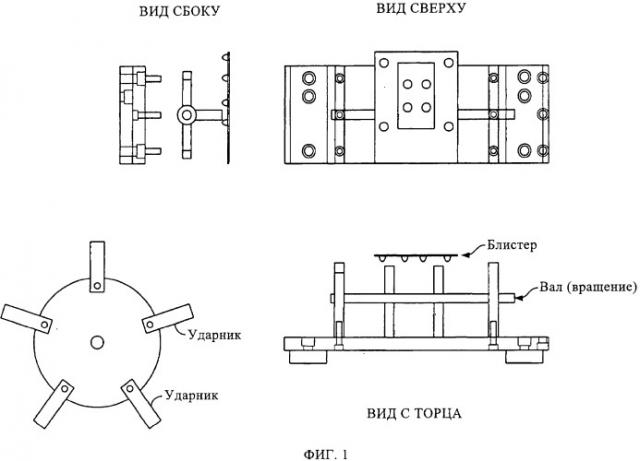
на фиг.1 показан механический встряхиватель;
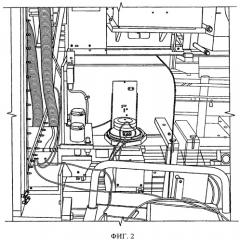
на фиг.2 показана акустическая система на расфасовочной/упаковочной машине;
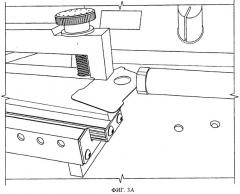
на фиг.3А и 3Б показана обработка блистерных упаковок ультразвуком;
на фиг.4 показана ультразвуковая ванна с блистерными упаковками;
на фиг.5 показано влияние различных способов обработки на подаваемую пациенту дозу и на время выдерживания блистерной упаковки;
на фиг.6 показано влияние ультразвуковой энергии на процесс обработки;
на фиг.7 показано влияние ультразвуковой обработки на примере блистерных упаковок до и после транспортировки при различных уровнях энергии;
на фиг.8 показано влияние ультразвуковой обработки на примере блистерных упаковок с препаратом в насыпном виде до и после транспортировки.
Осуществление изобретения
Следует отметить, что используемая в данном описании форма единственного числа существительных предполагает также возможность их использования во множественном числе, если только это явно не противоречит контексту.
В описании и формуле настоящего изобретения будет использована следующая терминология, согласно приведенным ниже определениям.
Определения
Если иное не оговорено особо, то термины, используемые в настоящем раскрытии изобретения, имеют ниже данные определения. Если в описании определенно не указано иное, то стандартные термины имеют стандартные, традиционные значения, понятные специалистам в данной области техники.
Термин "обработка (до требуемого состояния)" применяется для описания процессов, используемых для облегчения получения более однородного дисперсного порошкового препарата, который характеризуется меньшей степенью агломерации по сравнению с порошковыми препаратами, не прошедшими такую обработку. Термин "деагломерация" равнозначен по значению и может быть использован попеременно с термином "обработка".
Состав, являющийся "приемлемым для доставки к легким", относится к составам, которые могут быть переведены в аэрозольный состав для их вдыхания человеком так, чтобы часть распыленных частиц достигла легких, например, чтобы позволить им проникнуть в альвеолы и в кровь. Такие составы могут рассматриваться как "вдыхаемые" или "пригодные для ингаляции".
"Аэрозолированный" состав содержит твердые частицы, которые удерживаются во взвешенном состоянии в газообразной среде (в основном, воздушной среде), как правило, в результате активизации (или срабатывания) устройства для ингаляции. Ингалятор пассивного сухого порошка активируется вдохом пациента.
"Сухопорошковый ингалятор" представляет собой устройство, в котором находится емкость (например, блистер) с разовой (однократной) дозой лекарственного препарата в виде порошка. В зависимости от схемы лечения нуждающемуся в лекарственном препарате пациенту может потребоваться более одной разовой дозы препарата. Обычно ингалятор активируется вдохом. Например, в капсуле или блистере проделывают отверстия, и порошок распыляется таким образом, чтобы его можно было вдохнуть, как, например, в ингаляторах марок Spinhaler или Rotahaler. Ингаляторы марки Turbohaler оснащены контейнерами, в которых содержатся отмеренные дозы лекарственного препарата в виде порошка.
Используемый здесь термин "подаваемая доза (ПД)" указывает на подачу сухого порошка из устройства для ингаляции после его активизации или после диспергирования порошка в сухопорошковом устройстве или сосуде. ПД определяют как отношение дозы, подаваемой для приема устройством для ингаляции, к расчетной дозе (т.е. к массе порошка на разовую дозу, находящуюся в соответствующем устройстве для ингаляции до его срабатывания). ПД представляет собой количество препарата, полученное опытным путем, и которое может быть рассчитано при использовании лабораторного сосуда, имитирующего дозированный прием лекарственного препарата пациентом. Для расчета величины ПД, согласно использованию в настоящем изобретении, сухой порошок помещают в испытуемое устройство. Устройство активируют (например, путем загрузки блистера, вращения наконечника устройства и насаживания источника вакуума 30 л/мин на выходное отверстие наконечника) для диспергирования порошка. Полученное в результате аэрозольное облако затем отсасывают из устройства вакуумом (30 л/мин) в течение 2,5 секунд после активизации устройства, где оно осело на тарированном фильтре из стекловолокна (Gelman, диаметр 47 см), присоединенном к наконечнику устройства. Количество порошка, которое достигает фильтра, составляет подаваемую дозу. Например, если рассматривать капсулу с содержанием 5 мг сухого порошка, помещенную в устройство для ингаляции, то если в результате диспергирования порошка его количество на тарированном фильтре составит 4 мг, как описано выше, то ПД для данного сухопорошкового состава составит 80% (=4 мг (подаваемая доза)/5 мг (расчетная доза)).
Состав в виде "сухого порошка" представляет собой порошковый состав с содержанием влаги, как правило, менее чем примерно 20%, или менее чем примерно 10%, или менее чем примерно 5%, или менее чем примерно 3%, или менее чем примерно 1%.
Используемый здесь термин "масс-медианный диаметр (ММД)" относится к средней величине диаметра многочисленных частиц, как правило, в популяции полудисперсных частиц, например, состоящей из множества размеров частиц. Если в контексте явно не указано иное, то значения ММД, как описано здесь, определяют методом лазерной дифракции (Sympatec Helos, Clausthal-Zellerfeld, Германия). Образцы порошка, как правило, помещают непосредственно в воронку питателя устройства Sympatec RODOS для диспергирования сухих порошков. Это можно сделать вручную или за счет механического приведения в действие со стороны вибраторного элемента питателя VIBRI. Образцы порошка диспергируют на первичные частицы за счет нагнетаемого воздуха (давлением от 2 до 3 бар) при максимальном разрежении (вакуум-отсосе) для указанного давления диспергирования. Дисперсные частицы исследуют при помощи лазерного луча 632,8 нм, который пересекает траекторию частиц под правильными углами. Лазерный свет, рассеянный с совокупности частиц, воспроизводится на концентрическую антенную решетку элементов фотоумножителя, на котором используется сборка линз Фурье для обратного рассеяния. Рассеянный свет получают с интервалами 5 мс. Гранулометрический состав частиц рассчитывают методом от обратного, по результатам измерений пространственного распространения/распределения интенсивности рассеянного света, при использовании соответствующего алгоритма.
"Масс-медианный аэродинамический диаметр (ММАД)" представляет собой единицу измерения аэродинамического размера дисперсной частицы. Аэродинамический диаметр используют, чтобы описать аэрозолированный порошок с точки зрения его режима осаждения, и он представляет собой диаметр округлого тела какой-то единицы плотности, имеющего ту же самую скорость осаждения в воздухе, что и частица. Аэродинамический диаметр охватывает форму частицы, ее плотность и естественный размер. Согласно использованию в настоящем изобретении ММАД относится к среднему или медианному гранулометрическому составу частиц аэрозолированного порошка, определенному методом измерения количества аэрозолей в воздухе каскадным импактором, при типовых условиях (температура 20°С; относительная влажность 40%) для испытуемого устройства.
"Фракция тонкодисперсных частиц" - это фракция частиц с аэродинамическим диаметром менее 5 микрон (мкм). Если оговорено особо, то к фракции тонкодисперсных частиц может быть также отнесена фракция частиц с аэродинамическим диаметром менее 3,3 микрон.
"Приемное гнездо" представляет собой контейнер/емкость. Например, таким приемным гнездом может быть гнездо для разовой дозы, или же это может быть контейнер, вмещающий несколько доз. К примерам приемных гнезд для разовых доз могут быть отнесены блистерные порционные упаковки и капсулы. В некоторых примерах осуществления настоящего изобретения такие приемные гнезда могут быть удалены из ингалятора, или же такие приемные гнезда могут быть частью ингалятора. Приемные гнезда, как правило, изготавливают из любого материала, поддающегося разрыву, например контролируемому разрыву, например, из слоистого пластика с защитной пленкой фольги или из других материалов. К примерам таких контейнеров/приемных гнезд можно отнести по меньшей мере капсулы, блистеры, пузырьки, ампулы, или системы контейнер/упаковочный элемент, изготовленные из металла, полимера (например, из пластмассы, эластомеров), стекла, или из подобных материалов.
В одном из примеров осуществления настоящее изобретение включает встряхиватель ленты с лекарственным препаратом в блистерных упаковках или механический ударник, выполненный в виде гибких поворотных механических рук (рычагов), расположенных на чем-то типа округлого вала. Поворотная рука соединена с электродвигателем. Поворотная рука может иметь множество выступов. Рука ударяет по ленте (блистеру, включающему одну или несколько отдельных разовых доз лекарственного препарата в приемных гнездах). Такой удар может приходиться сбоку блистера или с его верха, или с низа, в зависимости от конфигурации руки. Скорость вращения вала или период времени между каждым "продвижением" упаковочной линии определяет степень разрушения таблетированного порошкового препарата. Поворотная рука может вращаться с частотой вращения от примерно 500 оборотов/минуту до примерно 4000 оборотов/минуту. Период времени, в течение которого ленту с препаратом в блистерных упаковках подвергают ударному встряхиванию, определяется балансом между производственной мощностью (временем продвижения упаковочной линии) и эффективностью разбивания таблетки на дисперсный порошок.
Во втором примере осуществления настоящего изобретения, получившим название акустической обработки, ленту с препаратом в блистерных упаковках, состоящую из герметично запечатанных блистеров, подвергают механической вибрации посредством акустической системы до того, как она начнет перемещение и будет выполнена вырубка индивидуальных блистеров на вырубном штампе. Система акустической обработки может располагаться сверху, снизу или сбоку ленты с препаратом в блистерных упаковках. В различных схемах акустической обработки может быть предусмотрено несколько таких систем для оптимизации процесса акустической обработки (например, две акустических системы, обращенные к ленте и расположенные с обеих ее сторон). Вибрацию ленты с препаратом в блистерных упаковках можно регулировать настройкой частоты и амплитуды акустической системы, которая, в свою очередь, регулируется напряжением катушки акустической системы. Период времени, в течение которого ленту с препаратом в блистерных упаковках подвергают акустической вибрации, определяется балансом между производственной мощностью (временем продвижения упаковочной линии) и эффективностью разбивания таблетки на дисперсный порошок.
В третьем примере осуществления настоящего изобретения, получившим название ультразвуковой обработки, ленту с препаратом в блистерных упаковках, состоящую из герметично запечатанных блистеров, подвергают механической вибрации посредством ультразвукового зонда (или ультразвукового звукоулавливателя) до того, как она начнет перемещение и будет выполнена вырубка индивидуальных блистеров на вырубном штампе. Зонд может располагаться снизу, сверху или сбоку такой ленты. Вибрацию ленты с препаратом в блистерных упаковках можно регулировать настройкой амплитуды ультразвукового зонда на заданную частоту. Частота механических вибраций может варьироваться примерно от 5 до примерно 100 кГц, предпочтительно примерно от 10 до примерно 40 кГц. Эффективность разбивания таблеток зависит от взаимодействия зонда и ленты. Амплитуда вибраций может варьироваться примерно от 0,001 до примерно 0,01 дюйма, предпочтительно от 0,0005 до 0,005 дюйма. Ультразвуковой зонд может быть использован в течение различного периода времени. Его можно использовать в течение периода примерно от 0,1 до примерно 3 секунд, предпочтительно, от 0,25 до примерно 2 секунд. Период времени, в течение которого ленту с препаратом в блистерных упаковках подвергают ультразвуковой обработке, определяется балансом между производственной мощностью (временем продвижения упаковочной линии) и эффективностью разбивания таблетки на дисперсный порошок. Гибкость настоящего подхода заключается в том, что зонд может располагаться как снизу, так и сверху и сбоку ленты с препаратом в блистерных упаковках.
Еще в одном примере осуществления настоящего изобретения положение ленты с препаратом в блистерных упаковках или блистеров может определяться при использовании поперечной балки, расположенной по горизонтали в поперечном направлении направлению перемещения ленты и являющейся подвижной в вертикальном направлении; и множества штырьков, структурно оформленных и расположенных на поперечной балке, в то время как поперечная балка имеет рабочее положение, при котором она структурно оформлена и расположена таким образом, что множество штырьков могут соприкасаться по меньшей мере либо с лентой, либо с наконечниками зонда, представляющими собой его рабочий орган, и нерабочее положение, когда она структурно оформлена и расположена таким образом, что множество штырьков могут не соприкасаться с лентой или наконечниками зонда.
Еще в одном примере осуществления настоящего изобретения положение ленты с препаратом в блистерных упаковках или блистеров может определяться при использовании пружинящих пальцев, расположенных на вращающемся валу, который вращается в направлении, поперечном направлению перемещения ленты. Пружинящие пальцы могут далее включать наконечники из пластика или резины для снижения шума и обеспечения плавной работы. Для облегчения работы пружинящие пальцы могут быть присоединены к валу с подшипниками. Ультразвуковая обработка некоторых порошков может привести к переходящему явлению трибозарядки. Для снятия напряжения перед использованием блистеров необходим непродолжительный период их складского хранения.
В четвертом примере осуществления настоящего изобретения, также получившим название ультразвуковой обработки, ленту, состоящую из герметично запечатанных блистеров, подвергают механической вибрации при использовании ультразвуковой ванны, до того как она начнет перемещение и будет выполнена вырубка индивидуальных блистеров на вырубном штампе.
Настоящее изобретение также может включать стадии, касающиеся получения герметично запечатанной упаковки, а именно стадии заполнения полости упаковки по меньшей мере одной однократной дозы лекарственного препарата и герметичного запечатывания указанной заполненной полости, при этом запечатывание может производиться путем нанесения покровного материала на указанную полость. Примером такой упаковки является блистер или блистерная упаковка. В таких упаковках, как правило, нижний слой имеет углубление, в которое помещают лекарственный препарат, а верхний слой герметически наносят на нижний слой способом термосклеивания и(или) прессования слоев, для гарантии нахождения лекарственного препарата внутри указанного углубления. Таким образом, углубление совместно с нанесенным термосклеиванием и/или термопрессованием верхним слоем образуют термоформованную коробочку.
Порошок может изначально храниться в герметично запечатанном приемном гнезде, которое открывается до начала его аэрозолизации, как это описано в патентах US 5785049, US 5415162 и в заявке на патент с регистрационным номером 09/583312. В качестве альтернативного варианта, порошок может содержаться в капсуле, как это описано в патентах US 4955385, US 3991761, US 6230707 и в публикации международной заявки WO 97/27892, при этом капсула открывается до, во время или после установки капсулы в устройство для аэрозолизации. В насыпном виде, в блистерной упаковке, в капсуле или в аналогичном виде, порошок может быть подвергнут аэрозолизации при использовании активного элемента, например сжатого воздуха, как это описано в патентах US 5458135, US 5785049 и US 6257233, или газа-вытеснителя, как описано в заявке US 09/556262, поданной 24 апреля 2000 года, и имеющей название "Способы и аппараты для аэрозолизации", и в публикации международной заявки WO 00/72904. В качестве альтернативного варианта, порошок может быть подвергнут аэрозолизации при вдохе пациента, как это описано, например, в вышеуказанной заявке US 09/583312 и в патенте US 4995385. Все упомянутые выше документы включены в настоящую заявку посредством их приведения в полном объеме в качестве ссылок.
Гнездо может быть вставлено в устройство для аэрозолизации. Оно может иметь приемлемую форму, размер и материал для содержания фармацевтического состава и для поддержания фармацевтического состава в пригодном для приема виде. Например, капсула или блистер могут иметь стенку, которая включает материал, не вступающий в нежелательные реакции с фармацевтическим составом. Кроме того, стенка может включать материал, позволяющий капсуле открыться для аэрозолизации фармацевтического состава. По одному из вариантов стенка включает один или более таких материалов, как желатин, гидроксипропил метилцеллюлоза (ГПМЦ), ГПМЦ, компаундированная с полиэтиленгликолем, гидроксипропилцеллюлоза, агар, алюминиевая фольга и им подобных материалов. По одному из вариантов капсула может быть выполнена в виде микроскопических, примыкающих друг к другу, секций, как это описано, например, в патенте US 4247066, который включен в настоящую заявку в качестве ссылки. Размер капсулы выбирают таким, чтобы она была достаточной для размещения дозы фармацевтического состава. Размеры, как правило, варьируются от размера 5 до размера 000 с наружными диаметрами примерно от 4,91 мм до 9,97 мм; высоты варьируются примерно от 11,10 мм до примерно 26,14 мм, а объемы, соответственно, варьируются примерно от 0,13 мл до примерно 1,37 мл. Промышленное производство приемлемых капсул налажено такими компаниями, как, например, Shionogi Qualicaps Co., Hapa, Япония и Capsugel, Гринвуд, Южная Каролина. После заполнения верхнюю часть можно наложить на нижнюю часть для придания капсуле соответствующей формы и хранить порошок внутри капсулы, как это описано в патентах US 4846876 и US 6357490, а также в заявке WO 00/07572, которые включены в настоящую заявку посредством ссылок. После того, как верхняя часть капсулы установлена на ее нижнюю часть, капсула, по желанию, может быть скреплена ободком.
До начала использования сухие порошки, как правило, хранят в условиях окружающей среды, предпочтительно при температуре 25°С макс. и относительной влажности от 30 до 60%. Более предпочтительная относительная влажность, например, менее 30% может быть достигнута за счет включения влагопоглощающего агента во вторичную упаковку в составе упаковки лекарственной формы.
Устройства
В отношении составов, упомянутых в одном или нескольких примерах осуществления настоящего изобретения, могут быть применены методы и технические средства, известные специалистам в данной области техники.
Например, согласно одному или нескольким примерам осуществления настоящего изобретения, описанные здесь составы могут быть поданы при использовании любого приемлемого сухопорошкового ингалятора (СПИ), например ингалятора, срабатывающего от вдоха пациента, в качестве средства доставки сухопорошкового лекарственного препарата к легким. Предпочтительными сухопорошковыми ингаляторами являются ингаляторы Nektar Therapeutics, как описано в патентах US 5458135; US 5740794 и US 5785049, которые включены в настоящую заявку в качестве ссылки.
При приеме лекарственного препарата с использованием устройства упомянутого выше типа порошок содержится в гнезде, имеющем покрытие с многочисленными точечными отверстиями или другую поверхность, обеспечивающую доступ к препарату, предпочтительно, блистерную упаковку или картридж, в которых в гнезде может содержаться дозированная форма для однократного приема или дозированные формы для многократного приема. Удобные способы заполнения большого количества ячеек (например, упаковок, содержащих лекарственное средство в однократных дозах), отмеренными дозами порошковых лекарственных препаратов, описаны, например в заявке WO 97/41031 (1997), включенной в настоящую заявку посредством ссылки.
Также приемлемыми средствами подачи порошковых препаратов, описанными в настоящей заявке, являются сухопорошковые ингаляторы, например ингаляторы, раскрытые в патентах US 3906950 и US 4013075, включенных в настоящую заявку посредством ссылки, в которых предварительно отмеренная доза сухого порошка, предназначенная для приема пациентом, содержится в жесткой желатиновой капсуле.
Другие устройства для распыления, используемые для ввода сухопорошковых лекарственных препаратов в легкие, раскрыты, например, в публикациях ЕР129985, ЕР472598, ЕР467172 и в патенте US 5522385, включенных в настоящую заявку посредством ссылки. Также приемлемыми средствами для ввода сухопорошковых препаратов по настоящему раскрытию предмета изобретения являются такие устройства для распыления, как Astra-Draco "TURBOHALER". Устройство этого типа подробно описано в патентах US 4668281, US 4667668 и US 4805811, каждый из которых включен в настоящую заявку в качестве ссылки. К другим приемлемым устройствам для распыления относятся сухопорошковые ингаляторы, например ROTAHALER™ (Glaxo), Discus™ (Glaxo), Spiros™ inhaler (Dura Pharmaceuticals) и Spinhaler™ (Fisons). Также в качестве приемлемых можно назвать устройства, в которых имеется поршень, используемый для подачи воздуха либо для захватывания порошкового лекарственного препарата, подъема лекарственного препарата с экрана носителя за счет пропуска воздуха сквозь экран, либо для смешения воздуха с порошковым лекарственным препаратом в смесительной камере с последующим вводом порошка пациенту через горлышко подобного устройства для распыления, как это раскрыто в патенте US 5388572, включенном в настоящую заявку посредством ссылки. Еще одна группа сухопорошковых ингаляторов, которые также могут быть использованы, раскрыта в предварительных заявках US 60/854601 и 69/906977, которые включены в настоящую заявку посредством ссылки, и которые являются собственностью Nektar Therapeutics.
Сухопорошковые препараты могут вводиться при использовании находящихся под давлением устройств для распыления отмеренных доз лекарственного препарата, например ингалятора для распыления отмеренных доз Ventolin™, в котором раствор или суспензия лекарственного препарата содержится в фармацевтически инертной сжатой вытесняющей среде, например хлорофторуглероде или фторуглероде, согласно раскрытию в патентах US 5320094 и US 5672581, оба из которых включены в настоящую заявку посредством ссылки.
Фармацевтический состав/композиция может содержать активно действующий компонент. Активно действующий компонент, описанный в настоящем раскрытии изобретения, представляет собой агент, лекарственное средство, сочетание лекарственных средств, химическое соединение или смесь химических соединений, которые оказывают фармакологическое, обычно благотворное, влияние. Сюда относятся пищевые продукты, пищевые добавки, питательные вещества, лекарственные средства, вакцины, витамины и другие благотворно влияющие вещества. При использовании в настоящем раскрытии изобретения эти термины далее включают любой физиологически или фармакологически активно действующий компонент, обеспечивающий локальное воздействие или общее воздействие на организм пациента. Активно действующий компонент для включения в фармацевтический состав по настоящему изобретению может быть неорганическим или органическим соединением, включая, без ограничений, лекарственные средства, воздействующие на: периферическую нервную систему, адренергические рецепторы, холинергические рецепторы, скелетные мышцы, сердечно-сосудистую систему, гладкие мышцы, систему кровообращения, синоптические локализации, атриовентрикулярные локализации нейроэффектора, эндокринную и гормональную системы, иммунную систему, репродуктивную систему, костную систему, легочный круг кровообращения, системы физиологически активных веществ, пищеварительную и выделительную системы, систему образования гистамина и центральную нервную систему. Приемлемые активно действующие компоненты могут быть выбраны, например, из снотворных средств, успокоительных средств, антидепрессантов, транквилизаторов, лекарственных препаратов, воздействующих на органы дыхания, противосудорожных препаратов, мышечных релаксантов, средств против дрожательного паралича (антагонистов дофаминовых рецепторов), анальгетиков, противовоспалительных средств, успокоительных (анксиолитических) средств, средств, подавляющих аппетит, средств против мигрени, средств для мышечных сокращений, противоинфекционных средств (антибиотиков, антивирусных средств, противогрибковых средств, вакцин), противоартритных препаратов, противомалярийных средств, противорвотных средств, противоэпилептических средств, бронходилататоров, цитокинов, стимуляторов роста, противоопухолевых препаратов, антитромботических препаратов, противогипертонических средств, сердечно-сосудистых средств, антиаритмических препаратов, антиоксидантов, противоастматических средств, гормональных средств, включая противозачаточные средства, симпатомиметических средств, мочегонных средств, липид-регулирующих средств, антиандрогенных веществ, антипаразитарных средств, антикоагулянтов, относящихся к опухолям и противоопухолевых средств, гипогликемических средств, питательных веществ и добавок, добавок, способствующих росту, противоэнтеритных средств, вакцин, антител, диагностических и контрастных веществ. Активно действующий компонент может быть введен ингаляцией, может иметь локальное или общее воздействие на организм пациента.
Активно действующий компонент может относится к одному из нескольких структурных групп, включая по меньшей мере небольшие молекулы, пептиды, полипептиды, протеины, полисахариды, стероиды, способные к физиологическим воздействиям протеины, нуклеотиды, олигонуклеотиды, полинуклиотиды, жиры, электролиты и т.п.
Примеры активно действующих компонентов, приемлемых для использования в настоящем раскрытии изобретения, включают, но не ограничиваются одним или несколькими такими активно действующими компонентами, как кальцитонин, амфоторицин В, эритропоэтин (ЕРО), фактор VIII, фактор IX, цередаза, церезим, циклоспорин, гранулоцитарный колониестимулирующий фактор (GCSF), тромбопоэтин (ТРО), ингибитор альфа-1 протеиназы, элькатонин, гранулоцитарный-моноцитарный колониестимулирующий фактор (GMCSF), гормон роста, гормон роста человека (HGH), гормон, высвобождающий гормон роста (GHRH), гепарин, низкомолекулярный гепарин (LMWH), интерферон-альфа, интерферон-бета, интерферон-гамма, рецептор интерлейкина-1, интерлейкин-2, гибридный белок интерлейкина-2, антагонист рецептора интерлейкина-1, интерлейкин-3, интерлейкин-4, интерлейкин-6, интерлейкин-11, рилизинг-фактор лютеинизирующего гормона (LHRH), инсулин, проинсулин, аналоги инсулина (например моноацильный инсулин, как описано в патенте US 5922675, включенном в настоящую заявку в качестве ссылки в полном объеме), амилин, С-пептид, соматостатин, аналоги соматостатина, включая октреодид, вазопрессин, фолликуло-стимулирующий гормон (FSH), инсулиноподобный фактор роста (IGF), белок, связывающий инсулиноподобный фактор роста (например IGFBP3), инсулинтропин, колониестимулирующий фактор макрофагов (M-CSF), фактор роста нервной ткани (NGF), факторы роста соединительный ткани, фактор роста кератиноцитов (KGF), фактор роста глии (GGF), фактор некроза опухолей (TNF), фактор роста эндотелия сосудов, паратиреоидный гормон (РТН), глюкагоноподобный пептид-тимозин альфа 1, ингибитор IIb/IIIa, альфа-1 антитрипсин, соединения фосфодиэстеразы (PDE), ингибиторы VLA-4, бифосфонаты, антитело респираторно-синцитиального вируса, фактор трансмембранного регулятора муковисцидоза (CFTR), дезоксирибонуклеаза (DNase), бактерицидный белок, увеличивающий проницаемость клеточной мембраны (BPI), антитело цитомегаловируса (anti-CMV), 13-цис ретиноевая кислота, 0-цис ретиноевая кислота, макролиды, например эритромицин, олеандомицин, тролеандомицин, рокситромицин, кларитромицин, даверцин, азитромицин, флуритромицин, диритромицин, джозамицин, спиромицин, мидекамицин, лейкомицин, миокамицин, рокитамицин, андацитромицин, и звинолид А; фторохинолоны, например ципрофлоксацин, офлоксацин, левофлоксацин, тровафлоксацин, алатрофлоксацин, моксифлоксицин, норфлоксацин, эноксацин, грепафлоксацин, гатифлоксацин, ломефлоксацин, спарфлоксацин, темафлоксацин, перфлоксацин, амифлоксацин, флероксацин, тозуфлоксацин, прулифлоксацин, ирлоксацин, пазуфлоксацин, клинафлоксацин и ситафлоксацин; аминогликозины, например гентамицин, нетилмицин, парамецин, тобрамицин, амикацин, канамицин, неомицин и стрептомицин, ванкомицин, тейкопланин, рамполанин, мидепланин, колистин, даптомицин, грамицидин, колистиметат, полимиксины, например полимиксин В, капреомицин, бацитрацин, пенемс; пенициллины, включая пеникллиназ-чувствительные соединения, например пенициллин G, пенициллин V, пеникллиназ-устойчивые соединения, например мецитиллин, оксациллин, клоксациллин, диклоксациллин, флоксациллин, нафциллин; активнодействующие компоненты грамотрицательных микроорганизмов, например ампициллин, амоксициллин и гетациллин, циллин и галампициллин; антипсевдомонадные пенициллины, например карбенициллин, тикарциллин, азлоциллин, мезлоциллин и пиперациллин; цефалоспорины, например цефподоксим, цефпрозил, цефтбутен, цефтизоксим, цефтриаксон, цефалотин, цефапирин, цефалексин, цефрадрин, цефокситин, цефамандол, цефазолин, цефалоридин, цефаклор, цефадроксил, цефалоглицин, цефуроксим, цефоранид, цефотаксим, цефатризин, цефацетрил, цефепим, цефиксим, цетоницид, цефоперазон, цефотетан, цефьетазол, цефтазидим, лоракарбеф и максалактам; монобактамы, например азтреонам; и карбапенемы, например имипенем, меропенем, пентамидин изеционат, альбутерол сульфат, лидокаин, метапротеренол сульфат, беклометазон дипрепионат, триамцинолон ацетонид, будесонид ацетонид, флутиказон, ипратропий бромид, флунизолид, натрий кромолин, эрготамин, тартрат; рилапладиб, дараздфвши, ремоглифлоцин этабонат, отеликсицумаб, карведилол, фондапарнукс, метформин, росиглитазон, фарглитизар, ситамааквин, тафеноквин, белимумаб, пазопаниб, ронакалерет, солабегрон, дутастерид, меполицумаб, офатумумаб, орвепитант, казопитант, фиратеграст, ламотриджин, ропинирол, ибоктадекин, ритуксимаб, тотромбопаг, лапатиниб, элескломол, топотекан, даротропиум, дзафирлукаст, анастрозол, кандесантан цилексетил, бамбутерол, тербуталин, мепивакаин, бикалутамид, прилокаин, розуваститин, пропофол, фулвестрант, изосорбид-5-мононитрат, изосорбид динитрат, пропанолол, гефитиниб, эналаприл, фелодипин, метопролол, омепразол, бупивакаин, примидон, ропивакаин, эзомепразол, атенолол, нифедипин, тамоксифен, формотерол, рамиприл, кветиапин, хлорталидон, ралтитрексед, вилоксацин, лизиноприл, гидрохлоротиацид, гозерелин, золмитриптан, заксаглиптин, дапаглифлоцин, мотавизумаб,