Фармакологическая геропротекторная композиция и способ ее получения
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и представляет собой фармакологическую геропротекторную композицию, включающую полифенольный компонент, витамины и микроэлементы, гуминовые кислоты, содержащие полифенольные компоненты, витамин C, витамин A, хлорид железа(II) и двуокись селена(IV), причем компоненты в композиции находятся в определенном соотношении в масс. %. Изобретение обеспечивает увеличение продолжительности жизни и замедление развития опухоли, 2 н.п. ф-лы, 3 ил., 2 табл., 4 пр.
Реферат
Изобретение относится к медицине, а именно к фармацевтической промышленности, и касается геропротекторных композиций на основе полифенольных компонентов, витаминов и минералов и способов ее получения.
Эпидемиологические данные и результаты экспериментальных исследований свидетельствуют о том, что разнообразные полифенольные компоненты (флавоноиды) играют большую роль в профилактике таких возрастзависимых заболеваний, как рак и сердечно-сосудистые заболевания (Graf В.А, Milbury Р.Е, Blumberg J.B. Flavonols, flavones, flavanones, and human health: epidemiological evidents // J.Med. Food. - 2005. - Fall; V.8, N 3. - P.281-290).
Есть данные, свидетельствующие о том, что высокий уровень флавоноидов напрямую связан со снижением риска развития инфаркта миокарда (Hernandez-Diaz S., Marinez-Losa Е., Fernandez-Jame Е., Serrano-Martinaz M., Martines-Gonzalez M. Dietary folate and the risk of nonfatal myocardial infarction // Epidemiology. - 2002. - V.13. - P.700-706) и других сердечно-сосудистых заболеваний (Kondo К., Matsumoto A., Kurata Н., Tanahashi H., Koda H., Amachi Т., Itakura H. Inhibition of oxidation of low-density lipoprotein with red wine // Lancet. - 1994. - V.344. - P.1152).
Кроме того, было обнаружено, что ресвератрол (флавоноид, который содержится в красном вине) обладает антиканцерогенным эффектом: подавляет рост индуцированных опухолей кожи у мышей (Jang М., Cai L., Udeani G.O., Slowing K.V., Thomas C.F., Beecher C.W., Fong H.H., Farnsworth N.R., Kinghorn A.D., Mehta R.G., Moon R.C., Pezzuto J.M. Cancer chemopreventive activity of resveratrol, a natural product derived from grapes // Science. - 1997. - V.275. - P.218-220).
Имеются данные о том, что другие полифенольные компоненты (катехины, содержащиеся в зеленом чае), не только снижают уровень липидов в организме и препятствуют развитию сердечно-сосудистых заболеваний (Arts I.C., Hollman P.Ch., Feskens E. J.M., De Mesquita H.B.B., Kromhout D. Catechin intake might explain the inverse relation between tea consumption and ischemic heart disease; the Zutphen elderly study // Am. J. Clin. Nutr. - 001. - V.74. - P.227-232), но и способны снижать риск развития онкологических заболеваний (Zheng W., Doyle T.J., Kushi L.H., Sellers T.A., Hong C-P., Folsom A.R. Tea consumption and cancer incidence in a prospective cohort study of postmenopausal women // Am. J. Epidemiol. - 1996. - V.144. - P.175-182).
В медицине описанные компоненты используются в основном в составе растительных экстрактов.
Известно гепатопротекторное средство на основе полифенолов артишока (RU 2281112, опубл. 10.08.2006), антиоксидантные средства на основе полифенолов чаги (RU 2339390, опубл. 10.08.2006) и травы псефеллюс (RU 2390347, опубл. 27.05.2010), лекарственное средство для лечения предраковых поражений кожи (RU 2366447, 27.11.2007), оздоравливающая БАД на основе экстракта виноградных косточек (RU 2350125, опубл. 27.03.2009) и др.
Известны фармацевтические композиции на основе полифенолов, дополнительно включающие аскорбиновую кислоту (RU 2229303, опубл. 27.05.2004; RU 2301666, опубл. 27.06.2007), которая обладает выраженным антиоксидантным действием. Также известны композиции, включающие ретинол (бета-каротин - витамин А-ретинол), участвующий в антиоксидантной защите организма (RU 2350125, опубл. 27.03.2009).
Кроме того, существуют полифенолсодержащие композиции для профилактики железо-дефицитных анемий на основе соединений железа (RU 2005130673, опубл. 10.04.2007) и средства для замедления старения, содержащие селен (RU 2433819, опубл. 20.11.2012). Известно, что недостаток селена может влиять на развитие сердечно-сосудистых заболеваний, атеросклероза (Alissa Е.М. et al., 2003), рака и нарушений иммунитета (Seiler W.O., 2001), а применение его препаратов значимо снижает риск развития рака легкого (Reid М.Е., 2002).
Известна фармацевтическая композиция на основе полифенолов, блокирующая пролиферацию раковых клеток и метастазирование, используемая при лечении рака (RU 2301666, опубл. 27.06.2007). В состав композиции включено, по меньшей мере, одно полифенольное соединение, выбранное из группы, состоящей из галата эпигаллокатехина, галата эпикатехина, эпигаллокатехина, эпикатехина и катехина. Используются полифенольные соединения, содержащиеся в экстракте зеленого чая. Композиции включают также аскорбиновую кислоту, лизин, пролин, соли селена, меди, магния. Эта композиция принята авторами за прототип.
Техническим результатом изобретения является создание стабильной фармакологической геропротекторной композиции, основанной на полифенольном компоненте гуминовых веществ, содержащей одновременно малорастворимые неорганические соединения селена и железа, и гидрофобные органические вещества (витамин A).
Указанный технический результат достигается тем, что фармакологическая геропротекторная композиция согласно изобретению содержит гуминовые кислоты, содержащие полифенольные компоненты, витамин C, витамин A, хлорид железа(II) и двуокись селена(IV) при следующем соотношении компонентов, мас.%:
| гуминовые кислоты, содержащие | |
| полифенольные компоненты | 0,45-0,55 |
| витамин C | 0,009-0,011 |
| витамин A | 0,0045-0,0055 |
| хлорид железа(II) | 0,02-0,025 |
| двуокись селена(IV) | 0,0012-0,0015 |
| остальное | вода |
Предложенная композиция отличается от прототипа тем, что в качестве источников полифенолов используются гуминовые кислоты, полученные из древесного лигнина (PA 2012 7059). Данное исходное сырье отличается высокой экономичностью получения и высокой воспроизводимостью химического состава.
Одним из самых выраженных эффектов от применения гуминовых кислот, является усиление общего иммунного ответа за счет присутствия полифенольных группировок в их составе (Филов В.А., Беркович А.М. Гуминовые вещества: возможности использования их биологических эффектов. Ветеринария. 2007. №8. С.14-17).
Известно, что витамин A (его предшественник - бета-каротин и собственно ретинол) является сильным антиоксидантом, участвует в обменных процессах организма.
Следует отметить, что изучение геропротекторного эффекта у мышей при введении животным только одного препарата, в частности бета-каротина, не оказывало существенного эффекта на показатели продолжительности жизни (Massie H.R., Ferreira J.R. Jr., DeWolfe L.K. Effect of dietary beta-carotene on the survival of young and old mice // Gerontology. - 1986. - V.32, N.4. - P.189-195), однако в экспериментах, когда были использованы так называемые диетические антиоксидантные смеси, состоящие из бета-каротина, альфа-токоферола, аскорбиновой кислоты, рутина, селена и цинка - у гибридных мышей при введении с пищей, начиная с двухмесячного возраста - эффект был статистически достоверным по сравнению с контрольными мышами - наблюдалось увеличение ПЖ (Bezlepkin V.G. et al., 1996).
Таким образом, исследования по оценке геропротекторных свойств бета-каротина у мышей свидетельствуют о том, что бета-каротин оказывает определенное усиление других действующих активных добавок или компонентов диеты, имеющих геропротекторные свойства.
Также имеются данные, свидетельствующие о способности витамина А и бета-каротина увеличивать выживаемость мышей линии СВА после гамма облучения, если препараты вводили через 2 дня после облучения (Seifter Е., Rettura G., Padawer J. et al. Morbidity and mortality reduction by supplemental vitamin A or beta-carotene in CBA mice given total-body gamma-radiation // J. Natl. Cancer Inst. - 1984. - V.73, N.5. - P.1167-1177).
Эти результаты подтверждают наличие у витамина A и бета-каротина антиоксидантных свойств, а также свидетельствуют о способности влиять на иммунные процессы.
Известно, что селен является необходимым для некоторых биохимических механизмов в организме и снижение содержания его уровня в крови может приводить к развитию таких заболеваний, как рак, сердечно-сосудистые заболевания, а также нарушению иммунитета (Seiler W.O. Clinical pictures of malnutrition in ill elderly subjects // Nutrition. - 2001. - V.17. - P.496-498).
Также в некоторых исследованиях на животных было показано, что дефицит селена приводит к смертельным случаям из-за острой сердечно-сосудистой недостаточности, а также нарушению пролиферации лимфоцитов (Alissa Е.М., Bahijri S.M., Ferns G.A. The controversy surrounding selenium and cardiovascular disease: a review of the evidence // Med. Sci. Monit. - 2003. - V.9. - P. RA9-RA18). Имеются и эпидемиологические данные (хотя по мнению авторов еще недостаточные для полного заключения о роли селена), свидетельствующие о том, что недостаток селена играет важную роль в этиологии сердечно-сосудистых заболеваний, а также в развитии атеросклероза (Alissa Е.М. et al., 2003).
Рандомизированное клиническое исследование по изучению эффекта селена свидетельствовало о статистически значимом снижении риска развития рака легкого (Reid М.Е., Duffield-Lillico A.J., Garland L., Turnbull B.W., Clark L.C., Marshall J.R. Selenium supplementation and lung cancer incidence: an update of the nutritional prevention of cancer trial // Cancer Epidemiol Biomarkers Prev. - 2002. - V.11. - P.1285-1291).
Известно, что железо относится к основным микроэлементам, необходимым для поддержания жизнедеятельности организма человека.
Имеются эпидемиологические данные, свидетельствующие о том, что с возрастом (при оценке возрастного уровня старше 70 лет) наблюдалось снижение содержания железа в организме как у мужчин, так и у женщин, что приводило к увеличению риска смертности, в основном, от сердечно-сосудистых заболеваний (Corti М.С., et al., 1997).
Также известно, что возникающие в пожилом возрасте гипомикроэлементозы (снижение уровня содержания в организме железа в том числе) вызывают развитие иммуносупрессий, а также увеличивают вероятность возникновения новообразований, в частности множественных миелом (Кудрин А.В., Скальный А.В., и др. Иммунофармакология микроэлементов. М.: изд-во КМК. 2000. 537 с.).
Есть данные о взаимодействии пищевых полифенолов и железа - как оказалось, полифенолы ингибируют абсорбцию гемового железа в основном за счет снижения уровня базолатерального выхода ионов (Qianyi М. Et al., 2010).
Проведенные исследования позволили создать фармакологическую геропротекторную композицию на основе гуминовых кислот, содержащих полифенольный компонент, витамина C, витамина A, хлорида железа(II), и двуокиси селена(IV) с учетом свойств и особенностей входящих в нее компонентов, описанных выше.
Предлагаемая композиция содержит одновременно малорастворимые неорганические соединения железа и селена, а также гидрофобные органические вещества (витамин A).
Для получения стабильности предлагаемой композиции предложен способ ее получения путем ультразвуковой обработки входящих в нее компонентов.
Известен способ получения противоопухолевого средства (RU 2102083, опубл. 20.01.98), в котором ультразвуковое воздействие применяют в качестве предварительной обработки медицинского лигнина, входящего в состав средства, причем ультразвуковое воздействие осуществляют при мощности излучения 40±0,5 Вт, частоте колебаний 22±0,5 кГц в течение 20-25 минут.
Известен способ получения антиракового средства на основе координационного соединения двухвалентной платины и гуминовых веществ (RU 2368379, опубл. 27.09.2009). Согласно данному изобретению водный раствор, содержащий гуминовые вещества, обрабатывают координационным соединением платины под воздействием ультразвукового излучения в диапазоне частот от 18 до 66 кГц с мощностью от 0,5 до 5 Вт/см3. При мощности излучения 5 Вт/см3 с частотой 22 кГц обработку проводят в течение 5-20 мин. Способ обеспечивает получение более однородного и более стабильного при хранении продукта. Этот способ выбран в качестве прототипа.
Однако все описанные способы неприменимы для получения стабильной композиции, содержащей одновременно малорастворимые неорганические соединения и гидрофобные органические вещества (витамин A).
Указанный технический результат достигается также тем, что в способе получения предлагаемой фармакологической геропротекторной композиции, включающем обработку водного раствора исходных гуминовых веществ соединениями металлов при ультразвуковом излучении, согласно изобретению водный раствор исходных гуминовых кислот, содержащих полифенольные компоненты, обрабатывают хлоридом железа(II) и двуокисью селена(IV) при ультразвуковом излучении мощностью 0,1-2 Вт/см3, частотой 15 кГц в течение 5 минут, затем витамином A при ультразвуковом излучении мощностью 0,1-2 Вт/см3, частотой 45 кГц в течение 2 минут, а затем витамином С при ультразвуком излучении мощностью 0,1-2 Вт/см3, частотой 35 кГц в течение 0,5 минут.
Сущность изобретения проиллюстрирована на чертежах, где:
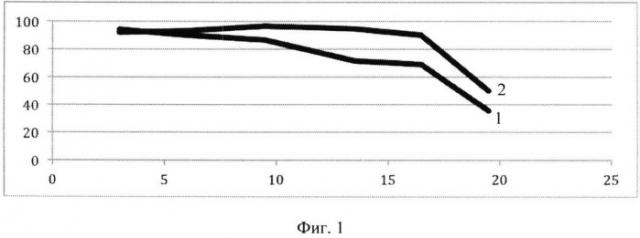
на Фиг.1 представлена зависимость, построенная в координатах: X - срок жизни животных, в месяцах, Y - количество мышей с регулярными астральными циклами, % от общего количества; кривая 2 отражает результаты для группы, получавшей геропротекторное средство, а кривая 1 отражает результаты для контрольной группы;
на Фиг.2 представлена зависимость, построенная в координатах: X - срок жизни животных, в месяцах, Y - количество особей погибших мышей, в штуках; кривая 2 отражает результаты для группы, получавшей геропротекторное средство, а кривая 1 отражает результаты для контрольной группы;
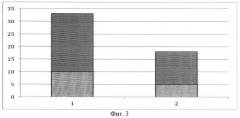
на Фиг.3 представлена диаграмма, в которой значение по оси Y отражает количество опухолей у животных в конце опыта; столбец 1 отражает результаты для контрольной группы, столбец 2 - результаты для группы животных, получавшей геропротекторное средство, верхняя часть столбцов показывает количество опухолей молочной железы, а нижняя - опухолей других локализаций.
Достижение технического результата предлагаемого изобретения подтверждается следующими примерами.
Пример 1. Получение геропротекторного средства, содержащего полифенолы, витамины и минеральные компоненты при однократной обработке ультразвуком.
Гуминовые кислоты, на 40% представленные полифенольными компонентами, в количестве 5 г растворяли в 1000 мл дистиллированной воды при периодическом перемешивании и постоянном нагреве до 50°C в течение 0,5 часов. Далее к раствору добавляли хлорид железа(II) в количестве 225 мг, двуокись селена(IV) в количестве 1,4 мг, витамин С (L-аскорбиновую кислоту) в количестве 100 мг и витамин А (масляный раствор ретинола), содержащий 50 мг действующего вещества, после чего раствор обрабатывали ультразвуком так, как описано в прототипе (RU 2368379): при мощности излучения 5000 Вт с частотой 22 кГц в течение 10 минут.
В дальнейшем исследовались химический состав и стабильность полученного геропротекторного средства (пример 3).
Пример 2. Получение геропротекторного средства, содержащего полифенолы, витамины и минеральные компоненты при трехкратной обработке ультразвуком.
Гуминовые кислоты, на 40% представленные полифенольными компонентами, в количестве 5 г растворяли в 1000 мл дистиллированной воды при периодическом перемешивании и постоянном нагреве до 50°C в течение 0,5 часов. Далее к раствору добавляли хлорид железа(II) в количестве 225 мг и двуокись селена(IV) в количестве 1,4 мг, после чего раствор обрабатывался ультразвуковым излучением с частотой 15 кГц при мощности излучения 2000 Вт в течение 5 минут. После этого в раствор вводили витамин A (масляный раствор ретинола), содержащий 50 мг действующего вещества в условиях одновременной обработки ультразвуком с частотой 45 кГц при мощности излучения 1000 Вт в течение 2 минут, а затем вводили витамин С (L-аскорбиновую кислоту) в количестве 100 мг и продолжали обработку с частотой 35 кГц при мощности излучения 2000 Вт в течение 0,5 минут.
В дальнейшем исследовались химический состав и стабильность полученного геропротекторного средства (пример 3), а также его специфическое действие (пример 4).
Пример 3. Исследования химического состава и стабильности полученного геропротекторного средства.
В исходных гуминовых веществах методом масс-спектрометрии ионно-циклотронного резонанса с Фурье преобразованием (ИЦР ФП МС) были идентифицированы следующие олиго- и полифенольные компоненты:
3-Бензолокси-4,5-дигидрокси-бензойная кислота;
5-(фуран-2-карбонилокси)-2-метил-бензофуран-3-карбоновая кислота;
2,6-диметил-бензо(1,2-b,4,5-b')дифуран-3,7-дикарбоновая кислота;
5-(фуран-2-карбонилокси)-2-метил-бензофуран-3-карбоновая кислота;
Рамнетин;
Метил ((4-метил1-6-оксо-6-бензо(с)хромен-3-ил)окси) уксусная кислота;
Сулохрин;
2,6-Диацетил-7,9-дигидрокси-8,9b-диметилдибензофуран-1,3(2H,9bH)-дион;
Метил 5-гилрокси-7,8-диметокси-1,3-диоксо-1,3,10,11-тетрагидробензо[5,6]цислоокта[1,2-c]фуран-4-карбоксилат;
(1-метокси карбонилметокси-6-оксо-6h-бензо(c)хромен-3-илокси)-уксусная кислота;
Атранорин;
Фенилпропаноид-замещенные эпикатехины и др.
Полученные по примерам 1 и 2 геропротекторные композиции характеризовались следующим составом (табл.1).
| Таблица 1 | ||
| Показатель | Композиция по примеру 1 | Композиция по примеру 2 |
| Гуминовые кислоты, содержащие полифенольные компоненты | 0,48% | 0,47% |
| 0,2% | 0,2% | |
| Витамин C | 0,009% | 0,008% |
| Витамин A | 0,004% | 0,005% |
| Железо | 0,01% | 0,009% |
| Селен | 0,0001% | 0,0001% |
Растворы полученных геропротекторных композиций помещались в условия ускоренного хранения при температуре 40°C для установления их стабильности. Результаты контроля pH и внешнего вида растворов в различные сроки исследования представлены ниже (табл.2).
| Таблица 2 | ||||
| Срок | Композиция по примеру 1 | Композиция по примеру 2 | ||
| Осадок | pH | Осадок | pH | |
| День 0 | Нет | 7,0 | Нет | 7,2 |
| День 46 | Да | 6,2 | Нет | 7,0 |
| День 91 | Да | 5,9 | Нет | 7,1 |
| День 137 | Да | 5,2 | Нет | 6,7 |
| День 183 | Да | 4,8 | Да | 6,1 |
Выявлено, что геропротекторная композиция по примеру 2 отличается более высокой стабильностью.
Пример 4. Исследование специфического действия геропротекторной композиции.
Геропротекторная композиция, полученная по примеру 2, испытывалось в опытах in vivo для установления ее токсичности и влияния на продолжительность жизни.
При разведении препарата для спаивания животным использовали водопроводную воду (2,5 мл исходного раствора препарата добавляли к 250 мл воды).
В опыте использовано 100 беспородных мышей - самок линии SHR 3-месячного возраста (50 подопытных и 50 контрольных) со средней массой 27 граммов с фиксированными датами рождения. Подопытные мыши постоянно получали с питьевой водой геропротекторную композицию в дозе 15 мг/кг ежедневно. Контрольные мыши получали водопроводную воду.
В течение всего опыта не выявлено существенного влияния геропротекторной композиции на общее состояние животных, динамику массы тела и потребление корма. Полученные данные свидетельствуют о том, что в исследованной дозе препарат не оказывает токсического эффекта.
Начиная с 13,5 мес жизни у контрольных мышей наблюдались возрастные нарушения эстральной функции, выражавшиеся в снижении относительной частоты регулярных циклов (Фиг.1). В то же время у подопытных мышей, получавших геропротекторную композицию, подобных изменений не отмечали. Выявленные различия (уменьшение частоты регулярных циклов в контрольной группе по сравнению с опытной на 20-25%) у 13,5 и 16,5-месячных мышей носили статистически достоверный характер. Таким образом, геропротекторная средство способствует нормализации астрального цикла.
За весь период наблюдения в контрольной и подопытных группах пало по 50 животных (100% от исходного количества). Средняя продолжительность жизни мышей составила: в контроле - 578,0±13,85 дней; в подопытной группе - 621,0±17,21 дня (по сравнению с контролем p<0,05) (Фиг.2). Таким образом, геропротекторная композиция достоверно увеличивает продолжительность жизни мышей.
Опухоли в контрольной группе выявлены у 33 мышей, а в опыте - у 19 мышей. Основными опухолями у животных обеих групп были новообразования молочных желез. В контроле они обнаружены у 23 мышей, в подопытной группе - у 13 животных (p<0,05) (Фиг.3). Все опухоли были единичными, за исключением двух мышей контрольной группы, у которой возникло два новообразования молочной железы. Первая опухоль у подопытной мыши обнаружена несколько позже, чем в контроле - в возрасте 338 дней. Средний латентный период обнаружения опухолей молочной железы составил в контроле - 461±21,97 дня, а в подопытной группе - 510±27,15 дня. Таким образом, у мышей, получавших геропротекторную композицию, новообразования молочной железы обнаруживали позже и реже, чем в контроле.
Предлагаемая фармакологическая геропротекторная композиция обладает стабильностью благодаря способу ее получения и может быть использована в качестве средства, увеличивающего продолжительность жизни и замедляющего развитие опухоли.
1. Фармакологическая геропротекторная композиция, включающая полифенольный компонент, витамины и микроэлементы, отличающаяся тем, что композиция содержит гуминовые кислоты, содержащие полифенольные компоненты, витамин C, витамин A, хлорид железа(II) и двуокись селена(IV) при следующем соотношении компонентов, мас. %:
| гуминовые кислоты, содержащие | |
| полифенольные компоненты | 0,45-0,55 |
| витамин C | 0,009-0,011 |
| витамин A | 0,0045-0,0055 |
| хлорид железа(II) | 0,02-0,025 |
| двуокись селена(IV) | 0,0012-0,0015 |
| остальное | вода |
2. Способ получения фармакологической геропротекторной композиции по п.1, включающий обработку водного раствора исходных гуминовых веществ соединениями металлов при ультразвуковом излучении, отличающийся тем, что водный раствор исходных гуминовых кислот, содержащих полифенольные компоненты, обрабатывают хлоридом железа(II) и двуокисью селена(IV) при ультразвуковом излучении мощностью 0,1-2 Вт/см3, с частотой 15 кГц в течение 5 минут, затем витамином А при ультразвуковом излучении мощностью 0,1-2 Вт/см3, с частотой 45 кГц в течение 2 минут, а затем витамином С при ультразвуком излучении мощностью 0,1-2 Вт/см3, с частотой 35 кГц в течение 0,5 минут.