Тозилатная соль производного 5-пиразолил-2-пиридона, полезная в лечении copd
Иллюстрации
Показать всеИзобретение относится к соединению, представляющему собой 4-метилбензолсульфонат 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида, и к его новой кристаллической форме. Изобретение также относится к способу получения указанного соединения и к фармацевтической композиции, для лечения заболевания или состояния, при котором полезно ингибирование активности нейтрофильной эластазы, содержащей указанное соединение и/или его кристаллическую форму. Технический результат: получено новое соединение и его кристаллическая форма, которые могут найти применение в медицине для лечения воспалительного заболевания или состояния, такого как COPD (хроническое обструктивное заболевание легких). 4 н. и 11 з.п. ф-лы, 8 ил., 10 табл., 16 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении раскрыты новая соль 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида, новая кристаллическая форма такой соли, способы получения такой соли и формы, фармацевтические композиции, содержащие такую соль и форму, и применение такой соли и формы в терапии.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В WO 2005/026123, которая включена сюда посредством ссылки во всей ее полноте, сообщается о классе ингибиторов нейтрофильной эластазы, которые являются полезными в терапии.
В WO 2005/026123 дополнительно раскрыто конкретное соединение - ингибитор нейтрофильной эластазы, идентифицированное там как 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамид (Пример 94, страница 85). Это соединение обозначено здесь как соединение (I):
.
В WO 2005/026123 дополнительно раскрыт способ получения соединения (I).
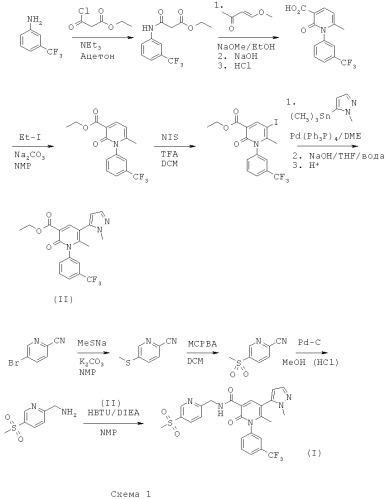
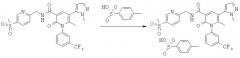
Так, в одном воплощении WO 2005/026123 соединение (I) получают путем, показанным на Схеме 1:
Полученное соединение (I) очищали препаративной HPLC (высокоэффективная жидкостная хроматография) и лиофилизировали с получением свободного основания в виде белого твердого вещества. В WO 2005/026123 не раскрыты ни конкретные соли, ни какие-либо кристаллические формы соединения (I).
Соединение (I) представляет собой мощный ингибитор нейтрофильной эластазы и, как таковое, является полезным в терапии.
Однако соединение (I) в виде свободного основания является малорастворимым, и прогнозы свидетельствуют о том, что данное соединение (введенное в виде свободного основания) демонстрировало бы в высоких дозах (например дозах, больших чем приблизительно от 10 до 20 мг) поглощение, лимитированное растворимостью.
Для того, чтобы получить фармацевтические композиции, содержащие соединение (I) в качестве активного ингредиента для введения человеку, необходимо получить соединение (I) в стабильной и более растворимой форме, такой как стабильная кристаллическая форма, имеющая подходящие физические свойства в твердом состоянии, которые обеспечивают фармацевтическую переработку.
Таким образом, существует потребность в нахождении способа(ов) для обеспечения поглощения малорастворимого фармакологически активного соединения (I) в достаточной степени в пределах таких временных рамок после перорального введения так, чтобы концентрация активного соединения (I) в данной(ых) биологической(их) жидкости(тях) являлась достаточной для получения желательного фармакологического эффекта на протяжении определенного периода времени.
Согласно настоящему изобретению предложена новая соль соединения (I) и стабильная кристаллическая форма такой соли, которая имеет подходящие и полезные физические свойства. Кроме того, в качестве дополнительного независимого отличительного признака настоящего изобретения, также предложена композиция, делающая возможным поглощение данного фармакологически активного соединения (I) в желательной степени.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг.1 представляет собой диаграмму дифракции рентгеновских лучей на порошке (XRDP) формы А тозилата соединения (I). Ось Х показывает значение 2-тета, и ось Y - интенсивность.
Фиг.2 представляет собой кривую дифференциальной сканирующей калориметрии (DSC) (сплошная линия) и кривую термогравиметрического анализа (TGA) (пунктирная линия) формы А тозилата соединения (I). Ось Х показывает температуру (°С), и ось Y - тепловой поток (Ватт/г) (DSC) и % массы образца (TGA).
На Фиг.3 показан профиль растворения таблеток, полученных в Примере 14 (соответствующих концентрации 30 мг соединения (I)); композиции в форме таблетки, содержащей форму А тозилата соединения (I) и микрокристаллическую целлюлозу (точки данных в форме квадратов); и композиции в форме таблетки, содержащей форму А тозилата соединения (I) и изомальт (точки данных в форме ромбов). Растворение измеряли при рН 6,8, как описано в Примере 14. Ось Х показывает время (часы), ось Y показывает % растворенного соединения (I) (как % заявленного в стандартной документации показателя (% LC)).
На Фиг.4 показана концентрация в крови (нМ) у собаки после введения формы А тозилата соединения (I) (эквивалентно 1,0 мг/кг соединения (I) в форме свободного основания) в желатиновой капсуле и соединения (I) (0,8 мг/кг) в форме свободного основания, введенного в водной суспензии. Ось Х показывает время (часы), ось Y показывает концентрацию в крови (нМ) у собаки.
На Фиг.5 показаны профили растворения таблетки, покрытой пленкой, содержащей форму А тозилата соединения (I) (эквивалентно 30 мг соединения (I) в форме свободного основания), описанную в Примере 10 (точки данных в форме квадратов), и кристаллическую форму А тозилата соединения (I) (эквивалентно 30 мг соединения (I) в форме свободного основания) в капсуле (точки данных в форме ромбов). Растворение измеряли в 900 мл 0,1 М HCl (рН 1), как описано в Примере 10. Ось Х показывает время (минуты), ось Y показывает % растворенного соединения (I).
На Фиг.6 показан профиль растворения композиций в форме таблетки А и Б (активный ингредиент, эквивалентный 30 мг соединения (I) в форме основания) согласно Таблице 7 (Пример 13). Композиция в форме таблетки А, содержащая 5% двухосновного фосфата кальция, представлена точками данных в форме квадратов, а композиция в форме таблетки Б (0% двухосновного фосфата кальция) представлена точками данных в форме ромбов. Растворение измеряли в 900 мл 0,1 М HCl (рН 1), как описано в Примере 13. Ось Х показывает время (минуты), ось Y показывает % растворенного соединения (I) (как % заявленного в стандартной документации показателя (% LC)).
Фиг.7 представляет собой диаграмму дифракции рентгеновских лучей на порошке формы Б тозилата соединения (I). Ось Х показывает значение 2-тета, и ось Y - интенсивность.
На Фиг.8 показана диаграмма дифракции рентгеновских лучей на порошке формы А 2,5-диметилбензолсульфоната соединения (I). Ось Х показывает значение 2-тета, и ось Y - интенсивность.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы изобретения неожиданно обнаружили, что тозилатная (4-метилбензолсульфонатная) соль 6-метил-5-(1-метил-1Н-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида (ниже - тозилат соединения (I)) обладает значительно улучшенными физическими свойствами в твердом состоянии по сравнению со свойствами исходного соединения (I) в форме свободного основания.
На соединении (I) провели эксперимент по тщательному скринингу солей. Он позволил установить, что тозилат соединения (I) имеет свойства твердого состояния, подходящие для обеспечения его представления в форме таблеток.
Кроме того, тозилат соединения (I) также обладает дополнительными полезными свойствами, включая высокую кратковременную растворимость и высокую скорость собственного растворения.
Было получено и протестировано несколько солей соединения (I) с сильными органическими и неорганическими кислотами, как описано ниже.
| Таблица 1 | ||
| Соль соединения (I) | Твердая форма | Растворимость (мг/мл) |
| Тозилат | Кристаллическая | 1,2 |
| пара-Ксилол-2-сульфонат | Кристаллическая | 1,3 |
| Хлорид | Аморфная | 0,047 |
| Мезилат | Кристаллическая | 0,43 |
| Эзилат | Кристаллическая | 0,096 |
| 1,5-Нафталиндисульфонат | Аморфная | не тестировали |
| Сульфат | Аморфная | не тестировали |
| Соединение (I) в форме свободного основания | Кристаллическая | 0,040 |
Пара-Ксилол-2-сульфонат в Таблице 1 представляет собой 2,5-диметилбензолсульфонатную соль соединения (I).
Растворимость (мг/мл), указанную в Таблице 1, измеряли через 1 час в 900 мл 0,1 М HCl при 75 об./мин и 37°С с использованием системы Zymark Multidose G3. Анализ проводили УФ спектрофотометром с длиной волны детекции 337 нм.
Высокая кратковременная растворимость и быстрое растворение тозилата соединения (I) свидетельствуют о том, что можно ожидать улучшенную биодоступность в тех дозах, в которых соединение (I) в форме свободного основания испытывало бы ограничение его поглощения растворимостью. Повышенную биодоступность тозилата соединения (I) продемонстрировали у собаки, где биодоступность формы А тозилата соединения (I), введенного в капсуле, была приблизительно в 3 раза выше, чем биодоступность, наблюдаемая для соответствующего свободного основания соединения (I), представленного в виде кристаллической суспензии (смотрите Пример по биодоступности и Фиг.4).
Следовательно, ожидается, что тозилат соединения (I) улучшит растворимость в воде соединения (I) в течение периода времени, достаточного для обеспечения повышенного поглощения у человека. Не ограничиваясь теорией, повышенная растворимость тозилата соединения (I) может возникать из комбинации более высокой истинной растворимости тозилата соединения (I) и длительной высокой растворимости в водных средах, когда соединение (I) выпадает в осадок из раствора в виде аморфного вещества. Наблюдаемая улучшенная растворимость, следовательно, может отражать как растворимость аморфного вещества, так и растворимость тозилата соединения (I), которые будут присутствовать in vivo в разных соотношениях после перорального введения тозилата соединения (I) в результате кинетического баланса между растворением и выпадением в осадок соединения (I). Таблица 2 показывает растворимость тозилата соединения (I) в разных растворяющих средах с течением времени. В Таблице 2 колонки, обозначенные «модификация», относятся к форме твердого вещества, присутствующего в данной растворяющей среде в указанный релевантный момент времени. Данные в Таблице 2 свидетельствуют о том, что растворимость остается высокой в течение по меньшей мере 3 часов, особенно при низком рН, показательном для рН, обнаруженного в желудке. Данный период времени 3 часа представляет собой временной интервал, релевантный для поглощения из ЖК (желудочно-кишечного) тракта у человека, хотя на протяжении более длительного периода времени данное вещество в конечном счете выкристаллизовывается после диссоциации в виде кристаллического свободного основания исходного соединения (I), и это объясняет значительно более низкую растворимость, наблюдаемую через 24 часа.
| Таблица 2 | ||||||
| Растворитель | Растворимость 1 ч (мкМ) | Модификация | Растворимость 3 ч (мкМ) | Модификация | Растворимость 24 ч (мкМ) | Модификация |
| 0,1 М HCl рН 1.0 | 1531±129 | Некоторое количество соли, главным образом аморфное (I) | 1098±145 | Следы соли, главным образом аморфное (I) | 58,4±1,2 | Аморфное (I) и исходное кристаллическое (I) |
| 0,2 М фосфатный буфер рН 3,0 | 493±97 | Аморфное (I) | 492±115 | Небольшие следы исходного кристаллического (I) | 11,8±0,9 | Исходное кристаллическое (I) |
| 0,2 М фосфатный буфер рН 5,0 | 490±42 | Аморфное (I) | 460±54 | Аморфное (I) | 12,2±0,6 | Исходное кристаллическое (I) |
| 0,2 М фосфатный буфер рН 6,5 | 416±48 | Аморфное (I) | 363±86 | Аморфное (I) | 10,1±0,8 | Исходное кристаллическое (I) |
| 0,2 М фосфатный буфер рН 8 | 412±29 | Аморфное (I) | 240±35 | Аморфное (I) | 8,4±0,7 | Исходное кристаллическое (I) |
Другие аспекты данного изобретения направлены на фармацевтические композиции, содержащие тозилат соединения (I), и на применения данной соли. Эти аспекты данного изобретения более подробно описаны ниже.
4-Метилбензолсульфонат 6-метил-5-(1-метил-1Н-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида может быть получен в виде стабильного безводного кристаллического твердого вещества, имеющего превосходные свойства в твердом состоянии.
Согласно первому аспекту данного изобретения предложен 4-метилбензолсульфонат 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида (тозилат соединения (I)).
Подходящим образом, тозилат соединения (I) является кристаллическим.
В одном воплощении согласно данному изобретению предложена кристаллическая форма, которая представляет собой 4-метилбензолсульфонат 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]-метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида, обозначенный как «форма А тозилата соединения (I)».
Форма А тозилата соединения (I) дает картину дифракции рентгеновских лучей на порошке по существу такую, как показано на Фиг.1. Наиболее значимые пики формы А тозилата соединения (I), измеренные с использованием CuKα излучения, показаны в Таблице 3.
| Таблица 3 | |
| Угол 2-тета° (2θ) | Угол 2-тета° (2θ) |
| 5,1 | 16,8 |
| 7,3 | 17,0 |
| 8,4 | 17,8 |
| 8,9 | 20,6 |
| 12,6 | 21,9 |
| 12,9 |
В одном воплощении предложена форма А тозилата соединения (I), где указанная форма А имеет картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, с по меньшей мере одним специфическим пиком при 2θ примерно 5,1; 7,3; 8,9; 17,0 или 17,8°.
В другом воплощении предложена форма А тозилата соединения (I), где указанная форма А имеет картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, со специфическими пиками при 2θ примерно 5,1; 7,3; 8,9; 17,0 и 17,8°.
В другом воплощении предложена форма А тозилата соединения (I), где указанная форма А имеет картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, с по меньшей мере одним специфическим пиком при 2θ примерно 5,1; 7,3; 8,9; 12,9; 16,8; 17,0; 17,8 или 21,9°.
В другом воплощении предложена форма А тозилата соединения (I), где указанная форма А имеет картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, со специфическими пиками при 2θ примерно 5,1; 7,3; 8,9; 12,9; 16,8; 17,0; 17,8 и 21,9°.
В другом воплощении согласно данному изобретению предложена форма А тозилата соединения (I), характеризующаяся картиной дифракции рентгеновских лучей на порошке, измеренной с использованием CuKα излучения, по существу такой, как показано на Фиг.1.
В другом воплощении согласно данному изобретению предложена форма А тозилата соединения (I), характеризующаяся кривой дифференциальной сканирующей калориметрии (DSC) по существу такой, как показано на Фиг.2.
Кристаллические формы тозилата соединения (I) согласно данному изобретению предпочтительно являются по существу чистыми, что означает, что данная кристаллическая форма соединения формулы (I) включает меньше чем 10%, предпочтительно меньше чем 5%, более предпочтительно меньше чем 3%, еще более предпочтительно меньше чем 1% по массе примесей, включая другие кристаллические формы данного соединения.
Таким образом, в одном воплощении согласно данному изобретению предложена по существу чистая форма А тозилата соединения (I), характеризующаяся картиной дифракции рентгеновских лучей на порошке, измеренной с использованием CuKα излучения, содержащей специфические пики при 2θ примерно 5,1; 7,3; 8,9; 17,0 и 17,8°.
В другом воплощении согласно данному изобретению предложена по существу чистая форма А тозилата соединения (I), характеризующаяся картиной дифракции рентгеновских лучей на порошке, измеренной с использованием CuKα излучения, содержащей специфические пики при 2θ примерно 5,1; 7,3; 8,9; 12,9; 16,8; 17,0; 17,8 и 21,9°.
В другом воплощении согласно данному изобретению предложена по существу чистая форма А тозилата соединения (I), характеризующаяся картиной дифракции рентгеновских лучей на порошке, измеренной с использованием CuKα излучения, по существу такой, как показано на Фиг.1.
Форму А тозилата соединения (I) получается в виде беловатого кристаллического порошка, содержащего кристаллы, обычно демонстрирующие игловидную морфологию. Данное вещество является высококристаллическим, как определено измерениями дифракции рентгеновских лучей на порошке.
Кристаллическую структуру формы А тозилата соединения (I) определяли дифракцией рентгеновских лучей на монокристалле. В таком кристалле молекулы упакованы в моноклинную пространственную группу (P21/n). В данной асимметричной элементарной ячейке присутствуют 4 молекулы (а=5,10 Å, b=30,01 Å, с=21,05 Å). Тесная упаковка, приводящая к недостатку внутреннего пространства, проявляется в относительно высокой плотности, 1,48 г/мл.
Симулированная картина дифракции рентгеновских лучей на порошке формы А тозилата соединения (I), рассчитанная с использованием данных по дифракции рентгеновских лучей на монокристалле, хорошо согласуется с экспериментально определенной картиной, показанной на Фиг.1. Положения пиков дифракции имеют очень близкое соответствие, а различия в относительных интенсивностях пиков приписываются к эффектам предпочтительной ориентации.
При нагревании форма А демонстрирует начало плавления/разложения при примерно 237°С. Значительной потери массы не наблюдали вплоть до 200°С, но значительная потеря массы из-за разложения начиналась при температуре, близкой к температуре плавления (Фиг.2). Таким образом, форма А является термостабильной при фармацевтически релевантных температурах.
Измерения сорбции влаги с использованием гравиметрической сорбции пара (GVS) показали, что форма А тозилата соединения (I) имеет очень низкое влагопоглощение - примерно 0,2% при относительной влажности (RH) 80%. Форма А тозилата соединения (I), как таковая, находится прямо на границе между слабогигроскопичной и негигроскопичной согласно критериям, определенным в Европейской фармакопее.
Форма А тозилата соединения (I) имеет превосходные и весьма полезные свойства в твердом состоянии. Она является кристаллической, от негигроскопичной до слабогигроскопичной и термостабильной до 200°С, не демонстрирующей ни потери растворителя, ни какого-либо другого теплового события до плавления (смотрите кривые DSC и TGA, Фиг.2).
Стабильность формы А тозилата соединения (I) в твердом состоянии исследовали при четырех совокупностях условий: при 25°С/осушение; при 25°С/60%-ная относительная влажность (RH); 40°С/75%-ная RH и 60°С/75%-ная RH. Образцы исследовали (LC (жидкостная хроматография) и XRPD) через 4, 8 и 12 недель, и оценивали химическую и физическую стабильность. За исключением некоторой потенциальной химической деградации при стрессовых условиях - 60°С/75%-ная RH, не наблюдали значимых химических или физических изменений при любом протестированном условии или в любой момент времени. Было сделано заключение, что форма А тозилата соединения (I) обладает превосходной и благоприятной химической и физической стабильностью в твердом состоянии при фармацевтически релевантных условиях хранения.
Стехиометрия формы А тозилата соединения (I) представляет собой 1:1 соединение (I) к тозилату. Стехиометрию данной соли можно определить с использованием известных способов, например, 1H ЯМР.
Авторы данного изобретения также обнаружили другую кристаллическую форму тозилата соединения (I), названную ниже форма Б тозилата соединения (I). Форма Б тозилата соединения (I) дает картину дифракции рентгеновских лучей на порошке по существу такую, как показано на Фиг.7. Форма Б тозилата соединения (I) может быть получена, как описано в Примерах.
Также обнаружили, что 2,5-диметилбензолсульфонат соединения (I) является кристаллическим и обладает благоприятными характеристиками растворения по сравнению с соединением (I) в форме свободного основания. 2,5-диметилбензолсульфонат соединения (I) представляет собой соль, образованную между соединением (I) и 2,5-диметилбензолсульфоновой кислотой (пара-ксилол-2-сульфоновая кислота).
Соответственно, в качестве дополнительного признака настоящего изобретения предложена форма А 2,5-диметилбензолсульфоната 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)фенил]-1,2-дигидропиридин-3-карбоксамида (ниже - форма А 2,5-диметилбензолсульфоната соединения (I)).
Форма А 2,5-диметилбензолсульфоната соединения (I) является кристаллической и дает картину дифракции рентгеновских лучей на порошке по существу такую, как показано на Фиг.8.
В одном воплощении предложена форма А 2,5-диметилбензолсульфоната соединения (I), имеющая картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, с по меньшей мере одним специфическим пиком при 2θ примерно 9,7; 22,8 или 22,4°.
В другом воплощении предложена форма А 2,5-диметилбензолсульфоната соединения (I), имеющая картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, с по меньшей мере одним специфическим пиком при 2θ примерно 4,8; 9,7; 15,1; 15,3; 19,1; 19,4; 19,9; 22,8 или 24,2°.
В одном воплощении предложена форма А 2,5-диметилбензолсульфоната соединения (I), имеющая картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, со специфическими пиками при 2θ примерно 9,7; 22,8 и 22,4°.
В другом воплощении предложена форма А 2,5-диметилбензолсульфоната соединения (I), имеющая картину дифракции рентгеновских лучей на порошке, измеренную с использованием CuKα излучения, со специфическими пиками при 2θ примерно 4,8; 9,7; 15,1; 15,3; 19,1; 19,4; 19,9; 22,8 и 24,2°.
В другом воплощении предложена форма А 2,5-диметилбензолсульфоната соединения (I), характеризующаяся картиной XRPD, измеренной с использованием CuKα излучения, по существу такой, как картина дифракции, показанная на Фиг.8.
Форма А 2,5-диметилбензолсульфоната соединения (I) может быть получена кристаллизацией из подходящего растворителя, такого как ацетонитрил, с использованием способов, аналогичных способам, описанным здесь в Примерах.
Когда делается ссылка на то, что соли соединения (I) являются кристаллическими, такие как форма А тозилата соединения (I) и форма А 2,5-диметилбензолсульфоната соединения (I), степень кристалличности, определенная по данным дифракции рентгеновских лучей на порошке, подходящим образом является, например, большей чем примерно 60%, как, например, большей чем примерно 80%, в частности большей чем примерно 90%, более конкретно - большей, чем примерно 95%. В воплощениях данного изобретения степень кристалличности, определенная по данным дифракции рентгеновских лучей на порошке, является большей чем примерно 98%, где данный % кристалличности относится к % по массе от общей массы образца, который является кристаллическим.
В предыдущих абзацах, определяющих пики дифракции рентгеновских лучей на порошке для следующих кристаллических форм: формы А тозилата соединения (I) и формы А 2,5-диметилбензолсульфоната соединения (I), термин «примерно» используется в выражении «… при 2θ примерно…» для того, чтобы указать, что точное положение пиков (т.е. перечисленных значений угла 2-тета) не должно истолковываться как абсолютные значения, потому что, как будет понятно специалистам в данной области, точное положение пиков может слегка варьировать между одним измерительным прибором и другим, от одного образца к другому или в результате небольших изменений в использованных условиях измерения. В предыдущих абзацах также утверждается, что форма А тозилата соединения (I) дает картины дифракции рентгеновских лучей на порошке «по существу» такие же, что и картины дифракции рентгеновских лучей на порошке, показанные на Фиг.1, и имеет по существу наиболее значительные пики (значения угла 2-тета), показанные в Таблице 3. Следует понимать, что также подразумевается, что использование термина «по существу» в этом контексте указывает на то, что значения угла 2-тета картин дифракции рентгеновских лучей на порошке могут слегка варьировать от одного прибора к другому, от одного образца к другому или в результате небольших вариаций использованных условий измерения, так что положения пиков, показанные на Фиг. или процитированные в Таблицах, вновь не следует истолковывать как абсолютные значения.
В этом отношении в данной области известно, что может быть получена картина дифракции рентгеновских лучей на порошке, которая имеет одну или более чем одну ошибку измерения в зависимости от условий измерения (таких как использованные оборудование или установка). В частности, хорошо известно, что интенсивности на картине дифракции рентгеновских лучей на порошке могут колебаться в зависимости от условий измерения и приготовления образца. Например, специалисты в области дифракции рентгеновских лучей на порошке понимают, что на относительную интенсивность пиков могут влиять, например, зерна, имеющие размер более 30 микрон, и неунитарные соотношения размеров, которые могут влиять на анализ образцов. Квалифицированный специалист также поймет, что на положение отражений может влиять точная высота, на которой находится образец в дифрактометре, и калибровка нуля данного дифрактометра. Небольшой эффект также может иметь планарность поверхности данного образца. Следовательно, специалист в данной области поймет, что данные картины дифракции, представленные здесь, не следует истолковывать как абсолютные (для дополнительной информации смотрите Jenkins, R & Snyder, R.L. 'Introduction to X-Ray Powder Diffractometry' John Wiley & Sons, 1996). Следовательно, следует понимать, что описанные здесь кристаллические формы тозилата соединения (I) не ограничиваются кристаллами, которые дают картины дифракции рентгеновских лучей на порошке, идентичные картине дифракции рентгеновских лучей на порошке, показанной на Фиг.1, и что любые кристаллы, дающие картины дифракции рентгеновских лучей на порошке, по существу такие же, что и картины дифракции, показанные на Фиг.1, попадают в объем настоящего изобретения. Специалист в области дифракции рентгеновских лучей на порошке способен судить о существенной идентичности картин дифракции рентгеновских лучей на порошке.
Обычно ошибка измерения угла дифракции на дифрактограмме рентгеновских лучей на порошке составляет примерно 2-тета=0,5° или менее, и такой уровень ошибки измерения следует принимать во внимание при рассмотрении картин дифракции рентгеновских лучей на порошке на Фиг.1 и при интерпретации положений пиков, на которые дается ссылка в приведенном выше тексте и в Таблице 3.
Описанные здесь температуры плавления и данные DSC более подробно описаны ниже. Специалист в данной области поймет, что небольшие вариации в температуре плавления, измеренной посредством DSC, могут происходить в результате вариаций чистоты образца, приготовления образца и условий измерения (например, скорости нагревания). Будет понятно, что альтернативные показания температуры плавления могут быть даны другими типами оборудования или при применении условий, отличных от условий, описанных ниже. Следовательно, процитированные здесь температура плавления и графические материалы, иллюстрирующие эндотермы, не следует принимать как абсолютные значения, и такие ошибки измерения следует принимать во внимание при интерпретации данных DSC. Типично температуры плавления могут варьировать на ±5°С или менее.
Кристаллические формы тозилата соединения (I) согласно данному изобретению также можно охарактеризовать и/или отличить от других физических форм с использованием других подходящих аналитических методик, например, спектроскопии в ближней инфракрасной области (NIR) или спектроскопии твердофазного ядерного магнитного резонанса.
Химическую структуру тозилата соединения (I) по настоящему изобретению можно подтвердить традиционными способами, например, посредством анализа методом протонного ядерного магнитного резонанса (ЯМР).
В контексте настоящего изобретения описанные здесь соли соединения (I) включают кристаллическое вещество, в котором соединение (I) и кислота (например 4-метилбензолсульфоновая кислота) являются ионизированными или, альтернативно, где оба компонента задействуют значительные межмолекулярные взаимодействия, такие как связывание водородными связями, для объединения и получения однородного кристаллического вещества (сокристалл). Следует понимать, что соль согласно данному изобретению может быть частично ионной и частично сокристаллической.
Получение формы А тозилата соединения (I)
Форму А тозилата соединения (I) воспроизводимо получают в результате кристаллизации 4-метилбензолсульфоната 6-метил-5-(1-метил-1H-пиразол-5-ил)-N-{[5-(метилсульфонил)пиридин-2-ил]метил}-2-оксо-1-[3-(трифторметил)-фенил]-1,2-дигидропиридин-3-карбоксамида из ацетонитрила. Форму А тозилата соединения (I) также можно кристаллизовать из тетрагидрофурана, циклогексанона, бутан-1-ола, бутиронитрила, метилизобутилкетона, метилэтилкетона или ацетона.
С использованием раскрытых здесь методик форму А тозилата соединения (I) можно воспроизводимо производить, следуя синтезу в малом, промежуточном или большом масштабе.
В дополнительном аспекте согласно настоящему изобретению предложены способы получения формы А тозилата соединения (I).
Так, в одном аспекте согласно данному изобретению предложен способ получения формы А тозилата соединения (I), включающий кристаллизацию или перекристаллизацию из растворителя, выбранного из ацетонитрила, тетрагидрофурана, циклогексанона, бутан-1-ола, бутиронитрила, метилизобутилкетона, метилэтилкетона и ацетона. В другом аспекте согласно данному изобретению предложен способ получения формы А тозилата соединения (I), включающий кристаллизацию или перекристаллизацию из ацетонитрила, тетрагидрофурана или ацетона. В другом аспекте согласно данному изобретению предложен способ получения формы А тозилата соединения (I), включающий кристаллизацию или перекристаллизацию из ацетонитрила.
Кристаллизацию или перекристаллизацию формы А тозилата соединения (I) можно проводить путем получения пересыщенного раствора тозилата соединения (I) из растворителя. Пересыщенности можно добиваться, например, концентрированием данного раствора путем удаления растворителя, охлаждением данного раствора или добавлением подходящего антирастворителя. При инициации кристаллизации концентрированием раствора растворитель можно удалять с использованием хорошо известных способов, таких как выпаривание или перегонка. Кристаллизацию или перекристаллизацию также можно стимулировать внесением затравки кристаллов формы А тозилата соединения (I) в данный раствор.
Тозилатную соль соединения (I) с удобством получают in situ путем осуществления взаимодействия пара-толуолсульфоновой кислоты с раствором соединения (I) в одном из вышеупомянутых растворителей. Молярное соотношение соединения (I) и пара-толуолсульфоновой кислоты соответствующим образом составляет примерно 1:1. После взаимодействия с пара-толуолсульфоновой кислотой форму А тозилата соединения (I) перекристаллизовывают из системы растворителей, как здесь описано.
При перекристаллизации формы А тозилата соединения (I) из одного из приведенных выше растворителей форму А тозилата соединения (I) растворяют в данном растворителе и затем кристаллизуют из раствора, как здесь описано. Перекристаллизация может быть полезной для очистки данной соли, повышения степени кристалличности или улучшения морфологии кристаллов формы А тозилата соединения (I).
В другом аспекте согласно данному изобретению предложен способ получения формы А тозилата соединения (I), включающий следующие стадии:
1) нагревание соединения (I) в ацетонитриле с получением раствора;
2) добавление пара-толуолсульфоновой кислоты к раствору со стадии (1);
3) охлаждение данной реакционной смеси для осуществления кристаллизации; и
4) сбор и сушка формы А тозилата соединения (I).
Как будет понятно, стадия (1) данного способа дает раствор соединения (I) в ацетонитриле. Данный раствор можно получать растворением любой формы соединения (I) в ацетонитриле. Например, исходная форма соединения (I) в форме свободного основания может быть кристаллической, полукристаллической или аморфной. Соединение (I) легко растворяют в ацетонитриле путем нагревания данной смеси. Например, смесь со стадии (1) нагревают до температуры примерно 50°С или выше, например, от примерно 50°С до температуры флегмообразования, предпочтительно от 50°С до примерно 80°С, более предпочтительно до примерно 80°С.
На стадии (2) к данному раствору может быть добавлена пара-толуолсульфоновая кислота в любой удобной форме, например в виде твердого вещества или, предпочтительно, в виде раствора, пара-толуолсульфоновую кислоту можно использовать в безводной форме или в виде моногидрата. Предпочтительно пара-толуолсульфоновую кислоту добавляют к раствору со стадии (1) в виде раствора кислоты в ацетонитриле. При использовании раствора кислоты в ацетонитриле его можно добавлять в раствор со стадии (1) при температуре окружающей среды или в виде горячего раствора. Если к раствору со стадии (1) добавляют горячий раствор кислоты, раствор данной кислоты может находиться при температуре, аналогичной температуре, использованной на стадии (1), например от 50°С до примерно 80°С. Предпочтительно раствор пара-толуолсульфоновой кислоты в ацетонитриле находится при температуре окружающей среды, когда его добавляют к раствору со стадии (1). Молярное соотношение соединения (I) и пара-толуолсульфоновой кислоты составляет примерно 1:1. После добавления пара-толуолсульфоновой кислоты реакционной смеси дают постоять, обычно с перемешиванием для обеспечения взаимодействия кислоты с соединением (I). Пара-толуолсульфоновую кислоту можно добавлять к раствору соединения (I). Однако раствор соединения (I) также может быть добавлен к пара-толуолсульфоновой кислоте.
На стадии (3) реакционную смесь охлаждают для осуществления кристаллизации тозилата соединения (I). Предпочтительно реакционную смесь охлаждают до примерно 20°С или ниже. В одном воплощении реакционную смесь на стадии (3) охлаждают до примерно 5°С. В одном воплощении данного способа реакционную смесь охлаждают до примерно 5°С и затем вновь нагревают до примерно 80°С, данное охлаждение и повторное нагревание можно повторять много раз, например, можно провести 1, 2, 3 или 4 цикла охлаждения и повторного нагревания перед конечным охлаждением и кристаллизацией формы А тозилата соединения (I). Периодическое изменение температуры может улучшать физическую форму кристаллического вещества и улучшать, например, свойства при переработке формы А тозилата соединения (I) на протяжении последующей переработки. Например, последующее приготовление в виде фармацевтически приемлемой композиции, такой как таблетка или капсула.
На стадии (4) данного способа форму А тозилата соединения (I) можно собирать традиционными способами, например фильтрованием. После сбора форму А тозилата соединения (I) возможно промывают ацетонитрилом и ее можно высушить. Предпочтительно форму А тозилата соединения (I) сушат под вакуумом при температуре примерно 50°С.
Форму А тозилата соединения (I) подходящим образом размалывают перед приготовлением в виде препарата. Размол может проводиться традиционными способами, например путем мокрого измельчения, с получением воспроизводимой физической формы и размера частиц до дальнейшей переработки формы А тозилата соединения (I). Предпочтительно форму А тозилата соединения (I) подвергают мокрому измельчению in situ после кристаллизации на стадии (3) данного способа. Такое мокрое измельчение можно осуществлять, например, используя встроенную в производственную линию роторно-статорную мельницу.
В дополнительном аспекте согласно настоящему изобретению предложен тозилат соединения (I) или его форма, описанная здесь, для применения в терапии.
В дополнительном аспекте согласно настоящему изобретению предложен тозилат соединения (I) или его форма, описанная здесь, для применения в изготовлении лекарственного средства для лечения или профилактики заболеваний или состояний, при которых ингибирование активности нейтрофильной эластазы является полезным.
В дополнительном аспекте согласно настоящему изобретению предложен способ лечения или профилактики заболевания или состояния, опосредованного активностью ней