Способ получения гидрохлорида этиламида l-пролина
Иллюстрации
Показать всеИзобретение относится к способу получения гидрохлорида этиламида L-пролина формулы I
Способ включает суспендирование L-пролина в пиридине, добавление при 0-100С и перемешивание дихлордиметилсилана в мольном соотношении к L-пролину 1,1-1,2:1, последующее перемешивание реакционной смеси при комнатной температуре, введение в реакционную смесь при охлаждении до 0-70С этиламина и перемешивание смеси при комнатной температуре, упаривание реакционной смеси в вакууме, добавление к образовавшемуся маслообразному осадку водного раствора карбоната натрия до рН 7,8-8,0 и смеси диэтилового эфира с петролейным эфиром в соотношении их 1:1, последующее отделение водного слоя, упаривание остатка в вакууме, перевод образовавшегося этиламида L-пролина в хлористоводородную соль обработкой соляной кислотой. Способ позволяет получать целевой продукт в одну стадию. 2 примера.
Реферат
Изобретение относится к получению химических соединений, касается получения производных аминокислот и конкретно относится к получению производных пролина, а именно к получению гидрохлорида этиламида L-пролина, являющегося исходным веществом для синтеза биологически активных пептидов, и может быть использовано в фармацевтической промышленности (фармацевтической химии).
Общеизвестно, что пролин (пирролидин-α-карбоновая кислота) -гетероциклическая аминокислота, существует в двух оптически изомерных формах - L и D, а также в виде рацемата; L-пролин одна из 20-и протеиногенных аминокислот. Известно, что этиламид L-пролина является важным промежуточным соединением (промежуточным полупродуктом) при синтезе некоторых биологически активных пептидов, являющихся фармацевтическими субстанциями, в частности при получении бусерелина (CN 101735308, 2010[1]; RU 2442791, 20.02.2012), лейпрорелина (WO 2007059921, 2007[2]; RU 2043362, 10.09.1995) - синтетических аналогов гонадотропин-рилизинг гормона (ГнРГ), а также других продуктов пептидного синтеза.
Известно, что традиционный синтез этиламида L-пролина основан на постановке защитной группы по атому азота L-пролина, последующего амидирования защищенного L-пролина и снятия защитной группы. Таким образом процесс получения целевого соединения включает 3 стадии. В качестве защитной группы обычно используют бензилоксикарбонильную (Z) (SU 1028663, 15.07.1983; RU 2442791, 20.02.2012; Collect. Czech. Chem. Commun. V. 52, №12, p. 3034, 1987 (3) или трет - бутилоксикарбонильную (Воc) (US 20080108632, 2008(4); RU 2084458, 20.07.1997).
При использовании Z-защиты [3] вначале получают Z-L-пролин реакцией L-пролина и бензилхлорформиата, который с использованием этилхлорформиата и этиламина затем переводят в этиламид Z-L-пролин и наконец деблокируют раствором бромоводорода в уксусной кислоте до целевого соединения. По другому варианту деблокирование может быть выполнено гидрированием этиламида Z-L-пролина на палладиевом катализаторе (Pd-C) [5].
В случае использования Boc-защиты из L-пролина и трет-бутилпирокарбоната получают Boc-L-пролин [6], конденсация которого с этиламином приводит к этиламиду Boc-L-пролина и далее деблокирование раствором хлороводорода в диоксане дает целевое соединение [4].
Таким образом, исходя из известных методов синтеза этиламида L-пролина, существенную роль при его получении имеют не только трудозатраты на 3-х стадийный синтез, но и стоимость реагентов постановки и снятия защитных групп.
Технической задачей данного изобретения является упрощение процесса получения производного пролина - этиламида L-пролина, за счет исключения реагентов на постановку и снятие защитных групп, а также разработка легко масштабируемого способа производства гидрохлорида этиламида L-пролина.
Поставленная техническая задача и достигаемый технический результат обеспечиваются способом получения гидрохлорида этиламида L-пролина, включающим суспендирование L-пролина в пиридине, добавление при 0-10°C и перемешивании дихлордиметилсилана (в мольном отношении к L-пролину 1,1-1,2:1), последующее перемешивание реакционной смеси при комнатной температуре, введение в реакционную смесь при охлаждении до 0-7°C этиламина и перемешивание смеси при комнатной температуре, упаривание реакционной смеси в вакууме, добавление к образовавшемуся маслообразному осадку водного раствора карбоната натрия до pH 7,8-8,0 и смеси диэтилового эфира с петролейным эфиром в соотношении их 1:1, последующее отделение водного слоя, упаривание остатка в вакууме, перевод образовавшегося этиламида L-пролина в хлористоводородную соль добавлением к полученному остатку (при охлаждении до 5-10°C) соляной кислоты до pH 2,0-2,3, отделение неорганических солей при помощи изопропилового спирта, кристаллизацию его, фильтрование и сушку в вакууме с выделением (получением) кристаллического целевого продукта.
При осуществлении заявленного способа используют 4,5-5,5%-ный раствор карбоната натрия, добавляемый до достижения pH ~ 7,8-8,0; соляную кислоту используют с концентрацией около 17% (16,5-17,5%-ную), добавляемую до достижения pH 2,0-2,3.
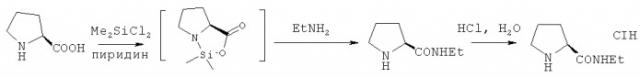
Итак, поставленная задача достигается заявленным способом, который заключается в том, что полученный из L-пролина и дихлордиметилсилана в пиридине циклический нестабильный кремнийсодержащий интермедиат без выделения из реакционной массы обрабатывают этиламином, с последующим переводом образующегося этиламида L-пролина в хлористоводородную соль обработкой соляной кислотой:
Таким образом, процесс получения целевого соединения сокращается до одной стадии, при этом не используются блокирующие и деблокирующие реагенты. Кроме того, показано, что данный способ является легко масштабируемым - выход гидрохлорида этиламида L-пролина существенно не меняется с увеличением загрузок исходных реагентов.
Чистота полученного гидрохлорида этиламида L-пролина подтверждена ВЭЖХ и ПМР спектроскопией. Аналитическую ВЭЖХ проводили на хроматографе фирмы Shimadzu. Колонка: Grom-Sil 12J ODS-4HE, 5мкм, 250·4,6 мм. Условия: градиент 20%В (0 мин), 60%В (10 мин), 70%В (15 мин), 70%В (30 мин). А - фосфатный буфер pH 3 (20,4 г KH2PO4 растворяли в 3 л дистиллированной воды и доводили pH до 3 добавлением концентрированной фосфорной кислоты), В - ацетонитрил. Спектры ПМР получены на приборе Bruker АМ-360 (рабочая частота 360.13 МГц). В качестве растворителя применяли DMSO-d6, D2O.
Описываемый способ иллюстрируется следующими примерами.
Экспериментальная часть
Пример 1
Суспендируют 8.2 г (0.071 моль) L-пролина в 32 мл пиридина, охлаждают до -10°C при перемешивании приливают 10.6 г (0.081 моль) дихлордиметилсилана. Отогревают до комнатной температуры и перемешивают реакционную массу 1 ч. Охлаждают до 0°C и при этой температуре прикапывают 12.9 г (0.286 моль) этиламина. Оставляют отогреваться реакционную массу до комнатной температуры и перемешивают еще 1 ч. Упаривают реакционную массу в вакууме (45°C, 2 мм рт.ст.), к маслообразному остатку приливают 5% водный раствор карбоната натрия до pH 8 и 50 мл смеси диэтиловый эфир - петролейный эфир (1:1). Отделяют водный слой и упаривают его в вакууме (45°C, 2 мм рт.ст.), к остатку добавляют 17% соляную кислоту до pH 2 при охлаждении до 5-10°C и снова упаривают в вакууме досуха. Остаток растворяют в 20 мл изопропилового спирта, отделяют фильтрованием неорганические соли и удаляют растворитель в вакууме (45°C, 2 мм рт.ст.). Полученное масло растирают до кристаллизации с диэтиловым эфиром (3 раза по 25 мл), фильтруют и сушат в вакууме до постоянного веса (45°C, 2 мм рт.ст.). Получают 10.3 г (81%) белого кристаллического гидрохлорида этиламида L-пролина. Содержание основного вещества 98.6% (ВЭЖХ). Т.пл. 96-98°C.[α]D 25=-52.15 (5% р-р, вода). Спектр ЯМР 1H (d6-DMSO, δ, м.д.): 1.04 (t, 3Н, СН 3), 1.72-1.89 (m, 3Н, γ-СН 2+1H-β-СН 2) 2.23-2.35 (m, 1Н, 1H-β-СН 2), 3.08-3.24 (m, 4Н, NCH 2+δ-CH 2), 4.12 (t, 1Н, α-СН), 8.81 (s, 1Н, CONH).
Пример 2
В реакторе на 10 л с механической мешалкой суспендируют 1150 г (10 моль) L-пролина в 4.4 л пиридина, поддерживая температуру 0-10°C при перемешивании прибавляют 1484 г (11.4 моль) дихлордиметилсилана. Отогревают до 20-22°C и перемешивают реакционную массу 1 ч при этой температуре. Снова охлаждают до 0°C и при температуре 0-7°C) приливают 1800 г (40 моль) этиламина. Перемешивают реакционную массу 30 мин при 10°C и 1 ч при 20-22°C. Отфильтровывают осадок гидрохлорида этиламина, промывают его на фильтре 3 л этилацетата. Объединенные жидкие фазы упаривают в вакууме (45°C, 2 мм рт.ст.), к маслообразному остатку приливают 3 л 5% водного раствора карбоната натрия (до pH 8) и 4 л смеси диэтиловый эфир - петролейный эфир (1:1). Отделяют водный слой, а органический дополнительно экстрагируют 0.7 л воды. Объединенные водные слои упаривают в вакууме (45°C, 2 мм рт.ст.), к остатку добавляют 2 л 17% соляной кислоты до pH 2 при охлаждении до 5-10°C и снова упаривают в вакууме досуха. Остаток растворяют в 3.5 л изопропилового спирта, отделяют фильтрованием неорганические соли и удаляют растворитель в вакууме (45°C, 2 мм рт.ст.). Полученное масло перемешивают до кристаллизации с диэтиловым эфиром (2 раза по 3 л), фильтруют и сушат в вакууме до постоянного веса (45°C, 2 мм рт.ст.). Получают 1394 г (78.3%) белого кристаллического гидрохлорида этиламида L-пролина. Содержание основного вещества 99.2% (ВЭЖХ). Т.пл. 98-100°C.[α]D 27=-52.44 (5% р-р, вода). Спектр ЯМР 1H (d6-DMSO, δ, м.д.): 1.04 (t, 3Н, СН 3), 1.72-1.89 (m, 3Н, γ-СН 2+1H-β-СН 2), 2.23-2.35 (m, 1Н, 1H-β-СH 2), 3.08-3.24 (m, 4Н, NCH 2+β-CH 2), 4.12 (t, 1Н, α-CH), 8.81 (s, 1H, CONH).
Как видно из вышеприведенных примеров, описанный способ отличается простотой, отсутствием блокирующих и деблокирующих реагентов и пригоден для получения целевого продукта с высоким выходом в полупромышленном масштабе.
Литература
1. Патент КНР CN 101735308, Method for liquid-phase synthesis of buserelin, 2010.
2. Международная заявка WO 2007059921, Solution-phase synthesis of leuprolide and its intermediates, 2007.
3. Collect.Czech.Chem.Commun. V.52, N12, p. 3034 (1987).
4. Патент США US 20080108632, Preparation of peptides as НСV protease inhibitors, 2008.
5. Polish J. Chem. V.69, N5, p.674 (1995).
6. Organic Lett. V.13, N2, p.216 (2011).
Способ получения гидрохлорида этиламида L-пролина, включающий суспендирование L-пролина в пиридине, добавление при 0-10°C и перемешивании дихлордиметилсилана (в мольном отношении к L-пролину 1,1-1,2:1), последующее перемешивание реакционной смеси при комнатной температуре, введение в реакционную смесь при охлаждении до 0-7°C этиламина и перемешивание смеси при комнатной температуре, упаривание реакционной смеси в вакууме, добавление к образовавшемуся маслообразному осадку водного раствора карбоната натрия до pH 7,8-8,0 и смеси диэтилового эфира с петролейным эфиром в соотношении их 1:1, последующее отделение водного слоя, упаривание остатка в вакууме, перевод образовавшегося этиламида L-пролина в хлористоводородную соль добавлением к полученному остатку (при охлаждении до 5-10°C) соляной кислоты до pH 2,0-2,3, отделение неорганических солей при помощи изопропилового спирта, кристаллизацию его, фильтрование и сушку в вакууме с выделением (получением) кристаллического целевого продукта.