Способ получения 3-арил -1,5,3-дитиазепанов
Иллюстрации
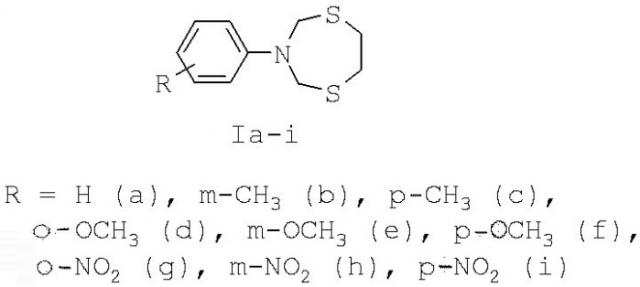
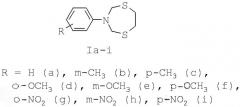
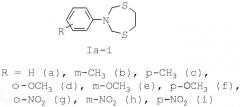
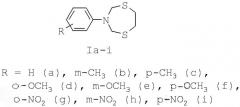
Показать всеИзобретение относится к области органической химии, в частности к способу получения 3-арил-1,5,3-дитиазепанов общей формулы (Ia-i), где R = H (a), m-CH3 (b), p-CH3 (c), o-OCH3 (d), m-OCH3 (e), p-OCH3 (f), o-NO2 (g), m-NO2 (h), p-NO2 (i), отличающемуся тем, что N,N-бис(метоксиметил)-N-ариламин (арил = фенил, m- и р-метилфенил, о-, m- и p-метоксифенил, о-, m- и p-нитрофенил) подвергают взаимодействию с 1,2-этандитиолом в присутствии катализатора CoCl2 в мольном соотношении N,N-бис(метоксиметил)-N-ариламин : 1,2-этандитиол : CoCl2=10:10:(0.3-0.7) при комнатной (~20°С) температуре и атмосферном давлении в хлороформе в качестве растворителя в течение 60-90 минут. Технический результат: разработан способ получения производных 3-арил-1,5,3-дитиазепанов, которые могут найти применение в качестве антибактериальных, антигрибковых и антивирусных агентов, в качестве биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах. 1 табл., 1 пр.
Реферат
Изобретение относится к области органической химии, в частности к способу получения 3-арил-1,5,3-дитиазепанов общей формулы (1):
Азот и серусодержащие гетероциклы известны как антибакториальные, антигрибковые и антивирусные агенты (Stillings M.R., Welbourn A.P., Walter D.J. Substituted 1,3,4-thiadiazoles with anticonvulsant activity // Med. Chem. 1986. 29. P.2280-2284. Kidwai M., Negi N., Chaudhary S.R. Cyclothiomethylation of arge hydrazines with formaldehyde // Acta Pharma. 1995. 45. P.511. Тюкавкина Н.А., Зурабян С.Э., Белобородов В.Л. и др. Органическая химия. M.: Дрофа, 2008. с.66-67). Они перспективны в качестве катализаторов, биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов [Deutsche Gold- und Silber-Scheidcanstalt vormals Roessler. P.P. 1,341,792/1963 (Chem. Abs., 1964, 60, 5528d)], специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах (от легкой промышленности до нефти) (Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р., Ковтуненко С.В., Калимуллин А.А., Андрианов В.М., Исмагилов Ф.Р., Гафиатуллин P.P. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат. РФ №2160233, 2000; Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат. РФ №2206726, 2003).
Известен способ (В.Р.Ахметова, Г.Р.Надыргулова, С.Р.Хафизова, Т.В.Тюмкина, А.А.Яковенко, M.Ю.Антипин, Л.М.Халилов, Р.В.Кунакова, У.М.Джемилев. Взаимодействие аминофенолов с формальдегидом и сероводородом. Изв. АН. Сер. хим., 2006, №3, с.305) получения шестичленных N,S-содержащих гетероциклов, а именно N-арил-1,3,5-дитиазинанов (2) взаимодействием соответственно о-, n-аминофенолов, водного формальдегида (37%) и сероводорода при температуре 40°С по схеме:
Известный способ нетехнологичен, так как предполагает применение газообразного и чрезвычайно токсичного сероводорода, который при высокой концентрации не имеет запаха, но даже однократное его вдыхание может вызвать мгновенную смерть. Кроме того, известным способом не могут быть получены 3-арил-1,5,3-дитиазепаны общей формулы (1a-i).
Известен способ (U.Wellmar. Urea as Leaving Group in the Synthesis of 3-(tert-Butyl)perhydro-1,5,3-dithiazepine. J. Heterocyclic Chem., 1998, 35, p.1531) получения соединений 1,5,3-дитиазепанового ряда, а именно 3-(трет-бутил)пергидро-1,5,3-дитиазепина (3) с выходом 45% взаимодействием 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина с 1,2-этапдитиолом в присутствии BF3·2НОАс при комнатной температуре за 2 ч по схеме:
Известным способом не могут быть получены 3-арил-1,5,3-дитиазепаны общей формулы (1a-i).
Таким образом, в литературе отсутствуют сведения по получению 3-арил-1,5,3-дитиазепанов общей формулы (1a-i).
Предлагается новый способ получения 3-арил-1,5,3-дитиазепанов общей формулы (1a-i).
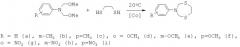
Сущность способа заключается во взаимодействии N,N-бис(метоксиметил)-N-ариламина (арил = фенил, m- и р-метилфенил, о-, m- и р-метоксифенил, о-, m- и р-нитрофенил) с 1,2-этандитиолом в присутствии катализатора CoCl2, взятыми в мольном соотношении N,N-бис(метоксиметил)-N-ариламин : 1,2-этандитиол : CoCl2=10:10:(0.3-0.7), предпочтительно 10:10:0.5 при комнатной (~20°С) температуре и атмосферном давлении в хлороформе в качестве растворителя в течение 60-90 минут, предпочтительно 75 минут. Выход соответствующих 3-арил-1,5,3-дитиазепанов общей формулы (1a-i) составляет 67-90%. Реакция протекает по схеме:
3-Арил-1,5,3-дитиазепаны общей формулы (1a-i) образуются только лишь с участием N,N-бис(метоксиметил)-N-ариламинов и 1,2-этандитиола, взятых в стехиометрических количествах. При другом соотношении исходных реагентов снижается селективность реакции. В присутствии других серусодержащих соединений (например, 1,3-пропандитиол, 1,4-бутандитиол) 3-арил-1,5,3-дитиазепаны (1a-i) не образуются. Без катализатора реакция идет с выходом, не превышающим 10%.
Проведение указанной реакции в присутствии катализатора CoCl2 больше 7 мол.% не приводит к существенному увеличению выхода целевого продукта (1a-i). Использование катализатора CoCl2 менее 3 мол.% снижает выход (1a-i), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°С. При температуре выше 20°С (например, 60°С) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°С (например, 10°С) снижается скорость реакции. Опыты проводили в хлороформе, т.к. в нем хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа
В известном способе реакция идет с участием в качестве исходного реагента 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина в присутствии BF3·2HOAc с образованием 3-(трет-бутил)пергидро-1,5,3-дитиазепина (2). Известный способ не позволяет получать индивидуальные 3-арил-1,5,3-дитиазоканы общей формулы (1a-i).
В предлагаемом способе в качестве исходных реагентов применяются N,N-бис(метоксиметил)-N-ариламины (арил = фенил, m- и р-метилфенил, о-, m- и р-метоксифенил, о-, m- и р-нитрофенил), реакция идет при комнатной температуре под действием каталитических количеств CoCl2. В отличие от известных предлагаемый способ позволяет получать индивидуальные 3-арил-1,5,3-диотиазепаны общей формулы (1a-i).
Способ поясняется следующими примерами.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 1.53 г (10 ммоль) N,N-бис(метоксиметил)-N-фениламина и 0.94 г (10 ммоль) 1.2-этандитиола, 5 мл хлороформа, 0.06 г (0.5 ммоль) катализатора CoCl2, перемешивают при комнатной (~20°С) температуре 75 мин, выделяют 3-фенил-1,5,3-дитиазепан (1а) с выходом 75%.
Другие примеры, подтверждающие способ, приведены в таблице.
| №№ п/п | Исходный N,N-бис(метоксиметил)-N-ариламин | Соотношение N,N-бис(метоксиметил)-N-ариламин : 1,2-этандитиол : CoCl2, ммоль | Время реакции, мин | Выход (1),% |
| 1 | N,N-бис(метоксиметил)-N-фениламин | 10:10:0.5 | 75 | 75 |
| 2 | -<<- | 10:10:0.3 | 75 | 67 |
| 3 | -<<- | 10:10:0.7 | 75 | 82 |
| 4 | -<<- | 10:10:0.5 | 60 | 70 |
| 5 | -<<- | 10:10:0.5 | 90 | 76 |
| 6 | N,N-бис(метоксиметил)-N-м-метилфениламин | 10:10:0.5 | 75 | 82 |
| 7 | N,N-бис(метоксиметил)-N-п-метилфениламин | 10:10:0.5 | 75 | 79 |
| 8 | N,N-бис(метоксиметил)-N-о-метоксифениламин | 10:10:0.5 | 75 | 80 |
| 9 | N,N-бис(метоксиметил)-N-м-метоксифениламин | 10:10:0.5 | 75 | 85 |
| 10 | N,N-бис (метоксиметил)-N-п-метоксифениламин | 10:10:0.5 | 75 | 87 |
| 11 | N,N-бис(метоксиметил)-N-о-нитрофениламин | 10:10:0.5 | 75 | 82 |
| 12 | N,N-бис(метоксиметил)-N-м-нитрофениламин | 10:10:0.5 | 75 | 90 |
| 13 | N,N-бис(метоксиметил)-N-п-нитрофениламин | 10:10:0.5 | 75 | 78 |
Все опыты проводили в хлороформе при комнатной температуре (~20°С).
3-Фенил-1,5,3-дитиазепан.
Спектр ЯМР 1Н, δ, м.д.: 3.08 (с, 4Н, СН2); 4.80 (с, 4Н, СН2); 6.91-7.35 (м, 4Н, CH).
Спектр ЯМР 13С, δ, м.д.: 35.78 (С6,7); 54.92 (C2,4); 115.93 (С9,13); 119.95 (С11); 129.30 (С10,12); 145.83 (С8). Масс-спектр, m/z (Iотн, %): 211 [М]+ (12), 78 [C6H5]+ (10), 91 [C6H5N]+ (15), 137 [C7H7NS]+ (100); 165 [C9H12NS] (95).
3-(м-Метилфенил)-1,5,3-дитиазепан (Ib).
Спектр ЯМР 1H, δ, м.д.: 2.38 (с, 3Н, СН3); 3.10 (с, 4Н, CH2); 4.81 (с, 4Н, CH2); 6.79-7.23 (м, 4Н, СН). Спектр ЯМР 13C, δ, м.д.: 21.83 (С14): 35.91 (С6,7) 55.06(С2,4); 112.29 (С13); 116.69 (С9); 120.93 (С11); 129.08 (С10); 138.90 (С12); 145.95 (С8). Масс-спектр, m/z (Iотн, %): 225 [M]+ (12), 91 [C7H8]+ (70), 106 [C7H8N]+ (100), 119 [C8H9N]+ (100); 165 [C11H14NS]+ (40). М 225.
3-(р-Метилфенил)-1,5,3-дитиазепан (Ic).
Спектр ЯМР 1H, δ, м.д.: 2.33 (с, 3Н, СН3); 3.91 (с, 4Н, CH2); 4.89 (с, 4Н, CH2); 6.53-6.67 (м, 4Н, СН). Спектр ЯМР 13С, δ, м.д.: 21.77 (С14); 35.83 (C6,7) 54.95 (С2,4); 114.76 (С9,13); 119.43 (С10,12); 139.04 (С11); 148.74 (С8).
3-(о-Метоксифенил)-1,5,3-дитиазепан (Id).
Спектр ЯМР 1Н, δ, м.д.: 2.71-2.95 (м, 4Н, СН3); 3.35 (с, 3Н, СН2); 4.53 (с, 4Н, CH2); 6.67-7.87 (м, 4Н, СН). Спектр ЯМР 13С, δ, м.д.: 33.48 (С6,7); 53.66 (С15) 58.93 (С2,4); 109.35 (С11); 115.76 (C13); 123.05 (С10); 128.96 (С12); 144.78 (C9); 147.20(C8).
3-(м-Метоксифенил)-1,5,3-дитиазепан (Ie).
Спектр ЯМР 1Н, δ, м.д.: 2.61-2.73 (м, 4Н, CH2); 3.42 (с, 3Н, CH3); 4.47 (с, 4Н, CH2); 6.71-7.53 (м, 4Н, СН). Спектр ЯМР 13C, δ, м.д.: 33.95 (С6,7); 52.00 (С15); 60.97 (С2,4); 109.89 (С11); 112.43 (С12); 119.97 (С13); 124.77 (С9); 144.55 (С10); 147.32 (С8). Масс-спектр, m/z (Iотн, %): 241 [М]+ (20), 77 [C6H5]+ (70), 106 [C7H6O]+ (40), 120 [C7H6ON]+ (100); 135 [C8H9NO]+ (60); 180 [C9H11NOS]+ (10); 208 [C11H15NOS]+ (80). М 241.
3-(п-Метоксифенил)-1,5,3-дитиазепан (If).
Спектр ЯМР 1H, δ, м.д.: 2.64-2.81 (м, 4Н, CH2); 3.51 (с, 3H, CH3); 4.39 (с, 4Н, CH2); 6.59-7.12 (м, 4Н, СН). Спектр ЯМР 13C, δ, м.д.: 34.28 (С6,7); 51.93 (С15); 59.99 (С2,4); 113.33 (С9,13); 125.07 (С10,12); 143.98 (С11); 148.98 (С8).
3-(о-Нитрофенил)-1,5,3-дитиазепан (Ig).
Спектр ЯМР 1H, δ, м.д.: 2.66-2.99 (м, 4H, СН2); 4.46 (с, 4Н, CH2); 6.67-7.87 (м, 4Н, CH). Спектр ЯМР 13C, δ, м.д.: 34.51 (С6,7); 59.65 (С2,4); 110.55 (С11); 114.71 (С15); 122.45 (С10); 129.01 (С12); 145.92 (C9); 147.20 (С8). Масс-спектр, m/z (Iотн, %): 256 [М]+ (20), 122 [C6H4NO2]+ (70), 136 [C6H4N2O2]+ (40), 181 [C7H8N2O2S]+ (100); 210 [C9H10N2O2S]+ (100). М 256.
3-(м-Нитрофенил)-1,5,3-дитиазепан (Ih).
Спектр ЯМР 1H, δ, м.д.: 2.74-2.79 (м, 4Н, СН2); 4.14 (с, 4Н, СН2); 7.12-7.74 (м, 4Н, СН). Спектр ЯМР 13C, δ, м.д.: 35.45 (С6,7); 61.59 (С2,4); 109.43 (С11); 113.55 (С13); 121.13 (С9); 128.73 (С12); 143.67 (С10); 147.01 (C8).
3-(р-Нитрофенил)-1,5,3-дитиазепан (Ii).
Спектр ЯМР 1Н, δ, м.д.: 2.79-2.90 (м, 4Н, СН2); 4.30 (с, 4Н, СН2); 6.91-7.85 (м, 4H, СН). Спектр ЯМР 13C, δ, м.д.: 36.41 (С6,7); 59.75 (С2,4); 111.92 (C9,13): 124.25 (C10,12); 138.90 (С11); 149.52 (С8).
Способ получения 3-арил-1,5,3-дитиазепанов общей формулы (Ia-i): отличающийся тем, что N,N-бис(метоксиметил)-N-ариламин (арил = фенил, m- и р-метилфенил, о-, m- и p-метоксифенил, о-, m- и p-нитрофенил) подвергают взаимодействию с 1,2-этандитиолом в присутствии катализатора CoCl2 в мольном соотношении N,N-бис(метоксиметил)-N-ариламин : 1,2-этандитиол : CoCl2=10:10:(0.3-0.7) при комнатной (~20°С) температуре и атмосферном давлении в хлороформе в качестве растворителя в течение 60-90 минут.