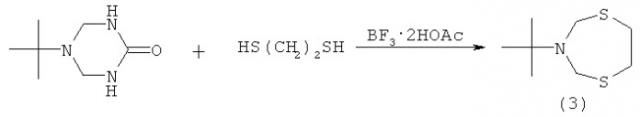Способ получения 3-арил-1,5,3-дитиазоцинанов
Иллюстрации
Показать всеИзобретение относится к способу получения 3-арил-1,5,3-дитиазоцинанов формулы (I). Сущность способа заключается во взаимодействии ароматических аминов (4-аминотиофенола, 4-аминобензойной кислоты, 4-аминофенола или 2-аминофенола, общей формулы R-C6H4-NH2, где R=4-SH, 4-СO2Н, 4-ОН, 2-ОН) с 1-окса-3,7-дитиациклооктаном в среде аргона в присутствии катализатора Sm(NO3)3·6Н2O при комнатной температуре (~20°С) и атмосферном давлении в среде растворителей этанол-хлороформ в течение 2,5-3,5 ч. Выход 3-арил-1,5,3-дитиазоцинанов (1) составляет 60-88%. 1 табл., 1 пр.
R=4-SH, 2-OH, 4-OH, 4-COOH
Реферат
Предлагаемое изобретение относится к органической химии, конкретно к способу получения 3-арил-1,5,3-дитиазоцинанов общей формулы (1):
Азот и серусодержащие гетероциклы известны как антибактериальные, антигрибковые и антивирусные агенты (Stillings М. R., Welbourn А.P., Walter D.J. Substituted 1,3,4-thiadiazoles with anticonvulsant activity // Med. Chem., 1986, 29, 2280; Kidwai M., Negi N., Chaudhary S.R. Cyclothiomethylation of arge hydrazines with formaldehyde // Acta Pharma, 1995, 45, 511; Тюкавкина H.А., Зурабян С.Э., Белобородов В.Л. и др. Органическая химия. М.: Дрофа, 2008, 66). Они перспективны в качестве катализаторов, биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов [Deutsche Gold- und Silber-Scheideanstalt vormals Roessler. F.P. 1,341,792/1963 (Chem. Abs., 1964, 60, 5528d)], специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах (от легкой промышленности до нефти) (Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р., Ковтуненко С.В., Калимуллин А.А., Андрианов В.М., Исмагилов Ф.Р., Гафиатуллин Р.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат. РФ №2160233, 2000; Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат.РФ №2206726, 2003).
Известен способ (М. Preiss. 1,2,5-Thiadiazolidin-1,1-dioxid und Homologe // Chem. Ber., 1978, 111, 1915) получения азот- и серусодержащих гетероциклов, а именно 3,4,5,6,7,8-гексагидро-2Н-1,2,8-тиадиазоцин-1,1-диоксида (2) с выходом 13% взаимодействием пентаметилендиамина с сульфамидом по схеме:
Известным способом не могут быть получены 3-арил-1,5,3-дитиазоцинаны общей формулы (1).
Известен способ (В.Р. Ахметова, З.Т. Ниатшина, Г.Р. Хабибуллина, И.С. Бушмаринов, А.О. Борисова, З.А. Старикова, Л.Ф. Коржова, Р.В. Кунакова. Синтез, кристаллическая структура и взаимные превращения новых N-арил-1,3,5-дитиазинанов, 1,3,5-тиадиазинанов и 1,5-дитиа-3,7-диазациклооктанов // Изв. АН. Сер. хим., 2010, №5, 980) получения восьмичленных N,S-содержащих гетероциклов, а именно N,N'-дифенил-1,5-дитиа-3,7-диазациклооктана (3), взаимодействием анилина, водного формальдегида (37%) и сероводорода при температуре 0°С по схеме:
Известным способом не могут быть получены 3-арил-1,5,3-дитиазоцинаны общей формулы (1).
Известен способ (U.Wellmar. Urea as Leaving Group in the Synthesis of 3-(tert-Butyl)perhydro-l,5,3-dithiazepine // J.Heterocyclic Chem., 1998, 35, 1531) получения 3-(трет-бутил)пергидро-1,5,3-дитиазепина (4) с выходом 45% взаимодействием 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина с 1,2-этандитиолом в присутствии стехиометрических количеств BF3·2HOAc при комнатной температуре за 2 ч по схеме:
Известным способом не могут быть получены 3-арил-1,5,3-дитиазоцинаны общей формулы (1).
Таким образом, в литературе отсутствуют сведения о получении 3-арил-1,5,3-дитиазоцинанов общей формулы (1).
Предлагается новый способ получения 3-арил-1,5,3-дитиазоцинанов общей формулы (1).
Сущность способа заключается во взаимодействии ароматических аминов общей формулы R-C6H4-NH2 (где R=4-SH, 2-ОН, 4-ОН, 4-СООН) с 1-окса-3,7-дитиациклооктаном в среде аргона в присутствии катализатора Sm(NO3)3·6H2O, взятыми в мольном соотношении ариламин: 1-окса-3,7-дитиациклооктан: Sm(NO3)3·6H2O=10:10:(0.3-0.7), предпочтительно 10:10:0.5, при комнатной температуре (~20°С) и атмосферном давлении в среде растворителей этанол-хлороформ в течение 2.5-3.5 ч. Выход 3-арил-1,5,3-дитиазоцинанов (1) составляет 60-88%. Реакция протекает по схеме:
3-Арил-1,5,3-дитиазоцинаны общей формулы (1) образуются только лишь с участием ароматических аминов и 1-окса-3,7-дитиациклооктана, взятых в эквимольном соотношении (стехиометрические количества). При другом соотношении исходных реагентов снижается селективность реакции. В присутствии других аминов (например, алкиламины, α, ω-алкандиамины) целевые продукты (1) не образуются. Без катализатора реакция идет с выходом, не превышающим 10%.
Проведение реакции в присутствии катализатора Sm(NO3)3·6H2О больше 7 мол. % по отношению к первичному ариламину не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора Sm(NO3)3·6H2O менее 3 мол. % снижает выход (1), что связано с уменьшением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре (20°С). При более высокой температуре (например, 60°С) увеличиваются энергозатраты, при меньшей температуре (например, -10°С) снижается скорость реакции. Опыты проводили в среде растворителей этанол-хлороформ, т.к. в них хорошо растворяются как исходные, так и целевые продукты.
Существенные отличия предлагаемого способа:
В предлагаемом способе реакция идет с участием в качестве исходных реагентов ароматических аминов (4-аминотиофенол, 4-аминобензойная кислота, 4-аминофенол, 2-аминофенол) и 1-окса-3,7-дитиациклооктана под действием катализатора Sm(NO3)3·6H2O при температуре 20°С. В отличие от известных, предлагаемый способ позволяет получать индивидуальные 3-арил-1,5,3-дитиазоцинаны общей формулы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 125 мг (10 ммолей) 4-аминотиофенола в 5 мл этанола, 22 мг (0.5 ммолей) Sm(NO3)3·6H2O и 150 мг (10 ммолей) 1-окса-3,7-дитиациклооктана в 5 мл хлороформа. Реакционную смесь перемешивают при комнатной температуре (~20°С) в течение 3 ч. Из реакционной массы выделяют 4-(1,5,3-дитиазоцинан-3-ил)-тиофенол с выходом 81%. Другие примеры, подтверждающие способ, приведены в табл.1.
| Таблица 1 | ||||
| №№ п/п | Исходный ариламин | Соотношение ариламин:1 -окса-3,7-дитиациклооктан:Sm(NO3)3·6H2O, ммоль | Время реакции, час | Выход (1), % |
| 1 | 4-аминотиофенол | 10:10:0.5 | 3 | 81 |
| 2 | -«- | 10:10:0.7 | 3 | 88 |
| 3 | -«- | 10:10:0.3 | 3 | 60 |
| 4 | -«- | 10:10:0.5 | 3.5 | 85 |
| 5 | -«- | 10:10:0.5 | 2.5 | 74 |
| 6 | 4-аминобензойная кислота | 10:10:0.5 | 3 | 76 |
| 7 | 4-аминофенол | 10:10:0.5 | 3 | 68 |
| 8 | 2-аминофенол | 10:10:0.5 | 3 | 63 |
Все опыты проводили в среде растворителей этанол-хлороформ при комнатной температуре (~20°С).
Спектральные характеристики 4-(1,5,3-дитиазоцинан-3-ил)-тиофенола:
Т. пл. 273-274°С, Rf0.8 (Sorbfil, толуол-этилацетат-ацетон (8:1:1). Спектр ЯМР 1Н (400 МГц, CDCl3), δ, м.д. (J, Гц): 1.67 (2Н, м, Н-7); 2.62 (4Н, т, J=5.8 Гц, Н-6, Н-8); 4.85 (4Н, уш. с, Н-2, Н-4); 6.89 (2Н, д, J=8.8 Гц, Н-10, Н-14); 7.37 (2Н, д, J=8.8 Гц, Н-11, Н-13). Спектр ЯМР 13С, δ, м.д.: 28.47 (С-6, С-8), 32.40 (С-7), 55.61 (С-2, С-4), 114.78 (С-10, С-14), 124.66 (С-9), 132.71 (С-11, С-13), 144.42 (С-12). MALDI TOF, m/z 256.251 [М-Н]+(C11H14NOS3).
Спектральные характеристики 4-(1,5,3-дитиазоцинан-3-ил)-бензойной кислоты:
Спектр ЯМР 1Н (400 МГц, CDCl3), δ, м.д. (J, Гц): 1.67 (2Н, м, Н-7); 2.63 (4Н, т, J-5.8 Гц, Н-6, Н-8); 4.89 (4Н, уш. с, Н-2, Н-4); 6.90 (2Н, д, J=8.8 Гц, Н-10, Н-14); 7.80 (2Н, д, J=8.8 Гц, Н-11, Н-13); 12.25 (1Н, уш. с, Н-16). Спектр ЯМР 13С, δ, м.д.: 27.99 (С-6, С-8), 31.87 (С-7), 55.06 (С-2, С-4), 112.96 (С-10, С-14), 119.89 (С-12), 130.58 (С-11, С-13), 147.11 (С-9), 167.37 (С-15). MALDI TOF, m/z 270.250 [М+Н]+(C12H15NO2S2H).
Спектральные характеристики 4-(1,5,3-дитиазоцинан-3-ил)-фенола:
Rf0.85 (Sorbfil, толуол-этилацетат-ацетон (4:1:1). Спектр ЯМР 1Н (400 МГц, CDCl3), δ, м.д. (J, Гц): 1.80 (2Н, м, Н-7); 2.72 (4Н, т, J=5.8 Гц, Н-6, Н-8); 4.50 (1Н, уш. с, Н-15); 4.76 (4Н, уш. с, Н-2, Н-4); 6.83 (4Н, м, Н-10, Н-11, Н-13, Н-14). Спектр ЯМР 13С, δ, м. д.: 28.99 (т, С-6, С-8), 32.24 (т, С-7), 57.05 (т, С-2, С-4), 114.50 (д, С-10, С-14), 116.29 (д, С-11, С-13), 137.45 (с, С-9), 148.49 (с, С-12). MALDI TOF, m/z 242.351 [М+Н]+(C11H15NOS2H).
Спектральные характеристики 2-(1,5,3-дитиазоцинан-3-ил)-фенола:
Rf0.80 (Sorbfil, хлороформ-этилацетат-гексан, 1:5:1). Спектр ЯМР 1Н (400 МГц, CDCl3), δ, м.д. (J, Гц): 1.75 (2Н, м, Н-7); 2.57 (4Н, м, Н-6, Н-8); 4.34 (4Н, м, Н-2, Н-4); 6.42 (1Н, уш. с, Н-15); 6.88 (1Н, т, J=6.2 Гц, Н-11); 6.96 (1H, д, J=6.4 Гц, Н-10); 7.11 (1H, д, J=6.4 Гц, Н-13); 7.22 (1Н, т, J=8.8 Гц, Н-12). Спектр ЯМР 13С, δ, м. д.: 29.43 (т, С-7), 30.78 (С-6, С-8), 55.93 (С-2, С-4), 115.07 (С-11), 120.37 (С-10), 125.25 (С-12), 127.43 (С-13), 135.40 (С-9), 151.39 (С-14). MALDI TOF, m/z 242.362 [М+Н]+(C11H15NOS2H).
Способ получения 3-арил-1,5,3-дитиазоцинанов общей формулы (1): где R=4-SH, 2-OH, 4-OH, 4-COOH,отличающийся тем, что ароматические амины общей формулы R-C6H4-NH2 (где R = указанное выше) подвергают взаимодействию с 1-окса-3,7-дитиациклооктаном в среде аргона в присутствии катализатора Sm(NO3)3·6H2O в мольном соотношении ариламин: 1-окса-3,7-дитиациклооктан: Sm(NO3)3·6H2O=10:10:(0,3-0,7) в среде растворителей этанол-хлороформ при комнатной температуре (~20°С) и атмосферном давлении в течение 2,5-3,5 ч.