Модуляторы рецепторов 5-нт и способы их применения
Иллюстрации
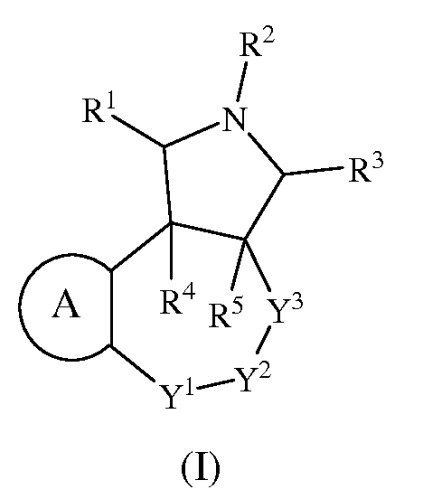
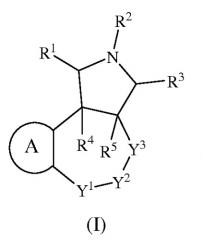
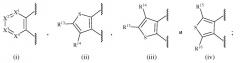
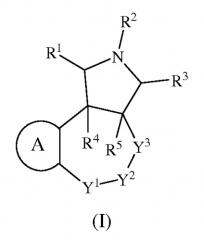
Показать всеИзобретение относится к соединениям формулы (I) и их фармацевтически приемлемым солям, обладающим свойствами модулятора рецептора 5-HT2C и/или 5-НТ6, фармацевтической композиции на их основе и способам их получения. В общей формуле (I) фрагмент А выбран из группы, состоящей из (i), (ii) или (iii), R1, R3, R4 и R5 означают водород или алкил; каждый из R4a и R5a представляет собой водород; G1 представляет собой арил или гетероарил, который может быть незамещенным или замещен 1, 2, 3, 4 или 5 заместителями, выбранными из группы, состоящей из алкила, галогена, циано, -OR1b, -S(O)R2b, -C(O)R1b, -С(O)OR1b, -ОС(O)N(Rb)(R3b), -(CR4bR5b)m-OR1b, -C(OH)[(CR4bR5b)m-R4b]2, и галогеналкила; G2 означает циклоалкил, циклоалкенил или гетероцикл, незамещенный или замещенный 1, 2, 3, 4 или 5 заместителями, выбранными из группы, состоящей из алкила; Rb представляет собой водород или алкил; R1b и R3b представляет собой водород, алкил или галогеналкил; R2b представляет собой алкил; R4b и R5b представляет собой водород, галоген, алкил или галогеналкил; m представляет собой 1, 2, 3, 4 или 5; R2 выбран из группы, состоящей из водорода, алкила, -(CR4aR5a)m-G1 и -S(O)2R6, R6 представляет собой G1, Х1 означает N или CR9; X2 означает N или CR10; X3 означает CR11; X4 означает N или CR12; при условии, что только один фрагмент из числа X1, X2 или X4 может представлять собой N; каждый из R9, R10, R11, R12, R13 и R14 независимо представляет собой водород, алкил, алкенил, галоген, -G1, -G2, -OR1a, -C(O)G3, -C(O)OR1a, -C(O)N(Rb)(R3a), -N(Rb)(R3a), -(CR4aR5a)m-G1, -CR4a=CR5a-G1, -(CR4aR5a)m-G2, -CR6a=C(R7a)2, галогеналкил и фрагмент (v); R1a и R3a представляет собой водород, алкил, галогеналкил, G1, -(CR4aR5a)m-G1, G2 или -(CR4aR5a)m-G2; R6a является алкилом или галогеналкилом; R7a представляет собой водород, алкил или галогеналкил; G3 представляет собой гетероцикл, присоединенный к соседнему карбонильному фрагменту через атом азота, входящий в гетероцикл; или R10 и R11 или R13 и R14 совместно с атомами углерода, к которым они присоединены, образуют незамещенный фенил или циклоалкил; Y1 означает NR17, CR18R19, C(O), S(O)n или О; Y2 означает NR20, CR18R19 или С(О); Y3 означает NR17, CR18R19 или С(О); или Y1 и Y2 вместе представляют собой CR18=CR19, n означает 2; R17 представляет собой водород; R18 и R19 представляют собой водород; и R20 выбран из группы, состоящей из водорода, алкила и -S(O)n-G1. 4 н. и 29 з.п. ф-лы, 7 табл., 20 ил., 278 пр.
, , ,
,
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка на патент претендует на приоритет предварительной заявки на патент США № 61/180569, поданной 22 мая 2009, содержание которой полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к соединениям, включающим декагидропирролазепин, октагидрооксепинопиррол, диоксид октагидропирролтиазепина, декагидроциклогепта[c]пиррол и октагидроциклогепта[c]пиррол, конденсированные с арилом или гетероарилом, к способам модулирования рецептора 5-HT2C, рецептора 5-HT6 или обоих рецепторов 5-HT2C и 5-HT6 при предупреждении или лечении состояний и расстройств, связанных с серотонином, с применением упомянутых выше соединений или композиций, содержащих эти соединения, а также к способам получения этих соединений и композиций.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям и фармацевтическим композициям, содержащим соединения, применимые в качестве агонистов или частичных агонистов рецептора 5-HT2C, антагонистов рецептора 5-HT6, или одновременно агонистов или частичных агонистов рецептора 5-HT2C и антагонистов рецептора 5-HT6 для лечения заболеваний, расстройств и состояний, при которых желательно модулирование рецепторов 5-HT2C или 5-HT6, например депрессии, тревожности, шизофрении, биполярного расстройства, обсессивно-компульсивного расстройства, мигрени, боли, эпилепсии, злоупотребления психотропными веществами, расстройств пищевого поведения, ожирения, диабета, эректильной дисфункции и т.д.
Серотонин (5-гидрокситриптамин, 5-HT), представляющий собой моноаминный нейротрансмиттер и местный гормон, образуется при гидроксилировании и декарбоксилировании триптофана. Наибольшая концентрация серотонина обнаружена в энтерохромаффинных клетках желудочно-кишечного тракта, а остальной серотонин находится преимущественно в тромбоцитах и центральной нервной системе (ЦНС). 5-HT вовлечен в очень широкий круг физиологических и патофизиологических сигнальных путей. На периферии он стимулирует сокращение ряда гладких мышц и вызывает эндотелий-зависимую вазодилатацию. В ЦНС серотонин, как полагают, выполняет широкий круг функций, включая управление аппетитом, настроением, тревогой, галлюцинациями, сном, тошнотой и ощущением боли.
Нейроны, которые секретируют 5-HT, именуют серотонинергическими. Действие 5-HT проявляется при его взаимодействии с определенными (серотонинергическими) нейронами. Было идентифицировано семь типов рецепторов 5-HT: 5-HT1 (с подтипами 5-HT1A, 5-HT1B, 5-HT1D, 5-HT1E и 5-HT1F), 5-HT2 (с подтипами 5-HT2A, 5-HT2B и 5-HT2C), 5-HT3, 5-HT4, 5-HT5 (с подтипами 5-HT5A и 5-HT5B), 5-HT6 и 5-HT7. Большая часть этих рецепторов сопряжена с G-белками, которые влияют на активность аденилат циклазы или фосфолипазы Cγ.
Изменение активности нескольких систем рецепторов нейротрансмиттеров (дофамина, серотонина, глутамата, GABA, ацетилхолина) влечет за собой проявление симптомов шизофрении. Наиболее общепризнанная «дофаминовая гипотеза шизофрении» в ее простейшей форме утверждает, что позитивные симптомы этого заболевания связаны с функциональной гиперактивностью мезолимбической дофаминергической системы, тогда как для негативных и когнитивных аспектов прослеживается связь с функциональной гипоактивностью мезокортикальных дофаминергических проекций. Атипические антипсихотические средства блокируют мезолимбическую дофаминергическую нейропередачу, что позволяет регулировать позитивные симптомы, но не оказывают или оказывают незначительное влияние на нигростриальную систему, что уменьшает стимулирование побочных эффектов экстрапирамидной системы (EPS).
Первичные негативные и когнитивные симптомы шизофрении отражают дисфункцию лобного отдела коры головного мозга («гипофронтальность»), которая, как полагают, является следствием пониженного тонуса поля мезокортикальных дофаминергических проекций [Davis KL., Kahn RS Ko G and Davidson M (1991). Dopamine in schizophrenia: a review and re-conceptualization. Am J Psychiatry 148: 1474-86. Weinberger DR and Berman KF (1996). Prefrontal function in schizophrenia: confounds and controversies. Philos Trans R Soc Lond B Biol Sci 351: 1495-503]. Агенты, которые селективно повышают уровни дофамина в коре головного мозга, обладают потенциалом для борьбы с негативными симптомами этого расстройства. Атипические антипсихотические средства не обладают надежной эффективностью против отрицательных и когнитивных компонентов шизофренического синдрома.
Симптоматика шизофрении дополнительно осложняется появлением вызванных лекарствами т.н. вторичных негативных симптомов и когнитивных нарушений, которые сложно отличить от первичных негативных и когнитивных симптомов [Remington G and Kapur S (2000). Atypical antipsychotics: are some more atypical than others? Psychopharmacol 148:3-15]. Появление вторичных негативных симптомов не только ограничивает терапевтическую эффективность, но, кроме того, в сочетании с этими побочными эффектами, отрицательно влияет на приверженность пациента лечению.
Можно предположить, что новый механизм подхода к лечению, заключающийся в блокировании дофаминергической нейротрансмиссии в лимбической системе при отсутствии воздействия на поля проекций полосатого тела и мозжечка и стимулировании фронтокортикальных полей проекций мог бы обеспечить эффективное лечение всех компонентов шизофренической патологии, включая ее позитивные, негативные и когнитивные симптомы. Кроме того, можно было бы ожидать, что соединение с селективным действием, которое практически не вызывает побочных фармакологических эффектов, характерных для существующих лекарственных средств, позволит избежать ряда нецелевых побочных эффектов, которые сопровождают способы лечения известного уровня техники, например, экстрапирамидальных побочных эффектов (EPS) и набора массы тела.
Рецептор 5-HT2C, ранее именовавшийся 5-HT1C, является рецептором, сопряженным с G-белком, который связан с большим числом эффекторных систем клетки, включая сигнальные пути C, A и D фосфолипазы. Вначале этот рецептор обнаружили в мозгу, и его содержание особенно высоко в хороидном сплетении, где, как считается, он регулирует выработку спинномозговой жидкости [Kaufman MJ, Hirata F (1996) Cyclic GMP inhibits phosphoinositide turnover in choroid plexus: evidence for interactions between second messengers concurrently triggered by 5-HT2C receptors. Neurosci Lett 206:153-156]. Очень высокие уровни рецептора были обнаружены также в ретроспленальной коре, грушевидной коре и энторинальной области коры, переднем обонятельном ядре, боковом ядре перегородки, субталамическом ядре, миндалевидном теле, основании гиппокампа и вентральной части CA3, латеральном поводке, компактной части черной субстанции, нескольких ядрах ствола головного мозга и всем сером веществе спинного мозга [Pompeiano M, Palacios JM, Mengod G (1994). Distribution of serotonin 5-HT2 receptor family mRNAs: comparison between 5-HT2A and 5-HT2C receptors. Brain Res Mol Brain Res 23: 163-178]. Сравнение распределения мРНК 5-HT2C с распределением белка 5-HT2C у обезьян и в мозге человека выявило как пре-, так и постсинаптическую локализацию [Lopez-Gimenes JF, Mengod G, Palacios JM, Vilaro MT (2001) Regional distribution and cellular localization of 5-HT2C receptor mRNA in monkey brain: comparison with [3H]mesulergine binding sites and choline acetyltransferase mRNA. Synapse 42: 12-26].
Ожидается, что модулирование рецептора 5-HT2C будет улучшать состояние при таких расстройствах, как депрессия, тревожность, шизофрения, когнитивные нарушения при шизофрении, обсессивно-компульсивное расстройство, биполярное расстройство, мигрень, эпилепсия, злоупотребление психотропными веществами, расстройства пищевого поведения, ожирение, диабет, сексуальные расстройства/эректильная дисфункция, расстройства сна, псориаз, болезнь Паркинсона, болевые состояния и расстройства, поражения спинного мозга, отказ от курения, глазная гипертензия и болезнь Альцгеймера. Кроме того показано, что модуляторы рецептора 5-HT2C полезны при регулировании функций мочевого пузыря, включая предупреждение или лечение недержания мочи.
Ожидается, что модулирование рецептора 5-HT6 подходящими соединениями улучшит состояние пациента при некоторых расстройствах, в т.ч. когнитивных нарушениях, например дефиците памяти, познавательных способностей и способности к обучению, связанных с болезнью Альцгеймера, возрастном уменьшении когнитивных способностей и умеренном нарушении когнитивных способностей, синдроме дефицита внимания/гиперактивности, личностных расстройствах, например шизофрении, в частности когнитивных нарушениях, связанных с шизофренией, аффективных расстройствах, например депрессии, тревожности и обсессивно-компульсивных расстройствах, расстройствах движения или моторики, например болезни Паркинсона и эпилепсии, мигрени, расстройствах сна (включая нарушения циркадного ритма), расстройствах пищевого поведения, например анорексии и булимии, некоторых желудочно-кишечных расстройствах, например синдроме раздраженного кишечника, заболеваниях, связанных с нейродегенерацией, например инсульте, травмах спины и головы и повреждениях головы, например гидроцефалии, злоупотреблении наркотиками и ожирении.
Существует насущная потребность в разработке соединений, обладающих высоким сродством и селективностью в отношении рецептора 5-HT6. Эти соединения, в том числе, должны обладать низким сродством к адренергическим рецепторам, например α1-адренергическому рецептору, гистаминовым рецепторам, например H1-рецептору, и дофаминергическим рецепторам, например D2-рецептору, с целью исключения или уменьшения побочных эффектов, связанных с модулированием этих рецепторов, например постуральной гипотензии, рефлекторной тахикардии, потенцирования противогипертонического эффекта празозина, теразозина, доксазозина и лабеталола или головокружения, связанного с блокированием α1-адренергического рецептора, набора массы тела, седативного эффекта, сонливости или потенцирования действия центральных супрессоров, связанного с блокированием H1-рецептора, или экстрапирамидальных двигательных расстройств, таких как дистония, болезнь Паркинсона, акатизия, поздняя дискинезия или синдром кролика, или эндокринных эффектов, например повышения пролактина (галактореи, гинекомастии, изменений менструации, сексуальных расстройств у мужчин), связанных с блокированием D2-рецептора.
В настоящем изобретении разработаны соединения, которые обладают сродством к рецептору 5-HT2C или 5-HT6, или обоим рецепторам 5-HT2C и 5-HT6, что дает возможность лечения расстройств, связанных или подвергающихся влиянию рецептора 5-HT2C или 5-HT6, или обоих рецепторов 5-HT2C и 5-HT6.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на соединения, включающие декагидропирролазепин и октагидро-1H-оксепино[4,5-c]пиррол, диоксид октагидропирролтиазепина, декагидроциклогепта[c]пиррол и октагидроциклогепта[c]пиррол, конденсированные с арилом или гетероарилом, на композиции, включающие эти соединения, а также на способы применения этих соединений и композиций.
В одном из аспектов настоящее изобретение относится к соединениям формулы (I):
или их фармацевтически приемлемым солям или пролекарствам, где
фрагмент A выбран из группы, состоящей из
R1, R3, R4 и R5 независимо выбраны из группы, состоящей из водорода, алкенила, алкила, галогеналкила, G1, G2, -(CR4aR5a)m-G1 и -(CR4aR5a)m-G2;
каждый из R4a и R5a в каждом случае независимо представляет собой водород, галоген, алкил или галогеналкил;
G1 в каждом случае независимо представляет собой арил или гетероарил, где каждый из фрагментов G1 независимо является незамещенным или замещен 1,2,3,4 или 5 заместителями, выбранными из группы, состоящей из алкила, алкенила, алкинила, галогена, циано, -NO2, -OR1b, -OC(O)R1b, -OC(O)N(Rb)(R3b), -SR1b, -S(O)R2b, -S(O)2R2b, -S(O)2N(Rb)(R3b), -C(O)R1b, -C(O)OR1b, -C(O)N(Rb)(R3b), -N(Rb)(R3b), -N(Ra)C(O)R1b, -N(Ra)C(O)O(R1b), -N(Ra)C(O)N(Rb)(R3b), -(CR4bR5b)m-NO2, -N(Rb)S(O)2(R2b), -(CR4bR5b)m-OR1b, -C(OH)[(CR4bR5b)m-R4b]2, -(CR4bR5b)m-OC(O)R1b, -(CR4bR5b)m-OC(O)N(Rb)(R3b), -(CR4bR5b)m-SR1b, -(CR4bR5b)m-S(O)R2b, -(CR4bR5b)m-S(O)2R2b, -(CR4bR5b)m-S(O)2N(Rb)(R3b), -(CR4bR5b)m-C(O)R1b, -(CR4bR5b)m-C(O)OR1b, -(CR4bR5b)m-C(O)N(Rb)(R3b), -(CR4bR5b)m-N(Rb)(R3b), -(CR4bR5b)m-N(Ra)C(O)R1b, -(CR4bR5b)m-N(Ra)C(O)OR1b, -(CR4bR5b)m-N(Ra)C(O)N(Rb)(R3b), -(CR4bR5b)m-N(Rb)S(O)2(R2b), цианоалкила и галогеналкила;
G2 означает циклоалкил, циклоалкенил, или гетероцикл, незамещенный или замещенный 1, 2, 3, 4 или 5 заместителями, выбранными из группы, состоящей из алкила, алкенила, алкинила, галогена, циано, оксо, -SR1b, -S(O)R2b, -S(O)2R2b, -S(O)2N(Rb)(R3b), -C(O)R1b, -C(O)OR1b, -C(O)N(Rb)(R3b), -N(Rb)(R3b), -N(Ra)C(O)R1b, -N(Ra)C(O)O(R1b), -N(Ra)C(O)N(Rb)(R3b), -(CR4bR5b)m-NO2, -N(Rb)S(O)2(R2b), -(CR4bR5b)m-OR1b, -(CR4bR5b)m-OC(O)R1b, -(CR4bR5b)m-OC(O)N(Rb)(R3b), -(CR4bR5b)m-SR1b, -(CR4bR5b)m-S(O)R2b, -(CR4bR5b)m-S(O)2R2b, -(CR4bR5b)m-S(O)2N(Rb)(R3b), -(CR4bR5b)m-C(O)R1b, -(CR4bR5b)m-C(O)OR1b, -(CR4bR5b)m-C(O)N(Rb)(R3b), -(CR4bR5b)m-N(Rb)(R3b), -(CR4bR5b)m-N(Ra)C(O)R1b, -(CR4bR5b)m-N(Ra)C(O)O(R1b), -(CR4bR5b)m-N(Ra)C(O)N(Rb)(R3b), -(CR4bR5b)m-N(Rb)S(O)2(R2b), цианоалкила и галогеналкила;
каждый из Ra и Rb в каждом случае независимо представляет собой водород, алкил или галогеноалкил;
каждый из R1b и R3b в каждом случае независимо представляет собой водород, алкил или галогеналкил;
R2b в каждом случае независимо представляет собой алкил или галогеналкил;
каждый из R4b и R5b в каждом случае независимо представляет собой водород, галоген, алкил или галогеналкил;
m в каждом случае независимо представляет собой 1, 2, 3, 4 или 5;
R2 выбран из группы, состоящей из водорода, алкоксиалкила, алкила, алкилкарбонила, галогеналкила, -(CR4aR5a)m-G1, -(CR4aR5a)p-O-G1, -C(O)-G1, -(CR4aR5a)m-G2, -(CR4aR5a)p-O-G2, -C(O)-G2, -S(O)2R6 и -C(O)NR7R8;
p в каждом случае независимо представляет собой 2, 3, 4 или 5;
R6 и R7 независимо выбраны из группы, состоящей из алкила, галогеналкила, G1, -(CR4aR5a)m-G1, G2 и -(CR4aR5a)m-G2;
R8 выбран из группы, состоящей из водорода, алкила и галогеналкила; или
R7 и R8 совместно с азотом, к которому они присоединены, образуют гетероцикл;
X1 означает N или CR9;
X2 означает N или CR10;
X3 означает N или CR11;
X4 означает N или CR12;
при условии, что только один или два фрагмента из числа X1, X2, X3 или X4 могут представлять собой N;
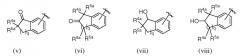
каждый из R9, R10, R11, R12, R13, R14, R15 и R16 независимо представляет собой водород, алкил, алкенил, алкинил, галоген, циано, -G1, -G2, -NO2, -OR1a, -OC(O)R1a, -OC(O)N(Rb)(R3a), -SR1a, -S(O)R2a, -S(O)2R2a, -S(O)2N(Rb)(R3a), -C(O)R1a, -C(O)G3, -C(O)OR1a, -C(O)N(Rb)(R3a), -N(Rb)(R3a), -N(Ra)C(O)R1a, -N(Ra)C(O)O(R1a), -N(Ra)C(O)N(Rb)(R3a), -N(Ra)S(O)2(R2a), -(CR4aR5a)m-NO2, -(CR4aR5a)m-OR1a, -(CR4aR5a)m-OC(O)R1a, -(CR4aR5a)m-OC(O)N(Rb)(R3a), -(CR4aR5a)m-SR1a, -(CR4aR5a)m-S(O)R2a, -(CR4aR5a)m-S(O)2R2a, -(CR4aR5a)m-S(O)2N(Rb)(R3a), -(CR4aR5a)m-C(O)R1a, -(CR4aR5a)m-C(O)OR1a, -(CR4aR5a)m-C(O)N(Rb)(R3a), -(CR4aR5a)m-N(Rb)(R3a), -(CR4aR5a)m-N(Ra)C(O)R1a, -(CR4aR5a)m-N(Ra)C(O)O(R1a), -(CR4aR5a)m-N(Ra)C(O)N(Rb)(R3a), -(CR4aR5a)m-G1, -CR4a=CR5a-G1, -(CR4aR5a)m-G2, -CR4a=CR5a-G2, -CR6a=C(R7a)2, цианоалкил, галогеналкил, фрагменты (v), (vi), (vii) или (viii); где
каждый из R1a и R3a в каждом случае независимо представляет собой водород, алкил, галогеналкил, G1, -(CR4aR5a)m-G1, G2 или -(CR4aR5a)m-G2;
R2a в каждом случае независимо представляет собой алкил, галогеналкил, G1 или -(CR4aR5a)m-G1;
R6a является алкилом или галогеналкилом;
R7a в каждом случае независимо представляет собой водород, алкил или галогеналкил;
G3 представляет собой гетероцикл, присоединенный к соседнему карбонильному фрагменту через имеющийся в цикле атом азота;
q представляет собой 1 или 2; или
R9 и R10, R10 и R11, R11 и R12, или R13 и R14 совместно с атомами углерода, к которым они присоединены, образуют замещенный или незамещенный фенил, циклоалкил, гетероцикл или гетероарильный цикл;
Y1 означает NR17, CR18R19, C(O), S(O)n или O;
Y2 означает NR20, CR18R19, C(O) или S(O)n;
Y3 означает NR17, CR18R19, C(O) или S(O)n; или
Y1 и Y2 вместе представляют собой CR18=CR19, при условии, что Y3 отличается от NR17; или
Y2 и Y3 вместе представляют собой CR18=CR19, при условии, что Y1 отличается от NR17 или O;
n означает 1 или 2;
при условии, что только один из фрагментов Y1 и Y3 может являться NR17; или Y1 и Y3 отличаются от NR17, если Y2 означает NR20; или только один из фрагментов Y1, Y2 или Y3 может представлять собой C(O) или S(O)n; или Y2 отличается от NR20 или S(O)n, если Y1 означает O; или Y3 отличается от NR17, если Y1 означает O;
R17 выбран из группы, состоящей из водорода, алкила, алкилкарбонила, галогеналкила, -C(O)-G1, -(CR4aR5a)m-G1, -C(O)-G2 и -(CR4aR5a)m-G2;
R18 и R19 независимо выбраны из группы, состоящей из водорода, алкила и галогеналкила; и
R20 выбран из группы, состоящей из водорода, алкила, алкилкарбонила, галогеналкила, -C(O)-G1, -C(O)-NRa-G1, -S(O)n-G1, -(CR4aR5a)m-G1, -C(O)-G2, -C(O)NRa-G2, -S(O)n-G2 и -(CR4aR5a)m-G2.
В другом аспекте настоящее изобретение относится к фармацевтическим композициям, включающим терапевтически эффективное количество по меньшей мере одного соединения описанной выше формулы (I), или его фармацевтически приемлемой соли, в комбинации по меньшей мере с одним фармацевтически приемлемым носителем.
Другой аспект изобретения относится к фармацевтическим композициям, включающим соединения по настоящему изобретению. Эти композиции могут вводиться согласно способу по настоящему изобретению, как правило, в качестве части терапевтической схемы для лечения или предупреждения состояний и расстройств, связанных с активностью 5-HT и, более конкретно, активностью 5-HT2c, активностью 5-HT6 или активностью обоих рецепторов 5-HT2c и 5-HT6.
В следующем аспекте настоящее изобретение относится к способам предупреждения или лечения когнитивных нарушений, синдрома дефицита внимания/гиперактивности, личностных расстройств, аффективных расстройств, расстройств движения или моторики, мигрени, боли, недержания мочи, расстройств сна, расстройств пищевого поведения, желудочно-кишечных расстройств, заболеваний, связанных с нейродегенерацией, болезненных зависимостей, ожирения, диабета, псориаза или глазной гипертензии, в которых применяются соединения формулы (I). Эти способы включают введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества по меньшей мере одного соединения формулы (I). Примерами когнитивных нарушений являются дефицит памяти, познавательных способностей и способности к обучению, болезнь Альцгеймера, возрастное снижение когнитивных способностей и незначительное ухудшение когнитивной способности или любые комбинации перечисленного. Примерами личностных расстройств являются шизофрения и расстройства познавательной способности, связанные с шизофренией. Примерами аффективных расстройств являются депрессия, тревожность, биполярное расстройство и обсессивно-компульсивные расстройства, или любые комбинации перечисленного. Примерами расстройств движения или моторики являются болезнь Паркинсона и эпилепсия. Примерами расстройств пищевого поведения являются анорексия и булимия. Примеры расстройств желудочно-кишечного тракта включают синдром раздраженного кишечника. Примерами заболеваний, связанных с нейродегенерацией, являются инсульт, травма спины или головы и повреждения головы.
В одном из вариантов осуществления настоящего изобретения разработан способ лечения млекопитающего, страдающего от шизофрении и/или когнитивных нарушений, связанных с шизофренией, который включает введение млекопитающему по меньшей мере одного соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном аспекте настоящее изобретение относится к применению соединения формулы (I) или его фармацевтически приемлемой соли в производстве лекарственного средства, предназначенного для предупреждения или лечения перечисленных выше расстройств, в чистом виде или в комбинации по меньшей мере с одним фармацевтически приемлемым носителем.
Далее в настоящей заявке описаны соединения формулы (I), композиции, включающие эти соединения, и способы предупреждения или лечения когнитивных нарушений, синдрома гиперактивности/дефицита внимания, личностных расстройств, аффективных расстройств, двигательных или моторных расстройств, мигрени, расстройств сна, расстройств пищевого поведения, желудочно-кишечных расстройств, заболеваний, связанных с нейродегенерацией, болезненных зависимостей, ожирения, диабета, псориаза или глазной гипертензии путем введения этих соединений или фармацевтических композиций.
Помимо этого, в заявке описаны соединения, композиции, включающие эти соединения, способы применения этих соединений и способы получения этих соединений, а также промежуточные соединения, получаемые в указанных способах.
Эти и другие объекты изобретения описаны в следующих разделах. Не следует считать, что эти объекты ограничивают объем настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНОГО МАТЕРИАЛА
На Фиг.1A показано графическое отображение дозозависимого эффекта соединения примера 115 при ослаблении действия фенилциклидина (PCP). Крысам вводили носитель, PCP или дозу соединения примера 115, с последующим введением фенилциклидина. По оси X отображены режимы введения, и ось Y отображает активность, которую определяли по расстоянию, преодоленному тестируемыми животными за время эксперимента.
На Фиг.1B показано графическое отображение дозозависимого эффекта соединения примера 115 при ослаблении действия фенилциклидина (PCP). Крысам вводили носитель, PCP или дозу соединения примера 115, с последующим введением фенилциклидина. По оси X отложено время эксперимента, а ось Y отображает расстояние, пройденное животным за 5-минутный интервал.
На фиг.2 приведено графическое отображение дозозависимого улучшения результатов в 24-часовом тесте на пассивное избегание, при однократном введении тестируемого соединения (пример 115) с последующим введением MK-801. Животным вводили носитель или соединение примера 115, и затем носитель или MK-801. На оси X показан распорядок введения в день помещения в условиях эксперимента и та же самая тестовая группа через 24 часа, ось Y отображает время ожидания перед вхождением на территорию, где животное получает электрический удар.
На Фиг.3 показано графическое отображение дозозависимого улучшения результатов в тесте на пассивное избегание с 5 экспериментами у детенышей крыс со спонтанной гипертензией (SHR) при однократном введении тестируемого соединения (пример 115). Ось X отображает дозировку тестируемого соединения, и ось Y отображает общее время ожидания в экспериментах 2-5 перед вхождением на территорию, где животное получает электрический удар.
На Фиг.4A приведено графическое отображение зависимого от концентрации эффекта соединения примера 44 по ослаблению влияния фенилциклидина (PCP). Мышам вводили носитель, d-амфетамин или дозу соединения примера 44 и затем PCP. По оси X отложено время (в минутах), и по оси Y отложены данные по активности за 5-минутный период времени.
На Фиг.4B показано графическое отображение зависимого от концентрации эффекта соединения примера 44 по ослаблению влияния фенилциклидина (PCP). Мышам вводили носитель, d-амфетамин или дозу соединения примера 44 и затем PCP. Фиг.4B демонстрирует общие показатели активности после инъекции PCP для различных групп.
На Фиг.5A приведено графическое отображение зависимого от концентрации эффекта соединения примера 106 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 106 и затем AMP. По оси X отложено время (в минутах), и по оси Y отложены данные по активности за 5-минутный период времени.
На Фиг.5B показано графическое отображение зависимого от концентрации эффекта соединения примера 106 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 106 и затем AMP. Фиг.5B демонстрирует общие показатели активности после инъекции AMP для различных групп.
На Фиг.6A приведено графическое отображение зависимого от концентрации эффекта соединения примера 115 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 115 и затем AMP. По оси X отложено время (в минутах), и по оси Y отложены данные по активности за 5-минутный период времени.
На Фиг.6B показано графическое отображение зависимого от концентрации эффекта соединения примера 115 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 115 и затем AMP. Фиг.6B демонстрирует общие показатели активности после инъекции AMP для различных групп.
На Фиг.7A приведено графическое отображение зависимого от концентрации эффекта соединения примера 158 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 158 и затем AMP. По оси X отложено время (в минутах), и по оси Y отложены данные по активности за 5-минутный период времени.
На Фиг.7B показано графическое отображение зависимого от концентрации эффекта соединения примера 158 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 158 и затем AMP. Фиг.7B демонстрирует общие показатели активности после инъекции AMP для различных групп.
На Фиг.8A приведено графическое отображение зависимого от концентрации эффекта соединения примера 225 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 225 и затем AMP. По оси X отложено время (в минутах), и по оси Y отложены данные по активности за 5-минутный период времени.
На Фиг.8B показано графическое отображение зависимого от концентрации эффекта соединения примера 225 по ослаблению влияния d-амфетамина (AMP). Мышам вводили носитель, AMP или дозу соединения примера 225 и затем AMP. Фиг.8B демонстрирует общие показатели активности после инъекции AMP для различных групп.
На Фиг.9A показано графическое отображение реакций избегания у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 115. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
На Фиг.9B показано графическое отображение реакций бегства у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 115. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
На Фиг.9С показано графическое отображение отсутствия реакции у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 115. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
На Фиг.10A показано графическое отображение реакций избегания у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 158. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
На Фиг.10B показано графическое отображение реакций бегства у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 158. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
На Фиг.10С показано графическое отображение отсутствия реакции у крыс в эксперименте по обусловленному избеганию после однократного введения соединения примера 158. На оси X показаны дозировки, и на оси Y показано число реакций этого типа.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном из аспектов настоящее изобретение относится к соединениям показанной ниже формулы (I):
где R1, R2, R3, R4, R5, A, Y1, Y2 и Y3 соответствуют определениям, приведенным выше в разделе «Сущность изобретения».
В другом аспекте настоящее изобретение относится к композициям, включающим соединения формулы (I), которые были описаны выше, и по меньшей мере один фармацевтически приемлемый носитель.
В следующем аспекте настоящее изобретение относится к способам предупреждения или лечения болезненных состояний, например лечения когнитивных нарушений, синдрома дефицита внимания/гиперактивности, личностных расстройств, аффективных расстройств, расстройств движения или моторики, мигрени, расстройств сна, расстройств пищевого поведения, желудочно-кишечных расстройств, заболеваний, связанных с нейродегенерацией, болезненных зависимостей, ожирения, диабета, псориаза или глазной гипертензии с применением описанных ранее соединений формулы (I).
В еще одном аспекте настоящее изобретение относится к применению описанных выше соединений формулы (I), самих по себе или в комбинации по меньшей мере с одним фармацевтически приемлемым носителем, в производстве лекарственного средства, предназначенного для предупреждения или лечения болезненных состояний, например для лечения когнитивных нарушений, синдрома дефицита внимания/гиперактивности, личностных расстройств, аффективных расстройств, расстройств движения или моторики, мигрени, расстройств сна, расстройств пищевого поведения, желудочно-кишечных расстройств, заболеваний, связанных с нейродегенерацией, болезненных зависимостей, ожирения, диабета, псориаза или глазной гипертензии.
В различных вариантах осуществления в настоящем изобретении встречается по меньшей мере один переменный фрагмент, который более одного раза появляется в каком-либо заместителе или в соединении по настоящему изобретению, или в любой другой формуле настоящей заявки. Определения переменного фрагмента при каждом его появлении независимы от определения этого же фрагмента при другом появлении. Далее, комбинации заместителей являются допустимыми только в том случае, если эти комбинации приводят к устойчивым соединениям. Устойчивыми соединениями являются соединения, которые можно выделить из реакционной смеси.
a. Определения
В данном описании и приложенной формуле изобретения, если не указано иное, следующие термины имеют указанные ниже значения:
Термин «алкенил» в настоящем описании означает линейную или разветвленную углеводородную цепь, содержащую от 2 до 10 атомов углерода и по меньшей мере одну двойную углерод-углеродную связь, образованную путем удаления двух атомов водорода. Типовые примеры алкенилов включают, не ограничиваясь этим этенил, 2-пропенил, 2-метил-2-пропенил, 3-бутенил, 4-пентенил, 5-гексенил, 2-гептенил, 2-метил-1-гептенил и 3-деценил.
Термин «алкокси» в настоящем описании означает алкильную группу, соответствующую данному в заявке определению, присоединенную к остальной части молекулы через атом кислорода. Типовые примеры алкоксигрупп включают, не ограничиваясь этим, метокси, этокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси и гексилокси.
Термин «алкоксиалкил» в настоящем описании означает алкоксигруппу, соответствующую данному в заявке определению, присоединенную к остальной части молекулы через алкильную группу, также соответствующую данному в заявке определению. Типовые примеры алкоксиалкилов включают, не ограничиваясь этим, трет-бутоксиметил, 2-этоксиэтил, 2-метоксиэтил и метоксиметил.
Термин «алкил» в настоящем описании означает линейную или разветвленную насыщенную углеводородную цепь, содержащую от 1 до 10 атомов углерода. Термин «низший алкил» или «C1-6 алкил» означает линейный или разветвленный углеводородный остаток, содержащий от 1 до 6 атомов углерода. Термин «C1-3 алкил» означает линейный или разветвленный углеводородный остаток, содержащий от 1 до 3 атомов углерода. Типовые примеры алкилов включают, не ограничиваясь этим, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-нонил и н-децил.
Термин «алкилкарбонил» в настоящем описании означает алкильную группу, соответствующую данному в заявке определению, присоединенную к остальной части молекулы через карбонильную группу, также соответствующую данному в заявке определению. Типовые примеры алкилкарбонилов включают, не ограничиваясь этим, метилкарбонил, этилкарбонил, изопропилкарбонил, н-пропилкарбонил и т.п.
Термин «алкилен» означает двухвалентную группу, образованную линейным или разветвленным углеводородным остатком, включающим от 1 до 10 атомов углерода. Типовые примеры алкилена включают, не ограничиваясь перечисленными, -CH2-, -CH(CH3)-, -C(CH3)2-, -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2- и -CH2CH(CH3)CH2-.
Термин «алкинил» в настоящем описании означает линейный или разветвленный углеводородный остаток, содержащий от 2 до 10 атомов углерода и по меньшей мере одну тройную углерод-углеродную связь. Типовые примеры алкинила включают, не ограничиваясь этим, ацетиленил, 1-пропинил, 2-пропинил, 3-бутинил, 2-пентинил и 1-бутинил.
Термин «арил» в настоящем описании означает фенил или бициклический арил. Бициклический арил представляет собой нафтил или фенил, конденсированный с моноциклическим циклоалкилом, или фенил, конденсированный с моноциклическим циклоалкенилом. Типовые примеры арильных групп включают, не ограничиваясь этим, дигидроиденил, инденил, нафтил, дигидронафталинил и тетрагидронафталинил. Бициклический арил присоединен к остальной части молекулы через любой атом углерода, входящий в бициклическую систему. Арильная группа в настоящем изобретении может быть незамещенной или замещенной.
Термин «карбонил» в настоящем описании означает группу -C(=O)-.
Термин «циано» в настоящем описании означает группу -CN.
Термин «цианоалкил» в настоящем описании означает цианогруппу, соответствующую данному в заявке определению, присоединенную к остальной части молекулы через алкиленовую группу, соответствующую данному в описании определению. Типовые примеры цианоалкила включают, не ограничиваясь этим, цианомет