Амид 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорид, проявляющий антигельминтное действие
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно амиду 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлориду формулы 1. Технический результат: получено новое производное изохинолина, обладающее антигельминтным действием. 1 табл.
Реферат
Изобретение относится к области органической химии, производным изохинолина, а именно, новому биологически активному амиду 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлориду (1) формулы:
обладающему антигельминтным действием, что позволяет предложить его использование в медицине в качестве антигельминтного препарата.
Ближайшими структурными аналогами к заявляемому соединению являются соединения общей формулы 2, проявляющие гипертензивный или гипотензивный эффекты [Синтез амидов 2-(3,3,7-триметил-3,4-дигидроизохинолил-1)-этановой кислоты и их влияние на артериальное давление / Е.С.Лиманский, А.Г.Михайловский, Б.Я.Сыропятов, М.И.Вахрин // Хим. - фарм. журнал. - 2009. - Т.43. - №1. - С.5-7].
Данных об их антигельминтной активности в литературе не имеется.
Целью предлагаемого изобретения является поиск среди производных изохинолина соединений, обладающих антигельминтной активностью.
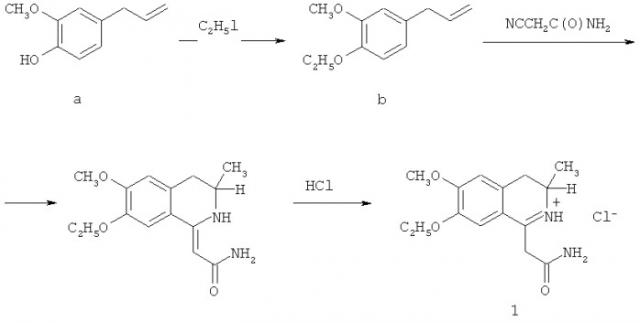
Поставленная цель достигается получением амида 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорида (1), который синтезируют реакцией циклоконденсации алкилированного эвгенола с соответствующим нитрилом. Заявляемое соединение в виде основания было получено ранее [Эвгенол в синтезе производных изохинолиновых алкалоидов / О.В.Сурикова, А.Г.Михайловский, Е.С.Лиманский, М.И.Вахрин // Химия природных соединений. - 2012. - №2 - С.254-256].
Методика получения амида 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорида
Смесь 21.6 мл (0.12 моль) эвгенола (a), 12.1 мл (0,15) моль йодистого этила (йодэтана) и 0.5 г (0.019 моль) 18-краун-6 в присутствии 20 г (0.36 моль) KOH в 150 мл бензола интенсивно перемешивают при температуре 40-50°C в течение двух часов, а затем охлаждают до 20°C. Охлажденный раствор отфильтровывают, промывая щелочь бензолом два раза по 50 мл. Фильтрат отгоняют до объема примерно 70 мл.
К полученному бензольному раствору соединения (b) добавляют 8,4 г (0,1 моль) амида цианоуксусной кислоты (цианоацетамида), 15 мл ледяной уксусной кислоты, а затем по каплям 30 мл концентрированной серной кислоты. Смесь интенсивно перемешивают при температуре 50-60°C в течение 30 минут, после чего выливают в 30 мл ледяной воды и отделяют бензольный слой. Водную фазу нейтрализуют раствором аммиака. Кристаллический осадок основания, выпадающий при охлаждении до 5-7°C, отфильтровывают, сушат, растворяют в 250 мл этилацетата и пропусканием сухого HCl получают гидрохлорид, который отфильтровывают, сушат и перекристаллизовывают из изопропанола.
Выход гидрохлорида 1 составляет 78% в расчете на цианид. Заявляемое соединение представляет собой желтое кристаллическое вещество, растворимое в воде, хлороформе, устойчивое при хранении. Tпл 198°C. Вычислено, % C 57,59; H 6,76; N 8,95; Cl 11,33. C15H20N2O3·HCl. Найдено, % C 58,78; H 6,88; N 8,75; Cl 11,53.
Спектр ЯМР 1H гидрохлорида 1 снят при рабочей частоте 300 МГц, внутренний эталон ГМДС. Спектр соединения 1 (CDCl3, δ, м.д., J, Гц): 1.25 (3H, т, J=7, CH3CH2O); 2.05 (3H, д, J=7, 3-CH3); 2.46 (2H, дд, JAB=9, 4-CH2); 2.82 (1H, м, 3-H); 3.86 (3H, с, CH3O); 3.97 (2H, к, J=7, CH3CH2O); 4.15 (2H, уш.с, CH2CO); 6.98 (1H, с, 5-H); 7.35 (1H, с, 8-H); 8.12 (2H, уш.с, CONH2); 13.07 (1H, с, NH+ цикла).
ИК-спектр снят для соединения 1 в виде основания в растворе CHCl3 в концентрации 0.01 моль/л. Основание соединения 1 получено обработкой раствора соответствующего гидрохлорида раствором NH3 с последующей экстракцией основания эфиром, сушкой и отгонкой растворителя. В ИК-спектре присутствуют уширенные полосы поглощения хелатированных групп C=O (1600-1620 см-1) и NH цикла (3100-3150 см-1). Это свидетельствует о том, что основание молекулы имеет Z-конфигурацию, стабилизированную внутримолекулярной водородной связью.
Соединение 1 исследовали на наличие антигельминтной активности. Антигельминтная активность изучалась на земляных червях по методике Николаева М.П. [Николаев М.П. Экспериментальные основы фармакологии и токсикологии / М.П.Николаев. - М: МЕДГИЗ, 1941. - 195 с.].
В 0,5%-ный раствор исследуемых соединений помещали земляных червей и фиксировали время наступления смерти. В качестве эталонов сравнения использовали пирантел и левамизол. Результаты исследования приведены в таблице.
| Антигельминтная активность заявляемого соединения и эталонов сравнения | ||
| Соединение | Продолжительность жизни червей, мин | ЛД50, мг/кг |
| Пирантел | 215,0±0,37 | 4470 (2983-5815) |
| Левамизол | 20,2±2,08 | 282(159-419) |
| Амид 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорид | 19,0±8,15 | 1290 (606-6820) |
Острую токсичность определяли при пероральном введении нелинейным белым мышам массой 20-25 г. Результаты обрабатывали по Прозоровскому с вычислением средней смертельной дозы (ЛД50) [Прозоровский В.В., Прозоровская М.П., Демченко В.М. // Фармакология и токсикология. - 1978. - Т.41. - №4. - С.497-502]. Острая токсичность (ЛД50) заявляемого соединения составила 1290 (606-6820) мг/кг.
Таким образом, заявляемое соединение 1-амид 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорид проявляет активность, равную активности левамизола, и значительно превосходит по активности пирантел. Заявляемое соединение 1 менее токсичное, чем левамизол (в 4.5 раза) и несколько уступает токсичности пирантела.
Литература
1. Синтез амидов 2-(3,3,7-триметил-3,4-дигидроизохинолил-1)-этановой кислоты и их влияние на артериальное давление / Е.С.Лиманский, А.Г.Михайловский, Б.Я.Сыропытов, М.И.Вахрин // Хим. - фарм. журнал. - 2009. - Т.43. - №1. - С.5-7.
2. Эвгенол в синтезе производных изохинолиновых алкалоидов / А.Г.Михайловский, О.В.Сурикова, Е.С.Лиманский, М.И.Вахрин // Химия природных соединений. - 2012. - №2. - С.254-256.
3. Николаев М.П. Экспериментальные основы фармакологии и токсикологии / М.П.Николаев. - М.: МЕДГИЗ, 1941. - 195 с.
4. Прозоровский В.В., Прозоровская М.П., Демченко В.М. // Фармакология и токсикология. - 1978. - Т.41. - №4. - С.497-502.
Амид 2-(3-метил-6-метокси-7-этокси-3,4-дигидроизохинолил-1)-этановой кислоты гидрохлорид (1), проявляющий антигельминтное действие: