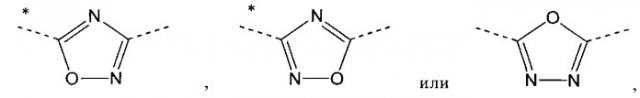
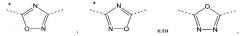
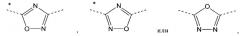
Производные пиридин-4-ила
Иллюстрации
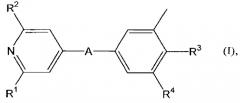
Показать всеНастоящее изобретение относится к соединению формулы (I), где A представляет собой 1,2,4-оксадиазол или 1,3,4-оксадиазол (формулы Ia), где звездочки указывают на связь, через которую осуществляется присоединение к пиридиновой группе формулы (I); R1 представляет собой 3-пентил, 3-метилбут-1-ил, циклопентил или циклогексил; R2 представляет собой метоксигруппу; R3 представляет собой 2,3-дигидроксипропоксигруппу, -ОСН2-СН(ОН)-CH2-NHCO-CH2OH, -OCH2-CH(OH)-CH2N(CH3)-CO-CH2OH, -NHSO2CH3 или -NHSO2CH2CH3; и R4 представляет собой этил или хлор; или его фармацевтически приемлемые соли. Изобретение также относится к фармацевтической композиции, обладающей активностью агонистов S1P1/EDG1 рецептора, включающей эффективное количество соединения формулы (I) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. Технический результат - производные пиридин-4-ила для профилактики или лечения заболеваний или нарушений, связанных с активированной иммунной системой. 3 н. и 23 з.п. ф-лы, 4 табл., 33 пр.
(формула Ia)
Реферат
Область изобретения
Настоящее изобретение относится к агонистам S1P1/EDG1 рецептора (липидактивируемый, сопряженный с G-белком, специфичный в отношении сфингозин-1-фосфата рецептор) формулы (I) и их применению в качестве активных ингредиентов при получении фармацевтических композиций. Изобретение также касается родственных аспектов, включающих способы получения соединений, фармацевтические композиции, содержащие соединение формулы (I), и их применение в качестве соединений, улучшающих сосудистую функцию, и в качестве иммуномоделирующих агентов, либо самостоятельно, либо в комбинации с другими активными соединениями или методами лечения.
Предпосылки создания изобретения
Человеческая иммунная система призвана защищать организм от посторонних микроорганизмов и субстанций, вызывающих инфекцию или болезнь. Комплексные регуляторные механизмы обеспечивают направленность иммунного ответа против внедрившейся субстанции или организма, но не направленного против хозяина. В некоторых случаях в таких контрольных механизмах нарушается регуляция, что может приводить к возникновению аутоиммунных ответов. Следствием неконтролируемого ответа на воспаление является серьезная опасность для органа, клетки, ткани или сустава. При современных методах лечения иммунная система в таких случаях в целом обычно подавляется, но при этом и способность организма реагировать на инфекцию также подвергается серьезному риску. Типичные лекарства, применяемые в этом случае, включают азатиоприн, хлорамбуцил, циклофосфамид, циклоспорин или метотрексат. Кортикостероиды, которые ослабляют воспаление и подавляют иммунный ответ, могут вызывать побочные эффекты при длительном лечении. Нестероидные противовоспалительные препараты (НПВП) могут уменьшать боль и воспаление, однако, они также проявляют нежелательные побочные эффекты. Альтернативные методы лечения включают применение агентов, активирующих или блокирующих цитокиновую передачу сигнала.
Орально активные соединения с иммуномоделирующими свойствами, без опасных иммунных ответов и с пониженными побочными эффектами значительно улучшают современные методы лечения воспалительных заболеваний.
В области трансплантации органов иммунный ответ хозяина должен быть подавлен для предотвращения отторжения органа. Трансплантируемый орган реципиента может подвергаться риску частичного отторжения даже при использовании иммунодепрессивных лекарств. Отторжение чаще всего происходит в первые несколько недель после трансплантации, но случаи отторжения могут наступить также и спустя несколько месяцев, или даже лет, после трансплантации. Комбинации вплоть до трех или четырех лекарственных препаратов, используемых вместе, максимально защищают от отторжения и при этом минимизируют побочные эффекты. Современные стандартные лекарства, используемые для лечения отторжения трансплантируемых органов, входят во взаимодействие с дискретным метаболизмом при активации Т-типа или В-типа лимфоцитов. Примерами таких лекарств являются циклоспорин, даклицумаб, вазиликсимаб, эверолимусили FK506, которые взаимодействуют с процессами цитокиновой секреции или передачи сигнала; азатиоприн или лефлуномид, которые ингибирует синтез нуклеотидов; или 15-деоксиспергуалин, являющийся ингибитором дифференцировки лейкоцитов.
Наилучшие результаты, полученные при иммуносупрессивной терапии крови, относятся к действию, оказываемому этими лекарственными препаратами; однако генерализованная иммуносупрессия, которая достигается с помощью этих лекарств, ослабляет иммунную защиту организма против инфекции и злокачественных новообразований. Кроме того, стандартные иммуносупрессивные лекарства часто используются в больших дозах и могут вызывать или ускорять повреждение органа.
Описание изобретения
Настоящее изобретение предлагает новые соединения формулы (I), которые являются агонистами для G белка-сопряженного рецептора S1P1/EDG1 и обладают сильнодействующим и продолжительным иммуномоделирующим эффектом, который достигается посредством сокращения числа циркулирующих и инфильтрацирующих Т- и В-лимфоцитов, без оказания при этом повреждающего воздействия на их созревание, память или экспансию. Сокращение циркуляции Т-/В-лимфоцитов в результате S1P1/EDG1 агонизма, вероятно в комбинации с наблюдаемым улучшением функции эндотелиального клеточного слоя, ассоциируемого с S1P1/EDG1 активацией, делает возможным применение таких соединений для лечения неконтролируемой воспалительной болезни и улучшения сосудистой функциональности. Являющийся документом предыдущего уровня техники WO 2008/029371 раскрывает соединения, относящиеся к агонистам S1P1/EDG1 рецептора и проявляющие иммуномоделирующий эффект, как описано выше. Неожиданно было найдено, что соединения по настоящему изобретению проявляют потенциальную способность снижать суживание тканей/сосудов верхних дыхательных путей по сравнению с соединениями, описанными в документе предыдущего уровня техники WO 2008/029371. Соединения по настоящему изобретению превосходят их в отношении профиля безопасности, например понижают риск возникновения бронхосуживающего эффекта.
Примеры документа WO 2008/029371, которые рассматриваются как предыдущие аналоги из области техники, представлены на Фиг.1:
Фиг.1: Структура примеров документа предыдущего уровня техники WO2008/029371, которые рассматриваются как близкие аналоги из области техники соединений по настоящему изобретению.
Данные по суживанию хрящевых колец трахеи крыс, приведенные в таблице 1, иллюстрируют превосходство соединений по настоящему изобретению по сравнению с соединениями, описанными в документе предыдущего уровня техники WO 2008/029371.
Например, соединения примера 1 и 6 по настоящему изобретению проявляют значительное понижение способности суживания хрящевых колец трахеи крыс по сравнению с соединениями примеров 222 и 226 предыдущего уровня техники, описанными в WO2008/029371, соответственно. Кроме того, соединения примеров 1 и 6 по настоящему изобретению также проявляют значительное понижение способности суживания хрящевых колец трахеи крыс по сравнению с соединениями примеров 196 и 204 предыдущего уровня техники, описанными в WO 2008/029371, соответственно. Эти данные демонстрируют, что соединения, где R1 представляет собой 3-фенил и R2 представляет собой метоксигруппу, значительно превосходят соединения предыдущего уровня техники, описанные в WO 2008/029371, то есть соединения, где R1 представляет собой изобутил и R2 представляет собой метоксигруппу или R1 представляет собой метил и R2 представляет собой 3-пентил. Кроме того, соединение примера 16 по настоящему изобретению, где R1 представляет собой 3-метилбут-1-ил и R2 представляет собой метоксигруппу, проявляет заметно пониженную способность к суживанию хрящевых колец трахеи крыс по сравнению с аналогичными соединениями примера 226 предыдущего уровня техники, описанными в WO 2008/029371, где R1 представляет собой изобутил и R2 представляет собой метоксигруппу.
Неожиданное превосходство соединений по настоящему изобретению также стало очевидным, когда выяснилось, что соединения примеров 2 и 7 по настоящему изобретению проявляют заметно пониженную способность к суживанию хрящевых колец трахеи крыс по сравнению с аналогичными соединениями примеров 229 и 233 предыдущего уровня техники, описанными в WO 2008/029371, соответственно. Это доказывает, что соединения, где R1 представляет циклопентил и R2 представляет метоксигруппу, превосходят соединения предыдущего уровня техники, описанные в WO 2008/029371, то есть соединения, где R1 представляет собой метил и R2 представляет циклопентил.
Также соединение примера 3 по настоящему изобретению проявляют такую же пониженную способность к суживанию хрящевых колец трахеи крыс, как и его S-энантиомер, то есть соединение примера 2 по настоящему изобретению, что указывает на то, что конфигурация этого положения не оказывает значительного влияния на суживание трахеи. Кроме того, пример 21 по настоящему изобретению также проявляет такую же пониженную способность к суживания хрящевых колец трахеи крыс, как и указанный пример 2, который отличается от примера 21 только связующим звеном А (образуя 5-пиридин-4-ил-[1,2,4]оксадиазол вместо 3-пиридин-4-ил-[1,2,4]оксадиазола). Это указывает на то, что природа оксадиазола также не оказывает критического влияния в отношении суживания трахеи.
| Таблица 1 | ||
| Суживание трахеи крыс в % по отношению к суживанию, вызываемому 50 мМ КСl (Экспериментальные подробности и дополнительные данные представлены в примере 33) | ||
| Соединение | Суживание трахеи (%) | |
| при 1 мкМ | при 10 мкМ | |
| Пример 196 предыдущего уровня техники | 82 | не определено |
| Пример 204 предыдущего уровня техники | 112 | не определено |
| Пример 222 предыдущего уровня техники | <5 | 124 |
| Пример 226 предыдущего уровня техники | 133 | не определено |
| Пример 229 предыдущего уровня техники | 18 | не определено |
| Пример 233 предыдущего уровня техники | 120* | не определено |
| Пример 1 | <5 | 24 |
| Пример 2 | <5 | <5 |
| Пример 3 | <5 | не определено |
| Пример 6 | <5 | 100 |
| Пример 7 | 50 | не определено |
| Пример 16 | <5 | не определено |
| Пример 21 | <5 | не определено |
| * результат, полученный с концентрацией соединения 300 нМ. |
Соединения по настоящему изобретению могут применяться самостоятельно или в комбинации со стандартными лекарственными средствами, ингибирующими Т-клеточную активацию, предоставляя новую иммуномоделирующую терапию с пониженной предрасположенностью к инфекциям по сравнению со стандартной иммуносупрессивной терапией. Кроме того, соединения по настоящему изобретению могут применяться в комбинации с пониженными дозами лекарств, традиционно используемых в иммуносупрессивной терапии для предоставления иммуномоделирующей активности, что является очень важным, учитывая, что снижение повреждения пересаженного органа ассоциируется с применением более высоких дозиммуносупрессивных лекарств. Результаты наблюдения по улучшению функции эндотелиального клеточного слоя, ассоциируемого с S1P1/EDG1 активацией, дополнительно свидетельствуют в пользу рассматриваемых соединений в связи с вызываемым ими улучшением сосудистой функции.
Нуклеотидная и аминокислотная последовательности для человеческого S1P1/EDG1 рецептора известна из области техники по публикациям, например, в: Нlа, Т., and Maciag, Т.J.Biol. Chem., 265 (1990), 9308-9313; WO 91/15583 (опубликован 17 октября 1991 г.); WO 99/46277 (опубликован 16 сентября 1999 г.). Потенциальная возможность и эффективность соединений формулы (I) исследовались с помощью GTPγS анализа по определению ЕС50 величин и посредством измерения циркулирующих лимфоцитов у крыс после орального введения соответственно (см. в экспериментальной части).
i) В первом варианте осуществления настоящее изобретение относится к соединениям пиридина формулы (I)
где
А представляет собой
, или ,
где звездочки указывают на связь, через которую осуществляется присоединение к пиридиновой группе формулы (I);
R1 представляет 3-пентил, 3-метилбут-1-ил, циклопентил или циклогексил;
R2 представляет метоксигруппу;
R3 - представляет 2,3-дигидроксипропоксигруппу, -OСН2-СН(OН)-СН2-NHCO-CH2OH, -ОСН2-СН(ОН)-СН2Н(СН3)-СО-СН2ОН, -NHSO2CH3 или -NHSO2CH2CH3; и
R4 представляет этил или хлор.
ii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно варианту i), где стереоцентр R3 групп 2,3-дигидроксипропоксигруппы, -OCH2-CH(OH)-CH2-NHCO-CH2OH и -ОСН2-CH(OH)-CH2N(CH3)-CO-CH2OH находится в S-конфигурации.
iii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно варианту 1), где стереоцентр R3 групп 2,3-дигидроксипропоксигруппы, -OCH2-CH(OH)-CH2-NHCO-CH2OH и -ОСН2-СН(ОН)-СН2N(СН3)-СО-СН2ОН находится в R-конфигурации.
iv) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-iii), где А представляет собой
,
где звездочка указывает на связь, через которую осуществляется присоединение к пиридиновой группе формулы (I).
v) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-iii), где А представляет собой
где звездочка указывает на связь, через которую осуществляется присоединение к пиридиновой группе формулы (I).
vi) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-iii), где А представляет собой
vii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-vi), где R1 представляет собой 3-пентил.
viii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-vi), где R1 представляет собой 3-метилбут-1-ил.
ix) Другой вариант осуществления настоящего изобретения относится к пиридиновым производным согласно одному из вариантов i)-vi), где R1 представляет собой циклопентил.
x) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-vi), где R1 представляет собой циклогексил.
xi) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-x), где R3 представляет собой 2,3-дигидроксипропоксигруппу.
xii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-x), где R3 представляет собой -OCH2-CH(OH)-CH2-NHCO-CH2OH.
xiii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-x), где R3 представляет собой -OCH2-CH(OH)-CH2N(CH3)-CO-CH2OH.
xiv) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-x), где R3 представляет собой -NHSO2CH3.
xv) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-x), где R3 представляет собой -NHSO2CH2CH3.
xvi) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-xv), где R4 представляет собой этил.
xvii) Другой вариант осуществления настоящего изобретения относится к производным пиридина согласно одному из вариантов i)-xv), где R представляет собой хлор.
Соединения формулы (I) могут содержать один или более стереогенных или асимметрических центров таких, как один или более асимметрических атомов углерода. Соединения формулы (I) могут таким образом присутствовать в виде смеси стереоизомеров или предпочтительно в виде чистых стереоизомеров. Смеси стереоизомеров могут быть разделены с использованием методов, известных специалистам в области техники.
При использовании множественной формы для соединений, солей, фармацевтических композиций, болезней и им подобных терминов, имеется в виду также единичная форма соединения, соли или им подобных терминов.
Любая ссылка выше и далее на соединение формулы (I) подразумевает также ссылку на соли, особенно фармацевтически приемлемые соли соединения формулы (I), и ее использование является уместным и целесообразным.
Термин "фармацевтически приемлемые соли" относится к нетоксичным, аддитивным солям неорганической или органической кислоты и/или основания. Более подробные данные могут быть найдены в публикации "Salt selection for basic drugs", Int. J. Pharm. (1986), 33, 201-217.
Настоящее изобретение также включает меченные радиоактивными изотопами, особенно 2Н (дейтерием), соединения формулы (I), которые идентичны соединениям формулы (I) за исключением того, что один или более атомов замещены атомом, имеющим тот же самый атомный номер, но атомную массу, отличную от атомной массы, обычно встречающейся в природе. Меченные изотопами, особенно 2Н (дейтерием), соединения формулы (I) и их соли включены в объем настоящего изобретения. Замещение водорода более тяжелым изотопом 2Н (дейтерием) или может привести к большей метаболической активности, в результате чего, например, увеличивается в условиях in vivo время полураспада или уменьшаются требования к дозированию, или может привести к снижению ингибирования цитохром Р450 ферментов, в результате чего, например, улучшается профиль безопасности. В одном варианте изобретения соединения формулы (I) не являются меченными изотопами или мечены только одним или более атомами. В подварианте соединения формулы (I) вообще не мечены изотопами. Меченные изотопами соединения формулы (I) могут быть получены аналогично методам, описанным далее, но с использованием соответствующих изотопных вариантов подходящих реагентов или исходных материалов.
Примеры пиридиновых соединений согласно формуле (I) выбраны из группы, включающей:
(S)-3-(2-этил-4-{5-[2-(1-этилпропил)-6-метоксипиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенокси)пропан-1,2-диол;
(S)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
(R)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
(S)-3-{4-[5-(2-циклогексил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
{2-хлор-4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метилфенил}амид этансульфоновой кислоты;
N-[(S)-3-(2-этил-4-{5-[2-(1-этилпропил)-6-метоксипиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенокси)-2-гидроксипропил]-2-гидроксиацетамид;
N-((S)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид;
N-((S)-3-{4-[5-(2-циклогексил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид;
N-((S)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидрокси-N-метилацетамид;
N-(2-хлор-4-{5-[2-(1-этилпропил)-6-метоксипиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенил)метансульфонамид;
N-{2-хлор-4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метйлфенил}метансульфонамйд;
(S)-3-{2-хлор-4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метилфенокси}пропан-1,2-диол;
N-((S)-3-{2-хлор-4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид;
(S)-3-(2-этил-4-{5-[2-метокси-6-(3-метилбутил)пиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенокси)пропан-1,2-диол;
N-[(S)-3-(2-этил-4-{5-[2-метокси-6-(3-метилбутил)пиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенокси)-2-гидроксипропил]-2-гидроксиацетамид;
N-{2-хлор-4-[5-(2-циклогексил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метилфенил}метансульфонамид;
N-(2-этил-4-{5-[2-(1-этилпропил)-6-метоксипиридин-4-ил]-[1,2,4]оксадиазол-3-ил}-6-метилфенил)метансульфонамид;
N-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенил}метансульфонамид;
N-{4-[5-(2-циклогексил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-2-этил-6-метилфенил}метансульфонамид;
(S)-3-{4-[3-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-5-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
(R)-3-{4-[3-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-5-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
N-((S)-3-{4-[3-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-5-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид;
N-((R)-3-{4-[3-(2-циклопентил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-5-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид;
(S)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
(R)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-2-этил-6-метилфенокси}пропан-1,2-диол;
N-((S)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид; и
N-((R)-3-{4-[5-(2-циклопентил-6-метоксипиридин-4-ил)-[1,3,4]оксадиазол-2-ил]-2-этил-6-метилфенокси}-2-гидроксипропил)-2-гидроксиацетамид.
Примеры пиридиновых соединений согласно формуле (I) также выбраны из группы, включающей:
(S)-3-{2-хлор-4-[5-(2-циклогексил-6-метоксипиридин-4-ил)-[1,2,4]оксадиазол-3-ил]-6-метилфенокси}пропан-1,2-диол; и
N-(2-этил-4-(5-(2-изопентил-6-метоксипиридин-4-ил)-1,2,4-оксадиазол-3-ил)-6-метилфенил)метансульфонамид.
Соединения формулы (I) и их фармацевтически приемлемые соли могут быть применены в качестве лекарственных средств, например в форме фармацевтических композиций для энтерального или парентерального введения, и являются пригодными для уменьшения количества циркулирующих лимфоцитов и для профилактики и/или лечения заболеваний или нарушений, связанных с активированной иммунной системой.
Приготовление фармацевтических композиций может быть осуществлено с использованием методов, известных любому специалисту в области техники (см., например: Remington, The Science and Practice of Pharmacy, 21st Edition (2005), Part 5, "Pharmaceutical Manufacturing" [published by Lippincott Williams & Wilkins]) посредством введения соединений формулы (I) или их фармацевтически приемлемых солей, необязательно в комбинации с другими терапевтически полезными субстанциями, в лекарственную форму вместе с соответствующим, нетоксичным, инертным, фармацевтически приемлемым твердым или жидким веществом, используемым в качестве носителя, и, если необходимо, стандартными фармацевтическими наполнителями.
Фармацевтические композиции, включающие соединение формулы (I) применимы для профилактики и/или лечения заболеваний или нарушений, ассоциированных с активированной иммунной системой.
Такие заболевания или нарушения, ассоциированные с активированной иммунной системой, для профилактики и/или лечения которых могут применяться соединения формулы (I), включают отторжение пересаженных органов, тканей или клеток; болезни «трансплантат против хозяина», возникающие при трансплантации; аутоиммунные синдромы, включая ревматоидный артрит; системную красную волчанку; антифосфолипидный синдром; тироидит Хашимото; лимфотический тироидит; рассеянный склероз; тяжелую псевдопаралитическую миастению; диабет типа I; увеит (воспаление сосудистой оболочки глаза); эписклерит; склерит; болезнь Кавасаки, увеоритинит; задний увеит; увеит, связанный с болезнью Бехчета; синдром увеоменингита; аллергический энцефаломиелит; хроническую аллотрансплантатную васкулопатию; постинфекционные аутоиммунные болезни, включая ревматическую лихорадку и постинфекционный гломерулонифрит; воспалительные и гиперпролиферативные кожные болезни; псориаз; псориатический артрит; атопический дерматит; миопатию; миозит; остеомиелит; контактный дерматит; экзематозный дерматит; себоррейный дерматит; плоский лишай; пузырчатку; буллезную пузырчатку; врожденный буллезный эпидермолиз; крапивницу; ангиодему; васкулит; эритему; кожную эозинофилию; угри; склеродерму; гнездную алопецию; кератоконъюнктивит; хронический двухсторонний конъюнктивит; кератит; герпический кератит; эпителиальную дистрофию роговицы; лейкому роговицы; глазную пузырчатку; язву Мурена; язвенный керотит; склерит; офтальмопатию Гравса; синдром Вогта-Коунаги-Харада; саркоидоз; сенную лихорадку; обратимую обструктивную болезнь дыхательных путей; бронхиальную астму; аллергическую астму; врожденную астму; полученную извне астму; пылевую астму; хроническую или застарелую астму; позднюю астму и гипервосприимчивость дыхательных путей; бронхиолит; бронхит; эндометриоз; орхит; язву желудка; ишемические болезни кишечника; воспалительные болезни кишечника; некротический энтероколит; повреждения кишечного тракта, связанные с термальными ожогами; болезнь брюшины; проктит; эозинофильный гастроэнтерит; мастоцитоз; болезнь Крона; язвенный колит; сосудистые повреждения, вызванные ишемической болезнью и тромбозом; атеросклероз; тучное сердце; миокардит; инфаркт миокарда; синдром воспаленной аорты; общий упадок сил, вызванный вирусной болезнью; тромбоз сосудов; мигрень; ринит; экзему; интерстициальный нефрит; IgA-индуцированную нефропатию; синдром Гудпасчера; гемолитико-уремический синдром; диабетическую нефропатию; гломерулосклероз; гломерулонефрит; табулоинтерстициальный нефрит; интерстициальный цистит; дерматомиозит; синдром Гийена-Барре; болезнь Миньера; полиневрит; мультиплетный неврит; миелит; мононеврит; радикулопатию; гипертиоридизм; базедову болезнь; тиротоксикоз; беспримесную красноклеточную аплазию; апластическую анемию; гипопластическую анемию; идиопатическую тромбоцитопеническую пурпуру; аутоиммунную гемолитическую анемию; аутоиммунную тромбоцитопению; агранулоцитоз; злокачественную анемию; мегалобластическую анемию; анеритроплазию; остеопароз; фиброидное легкое; идиопатическую интерстициальную пневмонию; дерматит; лейкодерму vulgaris; диффузную кератому vulgaris; фотоаллергическую чувствительность; кожную Т-клеточную лимфому; нодозный полиартрит; хорею Хантингтона; хорею Сиденхама; миокардоз; миокардит; склеродерму; гранулому Вегенера; синдром Шегрена; адипоз; эозинофильный фасцит; повреждения десен, периодонта, альвеольной соединительной ткани, зубной субстанции при лечении; мужскую очаговую алопецию или старческую алопецию; мускульную дистрофию; пиодерму; синдром Сезари; гипофизит; хроническую недостаточность надпочечников; болезнь Аддисона; ишемически-реперфузионное повреждение органов, имеющее место при хранении; эндотоксический шок; псевдомембранный колит; колит, вызываемый лекарством или радиацией; острую ишемическую почечную недостаточность; хроническую почечную недостаточность; рак легкого; злокачественность лимфоидного происхождения; острую или хроническую лимфотическую лейкемию; лимфому; энфизему легких; катаракту; сидероз; воспаление сетчатой оболочки глаза; старческую пятнистую дегенерацию; рубцевание стекловидного тела; щелочной ожог роговицы; дерматитную эритему; буллезный дерматит; цементный дерматит; воспаление десен; периодонтит; сепсис; панкреатит; болезнь периферийных артерий; карциогенез; твердые раковые опухоли; метастаз карциномы; гепербаропатию; аутоиммунный гепатит; первичный цирроз печени; склеротический холангит; частичную резекцию печени; острый некроз печени; цирроз; алкогольный цирроз; печеночную недостаточность; скоротечную печеночную недостаточность; скрытую печеночную недостаточность; и "нацеленную на хроническую" печеночную недостаточность.
Предпочтительные заболевания и нарушения, подлежащие лечению и/или профилактике с помощью соединений формулы (I), выбирают из группы, включающей отторжение пересаженных органов таких, как почка, печень, сердце, легкое, поджелудочная железа, роговица и кожа; болезни «трансплантат против хозяина», возникающие при трансплантации клеток спинного мозга; аутоиммунные синдромы, включающие ревматоидный артрит, рассеянный склероз, воспалительные заболевания кишечника такие, как болезнь Крона и язвенный колит, псориаз, псориатический артрит, тироидит такой, как тироидит Хашимото, увеоретинит; атопические болезни такие, как ринит, конъюнктивит, дерматит; астму; диабет типа I; постинфекционные аутоиммунные болезни, включая ревматоидную лихорадку и постинфекционный гломерулонефрит; твердые виды рака и опухолевое метастазирование.
Особенно предпочтительные заболевания или нарушения, подлежащие лечению и/или профилактике с помощью соединений формулы (I), выбирают из группы, включающей отторжение пересаженных органов таких, как почка, печень, сердце и легкое; болезнь «трансплантат против хозяина», возникающуя при трансплантации клеток спинного мозга; аутоиммунные синдромы, включающие ревматоидный артрит, рассеянный склероз, псориаз, псориатический артрит, болезнь Крона и тироидит Хашимото; и атопический дерматит. Наиболее предпочтительными заболеваниями или нарушениями, подлежащими лечению и/или профилактике с помощью соединений формулы (I), являются рассеянный склероз и псориаз.
Настоящее изобретение относится также к способу профилактики или лечения заболеваний или нарушений, упомянутых в описании выше, заключающемуся во введении субъекту фармацевтически активного количества соединения формулы (I).
Кроме того, соединения формулы (I) также применяются в комбинации с одним или несколькими иммуномоделирующими агентами, используемыми для профилактики и/или лечения заболеваний или нарушений, упомянутых в описании выше. Согласно предпочтительному варианту осуществления изобретения названные агенты выбираются из группы, включающей иммуносупрессанты, кортикостероиды, НПВП, цитотоксические лекарства, ингибиторы молекулярной адгезии, цитокины, ингибиторы цитокинов, антагонисты рецептора цитокина и рекомбинантные рецепторы цитокина.
Настоящее изобретение относится также к применению соединения формулы (I) для получения фармацевтической композиции необязательно для применения в комбинации с одним или несколькими иммуномоделирующими агентами, используемыми для профилактики и/или лечения заболеваний или нарушений, упомянутых в описании выше.
Соединения формулы (I) могут быть получены методами, приведенными ниже, методами, приведенными в примерах, или аналогичными методами. Оптимальные реакционные условия варьируются в зависимости от применяемых реагентов или растворителей, причем такие условия могут быть выбраны специалистом в области техники с помощью ряда оптимизированных методик.
Соединения формулы (I) по настоящему изобретению могут быть получены согласно общей последовательности реакций, представленной ниже. Далее описаны только некоторые из возможных синтетических путей, приводящих к соединениям формулы (I).
Соединения формулы (I), которые представляет производное 5-пиридин-4-ил-[1,2,4]оксадиазола, получают реакцией соединения структуры (1) в растворителе таком, как толуол, пиридин, ДМФ, ТГФ, диоксан, ДМЭ и им подобные, при комнатной температуре или повышенных температурах, в присутствии или отсутствие вспомогательных веществ таких, как кислоты (например, трифторуксусная кислота, уксусная кислота, НСl и т.п.), основания (например, NaH, NaOAc, Nа2СО3, К2СО3, NEt3 и т.п.), соли тетраалкиламмония или поглощающих воду агентов (например, оксалилхлорид, ангидрид карбоновой кислоты, POCl3, PCl5, Р4О10, молекулярные сита, реагент Бургесса и т.п.) (Литература: например, A.R.Gangloff, J.Litvak, Е.J.Shelton, D.Sperandio, V.R.Wang, K.D.Rice, Tetrahedron Lett., 42 (2001), 1441-1443; T.Suzuki, K.Iwaoka, N.Imanishi, Y.Nagakura, K.Miyta, H.Nakahara, M.Ohta, T.Mase, Chem. Pharm. Bull., 47 (1999), 120-122; R.F.Poulain, A.L.Tartar, B.P.Deprez, Tetrahedron Lett., 42 (2001), 1495-1498; R.M.Srivastava, F.J.S.Oliveira, D.S.Machado, R.M.Souto-Maior, Synthetic Commun., 29 (1999), 1437-1450; E.O.John, J.M.Shreeve, Inorganic Chemistry, 27 (1988), 3100-3104; B.Kaboudin, K.Navaee, Heterocycles, 60 (2003), 2287-2292).
Соединения структуры (1) могут быть получены реакцией соединения структуры (2) с соединением структуры (3) в растворителе таком, как ДМФ, ТГФ, ДХМ и им подобные, в присутствии одного или более конденсирующих агентов таких, как ТБТУ, ДЦК, ЭДК, ГБТУ, КДИ и им подобные, и в присутствии или отсутствие основания такого, как NEt3, ДИПЭА, NaH, К2СО3 и им подобные. (Литература: например, A. Hamze, J.-F. Hernandez, P. Fulcrand, J. Martinez, J. Org. Chem., 68 (2003) 7316-7321; и литература, цитируемая выше).
Соединения формулы (I), которые представляет производное 3-пиридин-4-ил-[1,2,4]оксадиазола, получают аналогичным методом. (Литература: например, С.Т. Brain, J. М. Paul, Y. Loong, P. J. Oakley, Tetrahedron Lett., 40 (1999) 3275-3278) посредством реакции соединения структуры (4) с соединением структуры (5) и последующей циклизации соответствующего промежуточного гидроксиамидинового сложного эфира.
Соединения структуры (3) и (4) могут быть получены реакцией соединения структуры (6) и (7) соответственно с гидроксиламином или одной из его солей в растворителе таком, как МеОН, EtOH, пиридин и им подобные, в присутствии или отсутствие основания такого, как Nа2СО3, К2СО3, трет-бутипат калия, NEt3 и им подобные. (Литература: например, Е.Meyer, А.С.Joussef, Н.Gallardo, Synthesis, 2003, 899-905, WO 2004/035538 (Merck & Co., Inc., USA)).
В зависимости от природы функциональных групп, присутствующих в остатке R3 в структурах (3), (5) и (6), этим функциональным группам может потребоваться временная защита. Соответствующие защитные группы известны специалистам в области техники и включают, например, бензильную или триалкилсилильную группу для защиты спирта, кетальную группу для защиты диола, и т.п. Эти защитные группы могут быть введены с использованием стандартных методов (например, Т.W.Greene, P.G.М.Wuts, Protective Groups in Organic Synthesis, 3rd Edition, Wiley New York, 1991; P.J.Kocienski, Protecting Groups, Thieme Stuttgart, 1994). Альтернативно, требуемые остатки R3 и R4, в частности R3, могут быть также введены на более поздних стадиях, которые, например, следуют за конденсацией пиридиновых соединений структуры (2) или (4) с фенильными производными структуры (3) или (5) с использованием соответствующего предшественника соединения структуры (3) и (5). Фенильные соединения структуры (3), (5) и (6) или их предшественники являются либо коммерчески доступными, либо могут быть получены согласно методам, известным специалисту в области техники.
Соединения формулы (I), которые представляет производное 2-пиридин-4-ил-[1,3,4]оксадиазола, получают подобным образом посредством реакции соединения структуры (2) с гидразином (с использованием конденсирующего агента такого, как ТБТУ, ДЦК, ЭДК, ГБТУ, РуБОФ, КДИ и им подобные) с образованием соединения структуры (8), которое затем конденсируют с соединением структуры (5), получая соединение структуры (9). Соединение структуры (9) может быть также получено следующим обратным реакционным путем, то есть посредством первоначальной конденсации соединения структуры (5) с гидразином и последующей реакции соответствующего промежуточного гидразида с соединением структуры (2). Дегидратация соединения структуры (9) для образования требуемого производного 2-пиридин-4-ил-[1,3,4]оксадиазола осуществляют путем обработки соединения структуры (9) таким реагентом, как POCl3, ССl4 или СВr4 в комбинации с PPh3, Р2О5, реагентом Бургесса и им подобные, в растворителе таком, как толуол, MeCN, диоксан, ТГФ, CHCI3 и им подобные, при температурах от 20 до 120°С в присутствии или отсутствие микроволнового облучения. (Литература: например, М.A.Garcia, S.Martin-Santamaria, М.Cacho, F.Moreno de la Llave, M.Julian, A.Martinez, B.De Pascual-Teresa, A.Ramos, J.Med. Chem., 48 (2005) 4068-4075; С.T.Brain, J.M.Paul, Y.Loong, P.J.Oakley, Tetrahedron Lett., 40 (1999) 3275-3278).
Методы, применяемые для перевода соединения структуры (2) или (5) в соединение структуры (7) или (6) соответственно, или наоборот, известны специалистам в области техники.
Соединения структуры (2) могут быть получены реакцией 2,6-дихлоризоникотиновой кислоты или ее соответствующего сложноэфирного производн