Составы таблетки с немедленным высвобождением
Иллюстрации
Показать всеПредложена группа изобретений, касающаяся лечения гипергликемии у пациентов с сахарным диабетом II типа и не вызывающая увеличения веса. Предложены: состав с немедленным высвобождением в форме таблетки, исходного гранулята или капсулы, содержащий дапаглифлозин или пропилегликольгидрат дапаглифлозина (S), гидрохлорид метформина, гидроксипропилцеллюлозу, микрокристаллическую целлюлозу, натриевый гликолят крахмала или гидроксипропилцеллюлозу с низкой степенью замещения в качестве разрыхлителя и стеарат магния; комбинация указанной фармацевтической композиции с противодиабетическим средством и комбинация указанной фармацевтической композиции со средством для снижения массы тела. Технический результат состоит в реализации заявленного назначения таблеток, а также в улучшенной однородности содержания, пределов прочности и времени дезинтеграции состава заявленного изобретения. 3 н. и 22 з.п. ф-лы, 3 ил., 14 пр.
Реферат
Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к фармацевтическому составу с немедленным высвобождением, который включает состав таблетки или капсулы, содержащий метформин, ингибитор натрий-зависимого переносчика глюкозы (SGLT2), и необязательно покрытие. Настоящее изобретение также относится к способам получения составов и способам лечения заболеваний или нарушений, связанных с активностью SGLT2, с использованием этих составов.
Предшествующий уровень техники настоящего изобретения
Сахарный диабет II типа является наиболее распространенной формой сахарного диабета, являющейся причиной 90% случаев сахарного диабета. Более 100 миллионов человек во всем мире страдают сахарным диабетом II типа (около 17 миллионов в США), и уровень распространения резко увеличивается как в развитых, так и в развивающихся странах. Сахарный диабет II типа является пожизненным заболеванием, которое обычно начинается в среднем возрасте или позже, хотя может начаться в любом возрасте. Больные сахарным диабетом II типа не реагируют должным образом на инсулин - гормон, который в норме обеспечивает в организме превращение глюкозы в крови в энергию или хранение ее в клетках до дальнейшего использования. Проблема сахарного диабета II типа заключается в состоянии, называемом инсулиновой резистентностью, при котором организм продуцирует инсулин в нормальных или даже больших количествах, но определенные механизмы препятствуют перемещению инсулином глюкозы в клетки. Поскольку организм не использует инсулин должным образом, содержание глюкозы в крови повышается до опасных уровней.
Со временем стойкая гипергликемия приводит к глюкотоксичности, которая усугубляет инсулиновую резистентность и способствует дисфункции бета-клеток поджелудочной железы. Степень стойкой гипергликемии напрямую связана с микрососудистыми осложнениями сахарного диабета, а также может способствовать макрососудистым осложнениям. Таким образом, гипергликемия поддерживает цикл вредных эффектов, которые препятствуют лечению сахарного диабета II типа и усиливают осложнения.
В настоящее время общепризнанным является тот факт, что контроль за уровнем глюкозы в крови приносит пользу больным сахарным диабетом II типа. На сегодняшний момент целью терапии сахарного диабета является достижение и поддержание по возможности нормальной гликемии для предотвращения хронических микрососудистых и макрососудистых осложнений, связанных с повышенным уровнем глюкозы в крови. Возможные методы перорального лечения сахарного диабета II типа предусматривают использование соединений, известных как сульфонилмочевины, бигуаниды (метформин), тиазолидиндионы и ингибиторы альфа-глюкозидазы. Активные агенты каждого класса пациентам обычно вводят отдельно. Однако, если монотерапии недостаточно, эффективным и рациональным способом действия для лечения гипергликемии становится комбинированная терапия.
Недавно был открыт новый класс противодиабетических средств, известный как ингибиторы переносчика натрия и глюкозы 2 (SGLT2). Ингибиторы SGLT2 предотвращают реабсорбцию почками глюкозы в кровь. Почки сначала позволяют глюкозе переходить из крови в мочевой пузырь. Однако, когда глюкоза оказывается в моче, она реабсорбируется обратно в кровь в проксимальных почечных канальцах. Девяносто процентов реабсорбции глюкозы в почках происходит в проксимальных почечных канальцах. SGLT2 является белком, преимущественно экспрессируемым в проксимальных почечных канальцах и, вероятно, является основным переносчиком, ответственным за эту реабсорбцию.
Соответственно, настоящее изобретение относится к фармацевтическим составам, содержащим метформин и ингибитор SGLT2, такой как дапаглифлозин, предназначенным для перорального введения при лечении заболеваний или нарушений, связанных с активностью SGLT2. Составы метформина/SGLT2 по настоящему изобретению обеспечивают пациентам противодиабетическое лечение, которое является как удобным, так и эффективным для контроля содержания глюкозы в крови.
Однако успешное составление фармацевтической композиции, содержащей комбинацию дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) и метформина, в гранулах или в составе таблетки, является затруднительным по нескольким причинам.
Во-первых, большое отношение между содержаниями метформина и ингибитора SGLT2 делает важным вопрос однородности содержания в отношении дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) в конечном составе. Необходимо равномерно распределить это относительно малое количество дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) в конечных гранулах и, таким образом, избежать какого-либо отклонения в содержании.
Дополнительно, большая разница в физических свойствах дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) и метформина, а в особенности слабая сжимаемость метформина, создает сложности для производства таблеток, характеризующихся приемлемой механической прочностью.
После нескольких неудачных попыток, включая сухое гранулирование с помощью вальцевания и традиционное влажное гранулирование, теперь обнаружено, что оба вышеуказанных требования могут быть удовлетворены с помощью распыления раствора или суспензии, содержащих дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S) и связующее вещество, на частицы метформина в аппарате с псевдоожиженным слоем, благодаря чему получаются гранулы, которые характеризуются однородным содержанием дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) и хорошей сжимаемостью. Хорошая сжимаемость этих гранул, предположительно, является результатом способа формирования гранул в ходе распылительного процесса гранулирования наряду с тем фактом, что этот процесс позволяет использовать большие количества связующего вещества, чем это было возможно в ранее протестированных процессах гранулирования. Способ, в котором гранулы образуются в ходе распылительного процесса гранулирования, придает им приемлемую плотность/пористость и приемлемое распределение размера частиц с небольшими отклонениями между партиями. Гранулы также характеризуются превосходной текучестью.
Дополнительно было обнаружено, что эти характеризующиеся выгодными качествами составы могут быть получены с поддержанием химической стабильности дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S) несмотря на использование процесса, в котором по меньшей мере часть дапаглифлозина растворяют в воде.
Краткое раскрытие настоящего изобретения
Согласно одному аспекту настоящее изобретение относится к фармацевтическому составу с немедленным высвобождением, который включает состав таблетки, исходного гранулята или капсулы, содержащий (1) ингибитор SGLT2 или его фармацевтически приемлемую соль или сольват, (2) метформин или его фармацевтически приемлемую соль или сольват и (3) необязательно покрытие. Предпочтительным является гидрохлорид (НС1) метформина. Предпочтительным ингибитором SGLT2 является дапаглифлозин, припиленгликольгидрат дапаглифлозина (S) (1:1:1) или припиленгликольгидрат дапаглифлозина (R) (1:1:1). Наиболее предпочтительным ингибитором SGLT2 является дапаглифлозин или припиленгликольгидрат дапаглифлозина (S) (1:1:1).
Согласно другому аспекту настоящее изобретение относится к способам лечения заболеваний или нарушений, связанных с активностью SGLT2, предусматривающим введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества фармацевтического состава по настоящему изобретению. Фармацевтический состав по настоящему изобретению может быть введен млекопитающим, предпочтительно людям, для лечения множества состояний и нарушений, связанных с активностью SGLT2, включая без ограничения лечение или замедление развития или возникновения сахарного диабета (включая сахарный диабет типа I и типа II), нарушенной толерантности к глюкозе, инсулинорезистентности и диабетических осложнений, таких как нефропатия, ретинопатия, невропатия и катаракта, гипергликемии, гиперинсулинемии, гиперхолистеринемии, дислипидемии, повышенного содержания свободных жирных кислот или глицерина в крови, гиперлипидемии, гипертриглицеридемии, ожирения, заживления ран, ишемии тканей, атеросклероза и гипертензии. Составы по настоящему изобретению также могут быть использованы для повышения содержания в крови липопротеидов высокой плотности (HDL). Дополнительно с использованием составов по настоящему изобретению можно лечить состояния, заболевания и нарушения, собирательно называемые «Синдромом X», или метаболическим синдромом.
Согласно другому аспекту изобретение относится к способам получения фармацевтического состава с немедленным высвобождением, который включает состав таблетки, исходного гранулята или капсулы, содержащего метформин или его фармацевтически приемлемую соль или сольват и ингибитор натрий-зависимого переносчика глюкозы (SGLT2) или его фармацевтически приемлемую соль или сольват.
Краткое описание графических материалов
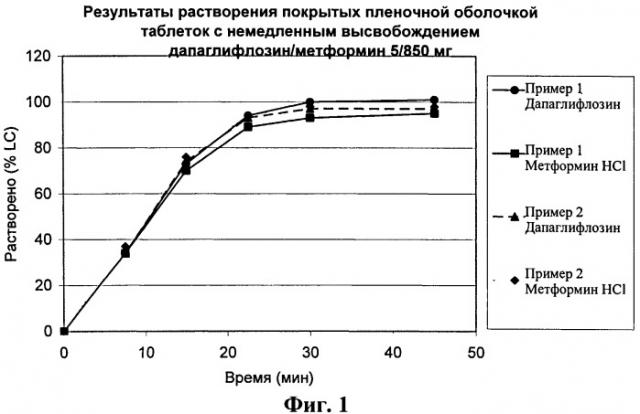
На фиг.1 описан профиль растворения составов с немедленным высвобождением (покрытых пленкой) согласно примерам 1 и 2, которые содержат дапаглифлозин и метформин.
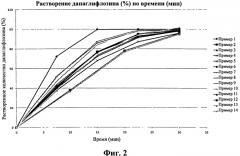
На фиг.2 описан профиль растворения составов с немедленным высвобождением согласно примерам 1-14.
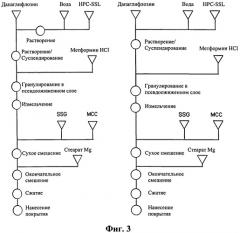
На фиг.3 в виде блок-схемы описаны способы получения составов по настоящему изобретению.
Подробное раскрытие настоящего изобретения
Настоящее изобретение относится к составам с немедленным высвобождением, содержащим дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S) и метформин в комбинации с другими эксципиентами. Составы находятся в форме таблетки, гранулята или капсулы, причем форма таблетки является предпочтительной. Составы содержат комбинацию эксципиентов и производятся в соответствии со способом, обеспечивающим однородность содержания, желаемый предел прочности на разрыв и приемлемое время дезинтеграции и время растворения таблетки, объединяющей в себе компонент с низкой дозой и компонент с высокой дозой. Предпочтительные свойства таблетки включают предел прочности на разрыв около 2 МПа (мегапаскаль), время дезинтеграции около 20 минут и растворение свыше 80% через 30 минут. Составы по настоящему изобретению характеризуются этими желаемыми свойствами несмотря на большое отношение между содержаниями метформина (500-1000 мг) и ингибитора SGLT2 (1,25-5 мг) и на известную проблему медленной дезинтеграции таблеток, характеризующихся высоким содержанием метформина.
Соответственно, настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат ингибитор SGLT2, метформин, одно или несколько связующих веществ, один или несколько наполнителей, один или несколько разрыхлителей, одно или несколько скользящих веществ и необязательно покрытие. Предпочтительным ингибитором SGLT2 является дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S) (1:1:1). Предпочтительные количества дапаглифлозина составляют от около 1 до 6 мг или от около 1,2 до 7,4 мг пропиленгликольгидрата дапаглифлозина (S). Наиболее предпочтительными количествами дапаглифлозина являются 2,5 мг и 5,0 мг, а наиболее предпочтительными количествами пропиленгликольгидрата дапаглифлозина (S) являются 3,08 мг и 6,15 мг. Предпочтительной формой метформина является гидрохлорид метформина. Предпочтительными количествами метформина являются 500 мг, 850 мг и 1000 мг. Предпочтительным связующим веществом является гидроксипропилцеллюлоза. Предпочтительным наполнителем является микрокристаллическая целлюлоза, а предпочтительным скользящим веществом является стеарат магния. Предпочтительными разрыхлителями являются натриевый гликолят крахмала и гидроксипропилцеллюлоза, причем наиболее предпочтительным разрыхлителем является натриевый гликолят крахмала. Составы находятся в форме таблетки, гранулята или капсулы, причем предпочтительной формой является таблетка. Необязательные покрытия выбирают из Opadry® II белого, Opadry® II коричневого, Opadry® II оранжевого или Opadry® II желтого.
Термин "однородность содержания (CU)" определяется как вариабельность содержания в отдельных таблетках из разных партий. CU измеряют для того, чтобы обеспечить единообразие единиц дозирования, т.е. чтобы каждая единица в партии характеризовалась содержанием активного вещества в пределах узкого диапазона вблизи целевого состава таким образом, чтобы партия соответствовала комплексу предельных значений. CU указывают в виде относительного стандартного отклонения в процентах % (%RSD).
Механическую прочность таблеток определяют с помощью метода, называемого испытанием диаметральным сжатием. Этот метод состоит в том, что дисковый образец, например, таблетку, подвергают воздействию нагрузки, прилагаемой к двум диаметрально противоположным точкам. Усилие непрерывно увеличивают до тех пор, пока таблетка не разрушается. Разрушающее усилие (H) делят на разрушаемую площадь таблетки (мм2) для того, чтобы компенсировать размер таблетки. Полученный результат указывается в настоящем документе как предел прочности (TS) таблетки и измеряется в МПа.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,1-2% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 55-85% гидрохлорида метформина; около 1-15% гидроксипропилцеллюлозы; около 2-25% микрокристаллической целлюлозы; около 1-12% натриевого гликолята крахмала или около 3-10% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,25-5% стеарата магния. Необязательное покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,1-1% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 60-80% гидрохлорида метформина; около 1-10% гидроксипропилцеллюлозы; около 2-25% микрокристаллической целлюлозы; около 4-10% натриевого гликолята крахмала или около 3-10% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,25-5% стеарата магния. Необязательное покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,25-0,8% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 62-77% гидрохлорида метформина; около 3-10% гидроксипропилцеллюлозы; около 5-21% микрокристаллической целлюлозы; около 5-9% натриевого гликолята крахмала или около 5-8% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,6-1,4% стеарата магния. Необязательное покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 70,5% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,25% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 71% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,4% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 61,5% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 21% микрокристаллической целлюлозы; около 8,5% натриевого гликолята крахмала; и около 1,4% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,4% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 72% гидрохлорида метформина; около 9% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 1% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 70,5% гидрохлорида метформина; около 5,5% гидроксипропилцеллюлозы; около 20,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 1% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 75,5% гидрохлорида метформина; около 6% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 77% гидрохлорида метформина; около 10% гидроксипропилцеллюлозы; около 5% микрокристаллической целлюлозы; около 7,5% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,8% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 69% гидрохлорида метформина; около 3% гидроксипропилцеллюлозы; около 20% микрокристаллической целлюлозы; около 6,5% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,8% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,4% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 68% гидрохлорида метформина; около 2,6% гидроксипропилцеллюлозы; около 20% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 0,2% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 70,7% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 500 мг гидрохлорида метформина; необязательно одно или несколько связующих веществ; необязательно один или несколько наполнителей, необязательно один или несколько разрыхлителей; необязательно одно или несколько скользящих веществ, и необязательно покрытие.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 500 мг гидрохлорида метформина; около 19 мг гидроксипропилцеллюлозы; около 150 мг микрокристаллической целлюлозы; около 60 мг натриевого гликолята крахмала; и около 4,5 мг стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Предпочтительным покрытием может быть Opadry® II белый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 850 мг гидрохлорида метформина; необязательно одно или несколько связующих веществ; необязательно один или несколько наполнителей, необязательно один или несколько разрыхлителей; необязательно одно или несколько скользящих веществ, и необязательно покрытие.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 850 мг гидрохлорида метформина; около 96 мг гидроксипропилцеллюлозы; около 150 мг микрокристаллической целлюлозы; около 96 мг натриевого гликолята крахмала; и около 7 мг стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Предпочтительным покрытием может быть Opadry® II белый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 5 мг дапаглифлозина или около 6,15 мг пропиленгликольгидрата дапаглифлозина (S); около 850 мг гидрохлорида метформина; необязательно одно или несколько связующих веществ; необязательно один или несколько наполнителей, необязательно один или несколько разрыхлителей; необязательно одно или несколько скользящих веществ, и необязательно покрытие.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 5 мг дапаглифлозина или около 6,15 мг пропиленгликольгидрата дапаглифлозина (S); около 850 мг гидрохлорида метформина; около 97 мг гидроксипропилцеллюлозы; около 151 мг микрокристаллической целлюлозы; около 97 мг натриевого гликолята крахмала; и около 7 мг стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Предпочтительным покрытием может быть Opadry® II коричневый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 1000 мг гидрохлорида метформина; необязательно одно или несколько связующих веществ; необязательно один или несколько наполнителей, необязательно один или несколько разрыхлителей; необязательно одно или несколько скользящих веществ, и необязательно покрытие.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 2,5 мг дапаглифлозина или около 3,08 мг пропиленгликольгидрата дапаглифлозина (S); около 1000 мг гидрохлорида метформина; около 113 мг гидроксипропилцеллюлозы; около 177 мг микрокристаллической целлюлозы; около 113 мг натриевого гликолята крахмала; и около 9 мг стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Предпочтительное покрытие может представлять собой Opadry® II оранжевый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 5 мг дапаглифлозина или около 6,15 мг пропиленгликольгидрата дапаглифлозина (S); около 1000 мг гидрохлорида метформина; необязательно одно или несколько связующих веществ; необязательно один или несколько наполнителей, необязательно один или несколько разрыхлителей; необязательно одно или несколько скользящих веществ, и необязательно покрытие.
Согласно другому аспекту настоящее изобретение относится к фармацевтическим составам с немедленным высвобождением, которые содержат около 5 мг дапаглифлозина или около 6,15 мг пропиленгликольгидрата дапаглифлозина (S); около 1000 мг гидрохлорида метформина; около 114 мг гидроксипропилцеллюлозы; около 177 мг микрокристаллической целлюлозы; около 114 мг натриевого гликолята крахмала; и около 9 мг стеарата магния. Покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Предпочтительное покрытие может представлять собой Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Настоящее изобретение также относится к способам лечения нарушений или заболеваний, связанных с активностью SGLT2, и которые включают сахарный диабет (включая сахарный диабет типа I и типа II), нарушенную толерантность к глюкозе, инсулинорезистентность, нефропатию, ретинопатию, невропатию и катаракту, гипергликемию, гиперинсулинемию, гиперхолистеринемию, дислипидемию, повышенное содержание свободных жирных кислот или глицерина в крови, гиперлипидемию, гипертриглицеридемию, ожирение, заживление раны, ишемию тканей, атеросклероз или гипертензию, у млекопитающих, предусматривающим введение нуждающемуся в таком лечении млекопитающему фармацевтического состава, который содержит: (1) ингибитор SGLT2; (2) метформин и (3) необязательно покрытие, отличающимся тем, что фармацевтический состав характеризуется немедленным высвобождением и находится в форме таблетки, исходного гранулята или капсулы. Предпочтительным способом лечения является способ лечения сахарного диабета II типа у людей. Предпочтительным ингибитором SGLT2 является дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S).
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит ингибитор SGLT2; метформин; одно или несколько связующих веществ; один или несколько наполнителей; один или несколько разрыхлителей и одно или несколько скользящих веществ. Предпочтительным ингибитором SGLT2 является дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S). Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит дапаглифлозин или пропиленгликольгидрат дапаглифлозина (S); гидрохлорид метформина; гидроксипропилцеллюлозу; микрокристаллическую целлюлозу; разрыхлитель, являющееся натриевым гликолятом крахмала или гидроксипропилцеллюлозой с низкой степенью замещения; и скользящее вещество, являющееся стеаратом магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,1-2% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 55-85% гидрохлорида метформина; около 1-15% гидроксипропилцеллюлозы; около 2-25% микрокристаллической целлюлозы; около 1-12% натриевого гликолята крахмала или 3-10% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,25-5% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,1-1% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 60-80% гидрохлорида метформина; около 1-10% гидроксипропилцеллюлозы; около 2-25% микрокристаллической целлюлозы; около 4-10% натриевого гликолята крахмала или около 3-10% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,25-2,5% стеарата магния. Необязательным покрытие может представлять собой Opadry® II белый, Opadry® II оранжевый, Opadry® II коричневый или Opadry® II желтый. Фармацевтический состав находится в форме таблетки, исходного гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,25-0,8% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 62-77% гидрохлорида метформина; около 3-10% гидроксипропилцеллюлозы; около 5-21% микрокристаллической целлюлозы; около 5-9% натриевого гликолята крахмала или около 5-8% гидроксипропилцеллюлозы с низкой степенью замещения; и около 0,6-1,4% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 70,5% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,25% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 71% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 8% натриевого гликолята крахмала; и около 0,6% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,4% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 61,5% гидрохлорида метформина; около 8% гидроксипропилцеллюлозы; около 21% микрокристаллической целлюлозы; около 8,5% натриевого гликолята крахмала; и около 1,4% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,4% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 72% гидрохлорида метформина; около 9% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 1% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 70,5% гидрохлорида метформина; около 5,5% гидроксипропилцеллюлозы; около 20,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 1% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевтического состава, который содержит около 0,5% дапаглифлозина или пропиленгликольгидрата дапаглифлозина (S); около 75,5% гидрохлорида метформина; около 6% гидроксипропилцеллюлозы; около 12,5% микрокристаллической целлюлозы; около 5% натриевого гликолята крахмала; и около 0,6% стеарата магния. Фармацевтический состав представляет собой состав с немедленным высвобождением в форме таблетки, гранулята или капсулы, причем предпочтительной является таблетка. Покрытие может представлять собой Opadry® II белый, Opadry® II коричневый, Opadry® II оранжевый или Opadry® II желтый.
Согласно другому аспекту настоящее изобретение относится к способу лечения сахарного диабета II типа у людей, предусматривающему введение нуждающемуся в таком лечении человеку фармацевт