Триазолпиридиновые соединения, ингибирующие jak, и способы
Иллюстрации
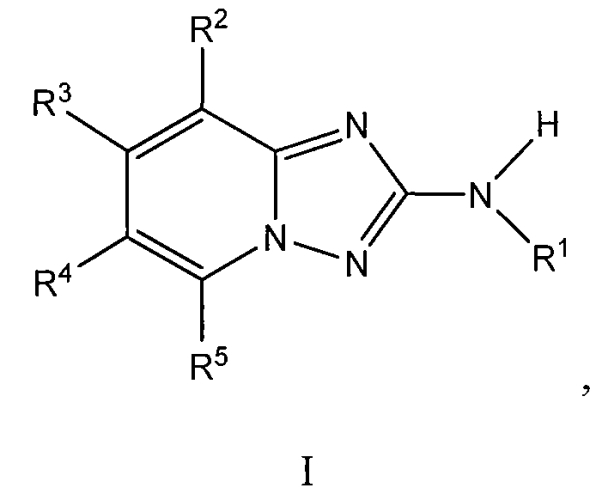
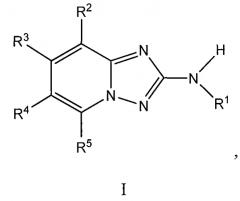
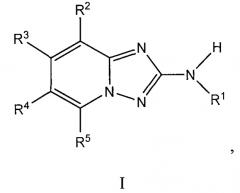
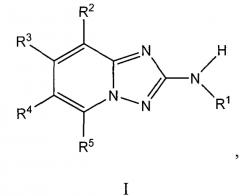
Показать всеИзобретение относится к соединениям формулы I или его фармацевтически приемлемым солям. Соединения изобретения обладают свойствами ингибитора JAK2 киназы. В формуле I
R1 представляет собой фенил, необязательно замещенный 1-3 R6; R2 представляет собой фенил, необязательно замещенный 1-2 R7; R3, R4 и R5 независимо представляют собой H. Значения остальных радикалов представлены в формуле изобретения. Изобретение также относится к конкретным соединениям, структурные формулы которых представлены в формуле изобретения. Технический результат: получены новые соединения, которые обладают свойствами ингибитора JAK2 киназы. 2 н. и 9 з.п. ф-лы, 2 табл., 312 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
Триазолпиридиновые соединения формулы I, которые являются ингибиторами янус киназ, например JAK2 киназы, а также композиции, содержащие данные соединения, и способы применения, включая, но не ограничиваясь, in vitro, in situ и in vivo диагностику или лечение клеток млекопитающих.
УРОВЕНЬ ТЕХНИКИ
Миелопролиферативные заболевания (MPD) возникают в гематопоэтических стволовых клетках и в первую очередь проявляются в повышенном количестве преимущественно нормальных клеток миелоидного ростка. Можно сделать первичное разделение на положительную филадельфийскую хромосому (Ph+) и отрицательную филадельфийскую хромосому (Ph-). Ph+ MPD приводит в результате к хронической гранулоцитной лейкемии и контролируется bcr-abl гибридным белком, который контролирует пролиферацию гематопоэтических клеток. Ph- MPD можно дополнительно разделить на три различных заболевания по соответствующим разновидностям, а именно, истинную полицитемию (PV), эссенциальную тромбоцитемию (ET) и идиопатический миелофиброз (IMF). Dameshek, W., Blood 6(4):372-375 (1951). Пациенты с PV страдают от повышенного количества красных кровяных тел, тогда как пациенты с ET имеют повышенные концентрации циркулирующих тромбоцитов. Если не лечить данные заболевания, оба из них могут привести к опасным для жизни тромботическим осложнениям. Пациенты с IMF страдают от фиброза костного мозга с последующим перемещением гематопоэза в селезенку и печень. Это приводит в первую очередь к спленомегалии, за которой следует анемия на более поздних стадиях заболевания, поскольку гематопоэзис становится непродуктивным. Данным пациентам делают неблагоприятные прогнозы, хотя при определенных условиях их можно вылечить посредством аллогенного трансплантата костного мозга. Неизвестно случаев вылечивания Ph- MPD заболеваний.
Активирующая мутация в тирозинкиназе JAK2 связана с PV, ET, IMF и другими заболеваниями. Практически все пациенты с PV и приблизительно 50% пациентов с ET и IMF содержат данную мутацию. Morgan, KJ. и Gilliland, D. G., Ann. Rev. Med. 59:213-222 (2008). Мутация представляет собой замену валина на фенилаланин в положении 617 в зрелом человеческом JAK2 белке (V617F). Дополнительные мутации в JAK2, обычно обнаруживаемые в экзоне 12 и называемые мутации в экзоне 12, также обладают активирующим действием и могут приводить к MPD. Кроме того, T875N мутация была связана с мегакариобластной лейкемией. Наконец, JAK2 гибридные белки обнаруживают при острой лейкемии.
V617F мутация действует, активируя JAK2, что приводит к MPD. В немутированной форме JAK2 связана с цитокиновыми рецепторами (например EPO-R, TPO-R и другими) и активируется только, если сам рецептор активирован стимулом родственного цитокинового лиганда. Затем, гематопоэзис в целом регулируется за счет присутствия лигандов. Например, цитокиновый эритропоэтин (EPO) стимулирует гематопоэтические клетки-предшественники, образуя красные кровяные клетки. Мутация, которая нарушает JAK2 активацию EPO, следовательно, приводит к повышенным концентрациям красных кровяных клеток. Аналогично, тромбопоэтин (TPO) регулирует рост тромбоцитов связыванием с TPO-R, который, в свою очередь, также передает сигнал посредством JAK2. Таким образом, повышенные концентрации тромбоцитов могут также быть результатом нарушений активации JAK2.
Необходимы соединения, которые ингибируют JAK2, что оказывало бы благоприятный эффект на пациентов с миелопролиферативными нарушениями, контролируемыми JAK2, а также, с другими заболеваниями, которые являются чувствительными к ингибированию JAK2. Данные заболевания включают и заболевания, при которых JAK2 активируется мутацией или амплификацией, и заболевания, при которых активация JAK2 является частью онкогенного каскада. Многочисленные линии опухолевых клеток и образцы опухолей имеют высокие концентрации фосфо-STAT3, который является JAK2 геном-мишенью.
Первоначально JAK1 была обнаружена при поиске новых киназ (Wilks A.F.,1989, Proc. Natl. Acad. Sci. U.S.A. 86:1603-1607). Генетические и биохимические исследования показали, что JAK1 функционально и физически связана с интерфероном типа I (например, IFNальфа), интерфероном типа II (например, IFNгамма), IL-2 и IL-6 цитокиновыми рецепторными комплексами (Kisseleva et al., 2002, gene 285:1-24; Levy et al, 2005, Nat. Rev. Mol. Cell Biol. 3:651-662; O'Shea et al., 2002, Cell, 109 (suppl.): S121-S131). JAK1 нокаутные мыши умирают на перинатальной стадии из-за нарушений в LIF рецепторной сигнализации (Kisseleva et al., 2002, gene 285:1-24; O'Shea et al., 2002, Cell, 109 (suppl.): S121-S131). Исследование тканей, полученных из JAK1 нокаутных мышей, показало, что данные киназы играют решающую роль в IFN, IL-10, IL-2/IL-4 и IL-6 путях. Гуманизированное моноклональное антитело, мишенью которого является IL-6 путь (тоцилизумаб), недавно было одобрено Европейской комиссией для лечения от умеренного до тяжелого ревматоидного артрита (Scheinecker et al., 2009, Nat. Rev. Drug Discov. 8:273-274).
JAK3 связывается только с общей гамма-цепью цитокинового рецептора, которая присутствует в IL-2, IL-4, IL-7, IL-9, IL-15 и IL-21 цитокиновых рецепторных комплексах. JAK3 является важной при дифференцировке и пролиферации лимфоцитов, и мутации в JAK3 приводят в результате к тяжелому комбинированному иммунодефициту (SCID) (O'Shea et al., 2002, Cell, 109 (suppl): S121-S131). На основании их роли в регуляции лимфоцитов, JAK3 и JAK3-опосредованные пути являются мишенью в случаях, когда необходимо подавить иммунитет (например, отторжение трансплантата и ревматоидный артрит) (Baslund et al., 2005, Arthritis & Rheumatism 52:2686-2692; Changelian et al., 2003, Science 302: 875-878).
TYK2 связывается с интерфероном типа I (например, IFNальфа), IL-6, IL-10, IL-12 и IL-23 цитокиновыми рецепторными комплексами (Kisseleva et al., 2002, gene 285:1-24; Watford, W.T. & O'Shea, J.J., 2006, Immunity 25:695-697). В соответствии с этим первичные клетки, полученные у людей с дефицитом TYK2, имеют нарушения в сигнализации с интерфероном I типа, IL-6, IL-10, IL-12 и IL-23. Полностью человеческое моноклональное тело, мишенью которого является общая p40 субъединица IL-12 и IL-23 цитокинов (устекинумаб), недавно было одобрено Европейской комиссией для лечения от умеренного до тяжелого пятнистого псориаза (Krueger et al., 2007, N. Engl. J. Med. 356:580-92; Reich et al., 2009, Nat. Rev. Drug Discov. 8:355-356).
Кроме того, антитело, мишенью которого является IL-12 и IL-23 пути, подвергалось клиническим экспериментам для лечения болезни Крона (Mannon et al., 2004, N. Engl. J. Med. 351:2069-79).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Один вариант осуществления включает соединение формулы I:
его энантиомеры, диастереомеры, таутомеры или фармацевтически приемлемые соли, в которых R1, R2, R3, R4 и R5 определяют в настоящем изобретении.
Другой вариант осуществления включает фармацевтическую композицию, которая содержит соединение формулы I и фармацевтически приемлемый носитель, вспомогательное вещество или среду.
Другой вариант осуществления включает способ лечения или снижения тяжести заболевания или состояния, чувствительного к ингибированию активностей одной или более янус киназ, выбранных из JAK1, JAK2, JAK3 и TYK2, у пациента. Способ включает введение пациенту терапевтически эффективного количества соединения формулы I.
Другой вариант осуществления включает способ лечения или снижения тяжести заболевания или состояния, чувствительного к ингибированию JAK2 киназной активности у пациента. Способ включает введение пациенту терапевтически эффективного количества соединения формулы I.
Другой вариант осуществления включает набор для лечения заболевания или расстройства, чувствительного к ингибированию JAK киназы. Набор содержит первую фармацевтическую композицию, содержащую соединение формулы I, и инструкции по применению.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В настоящее время будут делаться подробные ссылки на определенные варианты осуществления, примеры которых иллюстрируются сопровождающими их структурами и формулами. Когда настоящее изобретение будет описываться в соответствии с перечисленными вариантами осуществления, будет ясно, что предполагается, что они не ограничивают настоящее изобретение данными вариантами осуществления. И наоборот, предполагается, что настоящее изобретение включает все альтернативные варианты, модификации и эквивалентны, которые можно включить в объем настоящего изобретения, как описано в формуле изобретения. Специалистам в данной области техники известны многие способы и материалы, аналогичные или эквивалентные способам и материалам, описанным в настоящем изобретении, которые можно применять при осуществлении на практике настоящего изобретения. Настоящее изобретение никоим образом не ограничивается описанными способами и материалами. В случае если один или более из введенных в настоящее изобретение литературных источников, патентов и аналогичных материалов отличаются или противоречат данной заявке, включая, но не ограничиваясь, определенные термины, применение терминов, описанные методики или подобные, данная заявка имеет приоритет.
Термин "алкил" относится к насыщенному линейному или разветвленному моновалентному углеводородному радикалу, в котором алкильный радикал может необязательно быть замещенным независимо одним или более заместителями, описанными в настоящем изобретении. В одном примере алкильный радикал содержит от одного до восемнадцати атомов углерода (C1-C18). В других примерах алкильный радикал представляет собой C0-C6, C0-C5, C0-C3, C1-C12, C1-C1O, C1-C8, C1-C6, C1-C5, C1-C4 или C1-C3. Примеры алкильных групп включают C1-C8 углеводородные группы, такие как метил (Me, -CH3), этил (Et, -CH2CH3), 1-пропил (н-Pr, н-пропил, -CH2CH2CH3), 2-пропил (изо-Pr, изопропил, -CH(CH3)2), 1-бутил (н-Bu, н-бутил, -CH2CH2CH2CH3), 2-метил-1-пропил (изо-Bu, изобутил, -CH2CH(CH3)2), 2-бутил (втор-Bu, втор-бутил, -CH(CH3)CH2CH3), 2-метил-2-пропил (трет-Bu, трет-бутил, -C(CH3)3), 1-пентил (н-пентил, -CH2CH2CH2CH2CH3), 2-пентил (-CH(CH3)CH2CH2CH3), 3-пентил (-CH(CH2CH3)2), 2-метил-2-бутил (-C(CH3)2CH2CH3), 3-метил-2-бутил (-CH(CH3)CH(CH3)2), 3-метил-1-бутил (-CH2CH2CH(CH3)2), 2-метил-1-бутил (-CH2CH(CH3)CH2CH3), 1-гексил (-CH2CH2CH2CH2CH2CH3), 2-гексил (-CH(CH3)CH2CH2CH2CH3), 3-гексил (-CH(CH2CH3)(CH2CH2CH3)), 2-метил-2-пентил (-C(CH3)2CH2CH2CH3), 3-метил-2-пентил (-CH(CH3)CH(CH3)CH2CH3), 4-метил-2-пентил (-CH(CH3)CH2CH(CH3)2), 3-метил-3-пентил (-C(CH3)(CH2CH3)2), 2-метил-3-пентил (-CH(CH2CH3)CH(CH3)2), 2,3-диметил-2-бутил (-C(CH3)2CH(CH3)2), 3,3-диметил-2-бутил (-CH(CH3)C(CH3)3, 1-гептил и 1-октил.
Термин "алкенил" относится к линейному или с разветвленной цепью моновалентному углеводородному радикалу с, по меньшей мере, одним сайтом ненасыщенности, а именно, углерод-углеродной двойной связью, в котором алкенильный радикал можно необязательно замещать независимо одним или более заместителями, описанными в настоящем изобретении, и он включает радикалы, имеющие "цис" и "транс" ориентации, или альтернативно, "E" и "Z" ориентации. В одном примере алкенильный радикал содержит от двух до восемнадцати атомов углерода (C2-C18). В других примерах алкенильный радикал представляет собой C2-C12, C2-C10, C2-C8, C2-C6 или C2-C3. Примеры включают, но не ограничиваются, этенил или винил (-CH=CH2), проп-1-енил (-CH=CHCH3), проп-2-енил (-CH2CH=CH2), 2-метилпроп-1-енил, бут-1-енил, бут-2-енил, бут-3-енил, бута-1,3-диенил, 2-метилбута-1,3-диен, гекс-1-енил, гекс-2-енил, гекс-3-енил, гекс-4-енил, гекса-1,3-диенил.
Термин "алкинил" относится к линейному или разветвленному моновалентному углеводородному радикалу с, по меньшей мере, одним сайтом ненасыщенности, а именно, углерод-углеродной тройной связью, в котором алкинильный радикал можно необязательно замещать независимо одним или более заместителями, описанными в настоящем изобретении. В одном примере алкинильный радикал содержит от двух до восемнадцати атомов углерода (C2-C18). В других примерах алкинильный радикал представляет собой C2-C12, C2-C10, C2-C8, C2-C6 или C2-C3. Примеры включают, но не ограничиваются, этинил (-C≡CH), проп-1-инил (-C≡CCH3), проп-2-инил (пропаргил, -CH2C≡CH), бут-1-инил, бут-2-инил и бут-3-инил.
"Циклоалкил" относится к неароматической, насыщенной или частично ненасыщенной углеводородной кольцевой группе, в которой циклоалкильную группу можно необязательно замещать независимо одним или более заместителями, описанными в настоящем изобретении. В одном примере циклоалкильная группа содержит 3 - 12 атомов углерода (C3-C12). В других примерах циклоалкил представляет собой C3-C10 или C5-C10. В других примерах циклоалкильная группа, в виде моноцикла, представляет собой C3-C6 или C5-C6. В другом примере циклоалкильная группа, в виде бицикла, представляет собой C7-C12. Примеры моноциклического циклоалкила включают циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, циклогексадиенил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил и циклододецил. Примерное соотношение атомов в бициклических циклоалкилах, содержащих 7 - 12 кольцевых атомов, включает, но не ограничиваются, [4,4], [4,5], [5,5], [5,6] или [6,6] кольцевые системы. Примерные бициклические циклоалкилы с мостиковой связью включают, но не ограничиваются, бицикло[2.2.1]гептан, бицикло[2.2.2]октан и бицикло[3.2.2]нонан.
"Арил" относится к циклической ароматической углеводородной группе, необязательно замещенной независимо одним или более заместителями, описанными в настоящем изобретении. В одном примере арильная группа содержит 6-20 атомов углерода (C6-C20). В другом примере арильная группа представляет собой C6-C9. В другом примере арильная группа представляет собой C6 арильную группу. Арильные группы могут быть представлены в структурах примеров, как "Ar". Арил включает бициклическую группу, содержащую ароматическое кольцо, конденсированное неароматическим или частично насыщенным кольцом. Примеры арильных групп включают, но не ограничиваются, фенил, нафталенил, антраценил, инденил, инданил, 1,2-дигидронафталенил, 1,2,3,4-тетрагидронафтил и подобные.
"Галоген" относится к F, Cl, Br или I.
"Гетероциклил" относится к насыщенной или частично ненасыщенной (т.е., содержащей одну или более двойных и/или тройных связей в кольце) циклической группе, в которой, по меньшей мере, один кольцевой атом представляет собой гетероатом, независимо выбранный из азота, кислорода, фосфора и серы, причем оставшиеся кольцевые атомы представляют собой атомы углерода. Гетероциклильную группу можно необязательно замещать одним или более заместителями, описанными ниже. В одном варианте осуществления гетероциклил включает моноциклы или бициклы, содержащие 1-9 углеродных кольцевых членов (C1-C9). В других примерах гетероциклил включает моноциклы или бициклы, содержащие C1-C5, C3-C5 или C4-C5. Примеры бициклических систем включают, но не ограничиваются, [3,5], [4,5], [5,5], [3,6], [4,6], [5,6] или [6,6] системы. В другом варианте осуществления гетероциклил включает кольцевые системы с мостиковой связью, содержащие [2.2.1], [2.2.2], [3.2.2] и [4.1.0] расположения атомов, и содержащие 1-3 гетероатомы, выбранные из N, O, S и P. В другом варианте осуществления гетероциклил включает спиро группы, содержащие 1-3 гетероатома, выбранные из N, O, S и P. Гетероциклильная группа может быть группой, присоединенной через атом углерода, или группой, присоединенной через гетероатом. "Гетероциклил" включает гетероциклильную группу, конденсированную с циклоалкильной группой.
Примеры гетероциклильных групп включают, но не ограничиваются, оксиранил, азиридинил, тииранил, азетидинил, оксетанил, тиентанил, 1,2-дитиетанил, 1,3-дитиетанил, пирролидинил, пиперидинил, морфолинил, тиоморфолинил, тиооксанил, пиперазинил, гомопиперазинил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, дигидротиенил, дигидропиранил, дигидрофуранил, тетрагидрофуранил, тетрагидротиенил, тетрагидропиранил, тетрагидротиопиранил, 1-пирролинил, 2-пирролинил, 3-пирролинил, индолинил, 2H-пиранил, 4H-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, пиразолидинил, дитианил, дитиоланил, пиразолидинилимидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил и азабицикло[2.2.2]гексанил. Примерами гетероциклильной группы, в которой кольцевой атом замещают оксо (=O), являются индолинонил, пиримидинонил и 1,1-диоксотиоморфолинил. Гетероциклильные группы настоящего изобретения необязательно замещают независимо одним или более заместителями, описанными в настоящем изобретении. Гетероциклилы описывают в Paquette, Leo A.; "Principles of Modern Heterocyclic Chemistry" (W. A. Benjamin, New York, 1968), в частности в главах 1, 3, 4, 6, 7 и 9; "The Chemistry of Heterocyclic Compounds, A series of Monographs" (John Wiley & Sons, New York, с 1950 до настоящего времени), в частности в томах 13, 14, 16, 19, и 28; и J. Am. Chem. Soc.(1960) 82:5566.
Термин "гетероарил" относится к ароматическому углеводородному радикалу, в котором, по меньшей мере, один кольцевой атом представляет собой гетероатом, независимо выбранный из азота, кислорода и серы, причем оставшиеся кольцевые атомы представляют собой атом углерода. Гетероарильные группы необязательно замещены одним или более заместителями, описанными в настоящем изобретении. В одном примере гетероарильная группа содержит 1-9 углеродных кольцевых атомов (C1-C9). В других примерах гетероарильная группа представляет собой C1-C5, C3-C5 или C5-C10. В одном варианте осуществления примерные гетероарильные группы включают моноциклические ароматические 5-, 6- и 7-членные кольца, содержащие один или более гетероатомов, независимо выбранных из азота, кислорода и серы. В другом варианте осуществления примерные гетероарильные группы включают конденсированные кольцевые системы 8-20 атомов, в которых, по меньшей мере, одно ароматическое кольцо содержит один или более гетероатомов, независимо выбранных из азота, кислорода и серы. "Гетероарил" включает гетероарильные группы, конденсированные с арильной, циклоалкильной или гетероциклильной группой. Примеры гетероарильных групп включают, но не ограничиваются, пиридинил, имидазолил, имидазопиридинил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил.
В определенных вариантах осуществления гетероциклильную или гетероарильную группу присоединяют через C атом. Посредством примера и без ограничения, присоединенные через атом углерода гетероциклилы включают расположение связи в положении 2, 3, 4, 5 или 6 пиридина, положении 3, 4, 5 или 6 пиридазина, положении 2, 4, 5 или 6 пиримидина, положении 2, 3, 5 или 6 пиразина, положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положении 2, 4 или 5 оксазола, имидазола или тиазола, положении 3, 4 или 5 изоксазола, пиразола или изотиазола, положении 2 или 3 азиридина, положении 2, 3 или 4 азетидина, положении 2, 3, 4, 5, 6, 7 или 8 хинолина или положении 1, 3, 4, 5, 6, 7 или 8 изохинолина. (2-пиридил, 3-пиридил, 4-пиридил, 5-пиридил, 6-пиридил).
В определенных вариантах осуществления гетероциклильную или гетероарильную группу присоединяют через N атом. Посредством примера и без ограничения, присоединенная через атом азота гетероциклильная или гетероарильная группа включает расположение связи в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1H-индазола, положении 2 изоиндола или изоиндолина, положении 4 морфолина и положении 9 карбазола или β-карболина.
В одном варианте осуществления, в отношении формулы I, алкил, алкенил и алкинил необязательно замещены 1-5 заместителями, независимо выбранными из одного или более ORa, NRcRd, оксо и галогена, и арил, гетероциклил, гетероарил и циклоалкил необязательно замещены 1-5 заместителями, независимо выбранными из ORa, оксо, галогена, CF3, NRcRd, C1-C4 алкила и C(O)(C1-C4 алкила), в которых Ra, Rc и Rd определяют ниже для формулы I. В другом варианте осуществления, в отношении формулы I, алкил, алкенил и алкинил необязательно замещены 1-3 заместителями, независимо выбранными из одного или более ORa, NRcRd, оксо и галогена, и арил, гетероциклил, гетероарил и циклоалкил необязательно замещены 1-3 заместителями, независимо выбранными из ORa, оксо, галогена, CF3, NRcRd, C1-C4 алкила и C(O)(C1-C4 алкила), в которых Ra, Rc и Rd определяют ниже для формулы I.
В одном варианте осуществления, в отношении формулы I, алкил, алкенил и алкинил необязательно замещены 1-5 заместителями, независимо выбранными из оксо и галогена, и арил необязательно замещены 1-5 заместителями, независимо выбранными из ORa, галогена, CF3, NRcRd и C1-C4 алкила, в которых Ra, Rc и Rd определяют ниже в отношении формулы I. В другом варианте осуществления в отношении формулы I, алкил, алкенил и алкинил необязательно замещены 1-3 заместителями, независимо выбранными из оксо и галогена, и арил необязательно замещены 1-3 заместителями, независимо выбранными из ORa, галогена, CF3, NRcRd и C1-C4 алкила, в которых Ra, Rc и Rd определяют ниже в отношении формулы I.
В одном варианте осуществления, в отношении формулы I, алкил, арил и циклоалкил необязательно замещены 1-5 заместителями, независимо выбранными из C1-C4 алкила, (C0-C3 алкил)ORc, оксо, галогена, NRcRd и C4-C5 гетероциклила, в которых Rc и Rd определяют ниже в отношении формулы I. В другом варианте осуществления в отношении формулы I, алкил, арил и циклоалкил необязательно замещены 1-3 заместителями, независимо выбранными из C1-C4 алкила, (C0-C3 алкил)ORc, оксо, галогена, NRcRd и C4-C5 гетероциклила, в которых Rc и Rd определяют ниже в отношении формулы I.
В одном варианте осуществления в отношении формулы I, алкил, циклоалкил и фенил необязательно замещены 1-5 заместителями, независимо выбранными из галогена, CH3 OH, NH2, C(O)O(C1-C6 алкила) и C(O)NH(C1-C6 алкила). В другом варианте осуществления в отношении формулы I, алкил, циклоалкил и фенил необязательно замещены 1-3 заместителями, независимо выбранными из галогена, CH3 OH, NH2, C(O)O(C1-C6 алкила) и C(O)NH(C1-C6 алкила).
"Лечить" и "лечение" включает и терапевтическое лечение и профилактические или превентативные меры, при которых целью является предотвращение или замедление (облегчение) нежелательного физиологического изменения или заболевания, такого как развитие или распространение рака. Для целей настоящего изобретения, полезные или желательные клинические результаты включают, но не ограничиваются, облегчение симптомов, уменьшение длительности заболевания, стабилизирование (т.е., не ухудшение) состояния заболевания, задержку или замедление развития заболевания, уменьшение интенсивности или временное облегчение течения заболевания, и ремиссию (частичную ли или полную), обнаруживаемую ли или не обнаруживаемую. "Лечение" может также обозначать увеличение продолжительности жизни по сравнению с ожидаемым сроком жизни без осуществления лечения. Пациенты, нуждающиеся в лечении, включают пациентов уже с состоянием или заболеванием, а также пациентов, склонных иметь состояние или заболевание, (например, посредством генетической мутации) или пациентов, у которых состояние или заболевание нужно предотвратить.
Фраза "терапевтически эффективное количество" относится к количеству соединения настоящего изобретения, которое (i) лечит или предотвращает конкретное заболевание, состояние или расстройство, (ii) смягчает, облегчает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (iii) предотвращает или задерживает возникновение одного или более симптомов конкретного заболевания, состояния или расстройства, описанного в настоящем изобретении. В случае рака терапевтически эффективное количество лекарственного средства может уменьшить число раковых клеток; уменьшить размер опухоли; замедлить (т.е., замедлить до некоторой степени и предпочтительно остановить) инфильтрацию раковых клеток в периферические органы; замедлить (т.е., замедлить до некоторой степени и предпочтительно остановить) метастаз опухоли; замедлить, до некоторой степени, рост опухоли; и/или облегчить до некоторой степени один или более симптомов, связанных с раком. В тех случаях, когда лекарственное средство может предотвратить и/или убить существующие раковые клетки, оно может быть цитостатическим и/или цитотоксическим. Для терапии рака, эффективность можно, например, измерить оценкой времени до прогрессирования заболевания (TTP) и/или определением эффективности лекарственного средства (RR).
Термин "биодоступность" относится к системной доступности (а именно, концентрации в крови/плазме) данного количества лекарственного средства, введенного пациенту. Биодоступность представляет собой независимый термин, который показывает величину и времени (скорости) и суммарного количества (значение) лекарственного средства, которая достигает общего кровообращения из введенной лекарственной формы.
Термины "рак" и "раковый" относятся к или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым клеточным ростом. "Опухоль" включает одну или более раковых клеток. Примеры рака включают, но не ограничиваются, карциному, лимфому, бластому, саркому и лейкемию или лимфонеоплазию. Более конкретные примеры данных видов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак лёгкого, немелкоклеточный рак лёгкого ("NSCLC"), аденокарциному легкого и плоскоклеточный рак легкого, рак брюшной полости, гепатоцеллюлярный рак, рак желудочно-кишечного тракта или желудка, включая гастроинтестинальный рак, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, рак ободочной и прямой кишки, рак эндометрия или матки, рак слюнной железы, рак почек, рак предстательной железы, рак влагалища, рак щитовидной железы, рак печени, рак анального отверстия, рак полового члена, а также рак головы и шеи.
"Химиотерапевтический агент" представляет собой химическое соединение, пригодное для лечения рака. Примеры химиотерапевтических агентов включают эрлотиниб (TARCEVA®, Genentech, Inc./OSI Pharm.), трастузумаб (HERCEPTIN®, Genentech, Inc.); бевацизумаб (AVASTIN®, Genentech, Inc.); ритуксимаб (RITUXAN®, Genentech, Inc./Biogen Idee, Inc.), бортезомиб (VELCADE®, Millennium Pharm.), фульвестрант (FASLODEX®, AstraZeneca), сутент (SU11248, Pfizer), летрозол (FEMARA®, Novartis), мезилат иматиниба (GLEEVEC®, Novartis), PTK787/ZK 222584 (Novartis), оксалиплатин (Eloxatin®, Sanofi), 5-FU (5-фторурацил), лейковорин, рапамицин (Sirolimus, RAPAMUNE®, Wyeth), лапатиниб (GSK572016, Glaxo Smith Kline), лонафарниб (SCH 66536), сорафениб (BAY43-9006, Bayer Labs) и гефитиниб (IRESSA®, AstraZeneca), AG1478, AG1571 (SU 5271; Sugen), алкилирующие агенты, такие как тиотепа и CYTOXAN® циклофосфамид; алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфамид, триэтилентиофосфамид и триметиломеланин; ацетогенины (особенно буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекан); бриостатин; каллистатин; CC-1065 (включая его адозелезиновые, карзелезиновые и бизелезиновые синтетические аналоги); криптофицины (в частности криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и CBl-TМл); элеутеробин; панкратистатин; саркодиктин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, меклоретамин, гидрохлорид меклоретаминоксида, мелфалан, новэмбихин, фенестерин, преднимустин, трофосфамид, урамустин; нитромочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как энедииновые антибиотики, (например, калихимицин, особенно калихимицин гамма1I и калихимицин омегаI1 (Angew Chem. Intl. Ed. Engl. (1994) 33:183-186); динемицин, включая динемицин A; бисфосфонаты, такие как клодронат; эсперамицин; а также неокарзиностатиновый хромофор и родственные хромопротеиновые энедииновые антибиотические хромофоры), аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлеуцин, ADRIAMYCIN® (доксорубицин), морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, такие как митомицин C, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; пуриновые аналоги, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; пиримидиновые аналоги, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, пропионат дромостанолона, эпитиостанол, мепитиостан, тестолактон; препараты, подавляющие синтез стероидов корой надпочечников, такие как аминоглутетимид, митотан, трилостан; пополнители фолиевой кислоты, такие как фролиновая кислота; ацеглатон; альдофосфамидные гликозиды; аминолевулиновая кислота; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элфорнитин; ацетат эллиптиния; эпотилон; этоглуцид; нитрат галлия; гидроксимочевина; лентинан; лонидаинин; мэйтанзиноиды, такие как мейтанзин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; подофиллиновая кислота; 2-этилгидразид; прокарбазин; PSK® полисахаридный комплекс (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2',2"-трихлортриэтиламин; трихотецены (особенно T-2 токсин, верракурин A, роридин A и ангуидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Ara-C"); циклофосфамид; тиотепа; таксоиды, например, TAXOL® (паклитаксел; Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANE® (без кремофора), стабилизированные альбумином наночастицы паклитаксела (American Pharmaceutical Partners, Schaumberg, Illinois) и TAXOTERE® (доксетаксел; Rhône-Poulenc Rorer, Antony, France); хлорамбуцил; GEMZAR® (гемцитабин); 6-тиогуанин; меркаптопурин; метотрексат; платиновые аналоги, такие как цисплатина и карбоплатина; винбластин; этопозид (VP-16); ифосфамид; митоксантрон; винкристин; NAVELBINE® (винорелбин); новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; кселода; ибандронат; CPT-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота; капецитабин; и фармацевтически приемлемые соли, кислоты и производные любого из вышеперечисленных.
Также включенными в определение "химиотерапевтический агент" являются: (i) противогормональные агенты, которые действуют, регулируя или ингибируя действие гормонов на опухоли, такие как антиэстрогены и селективный модулятор рецепторов эстрогена (SERM), включая, например, тамоксифен (включая NOLVADEX®; цитрат тамоксифена), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и FARESTON® (торемифин цитрат); (ii) ингибиторы ароматазы, которые ингибируют фермент ароматазу, которая регулирует синтез эстрогена в надпочечниках, такие как, например, 4(5)-имидазолы, аминоглютетимид, MEGASE® (ацетат мегестрола), AROMASIN® (экземестан; Pfizer), форместан, фадрозол, RIVISOR® (ворозол), FEMARA® (летрозол; Novartis) и ARIMIDEX® (анастрозол; AstraZeneca); (iii) агенты, подавляющие синтез стероидов корой надпочечников, такие как флутамид, нилутамид, бикалутамид, лейпроледин и гозерелин; а также троксацитабин (1,3-диоксолановый нуклеозидный цитозиновый аналог); (iv) ингибиторы протеинкиназ; (v) ингибиторы липидных киназ; (vi) антисмысловые олигонуклеотиды, в частности антисмысловые олигонуклеотиды, которые ингибируют экспрессию генов в сигнальных путях, вовлеченных в нарушенную пролиферацию клеток, такие как, например, PKC-альфа, Ralf и H-Ras; (vii) рибозимы, такие как VEGF ингибиторы (например, ANGIOZYME®) и (viii) вакцины, такие как вакцины для генной терапии, например, ALLOVECTIN®, LEUVECTIN® и VAXID®; PROLEUKIN® rIL-2ингибитор топоизомеразы 1, такой как LURTOTECAN®; ABARELIX® rmRH; (ix) антиангиогенные агенты; и (x) фармацевтически приемлемые соли, кислоты и производные любого из вышеуказанных.
Гуманизированные моноклональные антитела с терапевтической активностью в качестве агентов в комбинации с ингибиторами янус киназы настоящего изобретения включают: алемтузумаб, аполизумаб, азелизумаб, атлизумаб, бапинеузумаб, бевацизумаб, мертансин биватузумаб, мертансин кантузумаб, цеделизумаб, цертолизумаб пегол, цидфузитузумаб, цидтузумаб, даклизумаб, экулизумаб, эфализумаб, эпратузумаб, эрлизумаб, фелвизумаб, фонтолизумаб, озогамицин гемтузумаб, озогамицин инотузумаба, ипилимумаб, лабетузумаб, линтузумаб, матузумаб, меполизумаб, мотавизумаб, мотовизумаб, натализумаб, нимотузумаб, ноловизумаб, нумавизумаб, окрелизумаб, омализумаб, паливизумаб, пасколизумаб, пекфузитузумаб, пектузумаб, пертузумаб, пекселизумаб, раливизумаб, ранибизумаб, ресливизумаб, реслизумаб, резивизумаб, ровелизумаб, руплизумаб, сибротузумаб, сиплизумаб, сонтузумаб, такатузумаб тетраксетан, тадоцизумаб, тализумаб, тефибазумаб, тоцилизумаб, торализумаб, трастузумаб, тукотузумаб целмолейкин, тукузитузумаб, умавизумаб, уртоксазумаб, устекинумаб, визилизумаб, адалимумаб, этанерцепт, инфликсимаб и антиинтерлейкин-12 (ABT-874/J695, Wyeth Research и Abbott Laboratories), который представляет собой рекомбинантное исключительно с человеческой последовательностью, полнодлинновое IgG1 λ антитело, генетически модифицированное для того, чтобы узнавать интерлейкин-12 p40 белок.
Термин "пролекарство", как применяют в настоящей заявке, относится к предшественнику или производному фармацевтически активного вещества, которое действует слабее на пациента или является менее цитотоксичным для клеток опухоли по сравнению с родственным лекарственным средством и которое может ферментативно или гидролитически активироваться, или превращаться в более активную родственную форму. Смотри, например, Wilman, "Prodrugs in Cancer Chemotherapy" Biochemical Society Transactions, 14, pp. 375-382, 615th Meeting Belfast (1986) и Stella et al., "Prodrugs: A Chemical Approach to Targeted Drug Delivery," Directed Drug Delivery, Borchardt et al., (ed.), pp. 247-267, Humana Press (1985). Пролекарства настоящего изобретения включают, но не ограничиваются, пролекарства, содержащие фосфат, пролекарства, содержащие тиофосфат, пролекарства, содержащие сульфат, пролекарства, содержащие пептид, пролекарства, модифицированные D-аминокислотой, гликозилированные пролекарства, пролекарства, содержащие β-лактам, пролекарства, содержащие необязательно замещенный феноксиацетамид или необязательно замещен