Позитивные аллостерические модуляторы (рам)
Иллюстрации
Показать всеНастоящее изобретение относится к новым производным фенилэтинила формулы (I) или к их фармацевтически приемлемым кислотно-аддитивным солям возможно в виде рацемической смеси, или ей соответствующему энантиомеру, и/или оптическому изомеру, и/или стереоизомеру. Соединения обладают свойствами позитивных аллостерических модуляторов (РАМ) метаботропных глутаматных рецепторов подтипа 5 (mGluR5) и могут быть использованы при лечении шизофрении или когнитивных расстройств. В формуле (I)
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном; R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси; X представляет собой N, CF или СН; L представляет собой -NR3-, -NHC(R3)2-, -O-, -OC(R3)2-, -CR4R4'-; R3 представляет собой водород или низший алкил; R4/R4' независимо друг от друга представляют собой водород или низший алкил; цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила; n представляет собой 1, 2 или 3. 3 н. и 20 з.п. ф-лы, 1 табл., 44 пр.
Реферат
Настоящее изобретение относится к производным фенилэтинила формулы
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
L представляет собой -NR3-, -NHC(R3)2-, -O-, -OC(R3)2-, -CR4R4′-;
R3 представляет собой водород или низший алкил;
R4/R4′ независимо друг от друга представляют собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или к их фармацевтически приемлемой кислотно-аддитивной соли, к рацемической смеси, или к ей соответствующему энантиомеру и/или оптическому изомеру и/или стереоизомеру.
Было неожиданно обнаружено, что соединения общей формулы I являются позитивными аллостерическими модуляторами (ПАМ или РАМ, от positive allosteric modulators) метаботропных глутаматных рецепторов подтипа 5 (mGluR5, от metabotropic glutamate receptor subtype 5).
В центральной нервной системе (ЦНС) передача стимулов происходит через взаимодействие нейромедиатора, посылаемого нейроном, с нейрорецептором.
Глутамат является главным возбуждающим нейромедиатором в головном мозге и играет уникальную роль в ряде функций центральной нервной системы (ЦНС). Рецепторы, зависящие от глутаматных стимулов, делят на две основные группы. Первую основную группу, а именно группу ионотропных рецепторов, образуют контролируемые лигандом ионные каналы. Метаботропные глутаматные рецепторы (mGluR) принадлежат ко второй основной группе и, кроме того, принадлежат семейству рецепторов, связанных с G-белками.
В настоящее время известно восемь разных типов этих рецепторов mGluR, и некоторые из них еще разделены на подтипы. На основании гомологии их последовательностей, механизмов передачи сигналов и селективности к агонистам эти восемь рецепторов могут быть подразделены на три подгруппы:
mGluRI и mGluR5 принадлежат к группе I, mGluR2 и mGluR3 принадлежат к группе II и mGluR4, mGluR6, mGluR7 и mGluR8 принадлежат к группе III.
Лиганды метаботропных глутаматных рецепторов, принадлежащих к первой группе, могут быть использованы для лечения или предотвращения острых и/или хронических неврологических нарушений, таких как психоз, эпилепсия, шизофрения, болезнь Альцгеймера, когнитивные расстройства и нарушения памяти, а также хроническая и острая боль.
Другие состояния, которые можно лечить при этом, представляют собой ограниченную функцию мозга, вызванную операциями шунтирования или трансплантациями, недостаточное мозговое кровоснабжение, травмы спинного мозга, травмы головы, гипоксию, вызванную беременностью, остановку сердца и гипогликемию. Кроме того, состояниями, которые можно лечить, являются ишемия, хорея Хантингтона, боковой амиотрофический склероз (ALS, от amyotrophic lateral sclerosis), слабоумие, вызванное СПИДом, травмы глаз, ретинопатия, идиопатический паркинсонизм или лекарственный паркинсонизм, а также состояния, которые ведут к глутамат-недостаточным функциям, таким, например, как спазмы мышц, конвульсии, мигрени, недержание мочи, никотиновая зависимость, опиатная зависимость, тревога, рвота, дискинезия и депрессии.
Заболеваниями, которые полностью или частично опосредованы mGluR5, являются, например острые, травматические и хронические дегенеративные процессы нервной системы, такие как болезнь Альцгеймера, старческое слабоумие, болезнь Паркинсона, хорея Хантингтона, боковой амиотрофический склероз и рассеянный склероз, психиатрические заболевания, такие как шизофрения и тревога, депрессия, боль и наркотическая зависимость (Expert Opin. Ther. Patents (2002), 12, (12)).
Новый способ разработки селективных модуляторов состоит в определении соединений, которые действуют посредством аллостерического механизма, модулирую рецептор путем связывания с сайтом, отличающимся от высоко консервативного ортостерического сайта связывания. Позитивные аллостерические модуляторы mGluR5 появились недавно в качестве новых фармацевтических объектов, предлагающих эту привлекательную альтернативу. Позитивные аллостерические модуляторы описаны, например в WO 2008/151184, WO 2006/048771, WO 2006/129199 и WO 2005/044797 и в Molecular Pharmacology, 40, 333-336, 1991; The Journal of Pharmacology and Experimental Therapeutics, Vol 313, No. 1, 199-206, 2005.
Позитивные аллостерические модуляторы представляют собой соединения, которые непосредственно сами не активируют рецепторы, а заметно усиливают агонист-стимулируемые отклики, увеличивают активность и максимум эффективности. Связывание этих соединения увеличивает сродство глутамат-сайта агониста на его внеклеточном N-концевом участке связывания. Таким образом, позитивная аллостерическая модуляция представляет собой привлекательный механизм увеличения активации соответствующего физиологического рецептора. Существует нехватка селективных позитивных аллостерических модуляторов рецептора mGluR5. Традиционные модуляторы рецептора mGluR5 обычно не имеют достаточной растворимости в воде и показывают низкую биодоступность при пероральном введении. Следовательно, остается необходимость в соединениях, которые преодолевают эти недостатки и которые по существу представляют собой селективные позитивные аллостерические модуляторы рецептора mGluR5.
Соединения формулы I отличаются ценными терапевтическими свойствами. Они могут быть использованы при лечении или предотвращении расстройств, при которых могут быть полезны позитивные аллостерические модуляторы рецептора mGluR5.
Наиболее предпочтительными показаниями для соединений, которые представляют собой позитивные аллостерические модуляторы, являются шизофрения и когнитивное нарушение.
Настоящее изобретение относится к соединениям формулы I и их фармацевтически приемлемым солям, к этим соединениям в качестве фармацевтически активных веществ, к способам их изготовления, а также к применению при лечении или предотвращении заболеваний, при которых могут быть полезны позитивные аллостерические модуляторы рецептора mGluR5, таких как шизофрения, туберозный склероз и когнитивное нарушение, и к фармацевтическим композициям, содержащим соединения формулы I.
Следующие определения общих терминов, используемых в настоящем описании, применяются независимо от того, появляются ли рассматриваемые термины отдельно или в сочетании.
Как используется здесь, термин «низший алкил» обозначает насыщенную, т.е. алифатическую углеводородную группу, включающую неразветвленную или разветвленную углеродную цепь с 1-4 атомами углерода. Примерами «алкила» являются метил, этил, н-пропил и изопропил.
Термин «алкокси» обозначает группу -O-R', где R' представляет собой низший алкил, как определено выше.
Термин «этинил» обозначает группу -С≡С-.
Термин «низший алкил, замещенный галогеном» обозначает низшие алкильные группы, как определено выше, где по меньшей мере один атом водорода замещен галогеном.
Термин «низший алкил, замещенный гидрокси» обозначает низшую алкильную группу, как определено выше, где по меньшей мере один атом водорода алкильной группы замещен ОН. Примерами являются гидроксиметил или гидроксиэтил, особенно гидроксиметил.
Термин циклоалкил обозначает насыщенное углеродное кольцо, содержащее от 3 до 7 углеродных кольцевых атомов, например циклопропил, циклобутил, циклопентил, циклогексил или циклогептил.
Термин гетероциклоалкил обозначает насыщенное 4, 5 или 6 членное углеродное кольцо, как описано выше для циклоалкила, где один или более чем один углеродный атом замещен гетероатомом, выбранным из N, О или S, предпочтительными гетероатомами являются N или О. Примерами таких колец являются тетрагидропиран-2, 3 или 4-ил, оксетан-3-ил, оксазолидинил, пирролидинил, 1,3-оксазинанил, тетрагидропиримидинил, имидазолидинил, пиразолидинил, пиперидинил, пиперазинил или морфолинил. Если по меньшей мере один кольцевой атом представляет собой N, то следующие гетероциклильные группы являются предпочтительными:
, выбранные из группы, состоящей из морфолин-3-она, оксазолидин-2-она, пирролидин-2-она, пиперидин-2-она, [1,3]оксазинан-2-она, имидазолин-2-она или пиримидин-2-она.
Термин «фармацевтически приемлемая соль» или «фармацевтически приемлемая кислотно-аддитивная соль» охватывает соли с неорганическими и органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и подобные.
Воплощением изобретения являются соединения формулы IA,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Дополнительным воплощением изобретения являются соединения формулы IA-1,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются, кроме того, соединения формулы IA-2,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются, кроме того, соединения формулы IA-3,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил,=O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются соединения формулы IБ,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил,=O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются соединения формулы IB,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
R4/R4' независимо друг от друга представляют собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются соединения формулы 1Г,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются соединения формулы IД,
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =О, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси; X представляет собой N, CF или СН;
R3 представляет собой водород или низший алкил;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Дополнительным воплощением изобретения являются соединения формулы
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, низший алкил, =O, низший алкокси, фенил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N, CF или СН;
L представляет собой -NR3-, -NHC(R3)2-, -O-, -OC(R3)2-, -CR4R4'-;
представляет собой 5 или 6 членный гетероциклоалкил, выбранный из группы, состоящей из морфолин-3-она, оксазолидин-2-она, пирролидин-2-она, пиперидин-2-она, [1,3]оксазинан-2-она, имидазолин-2-она или пиримидин-2-она;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Воплощением изобретения являются соединения формулы I, где L представляет собой -NR3- и X представляет собой N, например следующие соединения, охватываемые формулой IA-1:
циклопентил-(5-фенилэтинил-пиримидин-2-ил)-амин,
(5-фенилэтинил-пиримидин-2-ил)-(тетрагидро-пиран-4-ил)-амин,
рац-(2,2-диметил-тетрагидро-пиран-4-ил)-(5-фенилэтинил-пиримидин-2-ил)-амин,
рац-7-окса-бицикло[2.2.1]гепт-2-ил-(5-фенилэтинил-пиримидин-2-ил)-амин,
изомерная смесь (2,6-диметокси-циклогексил)-(5-фенилэтинил-пиримидин-2-ил)-амина,
транс-[4-(5-фенилэтинил-пиримидин-2-иламино)-циклогексил]-метанол,
транс-4-(5-фенилэтинил-пиримидин-2-иламино)-циклогексанол,
цис и транс смесь 2-(5-фенилэтинил-пиримидин-2-иламино)-циклогексанола,
цис и транс смесь 3-(5-фенилэтинил-пиримидин-2-иламино)-циклопентанола,
цис и транс смесь 2-(5-фенилэтинил-пиримидин-2-иламино)-циклопентанола,
циклогексил-(5-фенилэтинил-пиримидин-2-ил)-амин,
2,2-диметил-4-(5-фенилэтинил-пиримидин-2-иламино)-циклогексанол или
(1S,4S или 1R,4R)-2,2-диметил-4-(5-фенилэтинил-пиримидин-2-иламино)-циклогексанол.
Дополнительными предпочтительными соединениями из этой группы являются соединения формулы I, где L представляет собой -NR3- и X представляет собой СН, охватываемые формулой IA-2, например следующие соединения:
циклопентил-(5-фенилэтинил-пиридин-2-ил)-амин или
(5-фенилэтинил-пиридин-2-ил)-(тетрагидро-пиран-4-ил)-амин.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -О- и X представляет собой N, охватываемые формулой 1Б, например следующие соединения
рац-4-(5-фенилэтинил-пиримидин-2-илокси)-циклогексанол,
транс-4-(5-фенилэтинил-пиримидин-2-илокси)-циклогексанол или
транс-[3-(5-фенилэтинил-пиримидин-2-илокси)-циклобутил]-метанол.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -CR4R4'- и X представляет собой СН, охватываемые формулой IB, например следующие соединения
3-(5-фенилэтинил-пиридин-2-илметил)-оксазолидин-2-он,
1-метил-3-(5-фенилэтинил-пиридин-2-илметил)-имидазолидин-2-он,
5,5-диметил-1-(5-фенилэтинил-пиридин-2-илметил)-пирролидин-2-он,
1-фенил-3-(5-фенилэтинил-пиридин-2-илметил)-имидазолидин-2-он или
рац-3-[1-(5-фенилэтинил-пиридин-2-ил)-этил]-оксазолидин-2-он.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -CR4R4'- и X представляет собой N, охватываемые формулой IB, например следующее соединение 3-(5-фенилэтинил-пиримидин-2-илметил)-оксазолидин-2-он.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -OC(R3)2- и X представляет собой N, охватываемые формулой IГ, например следующее соединение
2-(3-метил-оксетан-3-илметокси)-5-фенилэтинил-пиримидин.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -NHC(R3)2- и X представляет собой N, охватываемые формулой IД, например следующие соединения
(3-метил-оксетан-3-илметил)-(5-фенилэтинил-пиримидин-2-ил)-амин или
метил-(5-фенилэтинил-пиримидин-2-ил)-(тетрагидро-пиран-4-ил)-амин.
Дополнительным воплощением изобретения являются соединения формулы I, где L представляет собой -NHC(R3)2- и X представляет собой СН, охватываемые формулой IД, например следующее соединение
3-(5-фенилэтинил-пиридин-2-илметил)-оксазолидин-2-он.
Дополнительным воплощением изобретения являются соединения формулы IE, где гетероциклоалкил представляет собой , например следующие соединения
4-(5-фенилэтинил-пиридин-2-илметил)-морфолин-3-он,
3-(5-фенилэтинил-пиридин-2-илметил)-оксазолидин-2-он,
1-(5-фенилэтинил-пиридин-2-илметил)-пиперидин-2-он,
4,4-диметил-1-(5-фенилэтинил-пиридин-2-илметил)-пирролидин-2-он,
3-(5-фенилэтинил-пиридин-2-илметил)-[1,3]оксазинан-2-он,
1-метил-3-(5-фенилэтинил-пиридин-2-илметил)-имидазолидин-2-он,
5,5-диметил-1-(5-фенилэтинил-пиридин-2-илметил)-пирролидин-2-он,
1-фенил-3-(5-фенилэтинил-пиридин-2-илметил)-имидазолидин-2-он,
5,5-диметил-1-(5-фенилэтинил-пиридин-2-илметил)-пиперидин-2-он,
рац-3-метил-1-(5-фенилэтинил-пиридин-2-илметил)-пирролидин-2-он,
1-метил-3-(5-фенилэтинил-пиридин-2-илметил)-тетрагидро-пиримидин-2-он,
рац-3-[1-(5-фенилэтинил-пиридин-2-ил)-этил]-оксазолидин-2-он или
3-(5-фенилэтинил-пиримидин-2-илметил)-оксазолидин-2-он.
Воплощением изобретения являются соединения формулы
где
R1 представляет собой водород, галоген, низший алкил или низший алкил, замещенный галогеном;
R2 представляет собой водород, галоген, низший алкил, =O, низший алкил, замещенный галогеном, низший алкокси, низший алкокси, замещенный галогеном, S(O)2-низший алкил, гидрокси или низший алкил, замещенный гидрокси;
X представляет собой N или СН;
L представляет собой -NH-, -NHC(R3)2-, -O-, -CHR4- или -S(O2)-;
R3 представляет собой водород или низший алкил;
R4 представляет собой водород, гидрокси или низший алкокси;
цик представляет собой циклоалкил или гетероциклоалкил, или представляет собой неароматический бицикл, выбранный из 7-окса-бицикло[2.2.1]гепт-1-ила или бицикло[2.2.1]гепт-1-ила;
n представляет собой 1, 2 или 3;
или их фармацевтически приемлемая кислотно-аддитивная соль, рацемическая смесь, или ей соответствующий энантиомер и/или оптический изомер и/или стереоизомер.
Получение соединений формулы I по настоящему изобретению можно осуществлять последовательными или сходящимися синтетическими процессами. Синтезы соединений по изобретению показаны на следующих схемах 1-8. Навыки необходимые для проведения реакций и очистки полученных в результате продуктов известны квалифицированному специалисту в данной области. Заместители и индексы, используемые в следующем описании способов, имеют значения, приведенные выше.
Соединения формулы I могут быть изготовлены способами, приведенными ниже, способами, приведенными в примерах, или аналогичными способами. Соответствующие реакционные условия для отдельных стадий реакций известны квалифицированному специалисту в данной области. Последовательность реакций не ограничивается той, что изображена на схемах, однако в зависимости от исходных веществ и их соответствующей реакционной способности последовательность стадий реакций может быть легко изменена. Исходные вещества либо имеются в продаже, либо могут быть получены способами, аналогичными способам, приведенным ниже, или способами, описанными в ссылках, приведенных в описании или в примерах, или способами, известными в данной области.
Настоящие соединения формулы I и их фармацевтически приемлемые соли могут быть получены способами, известными в данной области, например вариантами способов, описанных ниже, согласно которым
а) подвергают взаимодействию соединение формулы
с подходящим амином формулы
в присутствии основания, выбранного из триэтиламина, и растворителя, выбранного из ТГФ,
чтобы получить соединение формулы
где заместители описаны выше, или
б) проводят восстановительное аминирование соединения формулы
с соединением формулы
чтобы получить соединение формулы
где заместители описаны выше, или
в) подвергают взаимодействию соединение формулы
с подходящим фенилацетиленовым соединением формулы
в присутствии бис-(tpp)-Pd(ll)Cl2, Cul и основания, выбранного из триэтиламина, и растворителя, выбранного из ТГФ, чтобы получить соединение формулы
где заместители описаны выше, или
г) подвергают взаимодействию соединение формулы
с подходящим амином формулы
в присутствии основания, выбранного из триэтиламина, и растворителя, выбранного из ТГФ,
чтобы получить соединение формулы
где заместители описаны выше, или
д) подвергают взаимодействию соединение формулы
с подходящим соединением формулы
в присутствии CsCO3 и диоксана,
чтобы получить соединение формулы
где заместители описаны выше, или
е) подвергают взаимодействию соединение формулы
с подходящим соединением формулы
в присутствии основания, выбранного из триэтиламина, и растворителя, выбранного из ТГФ,
чтобы получить соединение формулы
где заместители описаны выше, или
ж) подвергают взаимодействию соединение формулы
с подходящим соединением формулы
в присутствии MeSO2Cl,
чтобы получить соединение формулы
где заместители описаны выше, или
при желании переводят полученные соединения в фармацевтически приемлемые кислотно-аддитивные соли.
Кроме того, получение соединений формулы I более подробно описано на схемах 1-8, и в примерах 1-44.
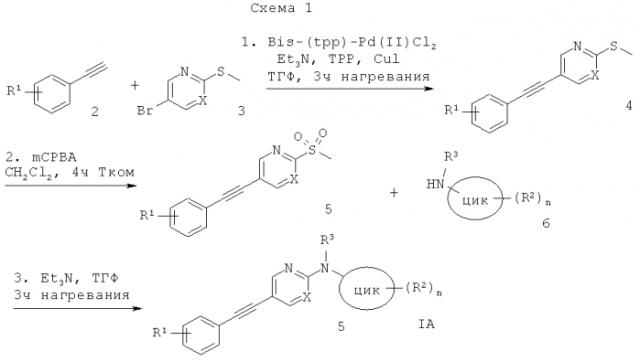
(5-Фенилэтинил-пиримидин-2-ил)-амин формулы IA можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с 5-бром-2-метилсульфанил-пиримидином (3), что дает соответствующие метансульфанильные производные (4). Окисление тиоэфирного соединения с окислителем, таким как mCPBA (м-хлорпероксибензойная кислота), в растворителе, подобном дихлорметану, дает соответствующее производное сульфона (5). Реакция производного сульфона с соответствующе замещенным амином (6) в присутствии основания, такого как триэтиламин, в растворителе, подобном ТГФ, дает требуемый (5-фенилэтинил-пиримидин-2-ил)-амин формулы IA.
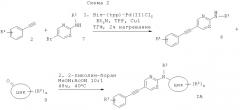
(5-Фенилэтинил-пиридин-2-ил)-амин формулы IA можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с амином (7), что дает соответствующие производные 5-фенилэтинил-пиридин-2-иламина (8). Восстановительное аминирование производных 5-фенилэтинил-пиридин-2-иламина с соответствующе замещенным кетоном (9) с восстановителем, таким как 2-пиколин-боран, в смеси растворителей, такой как метанол: уксусная кислота (10:1, об/об), дает требуемые (5-фенилэтинил-пиридин-2-ил)-амины формулы IA.
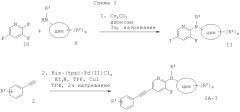
(5-Фенилэтинил-3-фторпиридин-2-ил)-амин формулы IA-3 можно получить по реакции 2,3-дифтор-5-йодпиридина с соответствующе замещенным амином (6) в присутствии основания, такого как Cs2CO3, в растворителе, подобном диоксану, что дает требуемый (5-йод-3-фторпиридин-2-ил)-амин (11). Сочетание Соногашира с соответствующе замещенным фенилацетиленом (2) давало требуемый (5-фенилэтинил-3-фторпиридин-2-ил)-амин формулы IA-3.
(5-Фенилэтинил-пиримидин-2-ил)-амин формулы IД (X=N) можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с 5-бром-2-метилсульфанил-пиримидином (3), что дает соответствующие метансульфанильные производные (4). Окисление тиоэфирного соединения с окислителем, таким как mCPBA, в растворителе, подобном дихлорметану, дает соответствующие производные сульфона (5). Реакция производных сульфона с соответствующе замещенным амином (12) в присутствии основания, такого как триэтиламин, в растворителе, подобном ТГФ, дает требуемый (5-фенилэтинил-пиримидин-2-ил)-амин формулы IД.
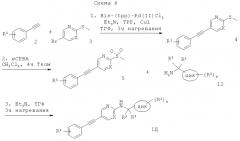
(5-Фенилэтинил-пиримидин-2-илокси)-производные или (5-фенилэтинил-пиридин-2-илокси)-производные формулы IB (X=-N= или -СН=) можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с 5-бром-2-метилсульфанил-пиримидином или пиридином (3), что дает соответствующие метансульфанильные производные (4). Окисление тиоэфирного соединения с окислителем, таким как плСРВА, в растворителе, подобном дихлорметану, дает соответствующее производное сульфона (5). Реакция производных сульфона с соответствующе замещенным спиртом (13) в присутствии основания, такого как Cs2CO3, в растворителе, подобном диоксану, дает требуемые (5-фенилэтинил-пиримидин-2-илокси)-производные или (5-фенилэтинил-пиридин-2-илокси)-производные формулы 1Б.
(5-Фенилэтинил-пиримидин-2-илокси)-производные или (5-фенилэтинил-пиридин-2-илокси)-производные формулы 1Г можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с 5-бром-2-метилсульфанил-пиримидином или пиридином (3), что дает соответствующие метансульфанильные производные (4). Окисление тиоэфирного соединения с окислителем, таким как mCPBA, в растворителе, подобном дихлорметану, дает соответствующие производные сульфона (5). Реакция производных сульфона с соответствующе замещенным спиртом (14) в присутствии основания, такого как Cs2CO3, в растворителе, подобном диоксану, дает требуемые (5-фенилэтинил-пиримидин-2-илокси)-производные или (5-фенилэтинил-пиридин-2-илокси)-производные формулы 1Г.
Производные (5-фенилзтинил-пиридин-2-ил)-спирта или производные (5-фенилэтинил-пиримидин-2-ил)-спирта формулы IB можно получить сочетанием Соногашира соответствующе замещенного фенилацетилена (2) с соответствующим 5-бром-2-пиридин-2-ил-спиртом или 5-бром-2-пиримидин-2-ил-спиртом (15), что дает соответствующие производные спирта (16). Реакция спирта (16) до соответствующего метансульфонильного эфира с метансульфонилхлоридом в присутствии основания, такого как триэтиламин, в растворителе, подобном дихлорметану, с последующим связыванием с соответствующе замещенным лактамом, гетероциклической мочевиной или гетероциклическим карбаматом (17), который был депротонирован с гидридом натрия в растворителе, подобном ДМФА, дает требуемые производные (5-фенилэтинил-пиридин-2-ил)-спирта или производные (5-фенилэтинил-пиримидин-2-ил)-спирта формулы IB.
Третичный (5-фенилэтинил-пиридин-2-ил)-амин или (5-фенилэтинил-пиримидин-2-ил)-амин формулы IA, где R3 представляет собой низший алкил, можно получить в ходе депротонирования соответствующе замещенного вторичного амина (IA) с сильным основанием, таким как гидрид натрия, в растворителе, подобном ДМФА, с последующим алкилированием с соответствующим алкилгалогенидом, что дает требуемый третичный (5-фенилэтинил-пиридин-2-ил)-амин или (5-фенилэтинил-пиримидин-2-ил)-амин формулы IA.
Предпочтительно соединение формулы I, как описано здесь, а также его фармацевтически приемлемую соль применяют для лечения или предотвращения психоза, эпилепсии, шизофрении, болезни Альцгеймера, когнитивных расстройств и нарушений памяти, хронической и острой боли, ограниченной функции мозга, вызванной операциями шунтирования или трансплантациями, недостаточного мозгового кровоснабжения, травм спинного мозга, травм головы, гипоксии, вызванной беременностью, остановки сердца и гипогликемии, ишемии, хореи Хантингтона, бокового амиотрофического склероза (ALS), слабоумия, вызванного СПИДом, травм глаз, ретинопатии, идиопатического паркинсонизма или лекарственного паркинсонизма, спазмов мышц, конвульсий, мигрени, недержания мочи, гастроэзофагеальной рефлюксной болезни, повреждения печени или печеночной недостаточности, вызванной либо лекарствами, либо болезнью, синдрома ломкой Х-хромосомы, синдром Дауна, аутизма, никотиновой зависимости, опиатной зависимости, тревоги, рвоты, дискинезии, расстройств пищевого поведения, а именно булимии или нервной анорексии, и депрессий, особенно для лечения и предотвращения, острых и/или хронических неврологических нарушений, тревоги, лечения хронической и острой боли, недержания мочи и ожирения.
Предпочтительными показаниями являются шизофрения и когнитивные расстройства.
Кроме того, настоящее изобретение относится к применению соединения формулы I, как описано здесь, а также его фармацевтически приемлемой соли для изготовления лекарства, предпочтительно для лечения и предотвращения вышеупомянутых расстройств.
Биологические анализ и данные:
Анализ внутриклеточной мобилизации Са2+
Получали линию моноклональных клеток НЕК-293, стабильно трансфицированных с кДНК, кодирующей рецептор mGlu5a человека; для работы с позитивными аллостерическими модуляторами mGlu5 (ПАМ) отбирали клеточную линию с низкими уровнями экспрессии рецепторов и низкой конститутивной рецепторной активностью, что позволяло дифференцировать агонистическую активность в сравнении с ПАМ. Клетки культивировали в соответствии со стандартными протоколами (Freshney, 2000) в модифицированной по способу Дульбекко среде Игла с высоким содержанием глюкозы с добавлением 1 мМ глутамина, 10% (об/об) термоинактивированной бычьей телячьей сыворотки, пенициллина/стрептомицина, 50 мкг/мл гигромицина и 15 мкг/мл бластицидина (все клеточные культуры, реагенты и антибиотики получали от Invitrogen, Базель, Щвейцария).
Приблизительно за 24 часа до эксперимента 5×104 клетки/лунка высеивали на покрытые поли-О-лизином черные / с прозрачным дном 96-луночные планшеты. Клетки загружали с 2,5 мкМ Fluo - 4АМ в загрузочный буфер (1×HBSS, 20 мМ HEPES) в течение 1 часа при 37°С и промывали пять раз загрузочным буфером. Клетки переносили в Functional Drug Screening System 7000 (Hamamatsu, Париж, Франция) и добавляли 11 с половиной логарифмически последовательно разведенных растворов исследуемого соединения при 37°С и клетки инкубировали в течение 10-30 минут с регистрацией флуоресценции в режиме реального времени. После этой стадии предварительной инкубации агонист L-глутамата добавляли в клетки при концентрации, соответствующей ЕС20 (обычно около 80 мкМ) с регистрацией флуоресценции в режиме реального времени, чтобы учесть суточные колебания в реакционной способности клеток, ЕС20 глутамата определяли непосредственно перед каждым экспериментом в ходе записи полной кривой доза - эффект глутамата.
Отклики измеряли как увеличение пика при флуоресценции за минусом основного (т.е. флуоресценция без добавления L-глутамата), приведенного к максимальному стимулирующему эффекту, полученному с насыщенными концентрациями L-глутамата. Графики строили с % максимального стимулирующего эффекта, используя XLfit, программу вычерчивания кривых, которая итерационно наносит данные, используя алгоритм Левенберга-Марквардта. Используемое уравнение анализа конкуренции одиночных сайтов представляло собой у=А+((B-A)/(1+((x/C)D))), где у представляет собой % максимального стимулирующего эффекта, А представляет собой минимальное значение у, В представляет собой максимальное значение у, С представляет собой ЕС50, x представляет собой log 10 концентрации конкурирующего соединения и D представляет собой наклон кривой (коэффициент Хилла). Из этих кривых рассчитывали ЕС50 (концентрация, при которой достигалась полумаксимальная стимуляция), коэффициент Хилла, а такж