Способ получения n-циклопентилзамещенных 1,5,3-дитиазепанов
Иллюстрации
Показать всеИзобретение относится к способу получения N-циклопентилзамещенных 1,5,3-дитиазепанов общей формулы (1):
, где
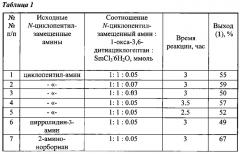
отличающийся тем, что N-циклопентилзамещенный амин (циклопентил-амин, пирролидин-3-амин, 2-амино-норборнан) подвергают взаимодействию с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O при мольном соотношении N-циклопентилзамещенный амин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O = 1:1:(0.03-0.07) при комнатной температуре (~20°C) в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч. Соединения могут найти применение в качестве противомикробных, антигрибковых и противовоспалительных агентов, а также селективных комплексообразователей. 1 табл., 1 пр.
Реферат
Предлагаемое изобретение относится к области органической химии, в частности к способу получения N-циклопентилзамещенных 1,5,3-дитиазепанов общей формулы (1):
S,N-содержащие гетероциклы известны как противомикробные (Bialy Serry А.А., Abdelal A.M., El-Shorbagi A., Kheira Samy M.M. Archiv der Pharmazie, 2005, 338, 1, 38-43), антигрибковые (Akhmetova V.R., Niatshina Z.T., Burakaeva A.D., Galimzyanova N.F., Kunakova R.V. Russian Journal of Applied Chemistry, 2011, 84, 3, 416-419) и противовоспалительные агенты (Akhmetova V.R., Khairullina R.R., Parfenova T.I., Sufiyarova R.Sh., Bashkatov S.A., Kunakova R.V. Pharmaceutical Chemistry Journal, 2011, 44, 10, 534-535), а также селективные комплексообразователи (Akhmetova V.R., Rakhimova E.B., Vagapov R.A., Minnebaev A.B., Korylova E.V., Buslaeva T.M., Kunakova R.V. Trends in Heterocyclic Chemistry, 2011, Vol. 15, No. 9, P. 33-41; Galves-Ruiz J.C., Noth H., Flores-Parra A. Inorg. Chem., 2003, 42, 7569-7578).
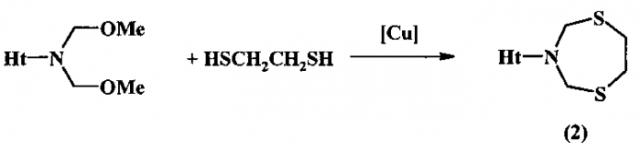
Известен способ (H.H. Махмудиярова, К.И. Прокофьев, Л.В. Мударисова, А.Г. Ибрагимов, У.М. Джемилев. ЖОрХ, 2013, 5, 658) получения 3-гетарил-1,5,3-дитиазепанов (2) реакцией N,N-бис(метоксиметил)гетариламинов с 1,2-этандитиолом под действием катализатора CuCl2.
Известным способом не могут быть получены N-циклопентилзамещенные 1,5,3-дитиазепаны общей формулы (1).
Известен способ (Tsotinis Α., Eleutheriades Α., Bari L. Di, Pescitelli G.J. Org. Chem. 2007, 72, 8928) получения конденсированного пергидро-1,5,3-дитиазепана (3) реакцией N-ацил индолов с 1,2-этандитиолом под действием катализатора BF3·Et2O.
Известным способом не могут быть получены N-циклопентилзамещенные 1,5,3-дитиазепаны общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению N-циклопентилзамещенных 1,5,3-дитиазепанов общей формулы (1).
Предлагается новый способ получения N-циклопентилзамещенных 1,5,3-дитиазепанов общей формулы (1).
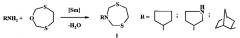
Сущность способа заключается во взаимодействии N-циклопентилзамещенных аминов (циклопентил-амин, пирролидин-3-амин, 2-амино-норборнан) с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O, взятыми в мольном соотношении N-циклопентилзамещенный амин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O=1:1:(0.03-0.07), предпочтительно 1:1:0.05, при комнатной температуре (~20°C) и атмосферном давлении в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч. Выход N-циклопентилзамещенных 1,5,3-дитиазепанов (1) составляет 49-67%. Реакция протекает по схеме:
N-Циклопентилзамещенные 1,5,3-дитиазепаны общей формулы (1) образуются только лишь с участием N-циклопентилзамещенных аминов и 1-окса-3,6-дитиациклогептана, взятых в стехиометрических количествах. При другом соотношении исходных реагентов снижается селективность реакции. Без катализатора SmCl3·6H2O реакция идет с выходом, не превышающим 15%. Проведение реакции в присутствии катализатора SmCl3·6H2O больше 7 мол.% по отношению к N-циклопентилзамещенному амину не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора SmCl3·6H2O менее 3 мол.% снижает выход (1), что связано с уменьшением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре ~20°C. При более высокой температуре (например, 60°C) увеличиваются энергозатраты, при меньшей температуре (например, 0°C) снижается скорость реакции. Опыты проводили в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа.
В известном способе реакция идет с участием в качестве исходных реагентов N,N-бис(метоксиметил)гетариламинов и 1,2-этандитиола в присутствии катализатора CuCl2 с образованием 3-гетарил-1,5,3-дитиазепанов (2). Известный способ не позволяет получать N-циклопентилзамещенные 1,5,3-дитиазепаны общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются N-циклопентилзамещенные амины (циклопентил-амин, пирролидин-3-амин, 2-амино-норборнан) и 1-окса-3,6-дитиациклогептан, реакция идет под действием катализатора SmCl3·6H2O.
Предлагаемый способ обладает следующими преимуществами.
Способ позволяет получать с высокой селективностью индивидуальные N-циклопентилзамещенные 1,5,3-дитиазепаны общей формулы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, помещают 85 мг (1 ммоль) циклопентил-амина в 5 мл этанола, 18 мг (0.05 ммоль) SmCl3·6H2O и 136 мг (1 ммоль) 1-окса-3,6-дитиациклогептана в 5 мл хлороформа. Реакционную смесь перемешивают при температуре ~20°C в течение 3 ч, колоночной хроматографией на SiO2 выделяют 3-циклопентил-1,5,3-дитиазепан с выходом 55%.
Другие примеры, подтверждающие способ, приведены в таблице 1.
Все опыты проводили при комнатной температуре (~20°C) в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них растворяются исходные и целевые продукты.
Спектральные характеристики
3-циклопентил-1,5,3-дитиазепана1: (1 Контроль реакции осуществляли методом ТСХ на пластинах Sorbfil (ПТСХ-АФ-В), проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Спектры ЯМР 1D (1Н, 13С) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Bruker Avance 400 (100.62 МГц для 13С и 400.13 МГц для 1Н) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс-спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker).
Спектр ЯМР 1H, δ, м.д.: 1.39-1.43 м (2Н, CH2, Ha-9,12); 1.60-1.66 м (2Н, CH2, Ha-10,11); 1.68-1.76 м (2Н, CH2, Hb-10,11); 1.89-1.94 м (2Н, CH2, Hb-9,12); 3.06 уш. с (4Н, CH2, H-6,7); 3.28-3.35 м (1Н, CH, H-8); 4.26 уш. с (4Н, CH2, H-2,4).
Спектр ЯМР13С, δ, м.д.: 23.52 (С-10,11), 30.75 (С-9,12), 36.01 (С-6,7), 58.74 (С-2,4), 60.07 (С-8).
MALDI TOF, m/z: 202 [М-Н]+ (100%), 204 [М+Н]+ (79%).
Спектральные характеристики
3-пирролидин-3-ил-1,5,3-дитиазепана.
Спектр ЯМР 1H, δ , м.д.: 1.40-1.47 м (2Н, CH2, Н-12); 2.46-2.51 м (2Н, CH2, Н-11); 2.75-2.81 м (2Н, CH2, Н-9); 3.10 уш. с (1H, CH, Н-8); 3.04 уш. с (4Н, CH2, Н-6,7); 4.72 уш. с (4Н, CH2, Н-2,4).
Спектр ЯМР13С, δ, м.д.: 30.82 (С-12), 35.44 (С-6,7), 44.21 (С-11), 53.25 (С-9), 58.33 (С-2,4), 60.12 (С-8).
Спектральные характеристики
3-бицикло[2.2.1]гепт-2-ил-1,5,3-дитиазепана.
Спектр ЯМР 1H, δ, м.д. (J, Гц): 1.11 уш. с (1Н, CH2, Ha-10); 1.13 уш. с (1Н, CH2, Ha-14); 1.17-1.23 м (1Н, CH2, Ha-13); 1.44-1.49 м (4Н, CH2, Hb-10, Н-12, Hb-14); 1.54-1.60 м (1Н, CH2, Hb-13); 2.29 уш. с (1Н, CH, Н-11); 2.36 уш. с (1Н, CH, Н-9); 2.94-2.96 м (1Н, СН, Н-8); 2.99-3.05 м (2Н, CH2, Ha-6,7); 3.09-3.15 м (2Н, CH2, Hb-6,7); 4.21 д (2Н, CH2, Ha-2,4, J 19.6); 4.23 д (2Н, CH2, Hb-2,4, J 19.6).
Спектр ЯМР13С, δ, м.д.: 27.52 (С-13), 28.38 (С-14), 35.20 (С-10), 35.82 (С-6,7), 36.26 (С-11), 37.30 (С-12), 38.14 (С-9), 57.26 (С-2,4), 61.50 (С-8).
MALDI TOF, m/z: 228 [М-Н]+ (100%), 230 [M+H]+ (49%).
Способ получения N-циклопентилзамещенных 1,5,3-дитиазепанов общей формулы (1): , где ,отличающийся тем, что N-циклопентилзамещенный амин (циклопентил-амин, пирролидин-3-амин, 2-амино-норборнан) подвергают взаимодействию с 1-окса-3,6-дитиациклогептаном в присутствии катализатора SmCl3·6H2O при мольном соотношении N-циклопентилзамещенный амин:1-окса-3,6-дитиациклогептан:SmCl3·6H2O = 1:1:(0.03-0.07) при комнатной температуре (~20°C) в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч.