Сложные арилалкиловые эфиры 4-амино-6-(замещенный фенил)пиколинатов и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоксилатов и их применение в качестве гербицидов
Иллюстрации
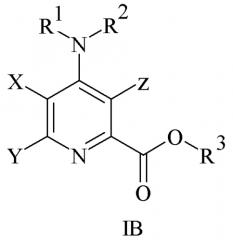
Показать всеИзобретение относится к новым сложным арилалкиловым эфирам 4-аминопиколиновых кислот формулы IB, которые обладают гербицидным действием и могут быть использованы для борьбы с нежелательной растительностью (сорняками). Соединения обладают избирательным действием и особенно применимы для борьбы на послевсходовой стадии с теми видами, которые, как правило, встречаются в системах для выращивания риса, пшеницы или кормовых растений. В формуле IB:
X представляет собой Н или F; Y представляет собой фенил, замещенный 1-4 заместителями, независимо выбранными из галогена, С3-С6циклоалкила, C1-C3алкокси, C1-C3галогеналкила, C1-C3галогеналкокси; Z представляет собой галоген; R1 и R2 представляют собой Н; R3 представляет собой арилалкил, выбранный из нафтил-(С1-2)алкила или фенил-(С1-2)алкила, который может быть незамещенным или замещенным 1-2 заместителями, независимо выбранными из галогена, нитро, циано, С1-С6алкила, С1-С6алкокси, галогенированного С1-С6алкила, галогенированной С1-С6алкокси, С1-С6алкилтио, С(О)OC1-С6алкила, или где два смежных заместителя, взятые вместе, представляют собой -O(СН2)nO- или -O(СН2)n-, где n=1 или 2. 4 н. и 5 з.п. ф-лы, 28 табл., 17 пр.
Реферат
Настоящее изобретение относится к конкретным новым сложным эфирам 4-амино-6-(замещенный фенил)пиколиновых кислот и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоновых кислот и к применению этих соединений в качестве гербицидов для борьбы с сорняками, особенно с теми видами, которые, как правило, встречаются в системах для выращивания риса и пшеницы и в программах улучшения пастбищ.
Многие пиколиновые кислоты и их пестицидные свойства описаны в области техники. Патент США 6784137 B2 и патент США 7314849 B2 раскрывают семейство 4-амино-6-арилпиколиновых кислот и их производные и их применение в качестве гербицидов избирательного действия, в частности, для риса и зерновых злаков, таких как пшеница и ячмень. WO 2005/063721 A1, WO 2007/082076 A1, патент США 7863220 B2, патент США 7300907 B2, патент США 7642220 B2 и патент США 7786044 B2 раскрывают конкретные 6-амино-2-замещенные-4-пиримидинкарбоновые кислоты и их производные и их применение в качестве гербицидов. В настоящее время обнаружено, что определенные сложные эфиры 4-амино-6-(замещенный фенил)пиколиновых кислот и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоновых кислот могут обеспечивать превосходную борьбу с сорняками, особенно, в системах для выращивания риса и пшеницы и в программах улучшения пастбищ.
Определенные сложные арилалкиловые эфиры 4-амино-6-(замещенный фенил)пиколиновых кислот и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоновых кислот являются превосходными гербицидами с широким спектром борьбы с широколиственными, травянистыми и осоковыми сорняками, особенно в системах для выращивания риса и пшеницы и в программах улучшения пастбищ. Соединения дополнительно обладают отличными токсикологическими или экологическими профилями.
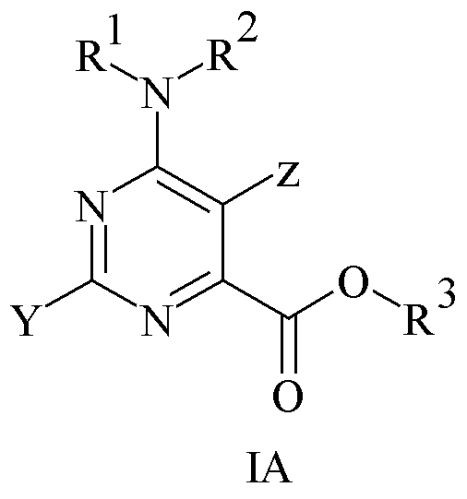
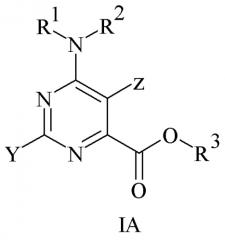
Настоящее изобретение включает соединения формулы IA:
где
Y представляет собой С1-C8 алкил, C3-C6 циклоалкил или фенил, замещенный 1-4 заместителями, независимо выбранными из галогена, C1-C3 алкила, C3-C6 циклоалкила, C1-C3 алкокси, C1-C3 галогеналкила, C1-C3 галогеналкокси, циано, нитро, NR1R2, или где два смежных заместителя, взятые вместе, представляют собой -O(CH2)nO- или -O(CH2)n-, где n=1 или 2;
Z представляет собой галоген, C1-C3 алкокси или C2-C4 алкенил;
R1 и R2 независимо друг от друга представляют собой H, C1-C6 алкил или C1-C6 ацил;
R3 представляет собой незамещенный или замещенный C7-C11 арилалкил.
Предпочтительные соединения включают такие, в которых Y представляет собой замещенный фенил, Z представляет собой Cl, -CH=CH2 или OCH3, R1 и R2 представляют собой H, R3 представляет собой незамещенный или орто-, мета- или пара-монозамещенный бензил.
Настоящее изобретение также включает соединения формулы IB:
где
X = H или F;
Y представляет собой галоген, C1-C8 алкил, C3-C6 циклоалкил или фенил, замещенный 1-4 заместителями, независимо выбранными из галогена, C1-C3 алкила, C3-C6 циклоалкила, C1-C3 алкокси, C1-C3 галогеналкила, C1-C3 галогеналкокси, циано, нитро, NR1R2, или где два смежных заместителя, взятые вместе, представляют собой -O(CH2)nO- или -O(CH2)n-, где n=1 или 2;
Z представляет собой галоген или C2-C4 алкенил;
R1 и R2 независимо представляют собой H, C1-C6 алкил или C1-C6 ацил;
R3 представляет собой незамещенный или замещенный C7-C11 арилалкил.
Предпочтительные соединения включают такие, в которых X представляет собой H или F, Y представляет собой замещенный фенил, Z представляет собой Cl, R1 и R2 представляют собой H, R3 представляет собой незамещенный или орто-, мета- или пара-монозамещенный бензил.
Настоящее изобретение включает гербицидные композиции, содержащие гербицидно эффективное количество соединения формулы IA или IB в смеси с приемлемым с точки зрения сельского хозяйства вспомогательным средством или носителем. Настоящее изобретение также включает способ применения соединений и композиций по настоящему изобретению для уничтожения или борьбы с нежелательной растительностью путем применения гербицидного количества соединения к растительности или к локусу растительности, а также к почве до появления растительности или к поливной или заливаемой воде до или после появления всходов. Настоящее изобретение дополнительно включает способ избирательной борьбы с нежелательной растительностью на послевсходовой стадии в присутствии риса, пшеницы или кормовых растений, включающий применение к указанной нежелательной растительности гербицидно эффективного количества соединения по настоящему изобретению. Настоящее изобретение также включает способ получения соединений по настоящему изобретению.
Гербицидные соединения по настоящему изобретению являются сложными арилалкиловыми эфирами 4-амино-6-(замещенный фенил)пиколиновых кислот и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоновых кислот и их производных. Пиколиновые кислоты, из которых получают сложные эфиры формулы IB, представляют собой новый класс соединений, обладающих гербицидным действием. Многие соединения пиколиновых кислот описаны в патенте США 6784137 B2 и патенте США 7314849 B2, включая inter alia, 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метокси-фенил)пиколиновую кислоту, 4-амино-3-хлор-5-фтор-6-(4-хлор-2-фтор-3-метоксифенил)пиколиновую кислоту и 4-амино-3-хлор-6-(2,4-дихлор-3-метоксифенил)пиколиновую кислоту. Пиримидинкарбоновые кислоты, такие, из которых получают сложные эфиры формулы IA, также представляют собой новый класс соединений, обладающих гербицидным действием. Многие соединения пиримидинкарбоновых кислот описаны в WO 2005/063721 A1, WO 2007/082076 A1, патенте США 7863220 B2, патенте США 7300907 B2, патенте США 7642220 B2 и патенте США 7786044 B2. Эти пиколиновые и пиримидинкарбоновые кислоты действуют против однолетних травянистых сорняков, широколиственных сорняков и осоковых сорняков в рисе и пшенице, но сложные арилалкиловые эфиры по настоящему изобретению демонстрируют более эффективное действие, чем известные сложные эфиры, особенно против сорняков, встречающихся в системах для выращивания риса и пшеницы и в программах улучшения пастбищ.
Предпочтительными сложноэфирными группами являются те, которые обеспечивают больший уровень борьбы с сорняками по сравнению с нормой внесения сложных метиловых эфиров в экв.иваленте кислоты. Предпочтительные сложноэфирные группы включают незамещенный сложный бензиловый эфир и орто-, мета- и пара-монозамещенные сложные бензиловые эфиры.
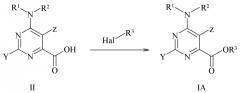
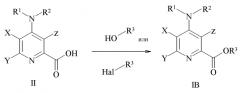
Сложные арилалкиловые эфиры 6-амино-2-(замещенный фенил)-4-пиримидинкарбоновых кислот могут быть получены путем реакции пиримидинкарбоновых кислот с арилалкилгалогенидом в присутствии основания.
Схема 1
Сложные арилалкиловые эфиры пиколиновых кислот могут быть получены путем связывания пиколиновой кислоты со спиртом с применением любого из числа подходящих активаторов, таких как применяемые для связывания пептидов, таких как дициклогексилкарбодиимид (DCC) или карбонилдиимидазол (CDI), или путем реакции соответствующей кислоты с соответствующим арилалкиловым спиртом в присутствии кислотного катализатор. Альтернативно, сложные арилалкиловые эфиры могут быть получены путем реакции пиколиновой кислоты с арилалкилгалогенидом в присутствии основания.
Схема 2
Считается, что некоторые реагенты и условия реакции, раскрытые в настоящем описании или в химической литературе с получением соединения формулы IA или IB, могут не быть совместимы с определенными функциональными свойствами, присущими промежуточным продуктам. В этих случаях введение блокирующих/снятие блокирующих последовательностей или взаимное превращение функциональных групп в ходе синтеза будет способствовать получению желаемых продуктов. Применение и выбор блокирующих групп будут очевидны специалисту области химического синтеза.
Термины «алкил», «алкенил» и «алкинил», а также производные термины, такие как «алкокси», «ацил» и «алкилтио», как используется в настоящем описании, охватывают фрагменты с прямой и разветвленной цепью. Если не указано иначе, каждый из них может быть незамещенным или замещенным одним или более заместителями, выбранными из, но не ограничиваясь ими, галогена, алкокси, алкилтио или аминоалкила, при условии, что заместители являются стерически совместимыми, и соблюдаются условия образования химической связи и энергии деформации. Термины «алкенил» и «алкинил» предназначены для обозначения включения одной или более ненасыщенных связей.
Термин «арилалкил», как используется в настоящем описании, относится к фенилзамещенной алкильной группе, содержащей в общей сложности 7-11 углеродных атомов, такой как бензил (-CH2C6H5), 2-метилнафтил(-CH2C10H7) и 1- или 2-фенэтил (-CH2CH2C6H5 или -CH(CH3)C6H5). Фенильная группа может быть сама по себе незамещенной или замещенной одним или более заместителями, независимо выбранными из галогена, нитро, циано, C1-C6 алкила, C1-C6 алкокси, галогенированного C1-C6 алкила, галогенированной C1-C6 алкокси, C1-C6 алкилтио, C(O)OC1-С6алкила, или где два смежных заместителя, взятые вместе, представляют собой O(CH2)nO-, где n=1 или 2, при условии, что заместители являются стерически совместимы, и соблюдаются условия образования химической связи и энергии деформации.
Если иначе конкретно не ограничено, термин "галоген" включает фтор, хлор, бром и иод.
Обнаружено, что соединения формулы IA или IB являются подходящими в качестве предвсходовых и послевсходовых гербицидов для системах для выращивания риса и зерновых злаков и для программ улучшения пастбищ. Термин "гербицид" используется в настоящем описании для обозначения активного ингредиента, уничтожающего, регулирующего или иным образом неблагоприятно модифицирующего рост растений. Гербицидно эффективным или регулирующим рост растительности количеством активного ингредиента является количество, которое вызывает неблагоприятный модифицирующий эффект, включающий отклонения от естественного развития, уничтожение, регулирование, высушивание, задержку роста и т.п. Термины "растения" и "растительность" включают прорастающие семена, появляющиеся всходы, надземные и подземные части растений, такие как побеги, корни, клубни, ризома и т.п. и установившуюся растительность.
Гербицидное действие, демонстрируемое соединениями по настоящему изобретению, при их применении непосредственно к растению или к локусу растения на любой стадии роста или до посадки или всхода. Наблюдаемый эффект зависит от видов растений, с которыми необходимо бороться, стадии роста растения, параметров разведения для применения и размера разбрызгиваемых капель, величины частиц твердых компонентов, условий окружающей среды во время применения, конкретного применяемого соединения, конкретных вспомогательных средств и применяемых носителей, типа почвы, качества воды и т.п., а также от количества применяемого химиката. Эти и другие факторы могут быть отрегулированы так, как известно в области техники, для усиления избирательного гербицидного действия. В целом, для достижения максимального результата борьбы с сорняками предпочтительно применение соединений формулы IA или IB на послевсходовой стадии путем разбрызгивания или с поливной водой к относительно незрелой нежелательной растительности.
Нормы внесения 1-500 грамм на гектар (г/га), в целом, применяют при листовых и водных обработках на послевсходовой стадии. Предпочтительные нормы внесения составляют 10-300 г/га. Для применений на довсходой стадии, в целом, применяют нормы внесения 5-500 г/га. Предпочтительные нормы внесения составляют 30-300 г/га. Более высокие указанные нормы внесения, в целом, приводят к неизбирательной борьбе с широким спектром нежелательной растительности. Более низкие нормы внесения, как правило, приводят к избирательной борьбе и могут быть применены к локусам сельскохозяйственных культур.
Гербицидные соединения по настоящему изобретению часто применяют вместе с одним или более другими гербицидами для борьбы с более широким спектром нежелательной растительности. При применении вместе с другими гербицидами, представленые в настоящем описании соединения могут быть составлены в композицию с другим гербицидом или гербицидами, смешаны с другим гербицидом или гербицидами в резервуаре или применены последовательно с другим гербицидом или гербицидами. Некоторые гербициды, которые могут быть применены вместе с соединениями по настоящему изобретению, включают: соли 2,4-Д, сложные эфиры и амины, ацетохлор, ацифлуорфен, алахлор, амидосульфурон, аминопиралид, аминотриазол, тиоциатат аммония, анилифос, атразин, азимсульфурон, бенфуресат, бенсульфурон-метил, бентазон, бентиокарб, бензобициклон, бензофенап, бифенокс, биспирибак-натрий, бромбутид, бутахлор, кафенстрол, карфентразон-этил, клодинафоп-пропаргил, хлоримурон, хлорпрофам, циносульфурон, клетодим, кломазон, кломепроп, клопиралид, клорансулам-метил, циклосульфамурон, циклоксидим, цигалофоп-бутил, кумилурон, даимурон, диклосулам, дифлуфеникан, дифлуфензопир, димепиперат, диметаметрин, дикват, дитиопир, EK2612, EPTC, эспрокарб, ET-751, этоксисульфурон, этбензанид, феноксапроп, феноксапроп-этил, феноксапроп-этил + изоксадифен-этил, фентразамид, флазасульфурон, флорасулам, флуазифоп, флуазифоп-P-бутил, флуцетосульфурон, флуфенацет, флуфенпир-этил, флуметсулам, флумиоксазин, флупирсульфурон, флуроксипир, фомесафен, форамсульфурон, глуфосинат, глуфосинат-P, глифосат, галосульфурон-метил, галоксифоп-метил, галоксифоп-R, галоксифоп-R-метил, имазаметабенз, имазамокс, имазапик, имазапир, имазаквин, имазетапир, имазосульфурон, инданофан, иоксинил, ипфенкарбазон, изоксабен, MCPA, MCPB, мефенацет, мезосульфурон, мезотрион, метамифоп, метазосульфурон, метолахлор, метосулам, метсульфурон, молинат, моносульфурон, MSMA, ортосульфамурон, оризалин, оксадиаргил, оксадиазон, оксацикломефон, оксифлуорфен, паракват, пендиметалин, пенокссулам, пентоксазон, петоксамид, пиклорам, пиперофос, претилахлор, профоксидим, прогексадион-кальций, пропахлор, пропанил, пропизохлор, пропизамид, пропирисульфурон, просульфурон, пирабутикарб, пираклонил, пиразогил, пиразолинат, пиразосульфурон-этил, пиразоксифен, пирибензоксим, пиридат, пирифталид, пириминобак-метил, пиримисульфан, примисульфурон, пирокссулам, квинокламин, квинклорак, квизалофоп-P-этил, S-3252, сентоксидим, симазин, симетрин, s-метолахлор, сулькотрион, сулфентразон, сульфосат, тефурилтрион, тенилхлор, тиазопир, тиобенкарб, триклопир, сложные эфиры и амины триклопира, трифлуралин, тринексапак-этил, тритосульфурон и другие 4-амино-6-(замещенный фенил)пиколинаты и 6-амино-2-(замещенный фенил)-4-пиримидинкарбоксилаты и их соли и сложные эфиры.
Соединения по настоящему изобретению могут быть дополнительно применены для борьбы с нежелательной растительностью во многих сельскохозяйственных культурах, которым придали устойчивость к или резистентность к этим или другим гербицидам путем генетической модификации или путем мутации и селекции. Гербицидные соединения по настоящему изобретению могут быть дополнительно применены вместе с глифосатом, глуфосинатом, дикамбой, имидазолинонами, арилоксифеноксипропионатами или 2,4-Д к сельскохозяйственным культурам устойчивым к глифосату, глуфосинату, дикамбе, имидазолинону, арилоксифеноксипропионату или 2,4-Д. В целом, предпочтительно применение соединений по настоящему изобретению в комбинации с гербицидами, которые являются избирательными в отношении обрабатываемой сельскохозяйственной культуры и которые дополняют спектр сорняков, контролируемых этими соединениями при применяемой норме внесения. Дополнительно, в целом, предпочтительно применение соединений по настоящему изобретению и других дополнительных гербицидов одновременно, либо в виде комбинированного состава, либо в виде танковой смеси. Аналогичные гербицидные соединения по настоящему изобретению могут быть применены вместе с ацетолактатсинтазными (ALS) ингибиторами к сельскохозяйственным культурам, устойчивым к ацетолактатсинтазным ингибиторам, или с ингибиторами 4-гидроксифенилпируватдиоксигеназы (HPPD) к сельскохозяйственным культурам, устойчивым к ингибиторами 4-гидроксифенилпируват диоксигеназы.
Соединения по настоящему изобретению могут быть, в целом, применены в комбинации с известными гербицидными антидотами, такими как беноксакор, бентиокарб, брассинолид, клоквинтоцет (мексил), циометринил, ципросульфамид, даимурон, дихлормид, дициклонон, диэтолат, димепиперат, дисулфотон, фенхлоразол-этил, фенклорим, флуразол, флуксофеним, фурилазол, белок гарпин, изоксадифен-этил, мефенпир-диэтил, мефенат, MG 191, MON 4660, нафталиновый ангидрид (NA), оксабетринил, R29148 и амиды N-фенилсульфонилбензойной кислоты, для увеличения их селективности. Они могут быть дополнительно применены для борьбы с нежелательной растительностью во многих сельскохозяйственных культурах, которым придали устойчивость или резистентности к этим или другим гербицидам путем генетической модификации или путем мутации и селекции. Например, можно обрабатывать кукурузу, пшеницу, рис, сою, сахарную свеклу, хлопок, канолу и другие сельскохозяйственные культуры, которым придали устойчивость или резистентность к соединениям, которые являются ингибиторами ацетолактатсинтазы у чувствительных растений. Многих устойчивые к глифосату и глуфосинату сельскохозяйственные культуры можно также обрабатывать этими гербицидами по отдельности или в комбинации. Некоторые сельскохозяйственным культурам придали устойчивость к ауксиновым гербицидам и гербицидам на основе АССазы, таким как 2,4-(дихлорфенокси)уксусная кислоты (2,4-Д) и дикамба и арилоксифеноксипропионаты. Эти гербициды могут быть применены для обработки подобных устойчивых сельскохозяйственных культур или других устойчивых к ауксину сельскохозяйственных культур. Некоторым сельскохозяйственным культурам придали устойчивость к гербицидам, ингибирующим 4-гидроксифенилпируватдиоксигеназу, и эти гербициды могут быть применены для обработки подобных устойчивых сельскохозяйственных культур.
В то время как соединения формулы IA или IB можно напрямую применять в качестве гербицидов, предпочтительно их применение в смесях, содержащих гербицидно эффективное количество соединения вместе с по меньшей мере одним приемлемым с точки зрения сельского хозяйства вспомогательным средством или носителем. Подходящие вспомогательные средства или носители не должны быть фитотоксичными для ценных сельскохозяйственных культур, особенно, в концентрациях, используемых при применении композиций для избирательной борьбы с сорняками в присутствии сельскохозяйственных культур, и не должны реагировать химически с соединениями формулы IA или IB или другими ингредиентами композиции. Такие смеси могут быть разработаны для применения непосредственно к сорнякам или их локусам или могут представлять собой концентраты или композиции, как правило, разбавляемые дополнительными носителями и вспомогательными средствами перед применением. Они могут представлять собой твердые частицы, такие как, например, пудры, гранулы, диспергируемые в воде гранулы или смачиваемые порошки или жидкости, такие как, например, эмульгируемые концентраты, растворы, эмульсии или суспензии. Они также могут быть предоставлены в виде готовых смесей или танковых смесей.
Подходящие сельскохозяйственные вспомогательные средства и носители, которые являются подходящими при получении гербицидных смесей по настоящему изобретению, известны специалистам в области техники. Некоторые из этих вспомогательных средств включают, но не ограничены ими, концентрат масла сельскохозяйственной культуры (минеральное масло (85%) + эмульгаторы (15%)); нонилфенолэтоксилат; бензилкокоалкилдиметиловую четвертичную аммониевую соль; смесь нефтяных углеводородов, алкилированные сложные эфиры, органическую кислоту и анионогенное поверхностно-активное вещество; C9-C11 алкилполигликозид; фосфатированный этоксилат спирта; этоксилат природного первичного спирта (C12-C16); блок-сополимер ди-втор-бутилфенол ЭО-ПО; полисилоксан-метиловую концевую группу; нонилфенолэтоксилат + мочевинно-аммониевый нитрат; эмульгированное метилированное масло семени; тридециловый спирт (синтетический) этоксилат (8ЭО); таллового амина этоксилат (15 ЭО); ПЭГ (400) диолеат-99.
Жидкие носители, которые могут быть применены, включают водные и органические растворители. Применяемые органические растворители, как правило, включают, но не ограничены ими, фракции нефти или углеводороды, такие как минеральное масло, ароматические растворители, парафиновые масла и т.п.; растительные масла, такие как соевое масло, рапсовое масло, оливковое масло, касторовое масло, масло семян подсолнечника, кокосовое масло, кукурузное масло, хлопковое масло, льняное масло, пальмовое масло, арахисовое масло, сафлоровое масло, кунжутное масло, тунговое масло и т.п.; сложные эфиры вышеуказанных растительных масел; сложные эфиры одноатомных спиртов или двухатомных, трехатомных или других низших многоатомных спиртов (содержащих 4-6 гидроксильные группы), такие как 2-этилгексилстеарат, н-бутилолеат, изопропилмиристат, пропиленгликоля диолеат, диоктилсукцинат, дибутиладипат, диокилфталат и т.п.; сложные эфиры моно, ди и поликарбоновых кислот и т.п. Конкретные органические растворители включают толуол, ксилол, бензино-лигроиновую фракцию, масло сельскохозяйственной культуры, ацетон, метилэтилкетон, циклогексанон, трихлорэтилен, перхлорэтилен, этилацетат, амилацетат, бутилацетат, монометиловый эфир пропиленгликоля и монометиловый эфир диэтиленгликоля, метиловый спирт, этиловый спирт, изопропиловый спирт, амиловый спирт, этиленгликоль, пропиленгликоль, глицерин, N-метил-2-пирролидинон, N,N-диметилалкиламиды, диметилсульфоксид, жидкие удобрения и т.п. Вода, в целом, является предпочтительным носителем для разбавления концентратов.
Подходящие твердые носители включают тальк, пирофиллитовую глину, кварц, аттапульгитовую глину, каолиновую глину, кизельгур, мел, диатомит, известь, карбонат кальция, бентонитовую глину, Фуллерову землю, шелуху семян хлопчатника, пшеничную муку, соевую муку, пемзу, древесную муку, муку из скорлупы грецкого ореха, лигнин и т.п.
Обычно желательно включение одного или более поверхностно-активных агентов в композиции по настоящему изобретению. Такие поверхностно-активные агенты выгодно применяются как в твердых, так и в жидких композициях, особенно в таких, которые разработаны для разбавления носителем перед применением. Поверхностно-активные агенты могут быть анионогенными, катионогенными или неионогенными по природе и могут быть применены в качестве эмульгирующих агентов, смачивающих агентов, суспендирующих агентов или в других целях. Поверхностно-активные вещества, традиционно применяемые в области составления препаративных форм, и которые также могут быть применены в композициях по настоящему изобретению, описаны, inter alia, в "McCutcheon's Detergents and Emulsifiers Annual" MC Publishing Corp., Риджвуд, Нью-Джерси, 1998 и в "Encyclopedia of Surfactants" Том I-III, Chemical Publishing Co., Нью-Йорк, 1980-81. Типичные поверхностно-активные агенты включают соли алкилсульфатов, такие как диэтаноламмония лаурилсульфат; алкиларилсульфонатные соли, такие как додецилбензолсульфонат кальция; продукты присоединения алкилфенола и алкиленоксида, такие как нонилфенол-С18 этоксилат; продукты присоединения спирта и алкиленоксида, такие как тридециловый спирт-С16 этоксилат; мыла, такие как стеарат натрия; алкилнафталенсульфонатные соли, такие как дибутил-нафталенсульфонат натрия; сложные диалкиловые эфиры сульфосукцинатных солей, такие как ди(2-этилгексил)сульфосукцинат натрия; сложные эфиры сорбита, такие как сорбитолеат; четвертичные амины, такие как лаурилтриметиламмония хлорид; сложные полиэтиленкликолевые эфиры жирных кислот, такие как полиэтилетгликольстеарат; блок-сополимеры этиленоксида и пропиленоксида; соли сложных моно-и диалкиловых фосфатных эфиров; масла из растений или семян, такие как соевое масло, рапсовое/каноловое масло, оливковое масло, касторовое масло, масло из семени подсолнечника, кокосовое масло, кукурузное масло, хлопковое масло, льняное масло, пальмовое масло, арахисовое масло, сафлоровое масло, кунжутное масло, тунговое масло и т.п.; и сложные эфиры вышеуказанных растительных масел, в частности, сложные метиловые эфиры.
Часто, некоторые из этих материалов, такие как растительные масла или масла из семян и их сложные эфиры, могут быть применены взаимозаменяемо в качестве сельскохозяйственного вспомогательного средства, в качестве жидкого носителя или в качестве поверхностно-активного агента.
Другие добавки, как правило, применяемые в сельскохозяйственных композициях, включают агенты улучшающие совместимость, противовспенивающие агенты, связывающие агенты, нейтрализующие агенты и буфера, ингибиторы коррозии, краски, отдушки, агенты, улучшающие растекание, улучшающие проникновение, клейкие агенты, диспергирующие агенты, загустители, агенты, понижающие температуру замерзания, противомикробные агенты и т.п. Композиции также могут содержать другие совместимые компоненты, например, другие гербициды, регуляторы роста растений, фунгициды, инсектициды и т.п. и могут быть составлены в композицию с жидкими удобрениями или твердыми, дисперсными носителями удобрений, такими как нитрат аммония, мочевина и т.п.
Концентрация активных ингредиентов в гербицидных композициях по настоящему изобретению, в целом, составляет от 0,001 до 98 процентов по весу. Часто применяют концентрации от 0,01 до 90 процентов по весу. В композициях, разработанных для применения в виде концентратов, активные ингредиенты, в целом, присутствуют в концентрации от 5 до 98 весовых процентов, предпочтительно, 10-90 весовых процентов. Такие композиции, как правило, разбавляют инертным носителем, таким как вода, перед применением. В разбавленных композициях, применяемых, как правило, к сорнякам или их локусам, в целом, содержание активного ингредиента составляет от 0,0001 до 1 весового процента и предпочтительно составляет от 0,001 до 0,05 весового процента.
Композиции по настоящему изобретению могут быть применены к сорнякам или их локусам при помощи традиционных наземных или воздушных распылителей, разбрызгивателей и устройств внесения гранул путем внесения в ирригационную воду или воду для залива в чеки и другими традиционными средствами, известными специалистам в области техники.
Следующие примеры приведены для иллюстрации различных аспектов настоящего изобретения и не должны быть рассмотрены как ограничивающие формулу изобретения.
Примеры
Общее: Микроволновое нагревание проводили с применением микроволнового реактора Biotage Initiator™. Реакции с микроволновым нагревом проводили в закрытых реакторах с перемешиванием магнитной мешалкой и с контролем температуры при помощи инфракрасного (ИК) датчика.
Пример 1. Получение бензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколината (соединение 1)
К раствору 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколиновой кислоты (полученной способами, описанными в патенте США 7314849 B2; 100 миллиграмм (мг), 0,29 миллимоль (ммоль)) в тетрагидрофуране (ТГФ; 1 миллилитр (мл)), добавляли карбонилдиимидазол (51 мг, 0,32 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 30 минут (мин) до прекращения выделения диоксид углерода (CO2). Добавляли бензиловый спирт (62 мг, 0,58 ммоль), и реакционную смесь нагревали в настольной микроволновой печи при 90°C в течение 20 минут. Реакционную смесь очищали хроматографией на силикагеле (вводили непосредственно в колонку RediSep® размером 40 грамм (г) Isco, с элюированием градиентом 0-100% простого диэтилового эфира (Et2O) в гексане) с получением белого твердого вещества (147 мг, 78%): температура плавления 132-133°C, 1H ЯМР (400 МГц, ДМСО-d6) δ 7,50-7,33 (м, 6H), 7,29 (дд, J=8,5, 7,1 Гц, 1H), 7,13 (с, 2H), 5,37 (с, 2H), 3,92 (с, 3H); ESIMS m/z 439 ([M+H]+).
Пример 2. Получение 4-хлорбензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколината (соединение 2)
Суспензию 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколиновой кислоты (150 мг, 0,43 ммоль), 1-(бромметил)-4-метилбензола (159 мг, 0,86 ммоль), карбоната калия (K2CO3; 118 мг, 0,86 ммоль) и иодида натрия (NaI; 6 мг, 0,04 ммоль) в N,N-диметилформамиде (ДМФ; 1 мл) нагревали в настольной микроволновой печи при 100°C в течение 5 минут. Затем реакционную смесь разбавляли при помощи Et2O, промывали солевым раствором, высушивали над сульфатом натрия (Na2SO4) и концентрировали в вакууме. Остаток очищали хроматографией на силикагеле (элюировали с помощью градиента 0-70% этилацетата (EtOAc)/гексан) с получением белого твердого вещества (148 мг, 73%): температура плавления 143°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 7,50-7,42 (м, 5H), 7,28 (дд, J=8,5, 7,1 Гц, 1H), 7,08 (с, 2H), 5,37 (с, 2H), 3,93 (д, J=0,8 Гц, 3H); ESIMS m/z 475 ([M+H]+).
Соединения 3-16 в таблице 1 синтезировали так, как в примере 2.
Пример 3. Получение 2,4-дихлорбензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)пиколината (соединение 17)
4-Амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)пиколиновую кислоту (полученную способами, описанными в патенте США 7314849 B2; 828 мг, 2,5 ммоль) растворяли в ДМФ (4 мл). Порциями добавляли гидрид натрия (NaH, 60% дисперсия в минеральном масле; 154 мг, 3,85 ммоль). К смеси добавляли 2,4-дихлор-1-(хлорметил)бензол (586 мг, 3,0 ммоль). Реакционную смесь оставляли перемешиваться в течение 24 часов (ч). В реакционную смесь добавляли воду, и водную фазу экстрагировали при помощи EtOAc (×3). Объединенные органические экстракты промывали солевым раствором, высушивали над Na2SO4, фильтровали и концентрировали. В результате очистки хроматографией с нормальными фазами получали белое твердое вещество (440 мг, 35%): температура плавления 165-168°C, 1H ЯМР (400 МГц, CDCl3) δ 7,68 (дд, J=8,6, 7,8 Гц, 1H), 7,54 (д, J=8,3 Гц, 1H), 7,43 (д, J=2,1 Гц, 1H), 7,28 (д, J=2,1 Гц, 1H), 7,23 (д, J=1,8 Гц, 1H), 7,21 (д, J=1,6 Гц, 1H), 5,50 (с, 2H), 4,83 (с, 2H), 3,97 (д, J=0,8 Гц, 3H); ESIMS m/z 489 ([M-H]).
Соединения 18 и 19 в таблице 1 синтезировали так, как в примере 3.
Пример 4. Получение 4-трифторметоксибензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколината (соединение 20)
Суспензию 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)-5-фторпиколиновой кислоты (200 мг, 0,573 ммоль), 1-(бромметил)-4-(трифторметокси)бензола (161 мг, 0,630 ммоль) и K2CO3 (119 мг, 0,859 ммоль) в ДМФ (2 мл) нагревали при 50°C в течение ночи. Затем реакционную смесь концентрировали под вакуумом. Остаток очищали хроматографией на силикагеле (элюировали градиентом 0-80% EtOAc/гексан) с получением белого твердого вещества (154 мг, 51,4%): температура плавления 155-156°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 7,60 (д, J=8,7 Гц, 2H), 7,47 (дд, J=8,5, 1,5 Гц, 1H), 7,41 (д, J=8,0 Гц, 2H), 7,29 (дд, J=8,5, 7,1 Гц, 1H), 7,14 (с, 2H), 5,41 (с, 2H), 3,95-3,90 (м, 3H); ESIMS m/z 523 ([M+H]+), 521 ([M-H]-).
Соединения 21-34 в таблице 1 синтезировали так, как в примере 4.
Пример 5. Получение бензил 6-амино-2-(4-хлор-2-фтор-3-метоксифенил)-5-винилпиримидин-4-карбоксилата (соединение 35)
6-Амино-2-(4-хлор-2-фтор-3-метоксифенил)-5-винилпиримидин-4-карбоновую кислоту (полученную способами, описанными в патенте США 7786044 B2; 0,150 г, 0,463 ммоль), (бромметил)бензол (0,103 г, 0,602 ммоль) и карбонат лития (Li2CO3; 0,044 г, 0,602 ммоль) объединяли в ДМФ (1,5 мл) и нагревали при 60°C в течение ночи. Охлажденную реакционную смесь концентрировали и затем разделяли между EtOAc и водой. Органическую фазу высушивали, концентрировали и очищали колоночной хроматографией (элюировали при помощи градиента EtOAc/гексаны) с получением бензил 6-амино-2-(4-хлор-2-фтор-3-метоксифенил)-5-винилпиримидин-4-карбоксилата в виде белого твердого вещества (0,154 г, 80%): температура плавления 119-121°C; 1H ЯМР (400 МГц, CDCl3) δ 7,67 (дд, J=8,5, 7,5 Гц, 1H), 7,49-7,42 (м, 2H), 7,42-7,32 (м, 3H), 7,21 (дд, J=8,6, 1,7 Гц, 1H), 6,70 (дд, J=17,8, 11,6 Гц, 1H), 5,60 (дд, J=7,7, 1,0 Гц, 1H), 5,57 (с, 1H), 5,39 (с, 2H), 5,35 (с, 2H), 4,00 (д, J=0,8 Гц, 3H); ESIMS m/z 414 ([M+H]+).
Пример 6. Получение 4-метоксибензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)пиколината (соединение 36)
К раствору 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метоксифенил)пиколиновой кислоты (600 мг, 1,81 ммоль) в ТГФ (10 мл) добавляли трифенилфосфин (475 мг, 1,81 ммоль), диэтилазодикарбоксилат (0,29 мл, 1,81 ммоль) и 4-метоксибензиловый спирт (0,34 мл, 2,72 ммоль). Реакционную смесь перемешивали в течение 48 ч. В реакционную смесь дополнительно добавляли трифенилфосфин (475 мг, 1,81 ммоль) и перемешивали в течение 24 ч. Реакционную смесь концентрировали досуха и очищали хроматографией на силикагеле (элюировали градиентом 0-100% EtOAc/гексан) с получением не совсем белого твердого вещества (170 мг, 26%): температура плавления 73-83°C; 1H ЯМР (400 МГц, CDCl3) δ 7,66 (дд, J=8,6, 7,8 Гц, 1H), 7,45-7,38 (м, 2H), 7,22 (дд, J=8,7, 1,8 Гц, 1H), 7,16 (д, J=1,7 Гц, 1H), 6,94-6,87 (м, 2H), 5,38 (с, 2H), 4,80 (с, 2H), 3,96 (д, J=0,8 Гц, 3H), 3,81 (с, 3H); ESIMS m/z 451 ([M+H]+), 449 ([M-H]-).
Соединение 37 в таблице 1 синтезировали так как в примере 6.
Пример 7. Получение бензил 4-амино-3-хлор-6-(2,4-дихлор-3-метоксифенил)пиколината (соединение 38)
Метил 4-амино-3-хлор-6-(2,4-дихлор-3-метоксифенил)пиколинат (соединение C, полученное способами, описанными в патенте США 7314849 B2; 500 мг, 1,4 ммоль) растворяли в бензиловом спирте (10 мл), обрабатывали изопропилатом титана (IV) (приблизительно 100 мкл) и нагревали при 85-90°C. Через 2 ч добавляли еще порцию изопропилата титана(IV) (100 мкл), и нагревание продолжали еще в течение 18 ч. Летучие компоненты удаляли под высоким вакуумом, и остаток очищали хроматографией на силикагеле (элюировали 5% Et2O - 30% дихлорметан (CH2Cl2) - 65% гексан). Вещество дополнительно очищали обращеннофазовой высокоэффективной жидкостной хроматографией (ОФ-ВЭЖХ; элюировали 70% ацетонитрилом) с получением соединения, указанного в заголовке (375 мг, 61%): температура плавления 107-108°C; 1H ЯМР (400 МГц, CDCl3) δ 7,50-7,26 (м, 8H), 6,97 (с, 1H), 5,42 (с, 2H), 4,85 (с, 2H), 3,91 (с, 3H); ESIMS m/z 437 ([M+H]+).
Соединение 39 в таблице 1 синтезировали так, как в примере 7.
Пример 8. Получение бензил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-(1-фторэтил)фенил)-5-фторпиколината (соединение 40)
Стадия A. Метил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-(1-фторэтил)фенил)-5-фторпиколинат (соединение H). 2-(4-Хлор-2-фтор-3-(1-фторэтил)фенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (510 мг, 1,7 ммоль, 1,0 экв.ивалент (экв.)) и метил 4-амино-3,6-дихлор-5-фторпиколинат (полученный способами, описанными в патенте США 6784137 B2; 400 мг, 1,7 ммоль, 1,0 экв.) последовательно добавляли в сосуд с микроволновым облучением Biotage объемом на 5 мл с последующим добавлением фторида цезия (CsF; 510 мг, 3,3 ммоль, 2,0 экв.), ацетата палладия(II) (19 мг, 0,084 ммоль, 0,05 экв.) и 3,3',3''-фосфинтриилтрибензолсульфоната натрия (95 мг, 0,17 ммоль, 0,10 экв.). Добавляли смесь вода-ацетонитрил 3:1 (3,2 мл), и полученную коричневую смесь нагревали в настольной микроволновой печи при 150°C в течение 5 минут. Охлажденную реакционную смесь разбавляли водой (150 мл) и экстрагировали при помощи CH2Cl2 (4×50 мл). Объединенные органические экстракты высушивали над сульфатом магния (MgSO4), безнапорно фильтровали и концентрировали на роторном испарителе. Остаток очищали обращеннофазовой колоночной хроматографией (элюировали при помощи градиента ацетонитрила от 5% до 100%) с получением требуемого продукта, метил 4-амино-3-хлор-6-(4-хлор-2-фтор-3-(1-фторэтил)фенил)-5-фторпиколината в виде желто-коричневого полутвердого вещества (220 мг, 35%): ИК (тонкопленочный) 3475, 3353 (м), 3204, 3001, 2955, 1738 (с), 1711 (с), 1624 (c) см-1; 1H ЯМР (300 МГц, CDCl3) δ 7,50 (м, 1H), 7,30 (м, 1H), 7,21 (д, J=2 Гц, 1H), 6,16 (дкв, J=46, 7 Гц, 1H), 4,96 (ушир.с, 2H), 3,97 (с, 3H), 1,75 (дд, J=23, 7 Гц, 3H); ES