Антитела против fgfr3 и способы их применения
Иллюстрации
Показать всеИзобретение относится к области иммунологии. Предложены выделенное антитело-антагонист против FGFR3 и его функциональный фрагмент, а также полинуклеотид, вектор экспрессии, клетка-хозяин и способ получения антитела против FGFR3 или его функционального фрагмента. Кроме того, рассмотрены фармацевтические композиции и применение антитела или его функционального фрагмента по изобретению для лечения или профилактики рака и болезни скелета, а также для ингибирования клеточной пролиферации и/или уменьшения количества раковых клеток. Данное изобретение может найти дальнейшее применение в терапии заболеваний, связанных с активацией и/или сверхэкспрессией FGFR3. 10 н. и 10 з.п. ф-лы, 24 ил., 5 табл.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет патентной заявки США номер 61/163222, поданной 25 марта 2009 года, содержание которой включено в настоящий документ в качестве ссылки в полном объеме.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится, главным образом, к области молекулярной биологии. Более конкретно, изобретение относится к антителам против FGFR3 и к их применению.
УРОВЕНЬ ТЕХНИКИ
Факторы роста фибробластов (FGF) и их рецепторы (FGFR) играют основную роль в процессе эмбрионального развития, гомеостаза тканей и метаболизма (1-3). У человека имеется 22 FGF (FGF1-14, FGF 16-23) и четыре рецептора FGF с тирозинкиназным доменом (FGFR1-4). FGFR состоят из внеклеточной области, связывающей лиганд, имеющий два или три иммуноглобулин-подобных домена (IgD1-3), трансмембранной области, однократно пронизывающей мембрану, и цитоплазматического разделенного тирозинкиназного домена. Каждый из FGFR1, 2 и 3 имеет две основных альтернативно сплайсированных изоформы, обозначаемых как IIIb и IIIc. Эти изоформы отличаются приблизительно 50 аминокислотами во второй половине IgD3 и имеют разную локализацию в тканях и отличную специфичность в отношении лиганда. Как правило, изоформа IIIb встречается в эпителиальных клетках, в то время как IIIc экспрессируется в мезенхимных клетках. При связывании FGF в тесном взаимодействии с гепаринсульфатными протеогликанами, FGFR димеризуются и фосфорилируются по конкретным остаткам тирозина. Это способствует привлечению основных адапторных белков, таких как субстрат FGFR 2α (FRS2α), что приводит к активации множества каскадов передачи сигнала, включая каскады митоген-активируемой протеинкиназы (MAPK) и PI3K-AKT (1, 3, 4). Следовательно, FGF и их рецепторы регулируют широкий набор клеточных процессов, включая пролиферацию, дифференцировку, миграцию и выживание, зависимым от условий образом.
FGFR с нарушенной активацией вовлечены в конкретные злокачественные опухоли человека (1, 5). В частности, хромосомная транслокация t(4;14) (p16.3;q32) происходит приблизительно у 15-20% пациентов с множественной миеломой, что приводит к сверхэкспрессии FGFR3, и коррелирует с более короткой общей выживаемостью (6-9). FGFR3 также вовлечен в придание хеморезистентности клеточным линиям миеломы в культуре (10), что согласуется с плохим клиническим ответом пациентов t(4;14)+ на общепринятую химиотерапию (8). Сверхэкспрессия мутационно активированного FGFR3 является достаточной для индукции онкогенной трансформации в кроветворных клетках и фибробластах (11-14, 15), трансгенных моделях на мышах (16) и на моделях трансплантации костного мозга у мышей (16, 17). Таким образом, FGFR3 был предложен в качестве возможной терапевтической мишени для лечения множественной миеломы. Действительно, несколько низкомолекулярных ингибиторов, нацеленных на FGFR, хотя и не селективных в отношении FGFR3 и имеющих перекрестную ингибиторную активность в отношении некоторых других киназ, продемонстрировали цитотоксичность против положительных по FGFR3 клеток миеломы в культуре и в моделях на мышах (18-22).
Сверхэкспрессия FGFR3 была описана в высокой доле случаев рака мочевого пузыря (23, 24). Более того, соматические активирующие мутации в FGFR3 были идентифицированы в 60-70% папиллярных и 16-20% мышечно-инвазивных карцином мочевого пузыря (24, 25). В экспериментах на клеточной культуре, РНК-интерференция (11, 26) или одноцепочечный Fv-фрагмент антитела против FGFR3 ингибировали пролиферацию клеток рака мочевого пузыря (27). В недавних исследованиях было показано, что конъюгат антитело против FGFR3-токсин снижает рост ксенотрансплантата клеточной линии рака мочевого пузыря через опосредуемую FGFR3 доставку токсинов в опухоли (28). Однако остается неясным, действительно ли передача сигнала FGFR3 является онкогенным пусковым фактором роста опухолей мочевого пузыря in vivo. Более того, не была определена терапевтическая мощность нацеливания на FGFR3 при раке мочевого пузыря на основе моделей in vivo. Публикации, касающиеся FGFR3 и антител против FGFR3 включают публикацию патента США No 2005/0147612; Rauchenberger et al., J Biol Chem 278 (40):38194-38205 (2003); WO2006/048877; Martinez-Torrecuadrada et al., (2008) Mol. Cancer Ther 7(4): 862-873; WO2007/144893; Trudel et al. (2006) 107(10): 4039-4046; Martinez-Torrecuadrada et al. (2005) Clin Cancer Res 11 (17): 6280-6290; Gomez-Roman et al. (2005) Clin Cancer Res 11: 459-465; Direnzo, R et al., (2007) Proceedings of AACR Annual Meeting, Abstract No. 2080; WO2010/002862.
Очевидно, что продолжает существовать необходимость в средствах, которые обладают клиническими признаками, оптимальными для разработки в качестве лекарственных средств. Изобретение, описанное в настоящем документе, удовлетворяет эту потребность и обеспечивает другие преимущества.
Все ссылки, цитированные в настоящем документе, включая патентные заявки и публикации, включены в качестве ссылок в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение частично основано на идентификации различных связывающих FGFR3 агентов (таких как антитела и их фрагменты). FGFR3 представляет собой важную и преимущественную терапевтическую мишень, и изобретение относится к композициям и способам, основанным на связывании этих агентов с FGFR3. Связывающие FGFR3 агенты по изобретению, как описано в настоящем документе, обеспечивают важные терапевтические и диагностические средства для использования для нацеливания на патологические состояния, связанные с экспрессией и/или активностью каскадов передачи сигнала FGFR3. Таким образом, изобретение относится к способам, композициям, наборам и изделиям, имеющим отношение к связыванию FGFR3.
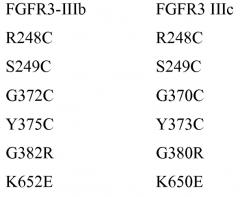
Настоящее изобретение относится к антителам, которые связываются с FGFR3. В одном из аспектов изобретение относится к выделенному антителу, которое связывает FGFR3. В некоторых вариантах осуществления антитело связывает изоформу FGFR3 IIIb и/или изоформу FGFR3 IIIc. В некоторых вариантах осуществления антитело связывает мутантный FGFR3 (например, один или несколько из R248C, S249C, G372C, Y375C, K652E FGFR3 IIIb, и/или один или несколько из R248C, S249C, G370C, Y373C, K650E FGFR3 IIIc). В некоторых вариантах осуществления антитело связывает мономерный FGFR3 (например, мономерные изоформы FGFR3 IIIb и/или IIIc). В некоторых вариантах осуществления антитело обеспечивает образование мономерного FGFR3, например, путем стабилизации мономерной формы FGFR3 относительно димерной формы FGFR3.
В одном из аспектов изобретение относится к выделенному антителу против FGFR3, где полноразмерная форма IgG антитела связывает FGFR3 человека с Kd 1×10-7 или прочнее. Как известно в данной области, аффинность связывания лиганда с его рецептором можно определять любым из множества анализов и выражать в виде различных количественных величин. Таким образом, в одном из вариантов осуществления аффинность связывания выражают как величины Kd и они отражают собственно аффинность связывания (например, с минимизированными эффектами авидности). Как правило, и предпочтительно, аффинность связывания измеряют in vitro, как в бесклеточных условиях, так и в условиях на основе клеток. Для получения показателей аффинности связывания можно использовать любой из множества анализов, известных в данной области, включая анализы, описанные в настоящем документе, в том числе, например, Biacore, радиоиммунный анализ (RIA) и ELISA. В некоторых вариантах осуществления полноразмерная IgG-форма антитела связывает FGFR3 человека с Kd 1×10-8 или прочнее, с Kd 1×10-9 или прочнее, или с Kd 1×10-10 или прочнее.
Главным образом, антитела против FGFR3 по настоящему изобретению представляют собой антитела-антагонисты. Таким образом, в одном из аспектов антитела против FGFR3 ингибируют активность FGFR3 (например, активность FGFR3-IIIb и/или FGFR3-IIIc). В некоторых вариантах осуществления антитело против FGFR3 (главным образом, в двухвалентной форме) не обладает существенной функцией агониста FGFR3. В некоторых вариантах осуществления антитело-антагонист против FGFR3 (главным образом, в двухвалентной форме) обладает небольшой функцией агониста FGFR3 или не обладает ей. В одном из вариантов осуществления антитело по изобретению (главным образом, в двухвалентной форме) не проявляет уровень активности агониста FGFR3, который превышает фоновый уровень и который обладает статистической значимостью.
В одном из аспектов связывание антитела с FGFR3 может ингибировать димеризацию рецептора с другой молекулой рецептора, причем активация рецептора ингибируется (вследствие, по меньшей мере частично, отсутствия димеризации рецептора). Ингибирование может быть прямым или непрямым.
В одном из аспектов изобретение относится к антителам против FGFR3, которые не обладают существенной апоптотической активностью (например, не индуцируют апоптоз клетки, например, клетки карциномы переходных клеток или клетки множественной миеломы, такие как клетка множественной миеломы, содержащая транслокацию FGFR3, такую как транслокация t(4;14)). В некоторых вариантах осуществления антитело против FGFR3 обладает небольшой апоптотической функцией или не обладает ей. В некоторых вариантах осуществления антитела против FGFR3 не обладают апоптотической функцией, которая превышает фоновый уровень и которая является статистически значимой.
В одном из аспектов изобретение относится к антителам против FGFR3, которые не индуцируют существенное подавление FGFR3. В некоторых вариантах осуществления антитело против FGFR3 индуцирует небольшое подавление рецептора или не индуцирует его. В некоторых вариантах осуществления антитела против FGFR3 не индуцируют подавление рецептора, которое превышает фоновый уровень и которое является статистически значимым.
В одном из аспектов изобретение относится к антителам против FGFR3, которые обладают эффекторной функцией. В одном из вариантов осуществления эффекторная функция включает антителозависимую клеточную цитотоксичность (ADCC). В одном из вариантов осуществления антитело против FGFR3 (в некоторых вариантах осуществления «голое» антитело против FGFR3) способно вызывать гибель клетки, в некоторых вариантах осуществления, клеток множественной миеломы (например, клеток множественной миеломы, содержащих транслокацию, например, транслокацию t(4;14)). В некоторых вариантах осуществления антитело против FGFR3 способно вызывать гибель клетки, которая экспрессирует приблизительно 10000 молекул FGFR3 на клетку или более (например, приблизительно 11000, приблизительно 12000, приблизительно 13000, приблизительно 14000, приблизительно 15000, приблизительно 16000, приблизительно 17000, приблизительно 18000 или более FGFR3 молекул на клетку). В других вариантах осуществления клетка экспрессирует приблизительно 2000, приблизительно 3000, приблизительно 4000, приблизительно 5000, приблизительно 6000, приблизительно 7000, приблизительно 8000 или более молекул FGFR3 на клетку.
В одном из аспектов антитело против FGFR3 по изобретению ингибирует конститутивную активность FGFR3. В некоторых вариантах осуществления конститутивная активность FGFR3 представляет собой зависимую от лиганда конститутивную активность FGFR3. В некоторых вариантах осуществления конститутивная активность FGFR3 представляет собой независимую от лиганда конститутивную активность FGFR3.
В одном из аспектов антитело против FGFR3 ингибирует FGFR3, содержащий мутацию, соответствующую FGFR3-IIIbR248C. Как используется в настоящем документе, термин "содержащий мутацию, соответствующую FGFR3-IIIbR248C," включает FGFR3-IIIbR248C и FGFR3-IIIcR248C, а также дополнительные формы FGFR3, содержащие мутацию R на C в положении, соответствующем R248 FGFR3-IIIb. Специалисту в данной области понятно, каким образом провести выравнивание последовательности FGFR3 для идентификации соответствующих остатков между соответствующими последовательностями FGFR3, например, выравнивание последовательности FGFR3-IIIc с последовательностью FGFR3-IIIb для идентификации положения в FGFR3, соответствующего положению R248 в FGFR3-IIIb. В некоторых вариантах осуществления антитело против FGFR3 ингибирует FGFR3-IIIbR248C и/или FGFR3-IIIcR248C.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3, который содержит мутацию, соответствующую FGFR3-IIIbK652E. Как используется в настоящей заявке термин "содержащий мутацию, соответствующую FGFR3-IIIbK652E," включает FGFR3-IIIbK652E и FGFR3-IIIcK650E, а также дополнительные формы FGFR3, содержащие мутацию K на E в положении, соответствующем K652 FGFR3-IIIb. Специалисту в данной области понятно, каким образом провести выравнивание последовательности FGFR3 для идентификации соответствующих остатков между соответствующими последовательностями FGFR3, например, выравнивание последовательности FGFR3-IIIc с последовательностью FGFR3-IIIb для идентификации положения в FGFR3, соответствующего положению K652 в FGFR3-IIIb. В некоторых вариантах осуществления антитело против FGFR3 ингибирует FGFR3-IIIbK652E и/или FGFR3-IIIcK650E.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3, содержащий мутацию, соответствующую FGFR3-IIIbS249C. Как используется в настоящей заявке термин "содержащий мутацию, соответствующую FGFR3-IIIbS249C," включает FGFR3-IIIbS249C и FGFR3-IIIcS249C, а также дополнительные формы FGFR3, содержащие мутацию S на C в положении, соответствующем S249 FGFR3-IIIb. В некоторых вариантах осуществления антитело против FGFR3 ингибирует FGFR3-IIIbS249C и/или FGFR3-IIIcS249C.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3, содержащий мутацию, соответствующую FGFR3-IIIbG372C. Как используется в настоящей заявке термин "содержащий мутацию, соответствующую FGFR3-IIIbG372C," включает FGFR3-IIIbG372C и FGFR3-IIIcG370C, а также дополнительные формы FGFR3, содержащие мутацию G на C в положении, соответствующем G372 FGFR3-IIIb. В некоторых вариантах осуществления антитело против FGFR3 ингибирует FGFR3-IIIbG372C и/или FGFR3-IIIcG370C.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3, содержащий мутацию, соответствующую FGFR3-IIIbY375C. Как используется в настоящей заявке термин "содержащий мутацию, соответствующую FGFR3-IIIbY375C," включает FGFR3-IIIbY375C и FGFR3-IIIcY373C, а также дополнительные формы FGFR3, содержащие мутацию S на C в положении, соответствующем S249 FGFR3-IIIb. В некоторых вариантах осуществления антитело против FGFR3 ингибирует FGFR3-IIIbY375C и/или FGFR3-IIIcY373C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIbK652E и (b) один или несколько из FGFR3-IIIbR248C, FGFR3-IIIbY375C, FGFR3-IIIbS249C и FGFR3IIIbG372C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIcK650E и (b) один или несколько из FGFR3-IIIcR248C, FGFR3-IIIcY373C, FGFR3-IIIcS249C и FGFR3IIIcG370C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIbR248C и (b) один или несколько из FGFR3-IIIbK652E, FGFR3-IIIbY375C, FGFR3-IIIbS249C и FGFR3-IIIbG372C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIcR248C и (b) один или несколько из FGFR3-IIIcK650E, FGFR3-IIIcY373C, FGFR3-IIIcS249C и FGFR3-IIIcG370C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIbG372C и (b) один или несколько из FGFR3-IIIbK652E, FGFR3-IIIbY375C, FGFR3-IIIbS249C и FGFR3-IIIbR248C.
В одном из аспектов антитела против FGFR3 ингибируют (a) FGFR3-IIIcG370C и (b) один или несколько из FGFR3-IIIcK650E, FGFR3-IIIcY373C, FGFR3-IIIcS249C и FGFR3-IIIcR248C.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3-IIIbR248C, FGFR3-IIIbK652E, FGFR3-IIIbY375C, FGFR3-IIIbS249C и FGFR3-IIIbG372C.
В одном из аспектов антитела против FGFR3 ингибируют FGFR3-IIIcR248C, FGFR3-IIIcK650E, FGFR3-IIIcY373C, FGFR3-IIIcS249C и FGFR3-IIIcG370C.
В одном из аспектов изобретение относится к выделенному антителу против FGFR3, содержащему:
(a) по меньшей мере одну, две, три, четыре или пять последовательностей гипервариабельных областей (HVR), выбранных из:
(i) HVR-L1, содержащей последовательность A1-A11, где A1-A11 представляет собой RASQDVDTSLA (SEQ ID NO:87),
(ii) HVR-L2, содержащей последовательность B1-B7, где B1-B7 представляет собой SASFLYS (SEQ ID NO:88),
(iii) HVR-L3, содержащей последовательность C1-C9, где C1-C9 представляет собой QQSTGHPQT (SEQ ID NO:89),
(iv) HVR-H1, содержащей последовательность D1-D10, где D1-D10 представляет собой GFTFTSTGIS (SEQ ID NO:84),
(v) HVR-H2, содержащей последовательность E1-E18, где E1-E18 представляет собой GRIYPTSGSTNYADSVKG (SEQ ID NO:85), и
(vi) HVR-H3, содержащей последовательность F1-F20, где F1-F20 представляет собой ARTYGIYDLYVDYTEYVMDY (SEQ ID NO:86); и
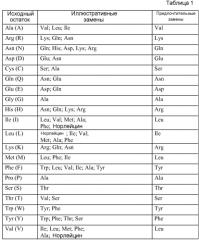
(b) по меньшей мере один вариант HVR, где последовательность варианта HVR содержит модификацию по меньшей мере одного остатка (по меньшей мере двух остатков, по меньшей мере трех или более остатков) последовательности SEQ ID NO:1-18, 48-131 и 140-145. Желательно, чтобы модификация представляла собой замену, вставку или делецию.
В некоторых вариантах осуществления вариант HVR-L1 содержит 1-6 (1, 2, 3, 4, 5 или 6) замен в любой комбинации из следующих положений: A5 (V или D), A6 (V или I), A7 (D, E или S), A8 (T или I), A9 (A или S) и A10 (V или L). В некоторых вариантах осуществления вариант HVR-L2 содержит 1-2 (1 или 2) замены в любой комбинации из следующих положений: B1 (S или G), B4 (F или S или T) и B6 (A или Y). В некоторых вариантах осуществления вариант HVR-L3 содержит 1-6 (1, 2, 3, 4, 5 или 6) замен в любой комбинации из следующих положений: C3 (G или S или T), C4 (T или Y или A), C5 (G или S или T или A), C6 (A или H или D или T или N), C7 (Q или P или S) и C8 (S или Y или L или P или Q). В некоторых вариантах осуществления вариант HVR-H1 содержит 1-3 (1, 2 или 3) замены в любой комбинации из следующих положений: D3 (S или T), D5 (W или Y или S или T), D6 (S или G или T). В некоторых вариантах осуществления вариант HVR-H2 содержит 1-6 (1, 2, 3, 4, 5 или 6) замен в любой комбинации из следующих положений: E2 (R или S), E6 (Y или A или L или S или T), E7 (A или Q или D или G или Y или S или N или F), E8 (A или D или G), E9 (T или S), E10 (K или F или T или S), E11 (Y или H или N или I).
В одном из аспектов изобретение относится к выделенному антителу против FGFR3, содержащему:
(a) по меньшей мере одну, две, три, четыре или пять последовательностей гипервариабельных областей (HVR), выбранных из:
(i) HVR-L1, содержащей последовательность RASQX1X2X3X4X5X6A, где X1 представляет собой V или D, X2 представляет собой V или I, X3 представляет собой D, E или S, X4 представляет собой T или I, X5 представляет собой A или S, и X6 представляет собой V или L (SEQ ID NO:146),
(ii) HVR-L2, содержащей последовательность X1ASFLX2S, где X1 представляет собой S или G и X2 представляет собой A или Y (SEQ ID NO:147),
(iii) HVR-L3, содержащей последовательность QQX1X2X3X4X5X6T, где X1 представляет собой G, S или T, X2 представляет собой T, Y или A, X3 представляет собой G, S, T или A, X4 представляет собой A, H, D, T или N, X5 представляет собой Q, P или S, X6 представляет собой S, Y, L, P или Q (SEQ ID NO:148),
(iv) HVR-H1, содержащей последовательность GFX1FX2X3TGIS, где X1 представляет собой S или T, X2 представляет собой W, Y, S или T, X3 представляет собой S, G или T (SEQ ID NO:149),
(v) HVR-H2, содержащей последовательность GRIYPX1X2X3X4X5X6YADSVKG, где X1 представляет собой Y, A, L, S или T, X2 представляет собой A, Q, D, G, Y, S, N или F, X3 представляет собой A, D или G, X4 представляет собой T или S, X5 представляет собой K, F, T или S, X6 представляет собой Y, H, N или I (SEQ ID NO:150), и
(vi) HVR-H3, содержащей последовательность ARTYGIYDLYVDYTEYVMDY (SEQ ID NO:151).
В некоторых вариантах осуществления HVR-L1 содержит последовательность RASQX1VX2X3X4VA, где X1 представляет собой V или D, X2 представляет собой D, E или S, X3 представляет собой T или I, X4 представляет собой A или S (SEQ ID NO:152). В некоторых вариантах осуществления HVR-L3 содержит последовательность QQX1X2X3X4X5X6T, где X1 представляет собой S, G или T, X2 представляет собой Y, T или A, X3 представляет собой T или G, X4 представляет собой T, H или N, X5 представляет собой P или S, X6 представляет собой P, Q, Y или L (SEQ ID NO:153). В некоторых вариантах осуществления HVR-H2 содержит последовательность GRIYPX1X2GSTX3YADSVKG, где X1 представляет собой T или L, X2 представляет собой N, Y, S, G, A или Q; X3 представляет собой N или H (SEQ ID NO:154).
В другом аспекте изобретение относится к выделенному антителу против FGFR3, которое содержит одну, две, три, четыре, пять или шесть HVR, где каждая HVR содержит последовательность, выбранную из SEQ ID NO:1-18, 48-131 и 140-145, состоит или по существу состоит из них, и где SEQ ID NO:1, 7, 13, 48, 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126 или 143 соответствует HVR-H1, SEQ ID NO:2, 8, 14, 49, 55, 61, 67, 73, 79, 85, 91, 97, 103, 109, 115, 121, 127 или 144 соответствует HVR-H2, SEQ ID NO:3, 9, 15, 50, 56, 62, 68, 74, 80, 86, 92, 98, 104, 110, 116, 122, 128 или 145 соответствует HVR-H3, SEQ ID NO:4, 10, 16, 51, 57, 63, 69, 75, 81, 87, 93, 99, 105, 111, 117, 123, 129 или 140 соответствует HVR-L1, SEQ ID NO:5, 11, 17, 52, 58, 64, 70, 76, 82, 88, 94, 100, 106, 112, 118, 124, 130 или 141 соответствует HVR-L2, и SEQ ID NO:6, 12, 18, 53, 59, 65, 71, 77, 83, 89, 95, 101, 107, 113, 119, 125, 131 или 142 соответствует HVR-L3.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему HVR-H1, содержащую последовательность SEQ ID NO:1, 7, 13, 48, 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126 или 143.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему HVR-H2, содержащую последовательность SEQ ID NO:2, 8, 14, 49, 55, 61, 67, 73, 79, 85, 91, 97, 103, 109, 115, 121, 127 или 144.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему HVR-H3, содержащую последовательность SEQ ID NO:3, 9, 15, 50, 56, 62, 68, 74, 80, 86, 92, 98, 104, 110, 116, 122, 128 или 145.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему область HVR-L1, содержащую последовательность SEQ ID NO:4, 10, 16, 51, 57, 63, 69, 75, 81, 87, 93, 99, 105, 111, 117, 123, 129 или 140.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему область HVR-L2, содержащую последовательность SEQ ID NO:5, 11, 17, 52, 58, 64, 70, 76, 82, 88, 94, 100, 106, 112, 118, 124, 130 или 141.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему область HVR-L3, содержащую последовательность SEQ ID NO:6, 12, 18, 53, 59, 65, 71, 77, 83, 89, 95, 101, 107, 113, 119, 125, 131 или 142.
В одном из аспектов антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:1, 2, 3, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:4, 5, 6.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:7, 8, 9, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:10, 11, 12.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:13, 14, 15, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:16, 17, 18.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:48, 49, 50, и/или вариабельную область легкой цепи HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:51, 52, 53.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:54, 55, 56, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:57, 58, 59.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:60, 61, 62, 63, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:63, 64, 65.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:66, 67, 68, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:69, 70, 71.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:72, 73, 74, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:75, 76, 77.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:78, 79 80, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:81, 82, 83.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:84, 85, 86, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2 и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:87, 88, 89.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:90, 91, 92, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:93, 94, 95.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:96, 97, 98, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:99, 100, 101.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:102, 103, 104, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:105, 106, 107.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:108, 109, 110, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:111, 112, 113.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:114, 115, 116, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:117, 118, 119.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:120, 121, 122, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:123, 124, 125.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:126, 127, 128, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:129, 130, 131.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую HVR-H1, HVR-H2, HVR-H3, где каждая из них, по порядку, содержит SEQ ID NO:140, 141, 142, и/или вариабельную область легкой цепи, содержащую HVR-L1, HVR-L2, и HVR-L3, где каждая из них, по порядку, содержит SEQ ID NO:143, 144, 145.
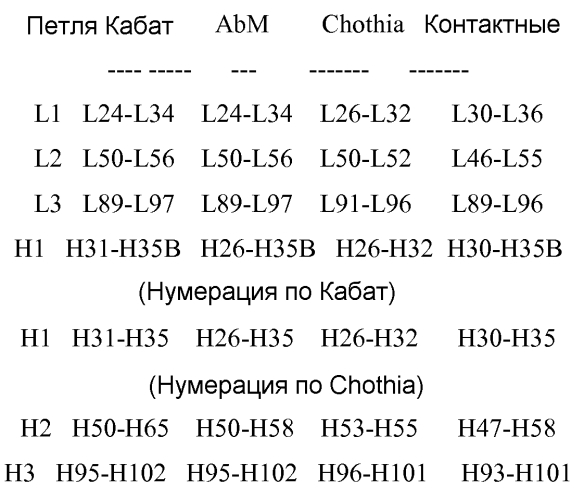
Аминокислотные последовательности SEQ ID NO:1-18, 48-131 и 140-145 пронумерованы относительно отдельных HVR (т.е., H1, H2 или H3), как указано на фигуре 1, причем нумерация соответствует системе нумерации Кабат, как описано ниже.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:132 и вариабельную область легкой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область легкой цепи, содержащую SEQ ID NO:133, и вариабельную область тяжелой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:132, и вариабельную область легкой цепи, содержащую SEQ ID NO:133.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:134, и вариабельную область легкой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область легкой цепи, содержащую SEQ ID NO:135, и вариабельную область тяжелой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область легкой цепи, содержащую SEQ ID NO:139, и вариабельную область тяжелой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:134, и вариабельную область легкой цепи, содержащую SEQ ID NO:135.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:136, и вариабельную область легкой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область легкой цепи, содержащую SEQ ID NO:137, и вариабельную область тяжелой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:136, и вариабельную область легкой цепи, содержащую SEQ ID NO:137.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:138, и вариабельную область легкой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область легкой цепи, содержащую SEQ ID NO:139, и вариабельную область тяжелой цепи.
В другом аспекте антитело против FGFR3 содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:138, и вариабельную область легкой цепи, содержащую SEQ ID NO:139.
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему: по меньшей мере одну, две, три, четыре, пять и/или шесть последовательностей гипервариабельной области (HVR), выбранных из группы, состоящей из:
(a) HVR-L1, содержащей последовательность SASSSVSYMH (SEQ ID NO:155), SASSSVSYMH (SEQ ID NO:156) или LASQTIGTWLA (SEQ ID NO:157),
(b) HVR-L2, содержащей последовательность TWIYDTSILAS (SEQ ID NO:158), RWIYDTSKLAS (SEQ ID NO:159) или LLIYAATSLAD (SEQ ID NO:160),
(c) HVR-L3, содержащей последовательность QQWTSNPLT (SEQ ID NO:161), QQWSSYPPT (SEQ ID NO:162) или QQLYSPPWT (SEQ ID NO:163),
(d) HVR-H1, содержащей последовательность GYSFTDYNMY (SEQ ID NO:164), GYVFTHYNMY (SEQ ID NO:165) или GYAFTSYNMY (SEQ ID NO:166),
(e) HVR-H2, содержащей последовательность WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:167), WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:168) или WIGYIDPYIGGTSYNQKFKG (SEQ ID NO:169), и
(f) HVR-H3, содержащей последовательность ASPNYYDSSPFAY (SEQ ID NO:170), ARGQGPDFDV (SEQ ID NO:171) или ARWGDYDVGAMDY (SEQ ID NO:172).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему: по меньшей мере одну, две, три, четыре, пять и/или шесть последовательностей гипервариабельной области (HVR), выбранных из группы, состоящей из:
(a) HVR-L1, содержащей последовательность SASSSVSYMH (SEQ ID NO:155),
(b) HVR-L2, содержащей последовательность TWIYDTSILAS (SEQ ID NO:158),
(c) HVR-L3, содержащей последовательность QQWTSNPLT (SEQ ID NO:161),
(d) HVR-H1, содержащей последовательность GYSFTDYNMY (SEQ ID NO:164),
(e) HVR-H2, содержащей последовательность WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:167), и
(f) HVR-H3, содержащей последовательность ASPNYYDSSPFAY (SEQ ID NO:170).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему: по меньшей мере одну, две, три, четыре, пять и/или шесть последовательностей гипервариабельной области (HVR), выбранных из группы, состоящей из:
(a) HVR-L1, содержащей последовательность SASSSVSYMH (SEQ ID NO:156),
(b) HVR-L2, содержащей последовательность RWIYDTSKLAS (SEQ ID NO:159),
(c) HVR-L3, содержащей последовательность QQWSSYPPT (SEQ ID NO:162),
(d) HVR-H1, содержащей последовательность GYVFTHYNMY (SEQ ID NO:165),
(e) HVR-H2, содержащей последовательность WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:168), и
(f) HVR-H3, содержащей последовательность ARGQGPDFDV (SEQ ID NO:171).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему: по меньшей мере одну, две, три, четыре, пять и/или шесть последовательностей гипервариабельной области (HVR), выбранных из группы, состоящей из:
(a) HVR-L1, содержащей последовательность LASQTIGTWLA (SEQ ID NO:157),
(b) HVR-L2, содержащей последовательность LLIYAATSLAD (SEQ ID NO:160),
(c) HVR-L3, содержащей последовательность QQLYSPPWT (SEQ ID NO:163),
(d) HVR-H1, содержащей последовательность GYAFTSYNMY (SEQ ID NO:166),
(e) HVR-H2, содержащей последовательность WIGYIDPYIGGTSYNQKFKG (SEQ ID NO:169), и
(f) HVR-H3, содержащей последовательность ARWGDYDVGAMDY (SEQ ID NO:172).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему (a) легкую цепь, содержащую (i) HVR-L1, содержащую последовательность SASSSVSYMH (SEQ ID NO:155); (ii) HVR-L2, содержащую последовательность TWIYDTSILAS (SEQ ID NO:158); и (iii) HVR-L3, содержащую последовательность QQWTSNPLT (SEQ ID NO:161); и/или (b) тяжелую цепь, содержащую (i) HVR-H1, содержащую последовательность GYSFTDYNMY (SEQ ID NO:164); (ii) HVR-H2, содержащую последовательность WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:167); и (iii) HVR-H3, содержащую последовательность ASPNYYDSSPFAY (SEQ ID NO:170).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему (a) легкую цепь, содержащую (i) HVR-L1, содержащую последовательность SASSSVSYMH (SEQ ID NO:156); (ii) HVR-L2, содержащую последовательность RWIYDTSKLAS (SEQ ID NO:159); и (iii) HVR-L3, содержащую последовательность QQWSSYPPT (SEQ ID NO:162); и/или (b) тяжелую цепь, содержащую (i) HVR-H1, содержащую последовательность GYVFTHYNMY (SEQ ID NO:165); (ii) HVR-H2, содержащую последовательность WIGYIEPYNGGTSYNQKFKG (SEQ ID NO:168); и (iii) HVR-H3, содержащую последовательность ARGQGPDFDV (SEQ ID NO:171).
В одном из аспектов изобретение относится к антителу против FGFR3, содержащему (a) легкую цепь, содержащую (i) HVR-L1, содержащую последовательность LASQTIGTWLA (SEQ ID NO:157); (ii) HVR-L2, содержащую последовательность LLIYAATSLAD (SEQ ID NO:160); и (iii) HVR-L3, содержащую последовательность QQLYSPPWT (SEQ ID NO:163); и/или (b) тяжелую цепь, содержащую (i) HVR-H1, содержащую последовательность GYAFTSYNMY (SEQ ID NO:166); (ii) HVR-H2, содержащую последовательность WIGYIDPYIGGTSYNQKFKG (SEQ ID NO:169); и (iii) HVR-H3, содержащую последовательность ARWGDYDVGAMDY (SEQ ID NO:172). Некоторые варианты осуществления антител по изобретению содержат вариабельный домен легкой цепи гуманизированного антитела 4D5 (huMAb4D5-8) (HERCEPTIN®, Genentech, Inc., South San Francisco, CA, USA) (также указываемого в патенте США No. 6407213 и Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093), как представлено в SEQ ID NO:173 ниже:
1 Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys 107 (SEQ ID NO:173)
(остатки HVR подчеркнуты)
В одном из вариантов осуществления последовательность вариабельного домена легкой цепи huMAb4D5-8 модифицирована в одном или нескольких положениях 30, 66 и 91 (Asn, Arg и His, как указано полужирным шрифтом/курсивом выше, соответственно). В конкретном варианте осуществления, модифицированная последовательность huMAb4D5-8 содержит Ser в положении 30, Gly в положении 66, и/или Ser в положении 91. Таким образом, в одном из вариантов осуществления антитело по изобретению содержит вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO:174 ниже:
1 Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys 107 (SEQ ID NO:174)
(остатки HVR подчеркнуты)
Остатки, замененные в huMAb4D5-8, указаны полужирным шрифтом/курсивом.
Антитела по изобретению могут содержать любую подходящую каркасную последовательность вариабельного домена, при условии, что активность связывания с FGFR3 по существу сохраняется. Например, в некоторых вариантах осуществления антитела по изобретению содержат консенсусную каркасную последовательность тяжелой цепи человека подгруппы III. В одном из вариантов осуществления этих антител, консенсусная каркасная последовательность содержит замену в положении 71, 73 и/или 78. В некоторых вариантах осуществления этих антител, положение 71 представляет собой A, 73 представляет собой T и/или 78 представляет собой A. В одном из вариантов осуществления эти антитела содержат каркасные последовательности вариабельного домена тяжелой цепи huMAb4D5-8 (HERCEPTIN®, Genentech, Inc., South San Francisco, CA, США) (также указываемого в патентах США No. 6407213 и 5821337, и Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093). В одном из вариантов осуществления эти антитела, кроме того, содержат консенсусную каркасную последовательность легкой цепи kI человека. В конкретном варианте осуществления эти антитела содержат последовательности HVR легкой цепи huMAb4D5-8, как описано в патентах США No. 6407213 и 5821337). В одном из вариантов осуществления эти антитела содержат последовательности вариабельных доменов легкой цепи huMAb4D5-8 (HERCEPTIN®, Genentech, Inc., South San Francisco, CA, США) (также казываемого в патентах США No. 6407213 и 5821337, и Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093).
В одном из вариантов осуществления антитело по изобретению содержит вариабельный домен тяжелой цепи, где каркасная последовательность содержит последовательность SEQ ID NO:19 и 203-205, 20 и 206-208, 21 и 209-211, 22 и 212-214, 23 и 215-217, 24 и 218-220, 25 и 221-223, 26 и 224-226, 27 и 227-229, 28 и 230-232, 29 и 233-235, 30 и 236-238, 31 и 239-241, 32 и 242-244, 33 и 245-247, 34 и 248-250, 35 и 251-253, 36 и 254-256, и/или 37 и 257-259, и последовательности H1, H2 и H3 HVR представляют собой SEQ ID NO:13, 14 и/или 15, соответственно. В другом варианте осуществления каркасная последовательность содержит последовательность SEQ ID NO:19 и 203-205, 20 и 206-208, 21 и 209-211, 22 и 212-214, 23 и 215-217, 24 и 218-220, 25 и 221-223, 26 и 224-226, 27 и 227-229, 28 и 230-232, 29 и 233-235, 30 и 236-238, 31 и 239-241, 32 и 242-244, 33 и 245-247, 34 и 248-250, 35 и 251-253, 36 и 254-256, и/или 37 и 257-259, и посл