Эпоксиды 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола-новые противопаркинсонические и противосудорожные средства
Иллюстрации
Показать всеИзобретение касается применения эпоксидов 3-метил-6-(1-метилэтенил)циклогекс-3-ен-1,2-диола, описываемых формулами 1-3, включая их пространственные изомеры, в том числе оптически активные формы, в качестве средств для лечения болезни Паркинсона и противосудорожных средств, и может быть использовано в медицине. Средства обладают высокой активностью и могут быть получены из доступного природного сырья. 2 н.п. ф-лы, 2 табл., 9 пр.
Реферат
Изобретение относится к области органической химии, а именно, к органическим соединениям, конкретно к эпоксидам 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола, описываемым формулами 1-3 (включая их пространственные изомеры, в том числе оптически активные формы),
которые могут применяться для лечения болезни Паркинсона и в качестве противосудорожных средств.
Болезнь Паркинсона - одно из наиболее распространенных неврологических заболеваний с преимущественно двигательными нарушениями, обусловленное утратой дофаминсодержащих клеток нигростриального пути. Число людей, страдающих болезнью Паркинсона, составляет 1% среди взрослого населения в возрасте до 60 лет, 5-10% - в группе 60-80-летних [1]. Лечение болезни Паркинсона проводят длительно, иногда в течение всей жизни пациентов, комбинируя между собой различные препараты, в основном дофаминомиметики и центральные холиноблокаторы.
Для лечения болезни Паркинсона применяются разные по механизму действия вещества. Более широко и чаще применяются средства, в состав которых входит предшественник дофамина L-ДОФА (леводопа). Эти средства используются как заместительная терапия, т.к. патогенез развития данного заболевания связан с прогрессирующим разрушением и гибелью нейронов, продуцирующих нейромедиатор дофамин, что приводит к резкому снижению содержания дофамина в головном мозге. Недостатками препаратов, содержащих L-ДОФА, являются [1, 2]: 1) недостаточно высокий процент эффективности; 2) наличие большого количества побочных эффектов (анорексия, рвота, тахикардия, дискинезия, психические нарушения и т.д.); 3) колебания реакции на препарат, заключающиеся во флуктуации двигательных симптомов (синдром «включения-выключения»); 4) привыкание.
Для снижения дозы и уменьшения побочных эффектов L-ДОФА обычно комбинируют с другими препаратами: ингибиторы периферической допа-декарбоксилазы (карбидопа), средства, снижающие стимулирующее действие кортикальных глутаматных рецепторов, которое развивается на фоне снижения уровня дофамина (мидантан), либо агонисты дофаминовых (периферических) рецепторов (ропинирол), ингибиторы МАО-В (селегин) и центральные холиноблокирующие средства, которые, однако, не устраняют полностью указанные недостатки [1, 2], а без L-ДОФА эти препараты недостаточно эффективны.
Эпилепсия - другое распространенное хроническое неврологическое заболевание, в основе которого могут лежать те же патогенетические механизмы, которые задействованы при болезни Паркинсона и других нейродегенеративных заболеваниях. В частности, это касается митохондриальных повреждений, обусловленных окислительным стрессом, образованием свободных радикалов при окислительном метаболизме дофамина, что может приводить как к нейродегенеарции, так и формированию очага возбуждения и судорожных приступов.
Для лечения эпилепсии используют различные противосудорожные средства (антиконвульсанты). Большинство противосудорожных средств являются агонистами ГАМК рецепторов (или блокаторами обратного захвата и катаболизма ГАМК), а также антагонистами NMDA-рецепторов (или ингибиторами высвобождения глутамата из окончаний возбуждающих нейронов). Вследствие того, что антиконвульсанты обладают тормозящим действием на ЦНС, часто развиваются множественные побочные эффекты: сонливость, астения, головокружение, нарушения когнитивных функций. Другой серьезной проблемой эпилепсии остаются резистентность более трети больных к медикаментозному лечению [3].
Таким образом, поиск и создание новых высокоэффективных и низкотоксичных противопаркинсонических и противосудорожных средств продолжают оставаться актуальными в настоящее время.
Задача, на решение которой направлено изобретение, заключается в поиске новых соединений, обладающих противопаркинсонической и противосудорожной активностью.
Поставленная задача решается использованием в качестве противопаркинсонических средств соединений, описываемых формулами 1-3,
включая их пространственные изомеры, в том числе оптически активные формы.
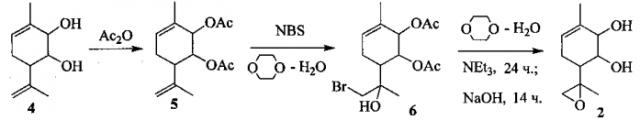
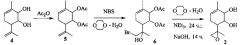
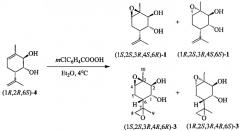
Соединения 1-3 могут быть получены из 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 4 следующими путями:
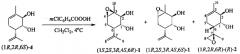
1) окислением соединения 4 эпоксидирующими агентами,
например, мета-хлорнадбензойной кислотой;
2) через промежуточное получение галогенгидринов с последующим образованием эпоксидного цикла, например:
Моноэпоксиды 1 и 2 могут быть далее окислены в диэпоксид 3 с использованием эпоксидирующих агентов, например, мета-хлорнадбензойной кислоты.
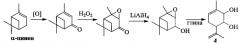
Исходное соединение 4 может быть синтезировано исходя из широко распространенного в отечественном растительном сырье монотерпена α-пинена с использованием доступных реагентов [4], или другими способами (например, из карвона в соответствии с работой [5]).
Для получения соединений 1-3 в виде различных стереоизомеров, в том числе и оптически активном виде, можно использовать в качестве исходных веществ различные пространственные изомеры соединения 4 в сочетании, при необходимости, с хроматографическим разделением изомерных эпоксидов и/или их предшественников.
Для изучения противопаркинсонической активности in vivo широко используется 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МФТП), вызывающий развитие болезни Паркинсона у людей, обезьян и грызунов [2, 5, 6].
Противопаркинсоническая активность соединений 1-3 изучалась in vivo на модели болезни Паркинсона, индуцированной введением МФТП. Индукцию паркинсонического синдрома осуществляли путем четырехкратного внутрибрюшинного введения МФТП в дозе 20 мг/кг на мышах самцах линии С57В 1/6.
Противопаркинсоническую активность агентов оценивали по олигокинезии по двигательно-ориентировочной активности в установке TraScan (США). В качестве эталона сравнения использовался (1R,2R,6S)-3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диол (1R,2R,6S)-4, обладающий высокой противопаркинсонической активностью [5, 7]. Результаты экспериментов приведены в Табл. 1 (Пример 8).
Из таблицы 1 видно, что соединения 1-3 в дозе 20 мг/кг достоверно увеличивают двигательную (двигательная активность, дистанция движения и скорость движения) и исследовательскую (количество вертикальных стоек и исследованных отверстий) активности, сниженные в результате действия нейротоксина МФТП, до уровня интактных животных. Соединение (1S,2S,3R,4S,6R)-1 превосходит по эффективности препарат сравнения (1R,2R,6S)-4, более существенно увеличивая дистанцию движения (двигательная активность) и достоверно повышая количество вертикальных стоек (исследовательская активность). В целом, соединения 1-3 оказывают более выраженное положительное действие на исследовательскую активность животных, чем препарат сравнения 4. Необходимо отметить, что болезнь Паркинсона характеризуется многочисленными психическими или поведенческими расстройствами (депрессия, повышенная тревожность, нарушения сна, психозы и т.д.) [8], что делает важным создание лекарственных средств, которые устраняли бы и двигательные, и психические симптомы болезни.
Судорожные состояния, также как и болезнь Паркинсона, проявляются в виде нарушения моторных, вегетативных и психических функций. В этой связи была изучена противосудорожная активность соединений 1-3 в тесте максимального электрошока (МЭШ). Результаты экспериментов приведены в Таблице 2 (Пример 9).
Из таблицы 2 видно, что соединения 1-3 в дозе 1 мг/кг достоверно уменьшали количество животных с тонико-экстензорной реакцией, вызванной электрошоком, с 78,6% до 30,0%, 37,5% и 25% соответственно. Соединение (1R,2S,3R,4R,6S)-(R)-3 в дозе 10 мг/кг также достоверно уменьшало количество животных с тонико-экстензорной реакцией до 37,5%. Соединения 1-2 в дозе 10 мг/кг существенно не снижало количество животных с реакцией. Полученные результаты показывают, что агенты 1, 2 и 3 в дозе 1 мг/кг обладают противосудорожной активностью, не уступая по эффективности карбамазепину (10 мг/кг).
Острая токсичность соединений (1R,2S,3R,4S,6R)-1 и (1R,2R,6R)-(R)-2 определялась на белых беспородных мышах массой 20-22 г при однократном внутрижелудочном введении по методу Кербера. Показано, что соединения (1R,2S,3R,4S,6R)-1 и (1R,2R,6R)-(R)-2 являются умерено токсичными веществами: ЛД50 превышает 1000 мг/кг.
Таким образом, можно заключить, что соединения 1-3 обладают высокой противопаркинсонической и противосудорожной активностью, не уступающей таковой у препаратов сравнения, и могут, после проведения соответствующих испытаний, использоваться в чистом виде или в качестве компонента новых высокоэффективных лекарственных форм для лечения болезни Паркинсона, а также в качестве противосудорожных средств. Назначаемые разовые дозы будут варьировать в зависимости от пола, возраста, веса, тяжести заболевания и могут составлять предпочтительно от 1 до 500 мг.
Изобретение иллюстрируется следующими примерами.
Пример 1. Синтез соединений 1 и 2 эпоксидированием 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 4.
Раствор 0.312 г (1.86 ммоль) соединения (1R,2R,6S)-4 ( [ α ] D 31 -49.1 (с 2.6, CHCl3)), в 40 мл CH2Cl2 охладили до 0°С. Добавили 1.55 г (18.5 ммоль) NaHCO3 и 0.589 г (~2.5 ммоль) мета-хлорнадбензойной кислоты (70-75%, «Acros Organics») и выдержали при 4°С в течение 7 сут. Добавили 30 мл H2O, отфильтровали, отделили органическую фазу. Водную фазу экстрагировали EtOAc (3×15 мл). Объединенные органические фазы промыли 15 мл насыщ. Na2S2O3 и 20 мл насыщ. NaCl. Сушили над Na2SO4. Растворитель отогнали. Остаток (0.293 г) делили на колонке с 9 г SiO2 (Macherey-Nagel, 60-200 µ, градиент этилацетата в гексане 0-100%). Вьщелили 0.028 г (0.17 ммоль, конверсия 91%) исходного соединения 4, 0.082 г (0.446 ммоль, 26% в пересчете на прореагировавшее соединение 4) (1S,2S,3R,4S,6R)-1-метил-4-(1-метилэтенил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1S,2S,3R,4S,6R)-1 0.034 г (0.185 ммоль, 11%) (1R,2S,3R,4S,6S)-1-метил-4-(1-метилэтенил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1R,2S,3R,4S,6S)-1 и 0.010 г (0.054 ммоль, 3%) (1R,2R,6R)-3-метил-6-((R)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диола (1R,2R,6R)-(R)-2.
Соединение (1S,2S,3R,4S,6R)-1. [α]D 24 -19.8 (с 1.06, CHCl3). 1Н NMR (CDCl3+CCl4, 1:1): δ 1.44 (s, C10H3), 1.77 (br.s, C9H3), (1.88 ddd, Н5е, J5e,5a=14.7 Hz, J5e,6a=4.5 Hz, J5e,4=2.2 Hz), 2.07 (ddd, H5a, J5a,5e=14.7 Hz, J5a,6a=12.0 Hz, J5a,4=1.9 Hz), 2.21 (br.dd, H6a, J6a,5a=12.0 Hz, http://J6a.se=4.5 Hz), 2.29 (br.d, OH-C1, JOH,1e=10.0 Hz), 3.31 (dd, H4, J4,5e=2.2 Hz, J4,5a=1.9 Hz), 3.58 (br.s, H2e), 3.76 (dd, H1e, J1e,OH=10.0 Hz, J1e,2e=2.5 Hz), 4.79 (br.s, H8), 4.94 (br.s, H9′). 13C NMR: δ 71.32 (d, C1), 69.43 (d, C2), 58.44 (s, C3), 63.32 (d, C4), 23.12 (t, C5), 35.95 (d, C6), 144.98 (s, C7), 111.78 (t, C8), 22.92 (q, C9), 22.17 (q, С10). Найдено M-H2O 166.1000. C10H14O2. Вычислено: M-H2O 166.0988.
Соединение (1R,2S,3R,4S,6S)-1. [α]D 26 - 24.1 (c 0.64, CHCl3). 1H NMR (CDCl3+CCl4, 1:1): δ 1.38 (s, C10H3), 1.75 (s, C9H3), 2.02 (dddd, H5e, J5e,5a=15.8 Hz, J5e,6a=7.5 Hz, J5e,4=5.0 Hz, J5e,1e 0.6 Hz), 2.07 (dd, H5a, J5a,5e=15.8 Hz, J5a,6a=12.0 Hz), 2.37 (br.dd, H6a, J6a,5a=12.0 Hz, http://J6a.se5e=7.5 Hz), 3.09 (d, OH-C1, JOH,1e=11.3 Hz), 3.16 (d, H4, J4,5e=5.0 Hz), 3.32 (br.s, OH-C2), 3.62 (dddd, H1e, J1e,OH=11.3 Hz, J1e,2e=3.2 Hz, J1e,6a=1.5 Hz, J1e,5e=0.6 Hz), 3.93 (br.d, H2e, J2e,1e=3.2 Hz), 4.78 (dd, H8, J8,8′=1.7 Hz, J8,6a=0.7 Hz), 4.84 (dqd, H8′, J8′,8=1.7 Hz, J8′,9-Me=1.4 Hz, J8′,6a=0.7 Hz). 13C NMR: δ 73.39 (d, C1), 70.19 (d, C2), 60.83 (s, C3), 60.43 (d, C4), 23.67 (t, C5), 37.42 (d, C6), 145.24 (s, C7), 111.74 (t, C8), 22.01 (q, C9), 19.85 (q, С10). Найдено M 184.1100. Вычислено M 184.1094.
Соединение (1R,2R,6R)-(R)-2. 1H NMR (CDCl3): δ 1.42 (d, C9H3, J9-Me,8trans=0.6 Hz), 1.79 (m, C10H3, all J≤2.5 Hz), 1.87 (dddq, H5e′, J5e′,5a′=16.8 Hz, J5e′,4=J5e′6a=5.2 Hz, J5e′10-Me=1.6 Hz), 1.92 (br.s, OH-C2), 1.96 (ddm, H5a′, J5a′,5e′=16.8 Hz, J5a′,6a=11.1 Hz), 2.01 (ddd, H6a, J6a,5a′=11.1 Hz, J6a,5e′=5.2 Hz, J6a,1e=1.6 Hz), 2.47 (br.d, OH-C1, JOH,1e=3.4 Hz), 2.51 (d, H8cis, J8cis,8trans=4.4 Hz), 2.81 (dq, H8trans, J8trans,8cis=4.4 Hz, J8trans,9-Me=0.6 Hz), 3.81 (br.s, H2e′), 4.17 (ddd, H1e, J1e,OH=3.4 Hz, J1e,2e′=2.8 Hz, J1e,6a=1.6 Hz), 5.59 (ddq, H4, J4,5e′=5.2 Hz, J4,5a′=2.2 Hz, J4,10-Me=1.5 Hz). 13C NMR: δ 71.16 (d, C1), 71.85 (d, C2), 131.85 (s, C3), 124.49 (d, C4), 22.24 (t, C5), 35.88 (d, C6), 58.92 (s, C7), 51.30 (t, C8), 21.19 (q, C9), 20.82 (q, C10).
Пример 2. Синтез соединений 1 и 3 эпоксидированием 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола 4.
К раствору 0.458 г (2.73 ммоль) соединения (1R,2R,6S)-4 в 30 мл эфира прибавили 0.982 г (~ 4.2 ммоль) мета-хлорнадбензойной кислоты (70-75%, «Acros Organics») и выдержали при 4°С в течение 21 сут. Растворитель отогнали, остаток делили на колонке с 17 г SiO2 (Macherey-Nagel, 60-200µ, градиент этилацетата в гексане 0-100%). Получили 0.161 г (0.875 ммоль, 32%) (1S,2S,3R,4S,6R)-1-метил-4-(1-метилэтенил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1S,2S,3R,4S,6R)-1, 0.049 г (0.266 ммоль, 10%) (1R,2S,3R,4S,6S)-1-метил-4-(1-метилэтенил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1R,2S,3R,4S,6S)-1, а также 0.150 г (0.750 ммоль, 27%) (1S,2S,3R,4R,6R)-1-метил-4-(2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1S,2S,3R,4R,6R)-3 и 0.080 г (0.400 ммоль, 15%) (1R,2S,3R,4R,6S)-1-метил-4-(2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1R,2S,3R,4R,6S)-3 в виде смесей стереоизомеров.
(1S,2S,3R,4R,6R)-1-Метил-4-((R)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диол (1S,2S,3R,4R,6R)-(R)-3. 1Н NMR (CDCl3): δ 1.38 (s, C9H3), 1.44 (s, C10H3), 1.77 (ddd, H5a, J5a,5e=14.4 Hz, J5a,6a=11.2 Hz, J5a,4=1.8 Hz), 1.80 (ddd, H5e, J5e,5a=14.4 Hz, J5e,6a=5.8 Hz, J5e,4=2.2 Hz), 1.88 (ddd, H6a, J6a,5a=11.2 Hz, J6a,5e=5.8 Hz, J6a,1e=1.2 Hz), 2.22 (br.d, OH-C2, JOH,2e=8.9 Hz), 2.50 (d, H8cis,8trans=4.2 Hz), 2.56 (br.s, OH-C1), 2.78 (br.d, H8trans, J8trans,8cis=4.2 Hz), 3.32 (dd, H4, J4,5e=2.2 Hz, J4,5a=1.8 Hz), 3.75 (br.dd, H2e, J2e,OH=8.9 Hz, J2e,1e=2.8 Hz), 3.98 (dd, H1e, J1e,2e=2.8 Hz, J1e,6a=1.2 Hz). 13C NMR: δ 69.79 (d, C1, 1JC,H=147 Hz), 71.20 (d, C2, 1JC,H=147 Hz), 58.56 (s, C3), 63.11 (d, С4, 1JC,H=173 Hz), 20.99 (t, C5), 31.49 (d, C6), 59.01 (s, C7), 51.00 (t, C8, 1JC,H=173 Hz), 21.58 (q, C9), 22.25 (q, C10).
(1S,2S,3R,4R,6R)-1-Метил-4-((S)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диол (1S,2S,3R,4R,6R)-(S)-3. 1H NMR (CDCl3): δ 1.33 (d, C9H3, =0.6 Hz), 1.43 (s, C10H3), 1.95 (ddd, H6a, J6a,5a=12.2 Hz, J6a,5e=4.8 Hz, J6a,1e=1-4 Hz), 2.05 (ddd, H5a, J5a,5e=14.6 Hz, J5a,6a=12.2 Hz, J5a,4=1.8 Hz), 2.17 (ddd, H5e, J5e,5a=14.6 Hz, J5e,6a=4.8 Hz, J5e,4=2.2 Hz), 2.25 (d, OH-C2, JOH,2e=9.7 Hz), 2.63 (d, H8cis, J8cis,8trans=3.7 Hz), 2.77 (s, OH-C1), 3.10 (dq, H8trans, J8trans,8cis=3.7 Hz, J8trans,9-Me=0.6 Hz), 3.37 (dd, H4, J4,5e=2.2 Hz, J4,5a=1.8 Hz), 3.59 (m, H1e, all J<3.0 Hz), 3.67 (dd, H2e, J2e,OH=9.7 Hz, J2e,1e=2.8 Hz). 13C NMR: δ 69.18 (d, C1, 1JC,H=146 Hz), 71.09 (d, C2, 1JC,H=147 Hz), 58.46 (s, C3), 63.18 (d, С4, 1JC,H=174 Hz), 21.44 (t, C5), 31.07 (d, C6), 60.03 (s, C7), 52.75 (t, C8, 1JC,H=173 Hz), 20.79 (q, C9), 22.19 (q, C10).
(1R,2S,3R,4R,6S)-1-Метил-4-((R)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диол (1R,2S,3R,4R,6S)-(R)-3. 1H NMR (CDCl3): δ 1.34 (d, C9H3, J9-Me,8trans=0.6 Hz), 1.41 (s, C10H3), 1.81 (ddd, H6a, J6a,5a=12.3 Hz, J6a,5e=7.3 Hz, J6a,1e=1.8 Hz), 2.06 (dd, H5a, J5a,5e=15.7 Hz, J5a,6a=12.3 Hz), 2.13 (ddd, H5e, J5e,5a=15.7 Hz, J5e,6a=7.3 Hz, J5e,4=5.0 Hz), 2.53 (d, H8cis, J8cis,8trans=4.8 Hz), 2.81 (br.d, H8trans, J8trans,8cis=4.8 Hz), 3.21 (d, H4, J4,5e=5.0 Hz), 3.68 (br.m, H1e, all J<3.5 Hz), 3.99 (dd, H2e, J2e,1e=3.2 Hz, J2e,4=1.2 Hz). 13C NMR: δ 71.59 (d, С1, 1JC,H=147 Hz), 70.19 (d, С2, 1JC,H=145 Hz), 60.86 (s, C3), 60.08 (d, C4, 1JC,H=175 Hz), 21.46 (t, C5), 36.62 (d, C6), 57.85 (s, C7), 53.06 (t, C8, 1JC,H=174 Hz), 20.08 (q, C9), 19.68 (q, C10).
(1R,2S,3R,4R,6S)-1-Метил-4-((S)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диол (1R,2S,3R,4R,6S)-(S)-3. 1H NMR (CDCl3): δ 1.36 (s, C9H3), 1.40 (s, C10H3), 1.77-1.85 (m, H5a, H6a), 1.95-2.03 (m, H5e), 2.56 (d, H8cis, J8cis,8trans=4.6 Hz), 2.67 (br.s, OH-C2), 2.73 (br.d, H8trans, J8trans,8cis=4.6 Hz), 3.08 (d, OH-C1, JOH,1e=11.5 Hz), 3.17 (dd, H4, J4,5e=5.1 Hz, J4,2e=1.2 Hz), 3.79 (br. dd, H1e, J1e,OH=11.5 Hz, J1e,2e=3.3 Hz), 3.99 (br. m, H2e, all J<3.5 Hz). 13C NMR: δ 72.11 (d, C1, 1JC,H=148 Hz), 70.01 (d, C2, 1JC,H=146 Hz), 60.91 (s, C3 or C7), 60.02 (d, C4, 1JC,M=175 Hz), 21.01 (t, C5), 36.60 (d, C6), 57.51 (s, C3 or C7), 52.85 (t, C8, 1JC,H=173 Hz), 20.10 (q, C9), 19.69 (q, C10).
Пример 3. Синтез диацетата (1R,2R,6S)-5.
К 0.168 г соединения (1R,2R,6S)-4 добавили 6 мл эфира, 1.00 мл триэтиламина, 0.50 мл уксусного ангидрида и один кристалл N,N-4-диметиламинопиридина (DMAP). Через 4 часа промыли смесь 2×10 мл 3.5% HCl, 2×10 мл 5% NaHCO3 и 10 мл воды, сушили над MgSO4, растворитель отогнали. Получили 0.252 г (100%) диацетата (1R,2R,6S)-3-метил-6-(1-метилэтенил)циклогекс-3-ен-1,2-диола (1R,2R,6S)-5. [α]D 27=-77.0 (с 6.87, CHCl3). Спектр ЯМР 1Н совпал со спектром, опубликованным в литературе [7].
Пример 4. Синтез соединений 6 и 7.
К раствору 3.004 г (11.91 ммоль) диацетата (1R,2R,6S)-5 в 80 мл диоксана прибавили 80 мл H2O и 4.099 г (23.03 ммоль) N-бромсукцинимида. Реакционную смесь перемешивали 20 мин. Добавили 50 мл насыщ. Na2SO3 и интенсивно перемешивали в течение 5 мин. Добавили 100 мл EtOAc. Водную фазу отделили и экстрагировали 3×100 мл EtOAc. Объединенную органическую фазу сушили Na2SO4. Осушитель отфильтровали, растворитель отогнали. Остаток (7.93 г) делили колоночной хроматографией на колонке с 100 г SiO2 градиентом EtOAc в гексане от 0 до 100%. Выделили (1R,2R,6R)-6-((R)-1-бром-2-гидроксипропан-2-ил)-3-метилциклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(R)-6 (0.578 г, 1.656 ммоль), (1R,2R,6R)-3-метил-6-((R)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диилдиацетата (0.290 г, 1.080 ммоль) (1R,2R,6R)-(R)-7, а также смесовые фракции в разных соотношениях попарно бромгидринов (1R,2R,6R)-(R)-6 и (1R,2R,6R)-(S)-6 и эпоксидов (1R,2R,6R)-(R)-7 и (1R,2R,6R)-(S)-7. Расчетный выход продуктов составляет: 1.769 г (5.065 ммоль, 43%) (1R,2R,6R)-6-((R)-1-бром-2-гидроксипропан-2-ил)-3-метилциклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(R)-6, 0.360 г (1.030 ммоль, 9%) (1R,2R,6R)-6-((S)-1-бром-2-гидроксипропан-2-ил)-3-метилциклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(S)-6, 0.474 г (1.765 ммоль, 15%) (1R,2R,6R)-3-метил-6-((R)-2метилоксиран-2-ил)циклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(R)-7, 0.033 г (0.123 ммоль, 1%) (1R,2R,6R)-3-метил-6-((S)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(S)-7.
Соединение (1R,2R,6R)-(R)-6. 1H HNMR (CDCl3): δ 1.23 (s, C9H3), 1.65 (m, С10Н3, all J≤2.5 Hz), 2.00 (s, C12H3), 2.06 (s, C14H3), 2.17-2.27 (m, 2H5, H6), 3.46 (d, H8, J8,8′=10.6 Hz), 3.60 (d, H8′, J8′,8=10.6 Hz), 4.98 (br. d, H2e′, J2e′,1e=2.7 Hz), 5.21 (br. d, H1e, J1e,2e′=2.7 Hz), 5.80-5.83 (m, H4). 13C NMR: δ 68.56 (d, C1), 70.52 (d, C2), 128.27 (s, C3), 127.88 (d, C4), 21.50 (t, C5), 39.63 (d, C6), 71.90 (s, C7), 43.94 (t, C8), 22.96 (q, C9), 20.37 (q, C10), 169.91 (s, C11), 21.04 (q, C12), 169.76 (s, C13), 20.81 (q, C14).
Соединение (1R,2R,6R)-(S)-6. 1H HNMR (CDCl3): δ 1.27 (s, C9H3), 1.68 (m, C10H3, all J≤2.5 Hz), 2.03 (s, C12H3), 2.08 (s, C14H3), 2.06-2.13 (m, H5e′), 2.18-2.26 (m, H5a′, H6), 3.46 (d, H8, J8,8′=10.5 Hz), 3.50 (d, H8′, J8′,8=10.5 Hz), 5.07 (br. d, H2e′, J2e′,1e=2.8 Hz), 5.32 (dd, H1e, J1e,2e′=2.8 Hz, J1e,6=1.4 Hz), 5.78-5.81 (m, H4). 13C NMR: δ 68.75 (d, C1), 70.17 (d, C2), 128.59 (s, C3), 127.53 (d, C4), 22.32 (t, C5), 38.86 (d, C6), 72.14 (s, C7), 42.86 (t, C8), 23.78 (q, C9), 20.47 (q, C10), 170.08 (s, C11), 21.17 (q, C12), 169.75 (s, C13), 20.87 (q, C14).
Соединение (1R,2R,6R)-(R)-7. 1H NMR (CDCl3): δ 1.27 (d, C9H3, J9-Me,8trans=0.6 Hz), 1.63 (m, C10H3, all J≤2.5 Hz), 1.88 (ddd, H6a, J6a,5a′=11.2 Hz, J6a,5e′=5.3 Hz, J6a,1e=2.0 Hz), 2.02 (s, C12H3), 2.04 (s, C14H3), 2.03-2.08 (m, H5e′), 2.18 (ddm, H5a′, J5a′,5e′=17.6 Hz, J5a′,6a=11.2 Hz, другие J<3.0 Hz), 2.47 (d, H8cis, J8cis,8trans=4.6 Hz), 2.59 (dq, H8trans, J8trans,8cis=4.6 Hz, J8trans,9-Me=0.6 Hz), 5.07 (br. d, H2e′, J2e′1e=2.8 Hz), 5.18 (dd, H1e, J1e,2e′=2.8 Hz, J1e,6a=2.0 Hz), 5.73 (ddq, H4, J4,5e′=5.3 Hz, J4,5a′=2.4 Hz, J4,10-Me=1.5 Hz). 13C NMR: δ 69.48 (d, C1), 69.91 (d, C2), 128.62 (s, C3), 127.12 (d, C4), 22.69 (t, C5), 38.01 (d, C6), 56.78 (s, C7), 51.81 (t, C8), 19.80 (q, C9), 20.37 (q, C10), 169.65 (s, C11), 20.93 (q, C12), 169.60 (s, C13), 20.79 (q, C14).
Соединение (1R,2R,6R)-(S)-7. 1H NMR (CDCl3): δ 1.34 (d, C9H3, http://J9.Mc.tom1s=0.6 Hz), 1.65 (m, C10H3, all J≤2.5 Hz), 1.84-1.93 (m, H5a′), 2.02 and 2.08 (2s, C12H3, C14H3), 2.01-2.10 (m, H5e′, H6a), 2.47 (d, H8cis, J8cis,8trans=4.7 Hz), 2.65 (dq, H8trans, J8trans,8cis=4.7 Hz, J8trans,9-Me=0.6 Hz), 5.09 (br. d, H2e′, J2e′,1e=2.8 Hz), 5.21 (dd, H1e, J1e,2e′=2.8 Hz, J1e,6a=1.8 Hz), 5.72-5.76 (m, H4). 13C NMR: δ 69.49 (d, C1), 70.06 (d, C2), 128.71 (s, C3), 127.12 (d, C4), 22.04 (t, C5), 37.99 (d, C6), 56.43 (s, C7), 51.21 (t, C8), 20.76 (q, C9), 20.36 (q, C10), 169.61 and 169.77 (2s, С11, C13), 20.87 and 20.90 (2q, С12, C14).
Пример 5. Синтез соединений (1R,2R,6R)-(R)-2 и (1R,2R,6R)-(S)-2.
К раствору 0.578 г (1.656 ммоль) бромгидрина (1R,2R,6R)-(R)-6 в 15 мл диоксана добавили 10 мл H2O и 0.500 мл (3.59 ммоль) NEt3. Реакционную смесь перемешивали 24 ч, затем упарили часть растворителя на ротационном испарителе до объема ~2 мл. Добавили 6 мл H2O. Экстрагировали EtOAc (4×5 мл). Объединенные экстракты сушили над Na2SO4. Осушитель отфильтровали, растворитель отогнали. Остаток (0.563 г) очищали колоночной хроматографией на колонке с 8 г SiO2 градиентом EtOAc в гексане от 0 до 40%. Получили 0.411 г (1.531 ммоль, 92%) (1R,2R,6R)-3-метил-6-((R)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диилдиацетата (1R,2R,6R)-(R)-7.
К раствору 0.271 г (6.77 ммоль) NaOH в 15 мл H2O добавили раствор 0.396 г (1.477 ммоль) эпоксидиацетата (1R,2R,6R)-(R)-7 в 25 мл диоксана. Реакционную смесь перемешивали 24 ч, затем упарили на ротационном испарителе до объема ~3 мл. Добавили 10 мл насыщ. NaCl. Экстрагировали EtOAc (5×5 мл). Объединенные экстракты сушили над Na2SO4. Осушитель отфильтровали, растворитель отогнали. Остаток (0.272 г) очищали колоночной хроматографией на колонке с 9 г SiO2 градиентом EtOAc в гексане от 0 до 50%. Получили 0.210 г (1.142 ммоль, 77%) (1R,2R,6R)-3-метил-6-((R)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диола (1R,2R,6R)-(R)-2.
Аналогично из эпоксидиацетата (1R,2R,6R)-(S)-7 за 8 ч с выходом 78% синтезировали эпоксид (1R,2R,6R)-(S)-2.
Соединение (1R,2R,6R)-(S)-2. 1Н NMR (CDCl3): δ 1.38 (s, C9H3), 1.80 (m, C10H3, all J≤2.5 Hz), 2.11 (ddd, H6a, J6a,5a′=10.0 Hz, J6a,5e′=6.7 Hz, J6a,1e=1.6 Hz), 2.16-2.21 (m, 2H5), 2.66 (d, H8cis, J8cis,8trans=3.9 Hz), 3.16 (br. d, H8trans, J8trans,8cis=3.9 Hz), 3.79 (br. d, H2e′, J2e′,1e=2.8 Hz), 3.90 (br. m, H1e, all≤2.8 Hz), 5.65-5.68 (m, H4). 13C NMR: δ 70.74 (d, C1), 71.68 (d, C2), 131.76 (s, C3), 124.87 (d, C4), 22.82 (t, C5), 34.98 (d, C6), 60.05 (s, C7), 52.46 (t, C8), 20.87 (q, C9), 20.80 (q, C10).
Пример 6. Синтез соединения (1R,2R,6R)-(R)-2.
К раствору 0.200 г (0.571 ммоль) бромгидрина (1R,2R,6R)-(R)-6 в 7.5 мл диоксана добавили 5 мл H2O и 0.170 мл (1.22 ммоль) NEt3. Реакционную смесь перемешивали 24 ч. Добавили раствор 0.083 г (2.06 ммоль) NaOH в 0.5 мл H2O и перемешивали еще 14 ч. Упарили часть растворителя на ротационном испарителе до объема ~4 мл. Добавили 10 мл насыщ. NaCl. Экстрагировали EtOAc (6×5 мл). Объединенные экстракты сушили над Na2SO4. Осушитель отфильтровали, растворитель отогнали. Остаток (0.113 г) очищали колоночной хроматографией на колонке с 4.5 г SiO2 градиентом EtOAc в гексане от 0 до 50%. Получили 0.097 г (0.525 ммоль, 92%) (1R,2R,6R)-3-метил-6-((R)-2-метилоксиран-2-ил)циклогекс-3-ен-1,2-диола (1R,2R,6R)-(R)-2.
Пример 7. Синтез соединения 3.
К раствору 0.076 г (0.410 ммоль) эпоксидиола (1R,2R,6R)-(R)-2 в 18 мл Et2O добавили в течение 1 мин. 0.280 г (~1.13 ммоль,) мета-хлорнадбензойной кислоты (содержание 70-75%). Реакционную смесь перемешивали 3 ч, затем оставили при комн. температуре на 4 сут. Растворитель отогнали. Остаток (0.341 г) делили колоночной хроматографией на 9 г SiO2 градиентом EtOAc в гексане от 0 до 100%. Получили 0.055 г (0.277 ммоль, 68%) (1S,2S,3R,4R,6R)-1-метил-4-((R)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1S,2S,3R,4R,6R)-(R)-3 и 0.019 г (0.093 ммоль, 23%) (1R,2S,3R,4R,6S)-1-метил-4-((R)-2-метилоксиран-2-ил)-7-оксабицикло[4.1.0]гептан-2,3-диола (1R,2S,3R,4R,6S)-(R)-3.
Пример 8. Исследование противопаркинсонической активности.
Эксперименты проводились на самцах мышей линии С57В 1/6 массой 25-30 г. Паркинсонический синдром индуцировали четырехкратным введением нейротоксина МФТП в дозе 20 мг/кг через каждые 2 ч. Исследуемые агенты вводили внутрижелудочно через 24 ч после последнего введения нейротоксина в дозе 20 мг/кг. Исследование двигательной и исследовательской активности животных проводили в группах по 8 мышей в автоматизированной установке TruScan через 1,5 ч после введения агентов.
Результаты экспериментов приведены в Таблице 1.
Из Таблицы 1 видно, что соединения 1-3 в дозе 20 мг/кг достоверно устраняют проявления олигокинезии, вызванной введением нейротоксина МФТП, а именно способствовали восстановлению параметров двигательной (время двигательной активности, дистанция движения и скорость движения) и исследовательской (количество вертикальных стоек и исследованных отверстий) активности животных, до уровня интактных животных. Соединение (1S,2S,3R,4S,6R)-1 превосходит по эффективности препарат сравнения (1R,2R,6S)-4, более существенно увеличивая дистанцию движения (двигательная активность) и достоверно повышая количество вертикальных стоек (исследовательская активность). В целом, соединения 1-3 оказывают более выраженное положительное действие на исследовательскую активность животных, чем препарат сравнения 4.
В результате экспериментов показано, что агенты 1, 2 и 3 в дозе 20 мг/кг обладают выраженной противопаркинсонической активностью, проявляющейся в восстановлении двигательной и исследовательской активности у животных с индуцированным паркинсоническим синдромом.
Пример 9. Исследование противосудорожной активности.
В экспериментах использованы аутбредные мыши (самцы) стока CD-1 СПФ качества. Исследование противосудорожной активности проводили в тесте максимального электрошока (МЭШ). Исследование проводили согласно «Методическим рекомендациям по доклиническому изучению противосудорожной активности лекарственных средств» (Руководство по проведению доклинических исследований лекарственных средств, 2012). Судороги у животных вызывали при помощи генератора прямоугольных импульсов постоянного тока и корнеальных электродов.
Исследуемые агенты вводили внутрижелудочно за 1 ч до максимального электрошока в дозах 1 мг/кг и 10 мг/кг. В качестве позитивного контроля использовали карбамазепин в дозе 10 мг/кг.
Определяли следующие показатели: количество животных с судорогами, количество животных с тонико-экстензорной реакцией.
Результаты экспериментов приведены в Таблице 2.
Представленные в Таблице 2 результаты показывают, что выбранные параметры электрического воздействия вызывали у 11 мышей (у 78,6%) контрольной группы развитие тонико-экстензорной реакции сразу после нанесения удара электрическим током. Препарат сравнения карбамазепин (10 мг/кг) достоверно снижал число животных с реакцией с 78,6% до 28,5%. Исследуемые соединения 1-3 в дозе 1 мг/кг достоверно уменьшали количество животных с тонико-экстензорной реакцией с 78,6% до 30,0%, 37,5% и 25% соответственно. Соединение (1R,2S,3R,4R,6S)-(R)-3 в дозе 10 мг/кг также достоверно уменьшало количество животных с тонико-экстензорной реакцией до 37,5%. Соединения 1-2 в дозе 10 мг/кг существенно не снижало количество животных с реакцией.
В результате экспериментов показано, что агенты 1, 2 и 3 в дозе 1 мг/кг обладают противосудорожной активностью, проявляющейся в снижении количества мышей с тонико-экстензорной реакцией в тесте максимально электрошока, не уступая по эффективности карбамазепину (10 мг/кг).
Источники информации
1. Венгеровский А.И. Лекции по фармакологии для врачей и провизоров. Томск: STT. 1998. С. 181-186.
2. Аминофф М.Д. Фармакотерапия паркинсонизма и других двигательных нарушений. В кн.: Базисная и клиническая фармакология. Т.1. Под ред. Катцунга Б.Г. М.: Бином. 2007. С. 539-555.
3. Perucca P., Gilliam F. Adverse effects of antiepileptic drugs. Lancet neurology, 2012, 11, 792-802.
4. Il′ina I.V., Volcho K.P., Korchagina D.V., Barkhash V.A., Salakhutdinov N.F. Helv. Chim. Acta, 2007, V. 90, №2, P. 353-368.
5. Ardashov О.V., Pavlova Α.V., Il′ina I.V., Morozova Ε.Α., Korchagina D.V., Karpova Ε.V., Volcho K.P., Tolstikova T.G., Salakhutdinov N.F. Highly Potent Activity of (1R,2R,6S)-3-Methyl-6-(prop-1-en-2-y1)cyclohex-3-ene-l,2-diol in Animal Models of Parkinson′s Disease. J. Med. Chem., 2011, 54, 3866-3874.
6. Jackson-Lewis V.; Przeborski S. Protocol for the MPTP mouse model of Parkinson′s disease. Nat. Protoc, 2007, 2, 141-151.
7. Толстикова Т.Г., Павлова A.B., Морозова E.A., Ильина И.В., Ардашов О.В., Волчо К.П., Салахутдинов Н.Ф. Средство для лечения болезни Паркинсона. Патент № RU 2418577 от 20.05.2011.
8. Sprenger F., Poewe W. Management of Motor and Non-Motor Symptoms in Parkinson′s Disease. CNS Drugs, 2013, 27, 259-272.
1. Применение эпоксидов 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола, описываемых формулами 1-3 включая их пространственные изомеры, в том числе оптически активные формы, в качестве средств для лечения болезни Паркинсона.
2. Применение эпоксидов 3-метил-6-(проп-1-ен-2-ил)циклогекс-3-ен-1,2-диола, описываемых формулами 1-3 включая их пространственные изомеры, в том числе оптически активные формы, в качестве противосудорожных средств.