Противосудорожное средство
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам, а именно к используемым при эпилепсии. Техническим результатом изобретения является повышение противосудорожной активности. Технический результат достигается применением дигидрохлорида 9-диалкил аминоэтил-2-(4-фторфенил)имидазо[1,2-а]-бензимидазола общей формулы
где a) NR2 = пирролидино;
б) NR2 = морфолино,
в качестве соединения, обладающего противосудорожной активностью. Соединение может быть использовано для изготовления противосудорожного средства. 1 з.п. ф-лы, 8 ил., 1 табл.
Реферат
Изобретение относится к лекарственным средствам, а именно к используемым при эпилепсии. Эпилепсия - это хроническое заболевание головного мозга, характеризующееся повторными непровоцируемыми приступами нарушения двигательных, чувствительных, вегетативных, мыслительных или психических функций, возникающими вследствие чрезмерных нейронных разрядов [Реабилитация детей с эпилепсией: Методическое пособие / О.В. Халецкая, В.А. Воробьева, Н.В. Караштина, О.В. Конурина. Н. Новгород: Изд-во Нижегородской государственной медицинской академии, 2001. С. 3].
В настоящее время фармакотерапия эпилепсии является одной из актуальных медицинских проблем. При этом за последние 15 лет в России не было зарегистрировано ни одного нового оригинального противоэпилептического препарата.
По данным Международной противоэпилептической лиги (МПЭЛ), в Западной и Центральной Европе эпилепсией страдают 6 млн. человек, в течение ближайших 20 лет предположительно будут болеть около 15 млн. Соответствующие цифры для России ориентировочно составляют около полумиллиона больных эпилепсией, при заболеваемости 54 тыс. в год [Зенков Л.Р. Лечение эпилепсии / Под ред. чл.-корр. РАМН Н.Н. Яхно. М., 2001. С. 8].
Альтернативные методы лечения только в редких случаях оказываются эффективными, при этом не существует профилактических мер по предотвращению развития эпилепсии. Противоэпилептические препараты первого и второго поколений представляются эффективными только в купировании остро возникающих приступов, а также некоторых симптомов, связанных с хроническим течением болезни [Белоусов Ю.Б. и др. Клинико-экономическая оценка эффективности лечения больных с эпилепсией // Качественная клиническая практика. - 2002. - №. 3. - С. 54-59].
Известны средства, используемые при эпилепсии - карбамазепин, фенитоин, фенобарбитал, этосуксимид, диазепам [Зенков Л.Р. Фармакологическое лечение эпилепсии // Русский медицинский журнал. - 2000. - Т. 8. - №. 10. - С.411-417].
Однако они вызывают серьезные побочные эффекты, которые связаны с воздействием на нервную систему и психическую сферу, а также прямым токсическим действием на внутренние органы. К наиболее частым побочным реакциям относятся: сонливость, снижение памяти, внимания, работоспособности, головокружение, тошнота, влияние на желудочно-кишечный тракт и печень, кроветворную систему, а также другие проявления, свойственные каждому препарату в отдельности [Glauser Т., Ben-Menachem E., Bourgeois В., Cnaan A., Chadwick D., Guerreiro С, et al. ILAE treatment guidelines: evidence-based analysis of antiepileptic drug efficacy and effectiveness as initial. monotherapy for epileptic seizures and syndromes // Epilepsia. - 2006. - V. 47. - P. 1094-120]. Значительная выраженность этих проявлений и плохая переносимость напрямую отражается на качестве жизни пациентов и часто являться поводом для поиска альтернативного препарата.
Известны средства - этосуксимид [Evason К. et al. Anticonvulsant medications extend worm life-span // science. - 2005. - T. 307. - №. 5707. - C. 258-262.], фенитоин [Rajasekhar K. K. et al. Comparative study of conventional and microwave induced synthesis of selected heterocyclic molecules // International Journal of ChemTech Research. - 2010. - T. 2. - №. 1.], примидон [Bogdanov G.N. et al. [Anticonvulsants as bioantioxidants under stress conditions] // Biomeditsinskaia khimiia. - 2008. - T. 55. - №. 4. - C. 519-524.], бензодиазепины [Narayana B. et al. Synthesis of some new substituted triazolo [4, 3-a] [1, 4] benzodiazepine derivatives as potent anticonvulsants //European journal of medicinal chemistry. - 2006. - T. 41. - №. 3. - C. 417-422.] и др. относящиеся к гетероциклическим структурам.
Известны средства с ГАМК-эргическим действием (прогабид, тиагабин) [Sato К. et al. An analysis of anticonvulsant actions of GABA agonists (progabide and baclofen) in the kindling model of epilepsy // Epilepsy research. - 1990. - T. 5. - №. 2. - С.117-124.] [Winhusen Т.M. et al. A placebo-controlled screening trial of tiagabine, sertraline and donepezil as cocaine dependence treatments //Addiction. - 2005. - T. 100. - №. s1. - C. 68-77].
Однако данные препараты проявляют значительную токсичность и могут обладать проконвульсивной активностью [Stahl, S. Stahl′s Essential Psychopharmacology: Prescriber′s Guide. Cambridge University Press: New York, NY. 2009. pp. 523-526].
Наряду с этим обнаружены производные бензимидазола, проявляющие агонистическое взаимодействие с ГАМК-А рецепторами [Larsen J. S. et al. Benzimidazole derivatives and their use for modulating the GABAA receptor complex: пат. 8492408 США. - 2013.]. Данный класс веществ рассматривается как высокоперспективный в отношении поиска новых антиконвульсивных средств [Jain P. et al. Design, synthesis and biological evaluation of some novel benzimidazole derivatives for their potential anticonvulsant activity //Archives of pharmacal research. - 2010. - T. 33. - №. 7. - C. 971-980].
Наиболее часто применяемым противосудорожным средством, рекомендуемым ВОЗ при эпилепсии, является вальпроат натрия [Зенков Л.Р. Фармакологическое лечение эпилепсии // Русский медицинский журнал. - 2000. - Т. 8. - №. 10. - С. 411-417].
Вальпроат натрия эффективно подавляет коразоловые судороги.
Однако его противосудорожная активность остается недостаточно высокой.
Техническим результатом изобретения является повышение противосудорожной активности.
Технический результат достигается применением дигидрохлорида 9-диалкил аминоэтил-2-(4-фторфенил) имидазо[1,2-а]-бензимидазола общей формулы
где a) NR2 = пирролидино;
б) NR2 = морфолино,
в качестве соединения, обладающего противосудорожной активностью.
Соединение может быть использовано для изготовления противосудорожного средства.
Дигидрохлорид 9-(2-морфолиноэтил)-2-(4-фторфенил)имидазо[1,2-а] бензимидазола и дигидрохлорид 9-(2-пирролидиноэтил)-2-(4-фторфенил)имидазо[1,2-а] бензимидазола известны как проявляющие обезболивающее действие (патент РФ №2412187, МПК C07D 487/04, 2011 г.) и каппа-опиоидную агонистическую активнось (патент РФ №2413512, МПК А61К 31/4188, 2011 г.). В предлагаемом случае соединения проявляют противосудорожное действие, новое в ряду имидазо[1,2-а]бензимидазола.
Ниже приведены испытания противосудорожной активности соединений I.
МЕТОДЫ ИССЛЕДОВАНИЯ
Объекты исследования: соединение РУ-1205 (дигидрохлорид 9-(2-морфолиноэтил)-2-(4-фторфенил)имидазо[1,2-а]бензимидазола) и РУ-1203 дигидрохлорид 9-(2-пирролидиноэтил)-2-(4-фторфенил)имидазо[1,2-а] бензимидазола, синтезированные в НИИ физической и органической химии Южного федерального университета (НИИ ФОХ ЮФУ). Эксперименты проводились в соответствии с правилами лабораторной практики (GLP), со статьей 11 Федерального закона от 12 апреля 2010 г. №61-ФЗ «Об обращении лекарственных средств» (Собрание законодательства Российской Федерации, 2010, №16, ст. 1815; №31, ст. 4161), «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ» под ред. Р.У. Хабриева, М. ОАО «Издательство «Медицина», 2005. (М., 2005).
Исследования проводились на 130 самцах белых нелинейных мышей массой 20-22 г, содержащихся в условиях вивария (температура 22-24°C, относительная влажность воздуха 40-50%) с естественным световым режимом на стандартной диете лабораторных животных в соответствии с ГОСТ Р 50258 92 [1993], с соблюдением правил лабораторной практики при проведении доклинических исследований в РФ, регламентированных ГОСТ Р 51000.3 96 [1996] и ГОСТ Р 51000.4 96 [1996], а также правил и Международных рекомендаций «Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях» [European convention for the protection of vertebral animals used for experimental and other scientific purpose: Council of Europe 18.03.1986. - Strasbourg, 1986. - 52 p].
Противосудорожная активность оценивалась на стандартной модели эпилептогенеза, вызванного подкожным введением антагониста ГАМК рецепторов коразолом («SIGMA», США) [Swinyard, 1969].
Изучаемые вещества вводились внутрибрюшинно в диапазоне доз 0,1-20,0 мг/кг. Группа позитивного контроля получала вальпроат натрия («Конвулекс», Австрия) в диапазоне доз 50-300 мг/кг. Группе негативного контроля инъецировался эквивалентный объем растворителя (дистиллированная вода). Противосудорожная активность веществ оценивалась по способности предотвращать развитие клонических судорог продолжительностью более 3 секунд.
Для исследуемых соединений и эталонного препарата определялись величины ЭД50 методом наименьших квадратов.
Острая токсичность изучалась на 60 белых нелинейных мышах-самцах массой 18-22 г при внутрибрюшинном введении. Расчет ЛД50 производили по классическому методу Личфилда-Вилкоксона с использованием регрессионной статистики (Microsoft Excel), позволяющей рассчитывать этот показатель на основе результатов фармакологических испытаний изучаемых веществ по тестам с альтернативной формой реакции.
В качестве интегрального показателя условной широты терапевтического действия (ТИ) использовался условный терапевтический индекс соединений, который рассчитывался как отношение ЛД50 к ЭД50.
Электрофизиологические исследования проводились на белых нелинейных крысах обоего пола, весом 200-250 г. в НИИ нейрокибернетики им. А.Б. Когана ЮФУ. Эксперименты выполнялись в области соматосенсорной коры крыс по методу [Сухов, 1992].
Для исследования влияния новых соединений на формирование нормальной и патологической ритмики мозга крыс использовалась методика микроаппликации 30,5 мкМ раствора РУ-1205 и 23,7 мкМ раствора РУ-1203 в объеме 1 мкл. Микроаппликация производилась методом локального введения на расстоянии до 100 мкм от регистрирующих микроэлектродов на глубине 1000 мкм. Объем вводимых веществ составлял доли микролитра, время микроаппликации занимало ≈30 секунд.
Для исследования противоэпилептических свойств соединений РУ-1205 и РУ-1203 использовали метод искусственного генеза эпиактивности с помощью электрической стимуляции поверхности мозга (ритмическая стимуляция током с параметрами: напряжение 120 В, длительность 10 с, частота стимуляции 10 Гц).
Для усиления биоэлектрической активности использовался 10 канальный усилитель УБС 1/10 (Россия) с полосой пропускания от 0,1 Гц до 2000 Гц. Регистрация фоновой фокальной и вызванной биоэлектрической активности проводилась на жесткий магнитный диск ЭВМ с помощью 16-канального АЦП L-761 (L-Card, Россия) с частотой дискретизации сигнала 1 кГц. Для стимуляции использовались электростимуляторы ЭСЛ-2 (Россия), ГЭФИ-3-БУ (Россия). Управление стимуляцией производилось через TTL выходы платы L-761 (L-Card, Россия) и задавалось программно.
Для обработки и анализа электрической активности использовались методы статистического анализа временных рядов: спектры мощности, спектры когерентности, фазовые кросспектры с помощью программ Spectrum [Строкун], DataViewRus [Гусач] и Statistica 5.0. Значимость различий между выборками оценивалась по критерию знаков (p<0,05) [В.Ю. Урбах, 1963]. При построении диаграмм и графиков использовали пакет программ MS Exel.
РЕЗУЛЬТАТЫ ИСПЫТАНИЙ
В тесте судорог, вызванных коразолом, соединения РУ-1205 (2-(4-фторфенил)-9-морфолиноэтилимидазо[1,2-а]бензимидазол) и РУ-1203 (2-(4-фторфенил)-9-пирролидиноэтилимидазо[1,2-а] бензимидазол) проявляли дозозависимое противосудорожное действие и статистически значимо предотвращали развитие клонических припадков продолжительностью более 3 секунд (p<0,05).
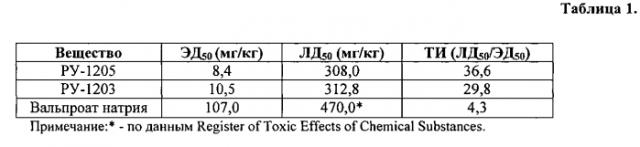
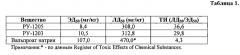
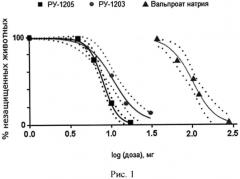
На рисунке 1 показано дозозависимое влияние соединения РУ-1205, РУ-1203 и вальпроата натрия на развитие клонических судорог, вызванных подкожным введением коразола (СI 95% обозначены пунктирной линией). В результате эксперимента было показано, что медианная антиконвульсивная активность соединений РУ-1205 (ЭД50=8,4 мг/кг) и РУ-1203 (ЭД50=10,5 мг/кг) превышает активность вальпроата натрия (ЭД50=107,0 (мг/кг) в 12 и 10 раз соответственно.
В таблице 1 приведены величина антиконвульсивной активности (ЭД50), показатель острой токсичности (ЛД50) и терапевтический индекс (ТИ=ЛД50/ЭД50) исследуемого вещества РУ-1205 и вальпроата натрия на модели коразоловых судорог. Расчеты показали, что терапевтический индекс соединения РУ-1205 составляет 36,6, то есть в 8,5 раз выше по сравнению референтным препаратом. Терапевтический индекс соединение РУ-1203 составляет 29,8, то есть в 7 раз выше, чем у вальпроата натрия. Полученные данные свидетельствует об относительно высокой терапевтической безопасности указанных соединений.
ВЛИЯНИЕ СОЕДИНЕНИЙ РУ-1203 И РУ-1205 НА ФОНОВЫЙ РИТМОГЕНЕЗ
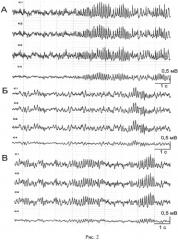
На рис. 2 показано влияние соединения РУ-1203 на формирование фоновой фокальной ритмики в отдельных соматосенсорных корковых колонках мозга крысы. А - до локальной микроаппликации. Б - 2 мин после введения. В - 5 мин после введения. Обозначения: К1 и К2 верхние (500 мкм) и нижние (1400 мкм) слои, соответственно, контрольной (соседней) корковой колонки; КЗ и К4 - верхние (400 мкм) и нижние (1500 мкм) слои нейронной колонки, в которую производилась микроаппликация 23,7 мкМ раствора соединения РУ-1203.
В ходе электрофизиологических исследований регистрировалась альфа подобная (8-12 Гц) ритмическая активность коры головного мозга крысы, что соответствует спокойному, дремотному состоянию животного. На рисунке 2А можно увидеть устойчивое развитие альфа ритмики в отдельных колонках соматосенсорной коры крысы, полученное в условиях до микроаппликации исследуемых веществ.
Соединение РУ-1203 (23,7 мкМ раствора в объеме 1 мкл) в непосредственной близости от регистрирующих каналов лишь на непродолжительное время (1-2 мин) в незначительной степени изменяет частотные характеристики фоновой ритмики (Рис. 2Б). Однако после 5 мин наблюдений доминирование альфа ритмики восстанавливается (Рис. 2В).
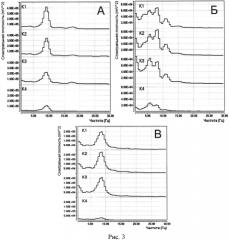
На рис. 3 представлены спектры мощности фокальной фоновой активности корковых нейронных колонок до и после локальной микроаппликации соединения РУ-1203. А - до локальной микроаппликации. Б - 2 мин после введения. В - 5 мин после введения.
Обозначения: К1 и К2 верхние (500 мкм) и нижние (1400 мкм) слои, соответственно, контрольной (соседней) корковой колонки; К3 и К4 - верхние (400 мкм) и нижние (1500 мкм) слои нейронной колонки, в которую производилась микроаппликация 23,7 мкМ раствора соединения РУ-1203.
На Рис. 3А представлена соответствующая гистограмма спектра мощности полученной электокортикограммы (ЭКоГ). На данном рисунке видно, что преобладающая фоновая ритмика имеет частоту 9 Гц.
Рассчитанные спектры мощности для представленной на Рис. 2Б и 2В ЭКоГ изображены на рисунках 3Б и 3В. Можно отметить, что в течение 1-2 мин после введения соединения РУ-1203 доминирующими частотами являются 1, 6, 9 и 12 Гц (Рис. 3Б). После 5 мин наблюдений ритмическая активность, почти восстановилась до исходного уровня, где ведущими частотами являются 1 и 9 Гц (Рис. 3В).
На рис. 4 показана фоновая фокальная активность сразу после введения соединения РУ-1205 (3,5 мкМ раствор). Микроаппликация раствора осуществлялась в непосредственной близости от К1 и К2. Обозначения те же.
Микроаппликация вещества РУ-1205 вызывала статистически значимое подавление амплитудных характеристик фокальной фоновой ритмики и изменение частотных параметров с ведущей частотой - 5 Гц.
Спустя 3 мин после введения соединения РУ-1205 в соответствии с рис. 5 можно отметить появление медленных (около 1 Гц) осцилляции на К1 и К2 (опытная нейронная колонка) и более высокочастотной ритмики на К3 (контрольная нейронная колонка, находящаяся на удалении 1000 мкм от опытной). После 5 мин наблюдений можно отметить тенденцию к восстановлению фокальной фоновой ритмики до исходного уровня (рис. 6).
ПРОТИВОЭПИЛЕПТИЧЕСКАЯ АКТИВНОСТЬ СОЕДИНЕНИЙ РУ-1203 И РУ-1205 НА МОДЕЛИ ЭЛЕКТРОСТИМУЛЯЦИИ ПОВЕРХНОСТИ МОЗГА
На рис. 7 показано антиэпилептическое действие соединения РУ-1203, выявленное в условиях предварительной ритмичной (10 Гц) стимуляции поверхности мозга (в течение 10 с) электрическим током (12 В). А - Электрокортикограмма отдельной нейронной колонки до и после электрической стимуляции перед микроаппликацией соединения РУ-1203. Б - до и после предварительной электрической стимуляции спустя минуту с момента введения соединения РУ-1203. В - до и после предварительной электрической стимуляции спустя 5 минут с момента введения РУ-1203. С* - Электрокортикограмма выделенного участка и рассчитанные спектры мощности. Обозначения: К1 и К2 верхние (400 мкм) и нижние (1500 мкм) слои, соответственно, нейронной колонки, в которую производилась микроаппликация 23,7 мкМ раствора соединения РУ-1203. Стрелками обозначено время стимуляции.
На рис. 7 видно, что перед электрической стимуляцией наблюдается формирование альфа-поподобной фоновой ритмики, а после электрической стимуляции в верхних и нижних слоях корковой колонки развиваются высокоамплитудные эпиразряды. Длительность вызванной эпиактивности составляет 16 с. Далее происходит постепенное восстановление фокальной активности, но с наличием тета-подобной ритмики, соответствующей стрессовому состоянию мозга крыс.
Соединение РУ-1203 статистически значимо устраняет эпилептиформные разряды, вызванные электрической стимуляцией (рисунок 7Б). На этом рисунке видно, что в течение 1-2 минут наблюдения после локального введения вещества в той же модели формирования эпилептиформного очага развитие эпиактивности не наблюдается.
Дальнейшие наблюдения (5-6 минут после введения соединения РУ-1203) показывают, что сразу после электрической стимуляции в отдельной нейронной колонке соматосенсорной коры не только не появляются эпилептиформные разряды, но устойчиво развивается альфа-подобная ритмическая активность, соответствующая спокойному или дремотному состоянию животного (рисунок 7В). Для более весомой достоверности этого факта на рисунке 8В рамкой выделен фрагмент (С*) альфа-веретена, а на рисунке 8С* приведены развернутый вариант этого отрезка ЭКоГ с амплитудными и временными отметками и его гистограмма спектра мощности. Важно отметить, что на гистограмме спектра мощности ведущей частотой является 9 Гц.
На рис. 8 показано влияние соединения РУ-1205 на развитие эпилептиформной активности, вызванной электрической стимуляцией поверхности мозга. А - до микроаппликации испытуемого вещества. Б - сразу после микроаппликации соединения РУ-1205 (0,457 мМ раствор) в нейронные колонки соматосенсорной коры крыс. В - 6 минут после внутрикорковой микроаппликации вещества. Г - 12 минут после локального введения соединения РУ-1205. Обозначения: К1 - верхние (500 мкм) и К2 - нижние (1300 мкм) слои соматосенсорной коры крыс.
Представлены данные, свидетельствующие о антиэпилептиформных свойствах соединения РУ-1205, которые были выявлены на модели эпилептиформной активности, вызванной электрической стимуляцией поверхности мозга животного.
На рисунке видно, что электрическая стимуляция приводит к длительной (более 40 с) эпилептиформной активности, как в верхних, так и нижних корковых слоях. Важно отметить, что на завершающей стадии эпилептиформной активности можно наблюдать более высокоамплитудные, но с меньшей частотой осцилляции фокального потенциала.
Микроаппликация раствора соединения РУ-1205 полностью блокирует развитие эпилептиформной активности после электрической стимуляции поверхности мозга, что говорит об антиэпилептических свойствах соединения (рисунок 8Б). Аналогичные результаты были получены у 10 животных, при этом средние величины статистически значимо отличаются от контрольных показателей (p<0,05).
Продолжительность действия соединения РУ-1205 составляет 5 минут с последующим угасанием эффекта (рисунок 8В и 8Г). С увеличением времени после локальной микроаппликации испытуемого вещества длительность эпилептиформной активности, вызванной электрической стимуляцией, растет (около 10 с на 6 минуте после введения вещества (рисунок 8В) и около 20 с на 12 минуте (рисунок 8Г). Важно отметить, что эпилептиформная активность, развивающаяся в ответ на электрическую стимуляцию спустя длительное время после введения соединения РУ-1205, имеет аплитудно-частотные параметры осцилляции фокального потенциала, аналогичные завершающей стадии эпиподобной активности вызванной до применения этого вещества.
ЗАКЛЮЧЕНИЕ.
На модели коразоловых судорог соединение РУ-1203 превосходило вальпроат натрия по активности в 10 раз и по величине терапевтического индекса в 7 раз. Соединение РУ-1205 превосходило вальпроат натрия по активности и индексу относительной безопасности в 12 и 8,5 раз соответственно.
В ходе изучения влияния веществ на фокальную фоновую ритмику микроаппликация раствора соединения РУ-1203 (23,7 мкМ) лишь на непродолжительное время (1-2 мин) в незначительной степени изменяла частотные характеристики фоновой ритмики с полным ее восстановлением после 5 минут наблюдений. Соединение РУ-1205 показало выраженное подавляющее действие при низкой концентрации раствора (3,5 мкМ). Действие соединения РУ-1205 носило обратимый характер: после несения раствора соединения РУ-1205 на поверхность мозга восстановление нормальной фоновой активности регистрировалось уже через 5 минут наблюдения.
Соединения РУ-1203 и РУ-1205 также эффективно подавляли электроиндуцированную эпилептическую активность и восстанавливали нормальный ритмогенез нейронов.
Таким образом, РУ-1203 и РУ-1205 превосходят вальпроат натрия по противосудорожной активности и по величине терапевтического индекса, а также подавляют электроиндуцированную эпилептическую активность и восстанавливают нормальный ритмогенез нейронов.
1. Применение дигидрохлорида 9-диалкиламиноэтил-2-(4-фторфенил)имидазо[1,2-а]-бензимидазола общей формулы где a) NR2 = пирролидино;б) NR2 = морфолино,в качестве соединения, обладающего противосудорожной активностью.
2. Применение по п. 1 для изготовления противосудорожного средства.