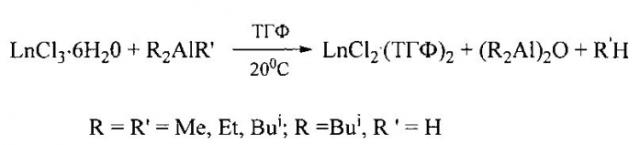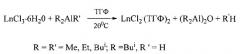Способ получения люминесцирующих растворимых комплексов двухвалентных лантанидов lncl2∙(тгф)2 (ln=eu, yb, sm)
Иллюстрации
Показать всеИзобретение относится к люминесцирующим растворимым соединениям двухвалентных лантанидов, находящих широкое применение в различных отраслях промышленности и науки. Описывается способ получения люминесцирующих растворимых комплексов двухвалентных лантанидов LnCl2·(ТГФ)2, где Ln = Eu, Yb, Sm. Способ состоит во взаимодействии кристаллогидрата трихлорида лантанида LnCl3·6Н2О, где Ln = Eu, Yb, Sm, с алюмоорганическим соединением (АОС) формулы R2ALR′, где R = R′ = Me, Et, изо-Bu; R = изо-Bu, R′ = H. Реакцию проводят при мольном отношении LnCl3·6Н2О/АОС = 1/40 в атмосфере аргона при 20-25°C и атмосферном давлении в среде апротонного растворителя - тетрагидрофурана. Выделение LnCl2·(ТГФ)2 ведут удалением растворителя вакуумной отгонкой и осаждением твердого комплекса добавлением гексана или толуола. Предложенный способ позволяет упростить технологический процесс за счет проведения его одностадийным методом в мягких условиях с использованием доступных кристаллогидратов трихлорида лантанидов по сравнению с труднодоступным металлическим Ln или безводным LnCl3. 1 табл., 3 пр.
Реферат
Предлагаемое изобретение относится к области химии, в частности к способам получения новых люминесцирующих растворимых соединений двухвалентных лантанидов LnCl2·(TГФ)2 (Ln=Eu, Yb, Sm). Эти три лантанида являются наиболее легко восстанавливаемыми представителями 4f-элементов: окислительно-восстановительный потенциал Eu3+/Eu2+=0.35 В, Yb3+/Yb2+=1.15 В и Sm3+/Sm2+=1.55 В относительно стандартного водородного электрода [1. L.J. Nugent, R.D. Baybarz, J.L. Burnett, J. L. Ryan, Electron-transfer and f-d absorption bands of some lanthanide and actinide complexes and the standard (II-III) oxidation potential for each member of the lanthanide and actinide series, J. Phys. Chem., 1973, 77 (12), pp. 1528-1539].
Широкое применение соединений двухвалентных лантанидов обусловлено главным образом их способностью к яркой люминесценции при возбуждении УФ-светом. На основе соединений Ln2+ разработаны новые источники света, люминесцирующие краски, оптические отбеливатели бумаги и т.д. [2. Патент РФ №2192444 от 10.11.2002; патент РФ №2329287 от 20.07.2008; патент РФ №2251761 от 19.11.2001; патент РФ №2276702 от 20.05.2006; В.W. Grouse, G.H. Snow, Fluorescent whitening agents in the paper industry, Tappi, 1981, v.64 (7), p.87]. Кроме того, соединения двухвалентных лантанидов находят практическое применение в качестве одноэлектронных восстановителей и катализаторов, в том числе реакций полимеризации диенов [3. H.В. Kagan, J.L. Namy, Lanthanides in organic synthesis, Tetrahedron, 1986, 42, pp.6583-6614; G.A. Molander, J. A.C. Romero, Lanthanocene catalysts in selective organic synthesis, Chem. Rev., 2002, 102, pp.2161-2185; W.J. Evans, D.G. Giarikos, N.Т. Allen, Polymerization of Isoprene by a Single Component Lanthanide Catalyst Precursor, Macromolecules, 2003, 36, pp.4256-4257].
Среди известных способов получения растворимых комплексов двухвалентных лантанидов можно выделить следующие. Известен способ [4. K. Rossmanith, E. Muckenhuber, Über die umsetzung von chloriden der seltenen erden mit lithiumborhydrid, 2. Mitt, Mh. Chem., Br., 1961, 92, H.3, pp.600-604) синтеза хлорида двухвалентного европия ЕuСl2 в среде тетрагидрофурана (ТГФ) в реакции безводного хлорида европия ЕuСl3 с боргидридом лития LiBH4.
EuCl3+LiBH4→EuCl2+LiCl+1/2В2Н6+1/2Н2
Важно отметить, что полученное таким образом соединение европия в ТГФ не растворяется и выпадает в виде осадка, состав которого был установлен только с помощью элементного анализа. В тоже время при добавлении двукратного избытка LiBH4 авторы [4] получили растворимые комплексы европия и иттербия, которым на основании элементного анализа приписали следующий состав: LnCl2·(BH4)2(Ln=Eu, Yb).
LnCl3+2LiBH4→LnCl2·(BH4)2+LiCl
Стоит отметить, что состав полученных комплексов был определен только с помощью элементного анализа, и других доказательств в пользу такого состава комплексов и валентного состояния лантанидов в этих комплексах авторы не приводят.
Главным недостатком данного способа является необходимость применения безводных трихлоридов европия (получение которых является энергозатратным и длительным процессом), а также протекание побочных реакций с образованием боргидридных комплексов состава LnCl2·(BH4)2. Кроме того, как отмечается в публикации Каменской [5. А.Н. Каменская. Низшее состояние окисления лантанидов в растворах, Ж. неорг. химии, 1984, т.29, с.439-449] в данной работе степень окисления 2+лантанидам была приписана на основании только элементного анализа, т.е. без спектральных доказательств.
Известен также способ [6. K. Rossmanith, Herstellung der klassischen Seltenerd(II)-chloride in Lösung, Monatshefte fur Chemie, 1979, v.110, pp.109-114] получения комплексов LnCl2·(THF)n (Ln=Eu, Yb, Sm; n=1, 3) в реакции безводных трихлоридов лантанидов LnСl3 с металлическим литием в присутствии нафталина в среде ТГФ. Реакцию проводили при комнатной температуре в течение 3.5 (Еu), 20 (Yb) и 6 (Sm) часов. Выход комплексов LnCl2·(THF)n составил 89.6%, 73.3% и 92% для Еu (n=1), Yb (n=1) и Sm (n=3) соответственно. Состав полученных соединений был установлен методом элементного анализа.
К недостаткам данного способа относится необходимость предварительного синтеза безводных трихлоридов лантанидов LnCl3, (трудоемкий, энергозатратный процесс) и длительность процесса, а также необходимость использования дополнительного реагента (нафталина).
Известен также способ [7. Р. Girard, J.L. Namy, H.В. Kagan, Divalent lanthanide derivatives in organic synthesis - I. Mild preparation of SmI2 and YbI2 and their use as reducing or coupling agents, J. Am. Chem. Soc., 1980, v.102, p.2693] получения Lnl2·(THF)n (Ln=Yb, Sm) при взаимодействии металлических лантанидов с 1,2-дииодэтаном C2H2I2 в среде ТГФ. В инертной атмосфере (азот) реакция протекает при комнатной температуре (20°С) за 24 ч. Образование комплексов LnI2·(THF)n подтверждалось методом спектрофотометрии. Так, спектр поглощения полученного в работе SmI2 к растворе ТГФ содержит характерные для Sm2+ максимумы при 250, 300, 557 и 618 им, а спектр поглощения YbI2 в ТГФ - максимумы Yb2+ при 250, 300, 343 и 383 им. Кроме того, полученные данным способом комплексы LnI2·(THF)n (Ln=Eu, Yb, Sm) обладают регистрируемой люминесценцией в растворе ТГФ с максимумами излучения при: 442 нм (λвозб=313,431 нм) для Eu, 500, 515 нм (λвозб=324, 435 нм) для Yb и 769 нм (λвозб=458, 495, 736 нм) в случае Sm [8. Y. Okaue, T. Isobe, Characterizations of Divalent Lanthanoid Iodides in Tetrahydrofuran by UV-Vis, Fluorescence and ESR Spectroscopy, Inorg. Chim. Acta, 1988, v.144, p.143]. Спектры поглощения растворов LnI2·(THF)n в ТГФ, приведенные в работе [8], содержат характерные для двухвалентных лантанидов максимумы при 341 нм для Eu, 342, 390 нм для Yb, 284, 349, 417, 553, 616 нм для Sm.
Отметим, что полученные таким образом растворимые комплексы LnI2·(THF)n (Ln=Eu, Yb, Sm) в ТГФ устойчивы только в присутствии металлического лантанида Ln. Другим недостатком данного способа является большая длительность процесса восстановления лантанидов до двухвалентного состояния (24 часа).
Известен способ получения комплексов трудно восстанавливаемых лантанидов LnI2·(L)n (где n=3,5; Ln=Nd, Dy; L=THF, DME) [9. M.N. Bochkarev, A.A. Fagin, A New Route to Neodymium(II) and Dysprosium(II) Iodides, Chem. Eur. J., 1999, v.5, p.2990]. Данные комплексы были получены при взаимодействии металлического лантанида Ln с кристаллическим йодом I2 при нагревании (около 200°С) в вакууме. В результате реакции были полученные твердые LnI2, которые затем растворяли в ТГФ или диметоксиэтане (ДМЭ) с образованием комплексов состава LnI2·(L)n (n==3, 5; Ln=Nd, Dy; L=THF, DME). Состав полученных комплексов был установлен методом элементного анализа и ИК-спектроскопии. Образование LnI2·(L)n(Ln=Nd, Dy) подтверждалось появлением характерных максимумов поглощения и магнитных моментов Ln2+: 2.7 µB и 2.8 µВ для комплексов Nd2+ с ТГФ и ДМЭ соответственно, 10.6 µВ, 10.7 µВ для комплексов Dy2+ с ТГФ, ДМЭ. Выход комплексов LnI2·(L)n (Ln=Nd, Dy; L=THF, DME) составил от 49 до 100%.
К недостаткам описанного способа можно отнести огне- и взрывоопасность реакции металлического лантанида с кристаллическим йодом и ее высокий температурный режим (200°С).
Вышеуказанным способом также были получены дииодиды других лантанидов LnI2 (Ln=Eu, Yb, Sm, Tm) [10. Патент РФ №2245302 от 27.01.2005]. Эти комплексы были получены в реакции металлического лантанида с кристаллическим йодом при нагревании до 600-800°С в вакууме.
Недостатками данного способа являются высокий температурный режим (600-800°С) и взрывоопасность химической реакции.
В то же время в литературе известны способы получения растворимых комплексов лантанидов в степени окисления 3+, основанные на взаимодействии соединений трехвалентных лантанидов с АОС. В частности, известен способ получения растворимых ацетилацетанатов лантанидов Ln(асас)3 (Ln=Tb, Nd, Но, Lu) в толуоле под действием Et3Al на кристаллогидраты En(асас)3·H2O [11. Р.Г. Булгаков, С.П. Кулешов, Р.Р. Вафин, А.Г. Ибрагимов, У.М. Джемилев. Взаимодействие ацетилацетанатов лантанидов с триэтилалюминием. Кинетика и катализ, 2008, т.49, №2, с.315-320]. Растворимые комплексы состава LnCl3·(ТВР)3 были получены при взаимодействии АОС (Bui 3Al, Et3Al, Et2AlCl, EtAlCl2) с LnCl3·6Н2О (Ln=Tb. Dy, Nd) в среде трибутилфосфата (ТВР) [12. R.G. Bulgakov, S.P. Kuleshov, A.N. Zuzlov, I.R. Mullagaleev, L.М. Khalilov, U.М. Dzhemilev, Dehydration of LnCl3·6Н2О (Ln=Tb, Nd, Dy) in the reaction with Bui 3Al, Еt3Аl, Et3AlCl, EtAlCl2 and formation of the complexes LnCl3·3(BuO)3РО, J. of Organometallic Chemistry, 2001, 636, p.56-62]. Отметим, что ион лантанида в полученных данным способом растворимых комплексах находится в трехвалентном состоянии. Это подтверждено наличием характерных максимумов Ln3+ в спектрах ФЛ.
В литературе также известны данные о восстановлении Eu(III) до Eu(II) под действием алюмоорганических соединений (АОС) - Bui 3Al, Et3Al [13. Р.Г. Булгаков, С.П. Кулешов, А.Р. Махмутов, 3. С. Кинзябаева, Яркая голубая фотолюминесценция Eu11 комплекса EuCl2·0.5H2O·0.05(Bui 2Al)2O, Изв. АН. Сер.хим., 2007, 3, с.549-550; Р.Г. Булгаков, С.П. Кулешов, А.Р. Махмутов. Влияние кристаллизационной воды и природа алюминийалкила на восстановление Eu3+ до Eu2+ при взаимодействии EuCl3·6Н2О с Bui 3A1 и Et3Al, Ж. прикл. химии, 2009, т.82, с.1248-1250]. Например, при взаимодействии кристаллогидрата EuCl3·6H2O с Bui 3Al в среде толуола при комнатной температуре и атмосферном давлении был получен ярко люминесцирующий комплекс двухвалентного европия EuCl2·0.5Н2О·0.05Bui 4Al2O. Состав полученного комплекса был установлен с применением методов элементного анализа, комплексонометрического титрования и метода Фольгарда. Двухвалентное состояние европия было доказано по спектрам поглощения и ФЛ, которые содержат максимумы Eu2+, существенно отличающиеся по положению от максимумов Eu3+ в исходном EuCl3·6Н2О.
Существенным недостатком данного способа является нерастворимость полученного комплекса EuCl2·0.5Н2О·0.05Bui 4Al2O в большинстве органических растворителей, что затрудняет их дальнейшее изучение и применение.
Получение растворимых соединений двухвалентных лантанидов LnCl2·(ТГФ)2 восстановлением кристаллогидратов трихлоридов лантанидов LnCl3·6Н2О алюминийорганическими соединениями (АОС) не известно.
Предлагается новый способ получения растворимых соединений двухвалентных лантанидов LnCl2(ТГФ)2.
Сущность способа заключается в реакции кристаллогидратов (КГ) трихлоридов лантанидов LnCl3·6Н2О (Ln=Eu, Yb, Sm) с АОС общей формулы R2AlR′ (где R=R′=Me, Et, Bui; R=Bui, R′=H) при мольном отношении LnCl3·6Н2О/AOC=1/40. Реакцию проводят в атмосфере аргона при атмосферном давлении и комнатной температуре (20-25°C), в среде апротонного координирующего растворителя - тетрагидрофурана (ТГФ). Реакция восстановления Ln3+ до Ln2+ протекает согласно схеме 1.
Схема 1
Отметим, что исходные КГ в ТГФ не растворяются, но при добавлении АОС происходит быстрое (<1 мин) исчезновение твердой фазы КГ с образованием гомогенного раствора. Химическое взаимодействие КГ с АОС начинается с удаления молекул кристаллизационной воды из координационной сферы Ln3+ в результате атаки АОС с образованием алюмоксана, газообразного углеводорода RH (и водорода, в случае применения в качестве АОС Bui 2AlH). Полное удаление кристаллизационной воды контролировали волюмометрическим методом. Далее избыток АОС восстанавливает лантанид с образованием комплекса LnCl2·(ТГФ)2. Время реакции восстановления зависит от природы лантанида и молярного отношении Ln/AOC. Выделение LnCl2·(ТГФ)2 осуществляют путем удаления растворителя вакуумной отгонкой и осаждением твердых комплексов добавками гексана или толуола.
Существенные отличия предлагаемого способа
В предлагаемом способе в качестве исходных соединений лантанидов используются доступные и относительно дешевые кристаллогидраты солей лантанидов LnCl3·6Н2О(Ln=Eu, Yb, Sm), а продуктами реакции являются растворимые соединения двухвалентных лантанидов LnCl2·(ТГФ)2, обладающие хорошо регистрируемой люминесценцией при комнатной температуре. Взаимодействие кристаллогидратов LnCl3·6Н2О с R3Al (Bui 2AlH) происходит при мольном отношении LnCl3·6Н2О/R3Al(Bui 2AlH)=1/40 в среде ТГФ. В известных способах в качестве исходных соединений лантанидов применяют безводные LnCl3, восстановление которых дает LnCl2·(ТГФ)n (n=1,3).
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с количественным выходом растворимые люминесцирующие соединения двухвалентных лантанидов LnCl2·(ТГФ)2 (Ln = Eu, Yb, Sm), синтез которых в литературе не описан.
2. Способ позволяет в качестве исходных соединений лантанидов использовать кристаллогидраты LnCl3·6Н2О, доступные и дешевые по сравнению с металлическими Ln и безводными LnCl3. Кроме того, исключается необходимость предварительного обезвоживания КГ и протекания высокотермической, взрывоопасной реакции между лантанидом и молекулярным иодом.
3. Способ позволяет проводить синтез в мягких условиях (20-25°C, атмосферное давление).
4. Способ позволяет легко отделять целевой продукт LnCl2·(ТГФ)2 от реакционного раствора, содержащего другие растворимые продукты реакции: R4Al2O, R2AlCl, RH и R-R, осаждением твердого комплекса LnCl2·(ТГФ)2 и последующей его отмывкой неполярными растворителями (гексан, толуол).
Способ поясняется следующими примерами:
ПРИМЕР 1. В сосуд Шленка объемом 10 мл, установленный на магнитную мешалку, в атмосфере аргона помещают кристаллогидрат EuCl3·6Н2О (0.02 ммоль, 7.30 мг), 2 мл свежеперегнанного ТГФ кетильной очистки, включают перемешивание и шприцем добавляют 0.8 ммоль Bui 2AlH. Наблюдается бурное газовыделение (BuiH и Н2) и быстрое, практически мгновенное растворение и окрашивание гомогенного раствора в соломенно-желтый цвет. Восстановление Eu(III) до Eu(II) на 95% протекает примерно за 7 минут. Для выделения комплекса Eu(II) в твердом виде из реакционного раствора сначала удаляли растворитель (ТГФ) вакуумной отгонкой (20-25°C, 5-6 Торр). Затем к жидкому остатку добавляли ~3 мл гексана, образующийся при этом осадок серовато-белого цвета промывали толуолом или гексаном (5×2 мл) до полного удаления избыточного Bui 2AlH и продуктов его превращения. Присутствие ионов Al3+ в маточном растворе контролировали по следующей методике. Суммарное содержание ионов лантанида и алюминия определяли обратным комплексонометрическим титрованием; затем содержание лантанида устанавливали прямым комплексонометрическим титрованием. После этого по разнице вычисляли содержание Al3+. Полученный после отмывки твердый остаток сушили в вакууме (не более 40°C, 1 Торр). В результате получен порошок вещества светло-желтого цвета, состав которого согласно данным элементного анализа соответствует брутто-формуле EuCl·C8H16O. Выход EuCl2·(ТГФ)2 составляет ~45% (3.85 мг). Элементный состав (С, Н, О) комплекса EuCl2·(ТГФ)2 определяли на элементном анализаторе фирмы «Carlo Erba». Содержание европия определяли прямым комплексонометрическим титрованием, а ионов Cl- - методом Шенингера согласно стандартным методикам. Спектры ФЛ растворов, полученных после реакции LnCl3·6Н2О с Bui 2AlH, а также твердых комплексов LnCl2·(THF)2 регистрировали в кварцевых герметичных кюветах (1=1 см) на спектрофлуориметре FluoroLog-3 Horiba Jobin Yvon (model FL-3-22). УФ-видимые спектры поглощения реакционных растворов регистрировали в герметичных кварцевых кюветах (1=1 см) на спектрофотометре Perkin Elmer Lambda 750, а ИК-спектры твердых (в таблетках KBr) и жидких (в кюветах из стекла KBr) образцов измеряли на приборе Bruker Vertex 70V. Спектры ЯМР 1Н и 13С измеряли на спектрометре Bruker Avance-400 (рабочая частота 400.13 и 100.62 мГц). В качестве растворителя использовали смесь C7D8 и С7Н8 (1:5 по объему), а внутреннего стандарта - Me4Si.
ПРИМЕР 2. В сосуд Шленка объемом 10 мл, установленный на магнитную мешалку, в атмосфере аргона помещают кристаллогидрат EuCl3·6Н2О (0.02 ммоль, 7.30 мг), 2 мл свежеперегнанного ТГФ кетильной очистки, включают перемешивание и шприцем добавляют 0.8 ммоль Bui 3Al. Наблюдается бурное газовыделение (BuiH) и быстрое растворение. Полное восстановление Eu3+ до Eu2+ происходит по истечении 1 часа от начала реакции, хотя раствор приобретает характерную желтую окраску уже через 10-15 минут. Для выделения комплекса Eu(II) в твердом виде из реакционного раствора проводят операции, описанные в примере 1. Состав полученного светло-желтого порошкообразного вещества был также установлен с применением методов элементного анализа (содержание С, Н, О), прямого (содержание иона Eu2+) и обратного комплексонометрического титрования (содержание иона Al3+), метода Шенингера (содержание Cl-). Согласно данным элементного анализа осадок соответствует брутто-формуле EuCl2·С8Н16О. Выход EuCl2·(ТГФ)2 составляет 43% (3.68 мг). Координирование молекул ТГФ к иону Eu2+ в комплексе EuCl2·(THF)2 было установлено методами ИК- и ЯМР-спектроскопии.
Другие примеры, подтверждающие способ получения растворимых соединений двухвалентных лантанидов, приведены в таблице.
Полученные комплексы LnCl2·(ТГФ)2 (Ln = Eu, Yb, Sm) имеют следующие физико-химические характеристики:
EuCl2·(ТГФ)2. Твердое вещество, светло-желтого цвета. Найдено (%): Eu - 41.42; Н - 3.6; О - 15.18; С - 21.3; Cl - 19.05. C8H16O2EuCl2. Вычислено (%): Eu - 40.19; Н - 4.36; О - 13.94; С - 22.16; Cl - 19.35. Спектр ФЛ: λmax=465 нм (λexc=280 нм). УФ-спектр (0.65 М HCl) λmax /нм: 251, 333. ИК-спектр (KBr), ν/см-1: 860 сл. (С-О, ТГФ); 1033 сл. (С-О, ТГФ); 603 ср. (Eu-Cl). Спектр ЯМР ′Н (толуол-d8, δ, м.д., J/Гц): 2.05 (м. 4Н, СН2); 3.51(м. 4Н, O-СН2). Спектр ЯМР 13С (толуол-d8, δ, м.д., J/Гц): 25.75 (β-СН2, ТГФ); 67.86 (α-СН2, ТГФ).
YbCl2·(ТГФ)2. Твердое вещество, белого цвета. Найдено, %: Yb - 44.28; Н - 4.77; О - 13.01; С - 23,36; Cl - 14,65. для C8H16O2YbCl2. Вычислено, %: Yb - 44.6; Н - 4.12; О - 8,25; С - 24,7; Cl - 18,33. Спектр ФЛ: λmax=437 нм (λехс = 280 нм). УФ-спектр (0.65 М HCl) λmax /нм: 379 нм. ИК-спектр (KBr), ν/см-1: 860 сл. (С-О, ТГФ); 1033 сл. (С-О, ТГФ); 606 ср. (Yb-Cl). Спектр ЯМР 1Н (толуол-d8, δ, м.д., J/Гц): 1.34 (м. 4Н, СН2); 3.20 (м. 4Н, O-СН2). Спектр ЯМР 13С (толуол-d8, δ, м.д., J/Гц): 25.07 (β-CH2, ТГФ); 67.11 (α-СН2, ТГФ).
SmCl2·(ТГФ)2. Твердое вещество, зеленого цвета. Найдено, %: Sm - 40.32; Н - 4.66; О - 9.50; С - 26,46; Cl - 19,06 для C8H16O2SmCl2. Вычислено, %: Sm - 41.98; Н - 4.98; О - 8,77; С - 26,3; Cl - 19,45. Спектр ФЛ: λmax=759 нм (λехс=488 нм). УФ-спектр (0.65 М HCl) λmax /нм: 350, 382, 414. ИК-спектр (KBr), ν/см-1: 872 сл. (С-О, ТГФ); 1030 сл. (С-О, ТГФ); 684 ср. (Sm-Cl). Спектр ЯМР 1Н (толуол-d8, δ, м.д., J/Гц): 1.34 (м. 4Н, СН2); 3.19 (м. 4Н, O-СН2). Спектр ЯМР 13С (толуол-d8, δ, м.д., J/Гц): 25.00 (β-CH2, ТГФ); 66.97 (α-СН2, ТГФ).
Способ получения люминесцирующих растворимых комплексов двухвалентных лантанидов LnCl2·(ТГФ)2, где Ln = Eu, Yb, Sm, взаимодействием кристаллогидратов трихлоридов лантанидов LnCl3·6Н2О с алюмоорганическими соединениями АОС, характеризующийся тем, что в качестве трихлоридов лантанидов используют кристаллогидраты LnCl3·6Н2О, где Ln = Eu, Yb, Sm, а в качестве АОС - соединения общей формулы R2ALR′, где R = R′ = Me, Et, изо-Bu; R = изо-Bu, R′ = H, реакцию проводят при мольном отношении компонентов LnCl3·6Н2О/АОС = 1/40 в атмосфере аргона при комнатной температуре 20-25°C и атмосферном давлении, в среде апротонного растворителя - тетрагидрофурана, с последующим выделением LnCl2·(ТГФ)2 путем удаления растворителя вакуумной отгонкой и осаждением твердых комплексов добавками гексана или толуола.