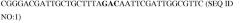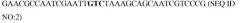Композиции и способы, включающие варианты субтилизина
Иллюстрации
Показать всеИзобретение относится к биотехнологии и представляет собой вариант субтилизина для применения в очистке, представляющий собой последовательность аминокислот, указанную в SEQ ID NO: 5. Изобретение относится также к чистящей композиции, включающей эффективное количество варианта субтилизина, к способу чистки, включающему обеспечение предмета для чистки, и композиции, включающей вариант субтилизина, указанный в SEQ ID NO: 5, и приведение в контакт указанного предмета и указанной композиции. Изобретение позволяет получить эффективный вариант субтилизина с высокой моющей способностью. 3 н. и 11 з.п. ф-лы, 19 табл., 14 пр.
Реферат
По настоящей заявке испрашивается приоритет временной заявки на патент США серийный номер 61/113552, поданной 11 ноября 2008 г., включенной в настоящее описание путем ссылки.
Область изобретения
Настоящее изобретение относится к варианту субтилизина, который является особенно подходящим для применения в очистке. В частности, настоящее изобретение относится к варианту субтилизина Bacillus sp. и чистящим композициям, включающим этот вариант.
Предпосылки создания изобретения
Как правило, обычные домашние и промышленные композиции для мытья посуды основаны на комбинации высокощелочного моющего средства и хлорного отбеливателя для чистки и дезинфекции посуды. Обычно такие системы хорошо работают на отбеливаемых пятнах. Однако удаление загрязнений, содержащих белки, которые часто присутствуют на посуде в домах, больницах, кафетериях и системе предприятий общественного питания, является проблематичным. Кроме того, высокощелочные и хлорсодержащие композиции потребителем не рассматриваются как безопасные для окружающей среды.
Предпринимались различные попытки получения композиций для мытья посуды, которые являлись бы эффективными для удаления белковых загрязнений. Эти композиции обычно включают протеазы, активные в щелочных условиях (например, рН по меньшей мере 9,5). Однако существенный недостаток таких композиций заключается в трудности их получения в виде жидкости или геля, обычно предпочитаемых покупателями средств для мытья посуды. Кроме того, щелочные моющие композиции часто рассматриваются как раздражающие.
Предпринимались попытки получения композиций для мытья посуды с низким рН (например, рН менее 9,5). Эти композиции являются более безопасными, более безвредные для окружающей среды и могут быть введены в состав рецептур гелей и жидкостей. Однако было доказано, что имеющиеся в настоящее время композиции для мытья посуды с низким значением рН являются очень неэффективными для удаления белковых загрязнений, даже при высоких концентрациях ферментов (например, протеаз).
Таким образом, в данной области сохраняется необходимость в композициях для мытья посуды, которые эффективно удаляют с посуды белковые загрязнения. Кроме того, сохраняется необходимость в композициях для мытья посуды, которые более безвредны для окружающей среды и для потребителя и существуют в том виде, который легко используется и выгоден по стоимости.
Аналогично, сохраняется необходимость в чистящих композициях для тканей, которые были бы эффективными для удаления с тканей белковых загрязнений.
Краткое изложение сущности изобретения
Настоящее изобретение относится к варианту субтилизина Bacillus sp., который является особенно подходящим для чистящих композиций. Кроме того, настоящее изобретение относится к чистящим композициях, включающим этот вариант субтилизина.
Настоящее изобретение относится к варианту субтилизина, включающему последовательность аминокислот, указанную в SEQ ID NO:5. В некоторых предпочтительных вариантах осуществления настоящее изобретение относится к композициям, включающим вариант субтилизина, имеющий последовательность аминокислот, указанную в SEQ ID NO:5. В некоторых особенно предпочтительных вариантах осуществления композиция представляет собой чистящую композицию. В некоторых предпочтительных альтернативных вариантах осуществления чистящая композиция представляет собой стиральный порошок, тогда как в некоторых других предпочтительных вариантах осуществления чистящая композиция представляет собой средство для мытья посуды. В некоторых вариантах осуществления средство для мытья посуды представляет собой моющее средство для автоматических посудомоечных машин, тогда как в других вариантах осуществления они представляют собой средства для мытья посуды вручную. В некоторых предпочтительных вариантах осуществления чистящие композиции представляют собой жидкие моющие средства, тогда как в некоторых других вариантах осуществления чистящие композиции представляют собой моющие средства в виде геля, таблетки, порошка или гранул. В некоторых вариантах осуществления чистящие композиции не содержат фосфата, тогда как в некоторых других вариантах осуществления чистящие композиции содержат фосфат. В некоторых предпочтительных вариантах осуществления чистящие композиции дополнительно включают по меньшей мере один отбеливающий агент. Еще в некоторых дополнительных предпочтительных вариантах осуществления чистящие композиции дополнительно включают по меньшей мере один дополнительный фермент. В некоторых вариантах осуществления дополнительный фермент выбирают из гемицеллюлаз, целлюлаз, пероксидаз, протеаз, металлопротеаз, ксиланаз, липаз, фосфолипаз, эстераз, пергидролаз, кутиназ, пектиназ, пектатлиаз, маннаназ, кератиназ, редуктаз, оксидаз, фенолоксилаз, липоксигеназ, лигниназ, паллуланаз, танназ, пентосаназ, маланаз, β-глюканаз, арабиносидаз, гуалуронидазы, хондроитиназы, лакказы и амилаз или их смесей.
Настоящее изобретение также относится к способам чистки, включающим обеспечение предмета для чистки и композиции, включающей вариант субтилизина, указанный в SEQ ID NO:5, и приведение в контакт указанного предмета и указанной композиции. В некоторых следующих вариантах осуществления способы дополнительно включают стадию споласкивания указанного предмета, предназначенного для чистки. В некоторых дополнительных вариантах осуществления предмет представляет собой посуду или изделие из ткани.
Описание изобретения
Настоящее изобретение относится к варианту субтилизина, который является особенно подходящим для применений в очистке. В частности, настоящее изобретение относится к варианту субтилизина Bacillus sp. и чистящим композициям, включающим этот вариант. Настоящее изобретение дополнительно относится к ферментативным композициям, обладающим сопоставимыми или улучшенными моющими характеристиками по сравнению с используемыми в настоящее время субтилизинпротеазами.
Если не указано иное, практическое осуществление настоящего изобретения включает обычные технологии, обычно используемые в молекулярной биологии, микробиологии, при очистке белков, в инжиниринге белков, секвенировании белков и ДНК, в области рекомбинантных ДНК и промышленного применения и разработки ферментов, все из которых известны специалисту в данной области.
Кроме того, приведенные в описании заголовки не являются ограничениями различных аспектов или вариантов осуществления изобретения, которые могут быть сделаны со ссылкой на описание в целом. Соответственно, термины, непосредственно определенные ниже, более полно определены при ссылке на описание в целом. Тем не менее, для облегчения понимания изобретения ниже приведены определения для ряда терминов.
Если не указано иное, все технические и научные термины, использованные в настоящем описании, имеют такие же значения, как обычно понимается обычным специалистом в данной области, к которой принадлежит изобретение. Хотя любые способы и материалы, аналогичные или эквивалентные здесь описанным, находят применение при практической реализации настоящего изобретения, в настоящем описании представлены предпочтительные способы и материалы. Соответственно, термины, непосредственно определенные ниже, более полно описаны путем ссылки на описание в целом. Также в настоящем описании термины, приведенные в единственном числе, включают отсылку на множественное число, если из контекста ясно не следует иное. Если не указано иное, нуклеиновые кислоты написаны слева направо в направлении от 5' к 3'; последовательности аминокислот написаны слева направо в направлении от амино к карбокси, соответственно. Следует понимать, что это изобретение не ограничивается описанными частными методологиями, протоколами и реагентами, поскольку они могут варьировать в зависимости от контекста, в котором они используются специалистом в данной области.
Подразумевается, что каждое максимальное числовое ограничение, приведенное в настоящем описании, включает каждый самый низкий числовой предел, как если бы такие более низкие числовые ограничения были ясно прописаны в настоящем описании. Каждое минимальное числовое ограничение, приведенное в настоящем описании, будет включать каждое более высокое числовое ограничение, как если бы такие более высокие числовые ограничения были ясно прописаны в настоящем описании. Каждый числовой диапазон, приведенный в настоящем описании, будет включать каждый более узкий числовой диапазон, который попадает в такой более широкий числовой диапазон, как если бы такие более узкие числовые диапазоны были ясно прописаны в настоящем описании.
В рамках изобретения термин «совместимый» означает, что вещества в чистящей композиции не уменьшают ферментативную активность протеазного фермента(ов), приведенного в настоящем описании, до той степени, что протеаза становится не эффективной, как это желательно при обычном использовании. Конкретные вещества чистящей композиции подробно проиллюстрированы далее в настоящем описании.
В рамках изобретения выражение «эффективное количество фермента» относится к количеству фермента, необходимому для достижения требуемой ферментативной активности в конкретном применении. Такие эффективные количества легко может оценить обычный специалист в данной области, и они основаны на множестве факторов, таких как конкретный использованный вариант фермента, применение чистящей композиции, конкретный состав чистящей композиции, и необходима ли жидкая или сухая (например, гранулированная) композиция и тому подобного.
В рамках изобретения выражение «обладающий улучшенными свойствами», использованное в сочетании со словами «вариант протеазы», относится к варианту протеазы с улучшенными эксплуатационными характеристиками и/или улучшенной стабильностью при сохраняющихся эксплуатационных характеристиках, по отношению к соответствующим протеазам дикого типа. В некоторых особо предпочтительных вариантах осуществления улучшенные свойства выбирают из группы, состоящей из улучшенных характеристик при мытье посуды и стирке и улучшенной стабильности, а также комбинации улучшенных характеристик при мытье посуды и стирке и улучшенной стабильности.
В рамках изобретения выражение «стабильность моющего средства» относится к стабильности композиций моющих средств. В некоторых вариантах осуществления, стабильность оценивают во время применения моющего средства, тогда как в других вариантах осуществления термин относится к стабильности композиции моющего средства во время хранения.
Термин «улучшенная стабильность» использован для указания лучшей стабильности варианта протеазы в композициях во время хранения и/или лучшей стабильности в мыльной пене. В предпочтительных вариантах осуществления вариант протеазы проявляет улучшенную стабильность при уходе за посудой и/или в стиральных порошках во время хранения и/или улучшенную стабильность в мыльной пене, которая включает стабильность против окислителей, секвенирующих агентов, к автолизу, поверхностно-активным веществам и высокой щелочности по сравнению с соответствующим ферментом дикого типа.
В рамках изобретения выражение «стабильность к протеолизу» относится к способности белка (например, фермента) выдерживать протеолиз. Не предполагается, что термин ограничен применением какой-либо конкретной протеазы для оценки стабильности белка.
В рамках изобретения выражение «окислительная стабильность» относится к стабильности белка функционировать в окислительных условиях. В частности, термин относится к способности белка функционировать в присутствии различных концентраций Н2О2, перкислот и других окислителей. Стабильность в различных окислительных условиях может быть измерена с помощью либо стандартных способов, известных специалистам в данной области, и/или с помощью способов, описанных в настоящем изобретении. Существенное изменение в окислительной стабильности рассматривается как повышение или понижение (в большинстве вариантов осуществления, предпочтительным является повышение) по меньшей мере приблизительно на 5% или более периода уменьшения наполовину ферментативной активности по сравнению с ферментативной активностью, имеющейся в отсутствие соединений-окислителей.
В рамках изобретения термин «рН стабильность» относится к способности белка функционировать при определенном рН. Обычно большинство ферментов имеет ограниченный диапазон рН, при котором они будут функционировать. Помимо ферментов, которые функционируют при среднем диапазоне рН (приблизительно рН 7), существуют ферменты, которые способны работать в условиях очень высокого или очень низкого рН. Стабильность при различных рН может быть измерена с помощью либо стандартных способов, известных специалистам в данной области, и/или с помощью способов, описанных в настоящем изобретении. Существенное изменение в рН стабильности рассматривается как повышение или понижение (в большинстве вариантов осуществления, предпочтительным является повышение) по меньшей мере приблизительно на 5% или более периода уменьшения наполовину ферментативной активности по сравнению с ферментативной активностью, ферментов при оптимальном рН. Однако предполагается, что настоящее изобретение не будет ограничено ни каким-либо уровнем рН стабильности, ни диапазоном рН.
В рамках изобретения термин «термическая стабильность» и «термостабильность» относится к способности белка функционировать при определенной температуре. В общем, большинство ферментов имеет ограниченный диапазон температур, при котором они будут функционировать. Помимо ферментов, которые функционируют при среднем диапазоне температур (например, комнатная температура), существуют ферменты, которые способны работать при очень высоких или очень низких температурах. Термическая стабильность может быть измерена либо с помощью известных способов и/или с помощью способов, описанных в настоящем изобретении. Существенное изменение в термической стабильности рассматривается как повышение или понижение (в большинстве вариантов осуществления, предпочтительным является повышение) по меньшей мере приблизительно на 5% или более периода уменьшения наполовину ферментативной активности при воздействии данной температуры. Однако предполагается, что настоящее изобретение не будет ограничено ни каким-либо уровнем термической стабильности, ни температурным диапазоном.
В рамках изобретения термин «химическая стабильность» относится к стабильности белка (например, фермента) по отношению к химическим реагентам, которые могут неблагоприятно влиять на его активность. В некоторых вариантах осуществления, такие химически реагенты включают, но не ограничиваются указанным, перекись водорода, перкислоты, анионные детергенты, катионные детергенты, неионные детергенты, комплексообразующие соединения и т.д. Однако не предполагается, что настоящее изобретение отграничивается ни каким-либо определенным уровнем химической стабильности, ни диапазоном химической стабильности.
В рамках изобретения термины «очищенный» и «выделенный» относятся к удалению загрязняющих примесей из образца. Например, представляющий интерес фермент очищают путем удаления загрязняющих ферментов и других соединений из раствора или препарата, которые не являются рассматриваемым ферментом. В некоторых вариантах осуществления представляющие интерес рекомбинантные ферменты экспрессируются в бактериальных или грибковых клетках-хозяевах, и эти представляющие интерес рекомбинантные ферменты очищают путем удаления других составляющих клеток-хозяев; тем самым в образце повышается процент полипептидов представляющего интерес рекомбинантного фермента.
В рамках изобретения выражение «представляющий интерес белок» относится к белку (например, ферменту, или «представляющему интерес ферменту»), который анализируют, идентифицируют и/или модифицируют. Природные, а также рекомбинантные (например, «мутант» или «вариант») белки находят применение в настоящем изобретении. В рамках изобретения термин «белок» относится к любой композиции, включающей аминокислоты и рассматриваемой в качестве белка специалистами в данной области. Термины «белок», «пептид» и «полипептид» используются в настоящем описании взаимозаменяемо. Когда пептид представляет собой часть белка, специалистам в данной области понятно применение термина в контексте.
В рамках изобретения термин «вектор экспрессии» относится к конструкции ДНК, которая является функционально связанной с подходящей контрольной последовательностью, способной к эффективной экспрессии ДНК в подходящем хозяине. Такие контрольные последовательности включают промотор для эффективной транскрипции, необязательную операторную последовательность для контроля такой транскрипции, последовательность, кодирующую походящие связывающие сайты рибосом мРНК, и последовательности, которые контролируют окончание транскрипции и трансляции. Вектор может представлять собой плазмиду, фаговую частицу или просто потенциальную геномную вставку. После трансформации в подходящем хозяине вектор может реплицировать и функционировать независимо от генома хозяина или может, в некоторых случаях, интегрироваться в сам геном. В настоящем описании термины «плазмида», «плазмида экспрессии» и «вектор» часто используются взаимозаменяемо, поскольку плазмида представляет собой наиболее обычно используемую форму вектора на сегодняшний день. Однако подразумевается, что изобретение включает другие формы векторов экспрессии, которые выполняют эквивалентные функции и которые известны или стали известными в данной области.
В некоторых предпочтительных вариантах осуществления ген протеазы лигируют в подходящую плазмиду экспрессии. Клонированный ген протеазы затем используют для трансформации или трансфекции клетки-хозяина для экспрессии гена протеазы. Эта плазмида может реплицировать в хозяевах в том смысле, что он содержит хорошо известные элементы, необходимые для репликации плазмиды, или плазмида может быть сконструирована для интеграции в хромосому хозяина. Необходимые элементы обеспечены для эффективной экспрессии гена (например, промотор, функционально связанный с рассматриваемым геном). В некоторых вариантах осуществления эти необходимые элементы обеспечиваются в качестве собственного гомологичного протомора гена, если он распознается (т.е. транскрибируется хозяином) и терминатора транскрипции, который является экзогенным или обеспечивается за счет эндогенной терминаторной области гена протеазы. В некоторых вариантах осуществления также включен селектируемый ген, такой как ген устойчивости к антибиотикам, который дает возможность непрерывного культурального поддержания клеток-хозяев, инфицированных плазмидами, посредством роста в среде, содержащей противомикробные агенты.
Следующий метод кассетного мутагенеза можно использовать для облегчения конструирования варианта протеазы по настоящему изобретению, хотя также можно использовать другие способы. Во-первых, как указано в настоящем описании, получают природный ген, кодирующий протеазу, и секвенируют полностью или частично. Затем последовательность сканируют до точек, в которых желательно провести мутацию (например, посредством делеции, инсерции или замещения) одной или нескольких аминокислот в кодируемой протеазе. Последовательности, примыкающие к этой точке, оценивают на присутствии сайтов рестрикции для замены короткого сегмента гена на олигонуклеотидный пул, который, при экспрессии, будет кодировать различные мутанты. Такие сайты рестрикции предпочтительно представляют собой единичные сайты в гене белка для облегчения замены сегмента гена. Однако можно использовать любой обычный сайт рестрикции, который не является чрезмерно дублируемым в гене протеазы, при условии, что фрагменты генов, генерируемые при рестрикционном расщеплении, могут повторно собираться в правильную последовательность. Если не имеется сайтов рестрикции, расположенных в пределах удобного расстояния от выбранной точки (от приблизительно 10 до приблизительно 15 нуклеотидов), такие сайты генерируют путем замещения нуклеотидов в гене таким образом, что ни рамка считывания, ни кодируемые аминокислоты не изменяются в конечной конструкции. Мутацию гена для изменения его последовательности, чтобы она соответствовала желаемой последовательности, проводят путем расширения праймера в соответствии с обычными известными способами. Задача расположения подходящих фланкирующих областей и оценки необходимых изменений для достижения по двум подходящим сайтам рестрикции последовательности стала общепринятой посредством сокращения генетического кода, рестрикции ферментативной карты гена и большого числа различных ферментов рестрикции. Следует отметить, что, если подходящий фланкирующий сайт рестрикции доступен, вышеуказанный способ требуется использовать только в связи с фланкирующей областью, которая не содержит сайта. После клонирования природной ДНК и/или синтетической ДНК, сайты рестрикции, расположенные сбоку от предназначенных для мутирования позиций, отщепляют с использованием родственных ферментов рестрикции и множество комплиментарных по концам олигонуклеотидных кассет лигируют в ген. Мутагенез упрощается при таком способе, поскольку все олигонуклеотиды могут быть синтезированы таким образом, чтобы иметь такие же сайты рестрикции, и синтетические линкеры не потребуются для создания сайтов рестрикции.
В рамках изобретения выражение «соответствующий» относится к остатку в нумерованном положении белка или пептида, или остатку, который является аналогичным, гомологичным или эквивалентным пронумерованному остатку в белке или пептиде. В рамках изобретения выражение «соответствующая область» обычно относится к аналогичному положению на протяжении цепи родственных белков или ссылочного белка.
Термины «молекула нуклеиновой кислоты, кодирующая», «последовательность нуклеиновых кислот, кодирующая», «последовательность ДНК, кодирующая», и «ДНК, кодирующая», относятся к порядку или последовательности дезоксирибонуклеотидов вдоль цепи дезоксирибонуклеиновой кислоты. Порядок этих дезоксирибонуклеотидов определяется порядком аминокислот вдоль полипепидной (белковой) цепи. Последовательность ДНК таким образом кодирует последовательность аминокислот.
В рамках изобретения белки «дикого типа» и «нативные» белки представляют собой те, которые существуют в природе. Термин «последовательность дикого типа» и «ген дикого типа» используются взаимозаменяемо для упоминания последовательности, которая является нативной или природной в клетке-хозяине. В некоторых вариантах осуществления выражение «последовательность дикого типа» относится к представляющей интерес последовательности, которая является отправным моментом в проекте инжиниринга белка. Гены, кодирующие природный белок, могут быть получены в соответствии с общими способами, известными специалистам в данной области. Способы обычно включают синтез меченых зондов, имеющих предполагаемые последовательности, кодирующие области целевого белка, получение геномных библиотек от организмов, экспрессирующих белок, и скрининг библиотек для выявления целевого гена посредством гибридизации зондов. Положительно гибридизируемые клоны затем картируют и секвенируют.
Термин «рекомбинантная молекула ДНК» в рамках изобретения относится к молекуле ДНК, которая состоит из сегментов ДНК, соединенных между собой с помощью методом молекулярной биологии. Термин «рекомбинантный олигонуклеотид» относится к олигонуклеотиду, созданному с использованием манипуляций молекулярной биологии, включая, но не ограничиваясь указанным, лигирование двух или более олигонуклеотидных последовательностей, генерированных с помощью рестрикционного ферментативного расщепления последовательности полинуклеотида, синтез олигонуклеотидов (например, синтез праймеров или олигонуклеотидов) и тому подобное.
В рамках изобретения термин «эквивалентные остатки» относится к белкам, которые используют совместно определенные аминокислотные остатки. Например, эквивалентные остатки могут быть выявлены путем определения гомологии на уровне третичной структуры белка (например, протеазы), чья третичная структура была определена методом рентгеноструктурной кристаллографии. Эквивалентные остатки определяют как те, для которых координаты атомов двух или более атомов основной цепи для конкретного остатка аминокислоты белка, имеющего предполагаемые эквивалентные остатки, и представляющего интерес белка, находятся в диапазоне 0,13 нм и предпочтительно приблизительно 0,1 нм после совмещения. Совмещение достигается после того, как лучшая модель была ориентирована и расположена так, чтобы давать максимальное перекрывание координат атомов для неводородных атомов белка в анализируемом белке. Предпочтительной моделью является кристаллографическая модель, дающая наиболее низкий R-фактор для экспериментальных дифракционных данных при наиболее высоком доступном разрешении, определенных с использованием методов, известных специалистам в области кристаллографии и характеризации/анализа белков.
Термин «регуляторный элемент» в рамках изобретения относится к генетическому элементу, который контролирует некоторые аспекты экспрессии последовательностей нуклеиновых кислот. Например, промотор представляет собой регуляторный элемент, который облегчает инициирование транскрипции функционально связанной кодирующей области. Дополнительные регуляторные элементы включают сигналы сплайсинга, сигналы полиаденилирования и сигналы завершения.
В рамках изобретения «клетки-хозяева» обычно представляют собой прокариотические или эукариотические хозяева, которые трансформируют или трасфектируют с использованием векторов, сконструированных с использованием методов рекомбинантной ДНК, известных в данной области. Трансформированные клетки-хозяева способны либо к репликации векторов, кодирующих вариант белка, либо к экспрессии желаемого варианта белка. В случае векторов, которые кодируют пред- или предпро-формы варианта белка, такой вариант, будучи экспрессированным, обычно секретируется из клетки-хозяина в среду клеток-хозяев.
Термин «введенный», в контексте вставки последовательности нуклеиновой кислоты в клетку, означает трансформацию, трансдукцию или трансфекцию. Способы трансформации включают, но не ограничиваются указанным, любые подходящие способы, известные в данной области, такие как трансформация протопласта, осаждение хлоридом кальция, электропорация, «голые» ДНК и тому подобные, как известно в данной области (см., например, Chang и Cohen, Mol Gen Genet, 168:111-115, 1979; Smith et al., Appl Env Microbiol, 51:634, 1986; и обзорная статья Ferrari et al., в Harwood, Bacillus. Plenum Publishing Corporation, pp. 57-72, 1989).
Термин «промотор/энхансер» означает сегмент ДНК, который содержит последовательности, способные обеспечивать как функции промотора, так и функции энхансера. Промотор/энхансер могут быть «эндогенными», или «экзогенными», или «гетерологичными». Эндогенный промотор/энхансер представляет собой тот, который природно связан с этим геном в геноме. Экзогенный (гетерологичный) промотор/энхансер представляет собой тот, который размещен в непосредственном соседстве с геном с помощью генетических манипуляций (т.е. методами молекулярной биологии).
Присутствие «сигналов сплайсинга» в векторе экспрессии часто приводит к более высокому уровню экспрессии рекомбинантного транскрипта. Сигналы сплайсинга опосредуют удаление интронов из первичного РНК транскрипта и состоят из донорного и акцепторного сайта сплайсинга (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, New York, pp. 16.7-16.8, 1989).
Термин «стабильная трансфекция» или «стабильно трансфицированный» относится к введению и интегрированию чужеродной ДНК в геном трансфицированной клетки. Термин «стабильный трансфектант» относится к клетке, которая содержит стабильно интегрированную чужеродную или экзогенную ДНК в геномной ДНК трансфицированной клетки.
Термин «селектируемый маркер» или «селектируемый генный продукт» в рамках изобретения относится к применению гена, который кодирует ферментативную активность, которая придает резистентность к воздействию антибиотика или лекарственного средства на клетку, в которой экспрессируется селектируемый маркер.
В рамках изобретения термины «амплификация» и «амплификация гена» относится к процессу, посредством которого специфические последовательности ДНК реплицируют непропорционально, так что амплифицированный ген начинает присутствовать в большем числе копий, чем первоначально присутствовало в геноме. В некоторых вариантах осуществления селекция клеток по росту в присутствии лекарственного средства (например, ингибитора фермента, способного к ингибированию) приводит к амплификации или эндогенного гена, кодирующего генный продукт, требуемый для роста в присутствии лекарственного средства, или амплификации экзогенной (т.е. исходной) последовательности, кодирующей этот генный продукт, или к обоим. Селекция клеток по росту в присутствии лекарственного средства (например, ингибитора фермента, способного к ингибированию) приводит к амплификации либо эндогенного гена, кодирующего генный продукт, требуемый для роста в присутствии лекарственного средства, или амплификации экзогенной (т.е. исходной) последовательности, кодирующей этот генный продукт, или к обоим.
«Амплификация» представляет собой специальный случай репликации нуклеиновой кислоты, включающий темплатную специфичность. Она противопоставляется неспецифической темплатной репликации, т.е. репликации, которая является темплат-зависимой, но не зависит от конкретного темплата). Темплатная специфичность в рамках изобретения отличается от точности воспроизведения репликации (т.е. синтеза правильной последовательности нуклеотида) и нуклеотидной (рибо- или дезоксирибо-) специфичности. Темплатную специфичность часто описывают в терминах «мишень»-специфичности. Мишень-специфичность относится к «мишеням» в том смысле, что их пытаются отсортировать от других нуклеиновых кислот. Методы амплификации в первую очередь были разработаны для такой сортировки.
В рамках изобретения термин «амплифицируемый маркер», «амплифицируемый ген» и «вектор амплификации» относятся к маркеру, ген или вектору, кодирующим ген, который дает возможность амплификации такого гена при подходящих условиях роста.
В рамках изобретения термин «амплифицируемая нуклеиновая кислота» относится к нуклеиновым кислотам, которые могут быть амплифицированы с помощью любого из методов амплификации. Подразумевается, что «амплифицируемая нуклеиновая кислота» обычно будет включать «темплат образца».
В рамках изобретения термин «темплат образца» относится к нуклеиновой кислоте, происходящей из образца, который был проанализирован на присутствие «мишени» (определено ниже). В противоположность этому, термин «фоновый темплат» используется для упоминания нуклеиновой кислоты, отличающейся от нуклеиновой кислоты темплата образца, которая может присутствовать или не присутствовать в образце. Фоновый темплат наиболее часто является случайным. Он может быть результатом переходящего остатка, или он может возникать вследствие присутствия примесей нуклеиновых кислот, от которых, как предполагается, был очищен образец. Например, нуклеиновые кислоты организмов, отличающихся от тех, которые предназначены для обнаружения, могут присутствовать в качестве фона в тестируемом образце.
В рамках изобретения термин «праймер» относится к олигонуклеотиду либо существующему в природе, как в очищенном продукте рестрикции, либо получаемому синтетически, который способен действовать в месте инициирования синтеза, будучи помещен в условия, в которых индуцируется синтез продукта удлинения праймера, который является комплементарным цепи нуклеиновой кислоты (т.е. в присутствии нуклеотидов и индуцирующего агента, такого как ДНК полимераза и при подходящей температуре и рН). Праймер предпочтительно является одноцепочечным для максимальной эффективности в амплификации, но альтернативно может быть и двухцепочечным. Если он является двухцепочечным, праймер первоначально обрабатывают для разделения его цепей перед использованием для получения продуктов удлинения. Предпочтительно праймер представляет собой олигодезоксирибонуклеотид. Праймер должен быть достаточно длинным для начала синтеза продуктов удлинения в присутствии индуцирующего агента. Точная длина праймеров зависит от множества факторов, включая температуру, источник праймер и применяемого способа.
В рамках изобретения термин «зонд» относится к олигонуклеотиду (т.е. последовательности нуклеотидов) либо существующему в природе, как в очищенном продукте рестрикции, либо получаемому синтетически, рекомбинантно или методом ПЦР амплификации, который способен к гибридизации с другим представляющим интерес олигонуклеотидом. Зонд может быть одноцепочечным или двухцепочечным. Зонды используют для обнаружения, идентификации и выделения определенных последовательностей генов. Подразумевается, что любой зонд, используемый в настоящем изобретении, будет меченым какой-либо «репортерной молекулой», так что он обнаруживается в какой-либо системе детектирования, включая, но не ограничиваясь указанным, ферментативную (например, ELISA, а также ферментативный гистохимический анализы), флуоресцентную, радиоактивную и люминесцентную системы. Не предполагается, что настоящее изобретение ограничивается какой-либо конкретной системой детектирования или меткой.
В рамках изобретения термин «мишень» при использовании со ссылкой на способ амплификации (например, полимеразная цепная реакция) относится к области нуклеиновой кислоты, связанной с помощью праймеров, использованных для полимеразной цепной реакции. Таким образом, «мишень» пытаются отсортировать от других последовательностей нуклеиновых кислот. Под «сегментом» определяют область нуклеиновой кислоты внутри последовательности-мишени.
В рамках изобретения термин «полимеразная цепная реакция» и «ПЦР» относится к способам в патентах США №№ 4683195, 4683202 и 4965188, которые включают способы увеличения концентрации сегмента последовательности-мишени в смеси геномной ДНК без клонирования или очистки.
В рамках изобретения термин «реагенты амплификации» относится к тем реагентам (дезоксирибонуклеотидтрифосфаты, буферы и т.д.), которые необходимы для амплификации, за исключением праймеров, темплата нуклеиновой кислоты и фермента амплификации. Обычно реагенты амплификации наряду с другими реакционными компонентами помещают и содержатся в реакционном сосуде (тест-пробирка, микролунка и т.д.).
В рамках изобретения термин «рестрикционные эндонуклеазы» или «ферменты рестрикции» относится к бактериальным ферментам, каждый из которых отрезает двухцепочечную ДНК в месте или около определенной нуклеотидной последовательности.
В рамках изобретения термин «чистящая композиция» относится к любой композиции, которая находит применение для чистки. Предполагается, что этот термин охватывает (если не указано иное) гранулированные или порошкообразные моющие агенты для всех целей или «предназначенные для работы в тяжелом режиме» (например, стиральные порошки), моющие агенты для всех целей в виде жидкости, геля или пасты (например, жидкие моющие средства, «предназначенные для работы в тяжелом режиме»), жидкие и порошкообразные моющие средства для деликатных тканей, средства для ручного мытья посуды, легкие агенты для мытья посуды (например, высокопенящиеся моющие средства), моющие средства для посудомоечных машин (т.е. моющие средства для автоматических посудомоечных машин), включая таблетированные, гранулированные, жидкие моющие средства, моющие средств