Способ получения монофазного кристаллического кремний-замещенного гидроксилапатита
Иллюстрации
Показать всеИзобретение относится к технологии получения кристаллического кремний-замещенного гидроксилапатита (Si-ГА), который может быть использован в ортопедии и стоматологии. Si-ГА получают методом осаждения из модельного раствора внеклеточной жидкости путем приготовления раствора состава: СаСl2 - 3,7424 г, MgCl2 - 0,6092 г, К2НРO4 - 2,8716 г, NaHCO3 - 4,5360 г, Na2SO4 - 0,0144 г, NaCl - 8,8784 г при рН 7,40±0,05, добавления в него модифицированного силиката натрия в молярном отношении Ca/(P+Si) 2,00÷2,50 в форме Na2SiO3, отстаивания в течение 48 часов, фильтрования, промывки и высушивания при температуре 80±5°C в течение 5 часов. Изобретение позволяет получать монофазный нанокристаллический (со средним размером кристаллов 6,0-7,1 нм) Si-ГА, имеющий повышенную биоактивность в среде, моделирующей внеклеточную жидкость человека. 5 ил., 3 табл.
Реферат
Изобретение относится к области медицины, а именно к способу получения кристаллического кремнийзамещенного гидроксилапатита, который может быть использован в ортопедии и стоматологии.
Ввиду того что гидроксилапатит Ca10(РО4)6(ОН)2 (ГА) является минеральным аналогом костной составляющей, материалы на их основе используются для создания искусственных заменителей костной ткани человека. Одним из путей решения этой проблемы является синтез наноразмерного гидроксилапатита с последующей термической обработкой ниже температуры спекания. Поэтому для получения наноразмерного ГА сегодня наибольшее распространение получили методы, основанные на осаждении гидроксилапатита из щелочных водных растворов реагентов, содержащих в стехиометрическом соотношении ионы кальция и фосфат-ионы. [1].
Наряду с этим результаты последних клинических испытаний показали, что приготовленные материалы с использованием ГА с преимуществами обладают рядом недостатков: низкая скорость биорезорбции и остеоиндукции, высокое значение наблюдаемой энергии активации. Химическое модифицирование гидроксилапатита является основным методом управления биологической активностью материала, изготовленного на его основе. Введение кремния в отличие от немодифицированного ГА вызывает значительно более высокий биологический отклик, что может быть связано с Si-индуцирущим изменением свойств материала. При введении кремния в кристаллическую структуру ГА изменяется эффективный заряд поверхности материла, что связано со специфическим расположением силикат-ионов относительно фосфат-ионов в кристаллической решетке кремний-замещенного гидроксилапатита (Si-ГА). Это подтвердилось в испытаниях, которые проводили in vivo, где было установлено, что на поверхности кремний-замещенного гидроксилапатита значительно быстрее происходит адсорбция протеинов, прикрепление клеток остеобластов, специфические клеточные реакции (синтез коллагена I типа, активация щелочной фосфатазы) и, соответственно, минерализация молодого костного матрикса [2, 3]. Ввиду полученных данных модифицирование ГА представляет собой перспективную и актуальную задачу. Si-ГА можно представить формулой: Ca10(PO4)6-x(SiO4)x(OH)2-x,
где x - степень замещения
Известен способ получения кремний-замещенного гидроксилапатита путем осаждения из водного раствора реагентов [1]. При получении кремнийсодержащего гидроксилапатита методом осаждения из водных растворов наиболее часто используют следующие реакции:
10Са(ОН)2+(6-х)Н3PO4+xSi(OR)4→Са10(РО4)6-x(SiO4)x(OH)2-х+
+4xROH+(18-x)H2O,
где R=Et, n-Pr, Ac.
Синтез проводят при температурах 60÷80°C, рН 9÷11 поддерживают раствором аммиака, иногда используют инертный газ для подавления поглощения продуктом синтеза углекислого газа из воздуха. Материал приготавливают по стехиометрии ГА при условии, что кремний замещает позиции фосфора в кристаллической решетке, а молярное отношение Са/(Р+Si) равно 1,67. Осадок ГА термообрабатывали при 1100°C в течение 2 часов в атмосфере воздуха. Недостатком этого способа, с одной стороны, является невысокая степень замещения кремния x<1, что соответствует содержанию кремния в материале 0,8-1,5 масс.%, а с другой, - появление примесных фаз, например оксида кальция или трикальцийфосфата после термообработки при использовании более высоких степеней замещения, например при x>1.
Наиболее близким по технической сущности и достигаемому результату является способ (патент РФ №2500840) получения монофазного кристаллического кремний-замещенного гидроксилапатита, который включает синтез Si-ГА методом осаждения при рН не менее 9 из реагентов, содержащих ортофосфорную кислоту, гидроксид кальция и тетраэтилортосиликат. Причем реагенты вводятся в реакционную смесь при условии обеспечения молярного отношения Са/Р в диапазоне от 2,0 до 2,5. Готовят композицию из 0,08-0,16%-ного водного раствора гидроксида кальция и тетраэтилортосиликата. Раствор ортофосфорной кислоты с 10-20%-ной концетрацией приливают со скоростью 0,2-0,8 мл/мин, на литр водного раствора композиции гидроксид кальция/тетраэтилортосиликат. Отстаивают для завершения процесса фазообразования, выделяют осадок и высушивают его. Термообработку ведут при температуре не ниже 300C, но не более 400C. Этот способ позволяет получать поликристаллический чистый или монофазовый кремнийзамещенный гидроксилапатит, состоящий из частиц размером 0,010-0,012 мкм (или 10-12 нм соответственно), обладающий относительно высокой скоростью растворения и способностью извлекать достаточные количества кремния в раствор. Преимуществом кремнийзамещенного гидроксилапатита данного решения является более высокая растворимость по сравнению с керамическим кремнийзамещенным гидроксилапатитом и обычным немодифицированным гидроксилапатитом, а также более высокий выход кремния при контакте с раствором. При выдерживании кремнийзамещенного гидроксилапатита в физиологическом растворе концентрация ионов кальция остается неизменной или увеличивается. Это выгодно отличает его от гидроксилапатитов с низким уровнем замещения кремния, для которых содержание кальция в физиологическом растворе снижается в тот же период времени. Также к преимуществам данного Si-ГА относится отсутствие побочных фаз в виде оксидов кальция, трикальцийфосфатов (ТКФ) при прокаливании на высоких температурах. Основными недостатками данного метода является то, что синтез ведут при рН, далеких от нормальных физиологических значений организма человека. Также данный образец не повторяет структуру кости человека, в нем отсутствует карбонатная группировка. При синтезе в качестве реагента носителя ионов кремния используется тетраэтоксисилан (ТЭС), который при гидролизе образует этиловый спирт, в результате происходит отравление живых тканей в отличие от силиката натрия, у которого продуктом гидролиза будет являться гидроокись натрия.
Технической задачей изобретения является создание способа получения монофазового нанокристаллического кремний-замещенного гидроксилапатита с повышенной биоактивностью в среде, моделирующей внеклеточную жидкость человека.
Указанный технический результат достигается тем, что предложен способ получения монофазного кристаллического кремний-замещенного гидроксилапатита методом осаждения из модельного раствора внеклеточной жидкости, в котором готовят раствор состава: CaCl2 - 3.7424 г, MgCl2 - 0.6092 г, K2НРO4 - 2.8716 г, NaHCO3 - 4.5360 г, Na2SO4 - 0,0144 г, NaCl - 8.8784 г при рН 7.40±0.05, добавляют модифицированный силикат натрия в молярном отношении Ca/(P+Si) 2.00÷2.50 в форме Na2SiO3, отстаивают в течение 48 часов, проводят фильтрование, промывку и высушивают при t=80±5°C в течение 5 часов.
Способ включает следующие новые признаки:
- синтез производится из раствора, максимально приближенного к физиологическому;
- рН среды при синтезе отвечает физиологическим значениям;
- в качестве промотера кремния используется силикат натрия;
- для увеличения биоактивности нет необходимости проводить термообработку.
Режим отстаивания в течение 48 часов, фильтрования, промывки и сушки при t=80±5°C в течение 5 часов подбирался экспериментально исходя из условия полного удаления адсорбционной воды. После этого осадок отделялся от корж-фильтра в агатовую ступку и растирался пестиком до получения однородного порошка.
При этом заявляемый способ позволяет получить:
стехиометричный монофазный Si-ГА со средним размером кристаллов 6.0-7.1 нм, имеющий повышенную биоактивность;
стабильный монофазный продукт формулы Са10(РО4)6-x(SiO4)x(OH)2-х, где 0.50<x<5.00% масс.,
Одной из проблем при синтезе Si-ГА является подбор массового содержания кремния в образце.
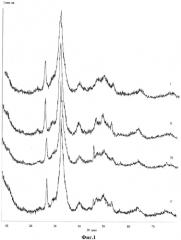
Результаты РФА показали, что все образцы, синтезируемые в среде модельного раствора внеклеточной жидкости при варьировании концентрации силикат-ионов, однофазны и представляют собой гидроксилапатит. На фиг. 1 представлены дифрактограммы образцов гидроксилапатита, модифицированных Na2SiO3: I - С Si исх. 0,5%; II - С Si исх 2,5%; ТЭС: III - С Si исх 0,5%; IV - С Si исх 2,5%. На данных дифрактограммах присутствуют рефлексы ГА при 25,8° (002), 31,7° (211), 32,2° (112) и 32,9° (300) (фиг. 1). Следует отметить, что дифрактограммы, соответствующие твердым фазам с различными источниками силикатных групп Na2SiO3, имеют схожий вид. Размеры кристаллитов полученного немодифицированного ГА составили 6.3 нм, для Si-ГА - 6.0÷7.1 нм, что указывает на образование соединений в нанокристаллическом состоянии.
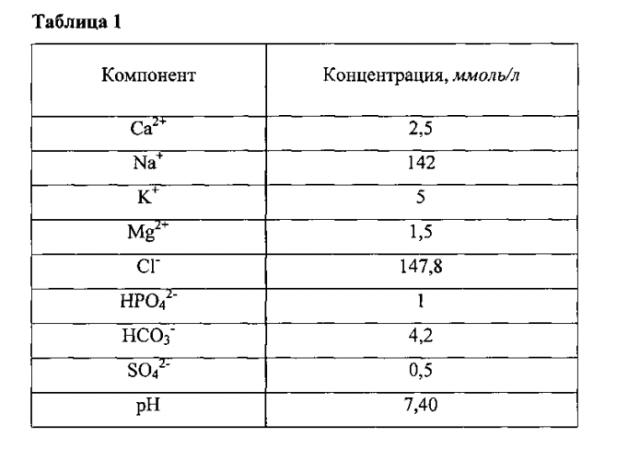
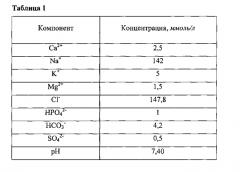
В таблице 1 представлены концентрации ионов в модельных растворах, приближенных по электролитному составу к внеклеточной жидкости, ммоль/л. Данная таблица используется для приготовления растворов синтеза.
В таблице 2 представлены параметры кристаллической решетки образованных твердых фаз.
Данные параметры увеличены по сравнению с немодифицированным гидроксилапатитом (ГА), что подтверждает возможное замещение различных по размеру ортофосфат-иона силикат-ионом (расстояния Si-О = 1.66 Å, Р-O = 1.55 Å [4]). Увеличение параметра свидетельствует о том, что силикат-ион занимает преимущественно позицию фосфат-иона в структуре ГА, а не гидроксил-иона [5].
На Фиг. 2. представлены ИК-спектры образцов гидроксилапатита, модифицированных: 1 - Na2SiO3C Si исх 0,5%; 2 и 3 - ТЭС С Si исх 0,5 и 2,5%. В ИК-спектрах образцов, полученных в присутствии силикат-ионов, присутствуют полосы поглощения, характерные для гидроксилапатита.
Структуру ГА определяют следующие полосы: 1040-1080 (ν3), 960, 840 (ν2), 602, 574 (ν4) и 473 (ν2) см-1, соответствующие колебаниям фосфатных групп, широкая полоса при 3440-3570 см-1 соответствует деформационным колебаниям ОН--групп и валентным колебаниям адсорбированной воды. Высокая интенсивность этого пика у модифицированного ГА связана с тем, что имеют высокое сродство к молекулам воды, вследствие чего происходит гидратация. Ввиду того что ГА синтезирован в воздушной среде, в процессе его образования из атмосферы воздуха сорбируется углекислый газ и в решетке локализуются ионы карбоната в положении фосфатного иона, которым в ИК-спектрах соответствуют полосы поглощения деформационных колебаний С-O связей иона при 875 см-1 и валентных колебаний при 1422-1457 см-1 [6].
В ИК-спектрах присутствует полоса поглощения низкой интенсивности колебания связей силикатной группы при 511 см-1, обусловленная деформационными колебаниями связей Si-O. Полоса поглощения колебания Si-О связи при 945 см-1 перекрывается с полосой поглощения, соответствующей колебаниям Р-O связи при 960 см-1. Наличие данных сигналов на спектре свидетельствует о замещении на в структуре ГА, что приводит к искажению тетраэдра, в результате чего происходит изменение параметров элементарной ячейки. Таким образом, данные ИК-Фурье-спектроскопии находятся в согласии с результатами РФА.
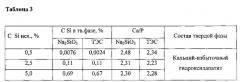
В таблице 3 представлены данные о концентрации силикат-ионов в твердой фазе, составы твердых фаз, полученные методами химического анализа надосадочной жидкости.
Их содержание значительно возрастает при увеличении исходной концентрации силикат-ионов до 5% в системе. Соотношение Са/Р в синтезируемых соединениях превышает заданное значение 1,67, характерное для стехиометрического гидроксилапатита, и соответствует фазе кальций-избыточного ГА. Это свидетельствует об уменьшении количества фосфат-ионов в полученных твердых фазах, что, по нашему мнению, связано с замещением фосфатных групп на силикатные группы.
На фиг. 3 представлены кинетические кривые растворения Si-ГА в соляной кислоте при t=37°C. Биоактивность материала проверяли методом растворения одинаковых навесок образца в разных растворителях (HCl, 0.9% NaCl, трис-HCl буфер) при 37°C (фиг. 3-5). Установлено, что образцы, в которых при синтезе используется силикат натрия, обладают большей резорбируемостью, чем материал, не содержащий добавки силикат-ионов.
Литература
1. Соин А.В., Евдокимов П.В., Вересов А.Г., Путляев В.И. Синтез и исследование анионмодифицированных апатитов // Международный научный журнал «Альтернативная энергетика и экология» - 2007 - Т. 1 - №45 - с. 130-132.
2. Pietak A.M., Reid J.W., Stott M.J., Sayer M. Silicon substitution in the calcium phosphate bioceramics // Biomaterials 2007; 28: 4023-4032.
3. Portera A.E., Patela N., Skepperb J.N., Besta S.M., Bonfielda W. Comparison of in vivo dissolution processes in hydroxyapatite and silicon-substituted hydroxyapatite bioceramics // Biomaterials 2003; 24: 4609-4620.
4. Солоненко А.П., Голованова О.А. Термодинамическое моделирование процессов образования ортофосфатов кальция. // Ж. Бутлеровские сообщения. 2011. Т. 24 №2. С. 106-112.
5. Маловская Е.А., Голованова О.А., Панова Т.В., Герк С.А., Осинцев В.А. Кристаллизация фосфатов кальция из прототипов биологических жидкостей на костных образцах. // Ж. Бутлеровские сообщения. 2013. Т. 36 №10. С. 21-28.
6. Solonenko А.Р., Golovanova О.А., Hydroxyapatite-Brushite ixtures: Synthesis and Physicochemical Characterization // J. Inorganic Chemistry 2014, Vol. 59, No. 1, pp. 12-20.
Способ получения монофазного кристаллического кремний-замещенного гидроксилапатита методом осаждения из модельного раствора внеклеточной жидкости, в котором готовят раствор состава: СаСl2 - 3,7424 г, MgCl2 - 0,6092 г, К2НРO4 - 2,8716 г, NaHCO3 - 4,5360 г, Na2SO4 - 0,0144 г, NaCl - 8,8784 г при рН 7,40±0,05, добавляют модифицированный силикат натрия в молярном отношении Ca/(P+Si) 2,00÷2,50 в форме Na2SiO3, отстаивают в течение 48 часов, проводят фильтрование, промывку и высушивают при t=80±5°C в течение 5 часов.