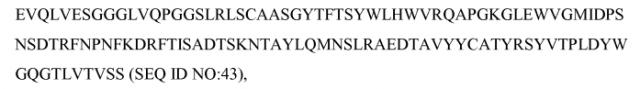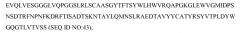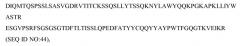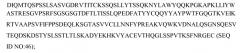Способы и композиция для секреции гетерологичных полипептидов
Иллюстрации
Показать всеНастоящее изобретение к биохимии, в частности к способу получения антитела. Указанный способ предусматривает культивирование клетки-хозяина, содержащей полинуклеотид, содержащий первую область инициации трансляции (TIR), функционально связанную с полинуклеотидом, кодирующим тяжелую цепь антитела, и вторую TIR, функционально связанную с полинуклеотидом, кодирующим лёгкую цепь антитела, и извлечение антитела из культуры клетки-хозяина. Первая TIR содержит вариант котрансляционной прокариотической сигнальной последовательности секреции DsbA и вторая TIR содержит котрансляционную или посттрансляционную прокариотическую сигнальную последовательность секреции. Благодаря наличию указанного полинуклеотида в клетке-хозяине происходит укладка и сборка тяжёлой и лёгкой цепей с формированием биологически активного антитела. Настоящее изобретение также раскрывает полинуклеотид и клетки-хозяева для получения антитела, т.е. для осуществления указанного выше способа. Настоящее изобретение позволяет увеличить выход получаемого антитела. 5 н. и 64 з.п. ф-лы, 7 ил., 4 табл., 1 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет по патентной заявке США № 61/258565, которая подана 5 ноября 2009 года, содержание которой включено в данный документ в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение в основном относится к области молекулярной биологии и белковой технологии. Более конкретно, изобретение относится к сигнальным последовательностям для секреции гетерологичных полипептидов бактериями. Изобретение также относится к продуцируемым прокариотами рекомбинантным полипептидам и их применению.
УРОВЕНЬ ТЕХНИКИ
Секреция гетерологичных полипептидов в периплазматическое пространство E. coli и других прокариотов или в их среды для культивирования зависит от различных параметров. Типично векторы для секреции полипептида, представляющего интерес, конструируют для того, чтобы поместить ДНК, кодирующую секреторную сигнальную последовательность, ближе к 5' относительно ДНК, кодирующей полипептид, представляющий интерес.
В последние годы расширились перспективы использования гетерологичных полипептидов, например, антител, в качестве диагностических и терапевтических средств для различных нарушений и заболеваний. Для многих исследовательских и клинических применений необходимы большие количества функционального полипептида, что, таким образом, требует увеличенных в масштабе и при этом экономичных систем для получения полипептида. В частности, можно использовать рекомбинантное получение антител с использованием различных экспрессирующих организмов-хозяев в диапазоне от прокариотов, таких как E. coli или B. subtilis, до клеток дрожжей, растений, насекомых и млекопитающих. Kipriyanov and Little (1999) Mol. Biotech. 12: 173-201.
По сравнению с другими системами получения полипептидов, бактерии, в частности, E. coli, обеспечивают многие уникальные преимущества. Используемое сырье (т.е. бактериальные клетки) недороги и просты в выращивании, вследствие чего снижается стоимость продуктов. Прокариотические организмы-хозяева растут значительно быстрее, чем, например, клетки млекопитающих, что допускает более быстрый анализ генетических манипуляций. Более короткое время жизни поколения и легкое масштабирование также делают бактериальную ферментацию более привлекательным средством для получения белка в больших количествах. Структура генома и биологическая активность многих бактериальных видов, включая E. coli, хорошо изучены, а также доступен широкий спектр подходящих векторов, что делает экспрессию желаемого антитела более удобной. По сравнению с эукариотами, процесс получения включает меньшее число стадий, включая манипуляцию рекомбинантными генами, стабильную трансформацию множественных копий в организм-хозяин, индукцию экспрессии и определение характеристик продуктов. Pluckthun and Pack (1997) Immunotech 3:83-105.
Для получения рекомбинантных полипептидов в бактериях использовались различные подходы. Рекомбинантные белки можно получить из бактерий или посредством повторной укладки телец включения, экспрессируемых в цитоплазме, или посредством экспрессии с последующей секрецией в бактериальную периплазму. Выбор между секрецией и повторной укладкой, как правило, обусловлен несколькими соображениями. Обычно секреция является более быстрой и более общеупотребительной стратегией получения антител. Kipriyanov and Little (1999), выше.
Экспрессию антител в прокариотических системах можно осуществлять в различных масштабах. Культуры во встряхиваемых колбах (в пределах 2-5 л) типично создают продукты в количестве менее чем 5 мг/л. Carter et al. (1992) Bio/Technology 10: 12-16 разработали систему ферментации при высокой плотности клеток, в которой достигали высокого уровня экспрессии фрагментов антител (до 2 г/л). Титры Fab' в граммах на литр, которых достигли Carter et al., в значительной степени обусловлены высокими плотностями клеток, что является результатом более точного контроля среды ферментатора, чем таковой в простой встряхиваемой колбе. Система содержит бицистронный оперон, сконструированный для совместной экспрессии фрагментов легких цепей и тяжелых цепей. Бицистронный оперон находится под управлением одного промотора phoA E. coli, который можно индуцировать посредством фосфатного голодания. Каждой цепи антитела предшествует сигнальная последовательность термостабильного энтеротоксина II (stII) E. coli, чтобы направить секрецию в периплазматическое пространство.
Общие обзоры получения антител в E. coli см. в Pluckthun and Pack (1997) Immunotech 3:83-105; Pluckthun et al. (1996) in ANTIBODY ENGINEERING: A PRACTICAL APPROACH, pp 203-252 (Oxford Press); Pluckthun (1994) in HANDBOOK OF EXP PHARMCOL VOL 3: THE PHARMCOL OF MONOCLONAL ANTIBODIES, pp. 269-315 (ed. M. Rosenberg and G.P. Moore; Springer-Verlag, Berlin).
Многие биологические анализы (такие как рентгенокристаллография) и клинические применения (такие как белковая терапия) требуют больших количеств белка. Соответственно, существует потребность в высокопродуктивных и при этом простых системах для получения правильно собранных, растворимых и функциональных гетерологичных полипептидов, таких как антитела.
Все цитируемые в данном документе ссылки, включая патентные заявки и публикации, включены в данный документ в качестве ссылки в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к новому средству для увеличения образования гетерологичных белков, которое содержит новые варианты области инициации трансляции (TIR), включая варианты TIR, содержащие котрансляционные сигнальные пептиды секреции (сигнальные пептиды, которые направляют транслокацию котрансляционным образом) и/или варианты TIR, содержащие посттрансляционные сигнальные пептиды секреции (сигнальные пептиды, которые направляют транслокацию посттрансляционным образом). Кроме того, в настоящем документе продемонстрировано увеличенное образование антител с использованием векторов, содержащих легкую цепь антитела, функционально связанную с TIR, содержащей ко- или посттрансляционный сигнальный пептид секреции, и тяжелую цепь антитела, функционально связанную с TIR, содержащей котрансляционный сигнальный пептид секреции для пиковой экспрессии. В настоящем документе предоставлены новые варианты TIR.
В одном из аспектов изобретение относится к вариантам областей инициации трансляции. В некоторых вариантах осуществления вариант содержит вариант области инициации трансляции (в некоторых вариантах осуществления прокариотическую посттрансляционную сигнальную последовательность секреции или прокариотическую котрансляционную сигнальную последовательность секреции). В некоторых вариантах осуществления вариант содержит варианты нуклеиновой кислоты сигнальной последовательности секреции, такой как PhoA, MalE, DsbA или STII. В некоторых вариантах осуществления вариант дополнительно содержит сайт рестрикции MlaI, BssHII или XbaI. В некоторых вариантах осуществления вариант содержит вариант области инициации трансляции, содержащий последовательность, представленную в таблице 3.
В одном из аспектов изобретение относится к вариантам сигнальных последовательностей секреции. В некоторых вариантах осуществления сигнальная последовательность секреции представляет собой прокариотическую посттрансляционную сигнальную последовательность секреции или прокариотическую котрансляционную сигнальную последовательность секреции. В некоторых вариантах осуществления сигнальная последовательность секреции представляет собой эукариотическую посттрансляционную сигнальную последовательность секреции или эукариотическую котрансляционную сигнальную последовательность секреции. В некоторых вариантах осуществления варианты представляют собой варианты нуклеиновой кислоты сигнальной последовательности секреции PhoA, MalE, DsbA или STII. В некоторых вариантах осуществления варианты содержат сигнальную последовательность секреции, представленную в таблице 3. Варианты сигнальных последовательностей секреции по изобретению пригодны для использования, например, в любом способе, описанном в настоящем документе.
В другом аспекте изобретение относится к полинуклеотиду, содержащему область инициации трансляции по изобретению. В некоторых вариантах осуществления область инициации трансляции содержит последовательность, представленную в таблице 3 (например, одну из SEQ ID NO: 1-42). В некоторых вариантах осуществления область инициации трансляции содержит одну из SEQ ID NO: 1-14, 16-24, 26-39, 41-42. Эти полинуклеотиды пригодны для использования, например, в любом из способов, описанных в настоящем документе.
В другом аспекте изобретение относится к полинуклеотиду, содержащему сигнальную последовательность секреции по изобретению. В некоторых вариантах осуществления сигнальная последовательность секреции содержит последовательность, представленную в таблице 3 (например, одну из SEQ ID NO: 1-42). В некоторых вариантах осуществления область инициации трансляции содержит одну из SEQ ID NO: 1-14, 16-24, 26-39, 41-42. Эти полинуклеотиды пригодны для использования, например, в любом из способов, описанных в настоящем документе.
В другом аспекте изобретение относится к полинуклеотиду, содержащему область инициации трансляции по изобретению, функционально связанную с полинуклеотидом, кодирующим гетерологичный полипептид, посредством чего при экспрессии гетерологичного полипептида в клетке-хозяине (например, прокариотической клетке-хозяине, например, клетке-хозяине E. coli) происходит укладка и сборка гетерологичного полипептида, чтобы сформировать биологически активный гетерологичный полипептид. Примеры гетерологичных полипептидов дополнительно описаны в настоящем документе. В некоторых вариантах осуществления гетерологичный полипептид представляет собой тяжелую цепь антитела. В некоторых вариантах осуществления гетерологичный полипептид представляет собой легкую цепь антитела. В некоторых вариантах осуществления гетерологичный полипептид представляет собой полипептид Fc. В некоторых вариантах осуществления гетерологичный полипептид представляет собой мультимерный полипептид. В некоторых вариантах осуществления гетерологичный полипептид представляет собой гетеромультимер. В некоторых вариантах осуществления область инициации трансляции представляет собой любую область инициации трансляции, описанную в настоящем документе, например, область инициации трансляции, которая содержит последовательность, представленную в таблице 3. В некоторых вариантах осуществления область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-42. В некоторых вариантах осуществления область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-14, 36-39, 41-42. В некоторых вариантах осуществления область инициации трансляции содержит вариант сигнальной последовательности STII, DsbI, PhoA или MalE.
В другом аспекте изобретение относится к полинуклеотиду, содержащему (1) первую область инициации трансляции (TIR), функционально связанную с полинуклеотидом, кодирующим первый гетерологичный полипептид, где TIR содержит котрансляционную прокариотическую сигнальную последовательность секреции; и (2) второй TIR, функционально связанный с полинуклеотидом, кодирующим второй гетерологичный, где второй TIR содержит котрансляционную или посттрансляционную прокариотическую сигнальную последовательность секреции, посредством чего при экспрессии антитела в клетке-хозяине происходит укладка и сборка первого и второго гетерологичных полипептидов, чтобы сформировать биологически активный полипептидный комплекс.
В другом аспекте изобретение относится к полинуклеотиду, кодирующему антитело, указанный полинуклеотид содержит (1) первую область инициации трансляции по изобретению, функционально связанную с полинуклеотидом, кодирующим тяжелую цепь антитела, и (2) вторую область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим легкую цепь антитела, посредством чего при экспрессии антитела в клетке-хозяине (например, прокариотической клетке-хозяине, например, клетке-хозяине E. coli) происходит укладка и сборка тяжелой и легкой цепей, чтобы сформировать биологически активное антитело.
В некоторых вариантах осуществления первая область инициации трансляции содержит котрансляционную прокариотическую сигнальную последовательность секреции (например, сигнальную последовательность, которая направляет трансляцию через сигнал-узнающий пептид). В некоторых вариантах осуществления первая область инициации трансляции содержит сигнальную последовательность STII или DsbA. В некоторых вариантах осуществления первая область инициации трансляции содержит сигнальную последовательность DsbA. В некоторых вариантах осуществления первая область инициации трансляции содержит сигнальную последовательность PhoA или MalE. В некоторых вариантах осуществления первая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-10 и 36-42. В некоторых вариантах осуществления первая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-10 и 36-29 и 41 и 42. В некоторых вариантах осуществления первая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-42. В некоторых вариантах осуществления первая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-14, 16-24, 26-39, 41-42.
В некоторых вариантах осуществления вторая область инициации трансляции содержит (i) котрансляционную прокариотическую сигнальную последовательность секреции или посттрансляционную прокариотическую сигнальную последовательность секреции (например, сигнальную последовательность, которая направляет трансляцию через путь sec). В некоторых вариантах осуществления вторая область инициации трансляции содержит сигнальную последовательность STII, DsbA, MalE или PhoA. В некоторых вариантах осуществления вторая область инициации трансляции содержит сигнальную последовательность PhoA или MalE. В некоторых вариантах осуществления вторая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-42. В некоторых вариантах осуществления вторая область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-14, 16-24, 26-39, 41-42.
В некоторых вариантах осуществления полинуклеотид, кодирующий антитело, дополнительно содержит (3) третью область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим полипептид Fc. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность STII, PhoA или DsbA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность DsbA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность PhoA.
В другом аспекте изобретение относится к полинуклеотиду, содержащему (1) первую область инициации трансляции (TIR), функционально связанную с полинуклеотидом, кодирующим тяжелую цепь антитела, где TIR содержит котрансляционную прокариотическую сигнальную последовательность секреции; и (2) вторую TIR, функционально связанную с полинуклеотидом, кодирующим легкую цепь антитела, где вторая TIR содержит котрансляционную или посттрансляционную прокариотическую сигнальную последовательность секреции, посредством чего при экспрессии антитела в клетке-хозяине происходит укладка и сборка тяжелой и легкой цепей, чтобы сформировать биологически активное антитело.
В другом аспекте изобретение относится к полинуклеотиду, кодирующему фрагмент антитела (такой как моновалентный фрагмент антитела), указанный полинуклеотид содержит (1) первую область инициации трансляции по изобретению, функционально связанную с полинуклеотидом, кодирующим тяжелую цепь антитела; (2) вторую область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим легкую цепь антитела; и (3) третью область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим полипептид Fc, посредством чего при экспрессии антитела в клетке-хозяине (например, прокариотической клетке-хозяине), происходит укладка и сборка тяжелой цепи, легкой цепи и полипептида Fc, чтобы сформировать биологически активное антитело (такой как антитело с одним Fab фрагментом). В некоторых вариантах осуществления третья область инициации трансляции содержит котрансляционную прокариотическую сигнальную последовательность секреции или посттрансляционную прокариотическую сигнальную последовательность секреции. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность STII, PhoA, MalE или DsbA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность DsbA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность PhoA. В некоторых вариантах осуществления третья область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-42. В некоторых вариантах осуществления третья область инициации трансляции содержит последовательность одной из SEQ ID NO: 1-14, 16-24, 26-39, 41-42.
В другом аспекте изобретение относится к полинуклеотиду, кодирующему антитело, указанный полинуклеотид содержит (1) первую область инициации трансляции по изобретению, функционально связанную с полинуклеотидом, кодирующим тяжелую цепь антитела, где первая область инициации трансляции содержит сигнальную последовательность STII или DsbA, и (2) вторую область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим легкую цепь антитела, где вторая область инициации трансляции содержит сигнальную последовательность STII, DsbA, MalE или PhoA, посредством чего при экспрессии антитела в клетке-хозяине (например, прокариотической клетке-хозяине) происходит укладка и сборка легкой и тяжелой цепей, чтобы сформировать биологически активное антитело. В некоторых вариантах осуществления первая область инициации трансляции содержит сигнальную последовательность DsbA, а вторая область инициации трансляции содержит сигнальную последовательность MalE или PhoA. В некоторых вариантах осуществления полинуклеотид, кодирующий антитело, дополнительно содержит (3) третью область инициации трансляции, функционально связанную с полинуклеотидом, кодирующим полипептид Fc. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность STII, PhoA или DsbA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность PhoA. В некоторых вариантах осуществления третья область инициации трансляции содержит сигнальную последовательность DsbA.
В некоторых вариантах осуществления интенсивность трансляции указанного варианта области инициации трансляции менее интенсивности трансляции области инициации трансляции дикого типа. В некоторых вариантах осуществления интенсивность трансляции указанного варианта области инициации трансляции превышает интенсивность трансляции область инициации трансляции дикого типа. В некоторых вариантах осуществления аминокислотная последовательность варианта области инициации трансляции не изменена относительно аминокислотной последовательности дикого типа. В некоторых вариантах осуществления аминокислотная последовательность варианта области инициации трансляции изменена относительно аминокислотной последовательности дикого типа. В некоторых вариантах осуществления область инициации трансляции содержит прокариотическую сигнальную последовательность секреции. В некоторых вариантах осуществления первая и вторая области инициации трансляции (и, в некоторых вариантах осуществления, третья область инициации трансляции) обеспечивают приблизительно одинаковые интенсивности трансляции. В некоторых вариантах осуществления относительная интенсивность трансляции составляет приблизительно один или два. В некоторых вариантах осуществления относительная интенсивность трансляции составляет приблизительно один. В некоторых вариантах осуществления относительная интенсивность трансляции составляет приблизительно два. В некоторых вариантах осуществления относительная интенсивность трансляции составляет один и/или два. В некоторых вариантах осуществления относительная интенсивность трансляции составляет приблизительно три или приблизительно четыре. В некоторых вариантах осуществления относительная интенсивность трансляции выбрана из одного или нескольких из 1, 2, 3, 4, 5 или более (например, 6 или 7 или более).
В некоторых вариантах осуществления полинуклеотид по изобретению дополнительно содержит промотор, функционально связанный с гетерологичным полипептидом. В некоторых вариантах осуществления промотор представляет собой прокариотический промотор, выбранный из группы, состоящей из промоторов phoA, tac, lpp, lac-lpp, lac, ara, trp и T7. В некоторых вариантах осуществления промотор представляет собой промотор phoA. В некоторых вариантах осуществления, включающих экспрессию тяжелой и легкой цепи антитела, полинуклеотид дополнительно содержит (a) первый промотор, где первый промотор функционально связан с легкой цепью и (b) второй промотор, где второй промотор функционально связан с тяжелой цепью. В некоторых вариантах осуществления первый и второй промоторы представляют собой промоторы phoA. В некоторых вариантах осуществления, включающих экспрессию тяжелой и легкой цепи антитела и полипептида Fc, полинуклеотид дополнительно содержит (c) третий промотор, где третий промотор функционально связан с полипептидом Fc. В некоторых вариантах осуществления третий промотор представляет собой полипептид Fc.
Когда экспрессируют полипептиды, которые содержат более чем один полипептид (например, антитело, содержащее тяжелую цепь и легкую цепь), полинуклеотид для экспрессии полипептида может представлять собой полицистронный полинуклеотид (т.е. один полинуклеотид, который содержит и экспрессирует несколько цистронов под регуляторным управлением одного промотора). Типичным примером полицистронного вектора является «бицистронный» вектор, который содержит и экспрессирует два различных полипептида под управлением одного промотора. При экспрессии бицистронного или полицистронного вектора сначала происходит транскрипция нескольких кодирующих областей (например, генов) в виде одной транскрипционной единицы, а затем раздельная трансляция. Цистрон относится к генетическому элементу, приблизительно эквивалентному трансляционной единице, содержащей нуклеотидную последовательность, кодирующую полипептидную цепь и смежные управляющие области (включая, например, TIR). В других вариантах осуществления полинуклеотид может содержать отдельные цистроны, которые относятся к одному полинуклеотиду, содержащему по меньшей мере две отдельные пары промотор-цистрон, где каждый цистрон находится под управлением своего собственного промотора. При экспрессии экспрессирующего вектора с отдельным цистроном, как процесс транскрипции, так и процесс трансляции различных генов происходит отдельно и независимо. В других вариантах осуществления полинуклеотид может содержать полицистронную часть и часть с отдельным цистроном.
В еще одном аспекте изобретение относится к векторам, содержащим полинуклеотид по изобретению. В некоторых вариантах осуществления векторы представляют собой экспрессирующие векторы.
В дополнительном аспекте изобретение относится к композициям, содержащим один или несколько полинуклеотидов по изобретению и носитель. В одном из вариантов осуществления носитель является фармацевтически приемлемым.
В одном из аспектов изобретение относится к клеткам-хозяевам, содержащим полинуклеотид или вектор по изобретению. В некоторых вариантах осуществления клетки-хозяева содержат полинуклеотид по изобретению, который кодирует антитело (в некоторых вариантах осуществления биспецифическое антитело или антитело с одним Fab фрагментом). Клетка-хозяин может содержать один или несколько полинуклеотидов, которые совместно кодируют антитело. Вектор может относиться к любому типу, например, к рекомбинантным векторам, таким как экспрессирующие векторы. Можно использовать любую из множества клеток-хозяев. В одном из вариантов осуществления клетка-хозяин представляет собой прокариотическую клетку, например, E. coli. В некоторых вариантах осуществления E. coli представляет собой штамм с дефицитом активностей эндогенных протеаз. В некоторых вариантах осуществления в генотипе E. coli отсутствуют гены degP и prc и присутствует мутантный ген spr.
В некоторых вариантах осуществления клетка-хозяин дополнительно содержит полинуклеотид, кодирующий прокариотический шаперон (такой как белки Dsb (DsbA, DsbB, DsbC, DsbD, FkpA и/или DsbG). В некоторых вариантах осуществления в клетке-хозяине происходит сверхэкспрессия шаперона. В некоторых вариантах осуществления шаперон представляет собой DsbA и/или DsbC.
В одном из аспектов клетка-хозяин содержит один или несколько полинуклеотидов, которые совместно кодируют антитело с одним Fab фрагментом. В одном из вариантов осуществления один полинуклеотид кодирует (a) компоненты легкой и тяжелой цепей антитела с одним Fab фрагментом, и (b) полипептид Fc. В одном из вариантов осуществления один полинуклеотид кодирует компоненты легкой цепи и полипептида Fc антитела с одним Fab фрагментом, и отдельный полинуклеотид кодирует полипептид тяжелой цепи. В одном из вариантов осуществления один полинуклеотид кодирует компоненты тяжелой цепи и полипептида Fc антитела с одним Fab фрагментом и отдельный полинуклеотид кодирует компонент легкой цепи антитела с одним Fab фрагментом. В одном из вариантов осуществления отдельные полинуклеотиды кодируют компонент легкой цепи антитела с одним Fab фрагментом, компонент тяжелой цепи антитела с одним Fab фрагментом и полипептид Fc, соответственно.
В настоящем документе описаны гетерологичные полипептиды. В некоторых вариантах осуществления гетерологичный полипептид представляет собой антитело. В некоторых вариантах осуществления антитело представляет собой моноклональное антитело. В других вариантах осуществления антитело представляет собой поликлональное антитело. В некоторых вариантах осуществления антитело выбирают из группы, состоящей из химерного антитела, аффинно зрелого антитела, гуманизированного антитела и антитела человека. В определенных вариантах осуществления антитело представляет собой биспецифическое антитело. В определенных вариантах осуществления антитело представляет собой фрагмент антитела. В некоторых вариантах осуществления антитело представляет собой моновалентное антитело. В некоторых вариантах осуществления антитело представляет собой Fab, Fab', Fab'-SH, F(ab')2 или scFv. В некоторых вариантах осуществления антитело представляет собой антитело с одним Fab фрагментом (т.е. вариабельный домен тяжелой цепи и вариабельный домен легкой цепи формируют один антигенсвязывающий фрагмент), содержащее Fc-область, где Fc-область содержит первый и второй полипептиды Fc, где первый и второй полипептиды Fc представлены в комплексе и формируют Fc-область, которая повышает стабильность указанного фрагмента антитела по сравнению с молекулой Fab, содержащей указанный антигенсвязывающий фрагмент.
В некоторых вариантах осуществления антитело связывает (в некоторых вариантах осуществления специфически связывает) c-met. В некоторых вариантах осуществления антитело против c-met содержит (a) первый полипептид, содержащий вариабельный домен тяжелой цепи, который имеет последовательность:
последовательность CH1 и первый полипептид Fc; (b) второй полипептид, содержащий вариабельный домен легкой цепи, который имеет последовательность:
и последовательность CL1; и (c) третий полипептид, содержащий второй полипептид Fc, где вариабельный домен тяжелой цепи и вариабельный домен легкой цепи представлены в виде комплекса и формируют один антигенсвязывающий фрагмент, где первый и второй полипептиды Fc представлены в виде комплекса и формируют Fc-область, которая повышает стабильность указанного фрагмента антитела по сравнению с молекулой Fab, содержащей указанный антигенсвязывающий фрагмент. В некоторых вариантах осуществления первый полипептид содержит последовательность Fc, изображенную на фиг.7 (SEQ ID NO: 68), а второй полипептид содержит последовательность Fc, изображенную на фиг.8 (SEQ ID NO: 47). В некоторых вариантах осуществления первый полипептид содержит последовательность Fc, изображенную на фиг.8 (SEQ ID NO: 47), и второй полипептид содержит последовательность Fc, изображенную на фиг.7 (SEQ ID NO: 68).
В некоторых вариантах осуществления антитело против c-met содержит (a) первый полипептид, содержащий вариабельный домен тяжелой цепи, указанный полипептид содержит последовательность:
(b) второй полипептид, содержащий вариабельный домен легкой цепи, полипептид содержит последовательность
и третий полипептид, содержащий полипептид Fc, полипептид содержит последовательность
где вариабельный домен тяжелой цепи и вариабельный домен легкой цепи представлены в виде комплекса и формируют один антигенсвязывающий фрагмент, где первый и второй полипептиды Fc представлены в виде комплекса и формируют Fc-область, которая повышает стабильность указанного фрагмента антитела по сравнению с молекулой Fab, содержащей указанный антигенсвязывающий фрагмент.
В одном из вариантов осуществления антитело против c-met содержит вариабельный домен тяжелой цепи, который содержит одну или несколько из последовательностей CDR1-HC, CDR2-HC и CDR3-HC, изображенных на фиг.7 (SEQ ID NO: 52-53 и 66). В некоторых вариантах осуществления антитело содержит вариабельный домен легкой цепи, содержащий одну или несколько из последовательностей CDR1-LC, CDR2-LC и CDR3-LC, изображенных на фиг.7 (SEQ ID NO: 49-51). В некоторых вариантах осуществления вариабельный домен тяжелой цепи содержит последовательности FR1-HC, FR2-HC, FR3-HC и FR4-HC, изображенные на фиг.7 (SEQ ID NO: 62-65). В некоторых вариантах осуществления вариабельный домен легкой цепи содержит последовательности FR1-LC, FR2-LC, FR3-LC и FR4-LC, изображенные на фиг.7 (SEQ ID NO: 57-60).
В некоторых вариантах осуществления антитело содержит по меньшей мере одну характеристику, которая способствует гетеродимеризации, при этом минимизируя гомодимеризацию последовательностей Fc в фрагменте антитела. Такая характеристика(и) повышает выход и/или чистоту и/или гомогенность популяций иммуноглобулинов, получаемых способами по изобретению, как описано в настоящем документе. В одном из вариантов осуществления первый полипептид Fc и второй полипептид Fc встречаются/взаимодействуют в области контакта. В некоторых вариантах осуществления, где первый и второй полипептиды Fc встречаются в области контакта, область контакта второго полипептида (последовательности) Fc содержит выпуклость (также называемый «выступ»), которую можно разместить в полости (также обозначаемой «отверстием») в области контакта первого полипептида (последовательности) Fc. В одном из вариантов осуществления антитело содержит мутации Fc, образующие «выступы» и «отверстия», как описано в WO 2005/063816. Например, мутация отверстия может представлять собой одну или несколько из T366A, L368A и/или Y407V в полипептиде Fc, а мутация выступа может представлять собой T366W.
Изобретение также относится к способам, в которых используют вариант TIR и сигнальные последовательности по изобретению. Понятно, что любое из варианта TIR, сигнальных последовательностей и полинуклеотидов, описанных в настоящем документе, пригодно для использования в способах, например, способах по изобретению, описанных в настоящем документе. В дополнительном аспекте изобретение относится к способам получения гетерологичного полипептида по изобретению. Например, изобретение относится к способам получения гетерологичного полипептида (например, антитела, которое, как определено в настоящем документе, включает полноразмерное антитело и его фрагменты), указанный способ включает культивирование клетки-хозяина, содержащей полинуклеотид по изобретению (например, полинуклеотид, содержащий область инициации трансляции) с тем, чтобы экспрессировать полинуклеотид, посредством чего при экспрессии указанного полинуклеотида в клетке-хозяине (например, прокариотической клетке-хозяине) происходит укладка гетерологичного полипептида, чтобы сформировать биологически активный гетерологичный полипептид. В вариантах осуществления, включающих экспрессию антител, при экспрессии указанного полинуклеотида в клетке-хозяине происходит укладка и сборка легкой и тяжелой цепей, чтобы сформировать биологически активное антитело. В некоторых вариантах осуществления способ дополнительно включает извлечение гетерологичного полипептида (например, антитела) из культуры клетки-хозяина. В некоторых вариантах осуществления гетерологичный полипептид извлекают из среды для культивирования клетки-хозяина. В некоторых вариантах осуществления способ дополнительно включает объединение извлеченного гетерологичного полипептида (например, антитела) с фармацевтически приемлемым носителем, эксципиентом или носителем для получения фармацевтического состава, содержащего гетерологичный полипептид (например, антитело).
В одном из аспектов изобретение относится к способам секреции гетерологичного полипептида, представляющего интерес, из клетки, указанный способ включает культивирование клетки-хозяина, содержащей полинуклеотид по изобретению, с тем, чтобы экспрессировать полинуклеотид и секретировать гетерологичный полипептид.
В одном из аспектов изобретение относится к способам транслокации гетерологичного полипептида, представляющего интерес, из клетки, указанный способ включает культивирование клетки-хозяина, содержащей полинуклеотид по изобретению, с тем чтобы экспрессировать полинуклеотид и транслоцировать гетерологичный полипептид.
В другом аспекте изобретение относится к способу оптимизации секреции гетерологичного полипептида, представляющего интерес, в клетке, который содержит сравнение уровней экспрессии полипептида под управлением группы полинуклеотидных вариантов области инициации трансляции, где группа вариантов представляет диапазон интенсивностей трансляции, и определение оптимальной интенсивности трансляции для получения зрелого полипептида. В некоторых вариантах осуществления оптимальная интенсивность трансляции ниже интенсивности трансляции области инициации трансляции дикого типа. В некоторых вариантах осуществления оптимальная интенсивность трансляции выше интенсивности трансляции области инициации трансляции дикого типа. В некоторых вариантах осуществления варианты содержат полинуклеотидные варианты сигнальной последовательности секреции. В некоторых вариантах осуществления варианты сигнальных последовательностей секреции представляют собой сигнальные последовательности пути sec и/или сигнальные последовательности пути SRP. В некоторых вариантах осуществления варианты сигнальных последовательностей секреции представляют собой варианты сигнальных последовательностей PhoA, MalE, DsbA или STII. В некоторых вариантах осуществления вариант представляет собой один или несколько вариантов, представленных в таблице 3. В некоторых вариантах осуществления вариант содержит последовательность одной из SEQ ID NO: 1-14, 36-39, 41-42.
В одном из аспектов изобретение относится к гетерологичному полипептиду, полученному способом по изобретению, как описано в настоящем документе. В некоторых вариантах осуществления гетерологичный полипептид представляет собой антитело.
В одном из аспектов изобретение относится к использованию гетерологичного полипептида, созданного с использованием способов по изобретению, в получении лекарственного средства для терапевтического и/или профилактического лечения заболевания, такого как злокачественная опухоль, опухоль, клеточное пролиферативное нарушение и/или иммунное (такое как аутоиммунное) нарушение. Гетерологи