Препарат антитела, обогащенного изоформами и способ его получения
Иллюстрации
Показать всеИзобретения относятся к области биохимии. Описана группа изобретений, включающая способ получения обогащенного изоформами препарата антител (варианты). В одном варианте способ получения обогащенного изоформами препарата антител включает этапы: а) нанесение буферного раствора, содержащего различные изоформы антител на материал катионообменной хроматографии, б) нанесение первого раствора с первой проводимостью на материал катионообменной хроматографии, при этом изоформы антител остаются связанными с материалом катионообменной хроматографии, и в) нанесение второго раствора со второй проводимостью на материал катионообменной хроматографии и тем самым получение препарата антител, где проводимость первого раствора составляет от 4 мСм/см до 5мСм/см, где проводимость второго раствора превышает проводимость первого раствора не более чем на 10%. В другом варианте способ получения изоформами препарата антител включает этапы: а) культивирование клеток млекапитающего, содержащих нуклеиновую кислоту, кодирующую антитело, и выделение антитела из клеток или культуральной среды, б) очистка антитела по меньшей мере одним этапом колоночной хроматографии. Изобретение расширяет арсенал способов получения препаратов антител. 2 н. и 8 з.п. ф-лы, 6 ил., 2 табл, 7 пр.
Реферат
В данном документе описан способ получения препарата антител, включающий этап способа элюирования на материале катионообменной хроматографии.
Уровень техники.
Хорошо известны и широко используются различные способы очистки белка, такие как аффинная хроматография с микробными белками (например, протеин A или протеин G аффинная хроматография), ионообменная хроматография (например, катионообменная (карбоксиметиловые смолы), анионообменная (аминоэтиловые смолы) и смешанного режима обмена), тиофильная адсорбция (например, с бета-меркаптоэтанолом и другими SH-лигандами), хроматография гидрофобного взаимодействия или ароматическо-адсорбционная хроматография (например, с фенил-сефарозой, аза-аренофильными смолами, или м-аминофенилбороновой кислотой) металл-хелатная аффинная хроматография (например, с Ni (II) - и Cu (II) аффинным материалом), гельфильтрация и электрофоретические методы (например, гель-электрофорез, капиллярный электрофорез) (Vijayalakshmi, М.А., Appl. Biochem. Biotech. 75 (1998) 93-102).
Промышленная очистка фармацевтических антител, особенно развитие, эксплуатация и ратификация процессов хроматографии описаны у Fahrner, R.L., et al., in Biotechnol. Gen. Eng. Rev. 18 (2001) 301-327. Follman, D.K. и Fahrner, R.L. (J. Chrom. A 1024 (2004) 79-85), описывают факториальный скрининг процессов очистки антител, используя три хроматографических этапа без протеина A. Захват человеческих моноклональных антител из супернатанта клеточной культуры ионообменной средой, имеющей высокую плотность заряда, описан Necina, R., et al. (Biotechnol. and Bioeng. 60 (1998) 689-698). Очистка белков с помощью ионообменной хроматографии описана в WO 99/057134. В WO 2004/076485 описана очистка антител путем протеин A и ионообменной хроматографии. В US 5,429,746 описана очистка антител. Очистка белков описана в WO 2003/066662.
WO 2006/125599 описывает способ очистки антител. Очистка антител путем протеин A и ионообменной хроматографии описывается в WO 2004/076485.
Краткое описание изобретения
Было обнаружено, что хроматографическое разделение и/или обогащение изоформами антител возможно при подходящем увеличении проводимости подвижной фазы материала катионообменной хроматографии. Требуемое увеличение проводимости составляет не более 50%, то есть второй раствор имеет проводимость от 101% до 150% от проводимости первого раствора.
Таким образом, одним аспектом, как описано в настоящем документе, является способ изготовления препарата антител, включающий следующие этапы:
а) нанесение буферного раствора, содержащего различные изоформы антител на материал катионообменной хроматографии,
б) нанесение первого раствора с первой проводимостью на материал катионообменной хроматографии, при этом изоформы антител остаются связанными с материалом катионообменной хроматографии, а также
в) нанесение второго раствора со второй проводимостью на материал катионообменной хроматографии и тем самым получение препарата антител,
где проводимость второго раствора превышает проводимость первого раствора, по крайней мере, на 1%, но не более чем на 50%.
В одном варианте исполнения проводимость второго раствора превышает проводимость первого раствора, по крайней мере, на 1%, но не более чем на 20%.
В одном варианте исполнения проводимость второго раствора превышает проводимость первого раствора, по крайней мере, на 1%, но не более чем на 15%.
В одном варианте исполнения проводимость второго раствора превышает проводимость первого раствора, по крайней мере, на 1%, но не более чем на 10%.
В одном варианте исполнения раствор стадии а) имеет такую же проводимость, как раствор стадии б). В одном варианте исполнения буферный раствор, содержащий различные изоформы антител, имеет первую проводимость и первый раствор имеет ту же (первую) проводимость.
В одном варианте исполнения материал катионообменной хроматографии содержит набухающую матрицу. В одном варианте исполнения набухающей матрицей является агароза.
В одном варианте исполнения материал катионообменной хроматографии является сильным материалом катионообменной хроматографии. В одном варианте исполнения сильным материалом катионообменной хроматографии является материал сульфопропил-катионообменной хроматографии.
В одном варианте исполнения происходит одноступенчатая замена первого раствора на второй раствор. В одном варианте исполнения одна ступень является изменением от 100% по объему первого раствора до 100% по объему второго раствора.
В одном варианте исполнения первый раствор изменяется на второй раствор по линейному градиенту. В одном варианте исполнения линейный градиент составляет приблизительно 30 объемов колонки. В одном варианте исполнения линейный градиент составляет приблизительно 20 объемов колонки.
В одном варианте исполнения первый раствор содержит 20 мМ цитрат натрия.
В одном варианте исполнения второй раствор содержит 20 мМ цитрат натрия и 5 мМ хлорид натрия.
В одном варианте исполнения первый раствор содержит 25 мМ трис-(гидроксиметил)-аминометан и 10 мМ хлорид натрия.
В одном варианте исполнения второй раствор содержит 25 мМ трис-(гидроксиметил)-аминометан и 70 мМ хлорид натрия.
В одном варианте исполнения второй раствор содержит 25 мМ трис-(гидроксиметил)-аминометан и 45 мМ хлорид натрия.
В одном варианте исполнения первый и второй растворы являются водными растворами.
В одном варианте исполнения антитела представляют собой анти-HER2 антитела. В одном варианте анти-HER2 антитела являются анти-HER2 антителами Трастузумаб или анти-HER2 антителами Пертузумаб. В одном варианте анти-HER2 антитела являются гуманизированными анти-HER2 антителами.
В данном документе в качестве другого аспекта описан препарат антител, полученный способом, как описано в данном документе. В одном варианте исполнения антитела представляют собой анти-HER2 антитела.
Другим аспектом, как описано в данном документе, является способ получения препарата антитела, включающий следующие этапы:
а) культивирование клеток млекопитающих, содержащих нуклеиновую кислоту, кодирующую антитело, и выделение антител из клеток или культуральной среды,
б) очистка антител по крайней мере одной стадией колоночной хроматографии, где по меньшей мере один этап колоночной хроматографии включает следующие этапы:
1) нанесение буферного раствора, содержащего различные изоформы антител на материал катионообменной хроматографии,
2) нанесение первого раствора с первой проводимостью на материал катионообменной хроматографии, при этом изоформы антител остаются связанными с материалом катионообменной хроматографии, а также
3) нанесение второго раствора со второй проводимостью на материал катионообменной хроматографии и, таким образом, получение препарата антител,
где проводимость второго раствора превышает проводимость первого раствора, по крайней мере, на 1%, но не более чем на 10%.
В одном варианте исполнения всех аспектов, описанных в данном документе, первый раствор имеет проводимость от 4 мСм/см до 5 мСм/см.
Описание изобретения
В данном документе описан способ получения препарата антител, включающий этапы: 1) нанесение буферного раствора, содержащего различные изоформы антител, на материал катионообменной хроматографии; 2) нанесение первого раствора с первой проводимостью на материал катионообменной хроматографии, при этом изоформы антител остаются связанными с материалом катионообменной хроматографии; 3) нанесение второго раствора со второй проводимостью на материал катионообменной хроматографии и тем самым получение препарата антител, где проводимость второго раствора превышает проводимость первого раствора не более чем на 50%.
В общем, моноклональные антитела (mAb), полученные рекомбинантным способом, выделяют из супернатанта культивируемых продуцирующих клеток, таких как ВНК, или Sp2/0, или CHO, или HEK клетки. Одновременно также выделяют другие белковые соединения, а также различные изоформы антител. Изоформы антител различаются лишь незначительными структурными характеристиками, такими как паттерн гликозилирования, гетерогенность C-концевого лизина тяжелой цепи и частичное деамидирование аспарагиновых или глутаминовых аминокислотных остатков.
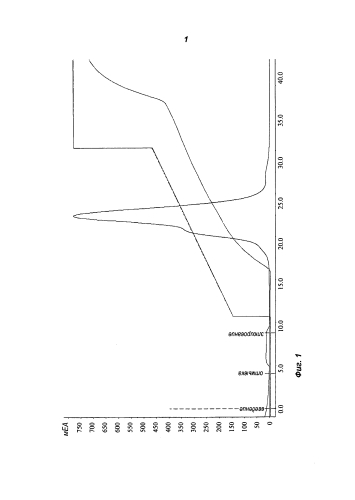
Антитело выделяют с колонки/материала катионообменной хроматографии, используя общие хроматографические методы, в одном (симметричном) пике (см., например, Пример 6 и Фиг.5).
Было обнаружено, что изоформы антител могут быть обогащены или частично разделены друг от друга с помощью способа катионообменной хроматографии. Разделение/обогащение достигается хроматографическим способом связывание-элюирование, используя градиент pH или градиент соли и используя градиент с особенно небольшим уклоном.
Было обнаружено, что обогащение препарата антител изоформами антител возможно с помощью колоночной хроматографии с подходящим увеличением проводимости подвижной фазы.
В одном варианте исполнения увеличение проводимости составляет 50% или менее, т.е. проводимость возрастает от 100% по крайней мере до 101% и не более чем до 150%, начиная с первого уровня до второго, более высокого уровня, для того чтобы осуществить элюирование антител.
В одном варианте исполнения увеличение проводимости составляет 10% или менее, т.е. проводимость возрастает от 100% по крайней мере до 101% и не более чем до 110%, начиная с первого уровня до второго, более высокого уровня, для того чтобы осуществить элюирование антител.
Было обнаружено, что матрица материала катионообменной хроматографии должна быть набухающей матрицей.
В одном варианте исполнения матрица представляет собой поперечно-сшитый сахарид. В одном варианте исполнения сахарид представляет собой полисахарид. В одном варианте исполнения полисахарид представляет собой агарозу, т.е. полисахарид, состоящий из гликозидно связанных D-галактозы и 3,6-ангидро-L-галактозы.
Увеличение может быть одноступенчатым. Таким образом, увеличение может быть выполнено путем полной смены элюирующего раствора, то есть со 100% первого буферного раствора до 100% второго (= элюирующего) буферного раствора.
Увеличение может быть в виде линейного градиента. Таким образом, увеличение может быть выполнено с помощью линейной смены элюирующего раствора, то есть со 100% первого буферного раствора до от 50% до 100% второго (= элюирующего) буферного раствора.
В одном варианте исполнения первый раствор сменяется на второй раствор по линейному градиенту. В одном варианте исполнения линейный градиент осуществляется в течение приблизительно 50 объемов колонки. В одном варианте исполнения линейный градиент осуществляется в течение приблизительно 30 объемов колонки. В одном варианте исполнения линейный градиент осуществляется в течение приблизительно 20 объемов колонки.
Общие хроматографические методы и их применение известны специалисту в данной области. См., например, Heftmann, Е., (ed.), Chromatography, 5th edition, Part A: Fundamentals and Techniques, Elsevier Science Publishing Company, New York, (1992); Deyl, Z., (ed.) Advanced Chromatographic and Electromigration Methods in Biosciences, vol. 60, Elsevier Science BV, Amsterdam, The Netherlands, (1998); Poole, C.F., and Poole, S.K., Chromatography Today, Elsevier Science Publishing Company, New York, (1991); Scopes, Protein Purification: Principles and Practice, Springer Verlag, (1982); Sambrook, J., et al., (ed.), Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., (1989); или Ausubel, F.M., et al., (eds.), Current Protocols in Molecular Biology, John Wiley & Sons, Inc., New York, (1998).
В следующей Таблице проводимости некоторых буферных растворов, которые обычно используются, даны как референсные.
| Таблица | |||||
| Буфер | NaCl [г/л] | буферная соль [г/л] | pH | проводимость [мСм/см] | изменение проводимости [%] |
| 10 мМ цитрат натрия | - | 1.92 | 5.5 | 1.74 | - |
| 20 мМ цитрат натрия | - | 3.84 | 5.5 | 3.49 | +101 |
| 30 мМ цитрат натрия | - | 5.76 | 5.5 | 5.05 | +190 |
| 40 мМ цитрат натрия | - | 7.68 | 5.5 | 6.45 | +271 |
| 50 мМ цитрат натрия | - | 9.60 | 5.5 | 8.04 | +362 |
| 10 мМ цитрат натрия с 25 мМ NaCl | 1.46 | 1.92 | 5.5 | 4.87 | - |
| 10 мМ цитрат натрия с 50 мМ NaCl | 2.92 | 1.92 | 5.5 | 7.34 | +51 |
| 10 мМ цитрат натрия с 100 мМ NaCl | 5.84 | 1.92 | 5.5 | 12.21 | +151 |
| 10 мМ цитрат натрия с 150 мМ NaCl | 8.77 | 1.92 | 5.5 | 17.17 | +253 |
| 10 мМ цитрат натрия с 200 мМ NaCl | 11.69 | 1.92 | 5.5 | 21.70 | +346 |
| Буфер | NaCl [г/л] | буферная соль [г/л] | pH | проводимость [мСм/см] | изменение проводимости [%] |
| 20 мМ цитрат натрия с 25 мМ NaCl | 1.46 | 3.84 | 5.5 | 6.65 | - |
| 20 мМ цитрат натрия с 50 мМ NaCl | 2.92 | 3.84 | 5.5 | 9.12 | +37 |
| 20 мМ цитрат натрия с 100 мМ NaCl | 5.84 | 3.84 | 5.5 | 13.82 | +108 |
| 20 мМ цитрат натрия с 150 мМ NaCl | 8.77 | 3.84 | 5.5 | 18.37 | +176 |
| 20 мМ цитрат натрия с 200 мМ NaCl | 11.69 | 3.84 | 5.5 | 22.80 | +243 |
| 30 мМ цитрат натрия с 25 мМ NaCl | 1.46 | 5.76 | 5.5 | 8.37 | - |
| 30 мМ цитрат натрия с 50 мМ NaCl | 2.92 | 5.76 | 5.5 | 10.65 | +27 |
| 30 мМ цитрат натрия с 100 мМ NaCl | 5.84 | 5.76 | 5.5 | 15.15 | +81 |
| 30 мМ цитрат натрия с 150 мМ NaCl | 8.77 | 5.76 | 5.5 | 19.69 | +135 |
| 30 мМ цитрат натрия с 200 мМ NaCl | 11.69 | 5.76 | 5.5 | 24.10 | +188 |
| 40 мМ цитрат натрия с 25 мМ NaCl | 1.46 | 7.68 | 5.5 | 9.78 | - |
| 40 мМ цитрат натрия с 50 мМ NaCl | 2.92 | 7.68 | 5.5 | 12.12 | +24 |
| 40 мМ цитрат натрия с 100 мМ NaCl | 5.84 | 7.68 | 5.5 | 16.71 | +71 |
| 40 мМ цитрат натрия с 150 мМ NaCl | 8.77 | 7.68 | 5.5 | 21.20 | +117 |
| 40 мМ цитрат натрия с 200 мМ NaCl | 11.69 | 7.68 | 5.5 | 25.30 | +159 |
| Буфер | NaCl [г/л] | буферная соль [г/л] | pH | проводимость [мСм/см] | изменение проводимости [%] |
| 50 мМ цитрат натрия с 25 мМ NaCl | 1.46 | 9.60 | 5.5 | 11.31 | - |
| 50 мМ цитрат натрия с 50 мМ NaCl | 2.92 | 9.60 | 5.5 | 13.61 | +20 |
| 50 мМ цитрат натрия с 100 мМ NaCl | 5.84 | 9.60 | 5.5 | 18.19 | +61 |
| 50 мМ цитрат натрия с 150 мМ NaCl | 8.77 | 9.60 | 5.5 | 22.40 | +98 |
| 50 мМ Цитрат натрия с 200 мМ NaCl | 11.69 | 9.60 | 5.5 | 26.70 | +136 |
| 25 мМ MES c 50 мМ NaCl | 2.92 | 5.53 | 5.6 | 7.65 | - |
| 25 мМ MES c 95 мМ NaCl | 5.55 | 5.53 | 5.6 | 12.15 | +59 |
| 25 мМ MES с 50 мМ NaCl и 5 г/л Герцептин® | - | 7.48 | 5.53 | 7.66 | - |
| 25 мМ MES с 95 мМ NaCl и 5 г/л Герцептин® | - | 11.26 | 5.50 | 12.22 | +60 |
| 25 мМ MES с 50 мМ NaCl и 15 г/л Герцептин® | - | 7.11 | 5.50 | 7.52 | - |
| 25 мМ MES с 95 мМ NaCl и 15 г/л Герцептин® | - | 9.22 | 5.50 | 11.97 | +59 |
| 20 мМ цитрат натрия | - | 3.84 | 6.2 | 4.22 | - |
| 20 мМ цитрат натрия с 5 мМ NaCl | 0.29 | 3.84 | 6.2 | 4.62 | +9 |
Термин "нанесение на" означает частичный этап способа очистки, в котором раствор вносится в контакт с материалом хроматографии. Это означает что либо а) раствор добавляют в хроматографическое устройство, в котором содержится материал хроматографии, или б) материал хроматографии добавляют в раствор. В случае а) раствор проходит через устройство, позволяя осуществлять взаимодействие между материалом хроматографии и веществами, содержащимися в растворе. В зависимости от условий, таких как, например, pH, проводимость, концентрация соли, температура и/или скорость потока, некоторые вещества из раствора могут быть связаны с материалом хроматографии, а другие вещества могут быть извлечены с материала хроматографии. Вещества, остающиеся в растворе или извлеченные с материала хроматографии, могут быть найдены в протоке. "Проток" означает раствор, полученный после прохождения через устройство, который может быть либо раствором для нанесения или буферным раствором, который используется для промывки колонки или для элюирования веществ, связанных с материалом хроматографии. В одном варианте исполнения устройство представляет собой колонку или кассету. В случае б) материал хроматографии может быть добавлен, например, в виде твердого вещества к раствору, например, содержащему интересующее вещество, которое должно быть очищено, что позволяет осуществить взаимодействие между материалом хроматографии и веществом в растворе. После взаимодействия материал хроматографии удаляется, например, фильтрацией, и вещество, связанное с материалом хроматографии, также удаляется с ним из раствора, в то время как вещества, не связанные с материалом хроматографии, остаются в растворе.
Термин "режим связывание-элюирование" означает режим работы этапа хроматографии, в котором раствор, содержащий интересующее вещество, которое должно быть очищено, наносят на материал хроматографии, в результате чего интересующее вещество связывается с материалом хроматографии. Таким образом, интересующее вещество удерживается на материале хроматографии, тогда как вещества, не представляющие интереса, удаляются с протоком или супернатантом. Интересующее вещество впоследствии выделяется с материала хроматографии на втором этапе с элюирующим раствором. В одном из вариантов исполнения способ, как описано в данном документе, работает в режиме связывание-элюирование.
Растворы, используемые в способе, как описано в данном документе, являются неочищенными или буферными растворами. Термин "буферный раствор" обозначает раствор, в котором изменения pH в результате добавления или высвобождения кислотных или щелочных веществ выравниваются при помощи растворенного буферного вещества. Любое буферное вещество с такими свойствами может быть использовано. Как правило, используются буферные вещества, фармацевтически приемлемые. В одном варианте исполнения буферный раствор выбирают из фосфатного буферного раствора, состоящего из фосфорной кислоты и/или ее солей, или ацетатного буферного раствора, состоящего из уксусной кислоты и/или ее солей, или цитратного буферного раствора, состоящего из лимонной кислоты и/или ее солей, или морфолин буферного раствора, или 2-(N-морфолино) этансульфонового буферного раствора, или гистидинового буферного раствора, или глицинового буферного раствора, или трис (гидроксиметил) аминометанового (трис) буферного раствора. В другом варианте исполнения буферный раствор выбирают из фосфатного буферного раствора, или ацетатного буферного раствора, или цитратного буферного раствора, или гистидинового буферного раствора. При необходимости буферный раствор может содержать дополнительные соли, такие как, например, хлорид натрия, сульфат натрия, хлорид калия, сульфат калия, цитрат натрия или цитрат калия.
Термины "градиентное элюирование" и "способ градиентного элюирования", которые в этом приложении используются как взаимозаменяемые, означают способ, в котором проводимость раствора, вызывающего элюирование, т.е. высвобождение связанного соединения с материала хроматографии, изменяется, т.е. поднимается или опускается непрерывно, т.е. концентрация изменяется последовательными малыми ступенями, каждая из которых не больше, чем изменение на 2% или на 1% от концентрации вещества, вызывающего элюирование. В этом "непрерывном элюировании" одно или более условий, например pH, ионная сила, концентрация соли, и/или поток хроматографии, могут быть изменены линейно, или экспоненциально, или асимптотически. В одном варианте исполнения изменение является линейным.
Термин "ступенчатое элюирование" означает способ, в котором, например, концентрация вещества, вызывающего элюирование, т.е. высвобождение связанного вещества с материала хроматографии, поднимается или опускается сразу, т.е. непосредственно от одного значения/уровня к следующему значению/уровню. В этом "ступенчатом элюировании" одно или более условий, например, pH, ионная сила, концентрация соли, и/или поток хроматографии, могут быть изменены все сразу от первого, например, начального значения до второго, например, финального значения. Таким образом, условия изменяются постепенно, т.е. ступенчато, в отличие от линейного изменения.
Термин "материал ионообменной хроматографии" означает неподвижную матрицу с высоким молекулярным весом, которая несет ковалентно связанные заряженные замещающие группы, используемые в качестве неподвижной фазы в ионообменной хроматографии. Для полной зарядовой нейтральности не ковалентно связанные противоионы также присоединены к ней. "Материал ионообменной хроматографии" имеет способность обменивать свои не ковалентно связанные противоионы на одинаково заряженные ионы из окружающего раствора. В зависимости от заряда замещающих его противоионов "ионообменные смолы" относятся к катионообменным смолам или анионообменным смолам. В зависимости от характера заряженной группы (замещающей группы) "ионообменная смола" относится, например, в случае катионообменных смол к смолам сульфоновой кислоты (S), или к сульфопропиловым смолам (SP), или к карбоксиметиловым смолам (CM).
Различные типы ионообменных материалов, то есть неподвижных фаз, доступны под разными названиями и разного производства множества компаний, таких как, например, катионообменные материалы Bio-Rex® (например, тип 70), Chelex® (например, тип 100), Macro-Prep® (например, типа CM, High S, 25 S), AG® (например, типа 50W, MP) производства BioRad лаборатории, WCX 2 производства Ciphergen, Dowex® МАС-3 производства Dow chemical company, Mustang C и Mustang S производства Pall Corporation, Cellulose CM (например, типа 23, 52), hyper-D, partisphere производства Whatman pic, Amberlite® IRC (например, типа 76, 747, 748), Amberlite® GT 73, Toyopearl® (например, типа SP, CM, 650M) производства Tosoh Bioscience GmbH, CM 1500 и CM 3000 производства BioChrom Labs, SP-Sepharose™, CM-Sepharose™ производства GE Healthcare, смолы Poros производства PerSeptive Biosystems, Asahipak ES (например, типа 502C), CXpak P, IEC CM (например, тип 825, 2825, 5025, LG), IEC SP (например, тип 420N, 825), IEC QA (например, типа LG, 825), производства Shoko America Inc., 50W катионообменная смола производства Eichrom Technologies Inc. В одном варианте исполнения катионообменный материал является сильным катионообменным материалом, таким как Macro-Prep® High S или 25S, или MacroCap SP, или Toyopearl® SP 650M, или Source S, или SP Sepharose, или POLYCAT A, или Mono S, или Highscreen SP.
Для специалиста в данной области техники хорошо известны процедуры и методы для преобразования аминокислотной последовательности, например полипептида, в соответствующую последовательность нуклеиновой кислоты, кодирующую эту аминокислотную последовательность. Таким образом, нуклеиновая кислота характеризуется последовательностью ее нуклеиновой кислоты, состоящей из отдельных нуклеотидов, а также аминокислотной последовательностью полипептида, кодируемого ею.
Термин "в условиях, подходящих для связывания» и его грамматические эквиваленты, используемые в этом приложении, означает, что интересующее вещество, например, изоформы антител, связывается с неподвижной фазой при попадании в контакт с ней, например, с ионообменным материалом. Это не обязательно означает, что 100% интересующего вещества связывается, но существенным образом 100% интересующего вещества связывается, т.е. по крайней мере 50% интересующего вещества связывается, предпочтительно по меньшей мере 75% интересующего вещества связывается, предпочтительно по меньшей мере 85% интересующего вещества связывается, более предпочтительно более чем 95% интересующего вещества связывается с неподвижной фазой.
Термин "терапевтическое антитело" означает антитело, которое проходит клинические испытания для утверждения в качестве терапевтического для человека и которое можно вводить индивидууму для лечения заболевания. В одном варианте исполнения антитело является терапевтическим антителом. В другом варианте исполнения терапевтическое антитело представляет собой моноклональное антитело. В еще одном варианте исполнения терапевтическое антитело получено от обезьяны или животного, трансформированного человеческим локусом антитела, или человеческое моноклональное антитело, или гуманизированное моноклональное антитело. В одном варианте исполнения терапевтическое антитело представляет собой человеческое моноклональное антитело. В еще одном варианте исполнения терапевтическое антитело представляет собой гуманизированное моноклональное антитело. Терапевтические антитела широко используются для лечения различных заболеваний, таких как онкологические заболевания (например, гематологические и солидные злокачественные опухоли, включая не-Ходжкинскую лимфому, рак молочной железы и колоректальный рак), иммунологические заболевания, заболевания центральной нервной системы, сосудистые заболевания или инфекционные заболевания. Такие антитела являются в одном варианте исполнения антителами против ALK, рецептора киназы, связанной с адгезией (adhesion related kinase receptor) (например, Axl), или ERBB рецепторов (например, EGFR, ERBB2, ERBB3, ERBB4), или эритропоэтин-продуцирующих гепатоцеллюлярных рецепторов (erythropoietin-producing hepatocellular (EPH) receptors) (например, EphA1; EphA2, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphB1, EphB2, EphB3, EphB4, EphB5, EphB6), или рецепторов фактора роста фибробластов (FGF) (например, FGFR1, FGFR2, FGFR3, FGFR4, FGFR5), или Fgr, или IGF1R, или инсулинового рецептора, или LTK, или M-CSFR, или MUSK, либо рецепторов тромбоцитарного фактора роста (PDGF) (например, PDGFR-A, PDGFR-В), или RET, или ROR1, или ROR2, или ROS, или RYK, или рецепторов фактора роста эндотелия (VEGF) (например, VEGFR1/FLT1, VEGFR2/FLK1, VEGF3), или рецепторов тирозинкиназы с иммуноглобулин-подобным и EGF-подобным доменом (TIE)(например, TIE-1, TIE-2/TEK), или Тес, или TYRO10, или рецепторов инсулиноподобного фактора роста (IGF) (например, INS-R, IGF-IR, IR-R), или рецепторов дискоидин домена (DD) (например, DDR1, DDR2), либо рецептора c-Met (МЕТ), или recepteur d′origine nantais (RON, так же известный как рецептор, стимулирующий макрофаги-1), либо Flt3 (fins-related tyrosine kinase 3), или рецептора колониестимулирующего фактора 1 (CSF1), или рецептора C-kit (KIT, или SCFR), или рецепторов, связанных с инсулиновыми рецепторами (IRR), или CD19, или CD20, или HLA-DR, или CD33, или CD52, или G250, или GD3, или PSMA, или CD56, или СЕА, или антигена Lewis Y, или рецептора IL-6.
Термин "антитело" охватывает различные формы структур антитела, включая целые антитела и фрагменты антител. Антитела, описанные в данном документе, в одном варианте исполнения являются человеческими антителами, гуманизированными антителами, химерными антителами, или обедненными антителами T-клеточных антигенов. Генная инженерия антител описана, например, в Morrison, S.L, et al., Proc. Natl. Acad. Sci. USA 81 (1984) 6851-6855; US 5,202,238 и US 5,204,244; Riechmann, L, et al., Nature 332 (1988) 323-327; Neuberger, M.S., et al., Nature 314 (1985) 268-270; Lonberg, N., Nat. Biotechnol. 23 (2005) 1117-1125. В зависимости от аминокислотной последовательности константной области тяжелой цепи антитела разделены на классы: IgA, IgD, IgE, IgG и IgM. Некоторые из этих классов делятся на подклассы (изотипы), т.е. IgG на IgG1, IgG2, IgG3 и IgG4, или IgA на IgA1 и IgA2. В соответствии с классом иммуноглобулина, к которому принадлежит антитело, константные области тяжелой цепи иммуноглобулинов называются α(IgA), δ(IgD), ε(IgE), γ(IgG), and µ(IgM) соответственно. Термин "антитело человека класса IgG1" означает антитело, в котором аминокислотная последовательность константных доменов получена из аминокислотной последовательности человеческого IgG1. Этот термин включает человеческие антитела, гуманизированные антитела, химерные антитела и конъюгаты антител.
"Гуманизированные" формы не человеческих антител (например, грызунов) представляют собой химерные антитела, которые частично содержат последовательности, полученные от не человеческого антитела и от антитела человека. По большей части, гуманизированные антитела получают из человеческих антител (реципиентные антитела), в которых остатки из гипервариабельной области заменены на остатки из гипервариабельной области не человеческого вида (донорские антитела), такого как мышь, крыса, кролик или не человеческие приматы, имеющие желаемую специфичность и аффинность. В некоторых случаях остатки из каркасной области (FR) антитела человека заменены соответствующими не человеческими остатками. Кроме того, гуманизированные антитела могут содержать дополнительные модификации, например аминокислотные остатки, которые не встречаются в реципиентном антителе или в донорском антителе. Такие модификации в результате приводят к вариантам таких реципиентных или донорских антител, которые являются гомологичными, но не идентичными соответствующей последовательности родителя. Эти изменения сделаны для дальнейшего усовершенствования изготовления антител.
В общем, гуманизированное антитело содержит практически все из по меньшей мере одного, а обычно из двух вариабельных доменов, в которых все или по существу все гипервариабельные петли соответствуют таковым из не человеческих донорских антител, и все или в основном все из FR являются человеческими реципиентными антителами. Гуманизированное антитело необязательно также будет содержать, по меньшей мере, часть константной области антитела, обычно от человеческого антитела.
Способы гуманизации не человеческих антител описаны в литературе. В одном варианте исполнения гуманизированное антитело имеет один или несколько аминокислотных остатков, введенных в него из источника, который не является человеком. Эти не человеческие аминокислотные остатки часто называют "импортированными" остатками, которые обычно берут из "импортного" вариабельного домена. Гуманизация может быть выполнена в соответствии со способом Winter и сотрудников, заменяя последовательности гипервариабельной области на соответствующие последовательности не человеческого антитела. Соответственно такие "гуманизированные" антитела представляют собой химерные антитела, в которых по существу меньше, чем интактный человеческий вариабельный домен заменен на соответствующую последовательность из не человеческого вида. На практике гуманизированные антитела обычно представляют собой человеческие антитела, в которых некоторые остатки гипервариабельной области и, возможно, некоторые остатки FR-регионов заменены остатками из аналогичных участков грызунов или антител не человеческих приматов.
Термин "моноклональное антитело", используемый в данном документе, означает антитело, полученное из популяции, по существу, гомогенных антител, т.е. индивидуальные антитела, составляющие популяцию, являются идентичными, за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела являются высокоспецифичными, направленными против одного антигенного сайта. Кроме того, в отличие от препаратов поликлональных антител, которые включают различные антитела, направленные против различных антигенных сайтов (детерминантов или эпитопов), каждое моноклональное антитело направлено против одного антигенного сайта на антигене. В дополнение к их специфичности моноклональные антитела обладают тем преимуществом, что они могут быть синтезированы без загрязнения другими антителами. Определение «моноклональное» указывает на характер антитела, полученного, по существу, из гомогенной популяции антител, и не должно быть истолковано как требующее получения антитела каким-либо конкретным способом.
Термин "химерное антитело" означает антитело, содержащее вариабельный домен, то есть связывающий участок, от первого вида и, по крайней мере, часть константной области, полученной из другого источника или второго вида, обычно полученное методами рекомбинантных ДНК.
Варианты аминокислотных последовательностей антител могут быть получены путем внесения соответствующих изменений в нуклеотидную последовательность, кодирующую цепи антитела, или пептидным синтезом. Такие модификации включают, например, делеции, и/или инсерции, и/или замены остатков аминокислотной последовательности интерферона. Любая комбинация делеции, инсерции и замены может быть сделана для достижения конечной конструкции, в том случае если конечная конструкция обладает антигенсвязывающими свойствами, как и родительское антитело.
Консервативные замены аминокислот приведены в Таблице 1 под заголовком «предпочтительные замены». Более существенные изменения приведены в последующей таблице под заголовком "примерные замены", и, как описано ниже, со ссылкой на классы боковых цепей аминокислот. Аминокислотные замены могут быть введены в цепи антител и продукты, прошедшие скрининг на сохранение биологической активности родительского антитела.
| Таблица 1 | ||
| Исходный остаток | Примерные замены | Предпочтительные замены |
| Ala (A) | Val; Leu; Ile | Val |
| Arg (R) | Lys; Gln; Asn | Lys |
| Asn (N) | Gln; His; Asp, Lys; Arg | Gln |
| Asp (D) | Glu; Asn | Glu |
| Cys (C) | Ser; Ala | Ser |
| Gln (Q) | Asn; Glu | Asn |
| Glu (E) | Asp; Gln | Asp |
| Gly (G) | Ala | Ala |
| His (H) | Asn; Gln; Lys; Arg | Arg |
| Ile (I) | Leu; Val; Met; Ala; Phe; Norleucine | Leu |
| Leu (L) | Norleucine; Ile; Val; Met; Ala; Phe | Ile |
| Lys (K) | Arg; Gln; Asn | Arg |
| Met (M) | Leu; Phe; Ile | Leu |
| Phe (F) | Trp; Leu; Val; Ile; Ala; Tyr | Tyr |
| Pro (P) | Ala | Ala |
| Ser (S) | Thr | Thr |
| Thr (T) | Val; Ser | Ser |
| Trp (W) | Tyr; Phe | Tyr |
| Tyr (Y) | Trp; Phe; Thr; Ser | Phe |
| Val (V) | Ile; Leu; Met; Phe; Ala; Norleucine | Leu |
Аминокислоты могут быть разделены на группы в соответствии с общими свойствами боковых цепей:
(1) гидрофобные: Norleucine, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, которые влияют на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
Неконсервативные замены повлекут за собой смену члена одного из этих классов на другой класс.
Hudziak, R.M., et al., Mol. Cell. Biol. 9 (1989) 1165-1172 описывают генерацию панели HER2 антител, которые были охарактеризованы с использованием клеточной линии человеческой опухоли молочной железы SK-BR-3. Относительную пролиферацию клеток SK-BR-3 после воздействия антител определяли путем окрашивания монослоя кристаллическим фиолетовым через 72 часа. С помощью этого теста максимальное ингибирование было получено с антителом, называемым 4D5, которое ингибировало клеточную пролиферацию на 56%. В этом анализе другие антитела в панели уменьшали клеточную пролиферацию в меньшей степени. Было также обнаружено, что антитело 4D5 сенсибилизировало HER2-гиперэкспрессирующие клетки из линии опухоли молочной железы к цитотоксической активности TNF-α (см. также US 5,677,171). HER2 антитела обсуждаются в Hudziak, R.M., et al.. дополнительно охарактеризованы в Fendly, В.М., et al., Cancer Research 50 (1990) 1550-1558; Kotts, C.E., et al., In Vitro 26 (1990) 59A; Sarup, J.C., et al., Growth Regulation 1 (1991) 72-82; Shepard, H.M., et al., J. Clin. Immunol. 11 (1991) 117-127; Kumar, R., et al., Mol. Cell. Biol. 11 (1991) 979-986; Lewis, G.D., et al., Cancer Immunol. Immunother. 37 (1993) 255-263; Pietras, R.J., et al., Oncogene 9 (1994) 1829-1838; Vitetta, E.S., et al., Cancer Research 54 (1994) 5301-5309; Sliwkowski, M.X., et al., J. Biol. Chem. 269 (1994) 14661-14665; Scott, G.K., et al., J. Biol. Chem. 266 (1991) 14300-14305; D′souza, В., et al., Proc. Natl. Acad. Sci. 91 (1994) 7202-7206; Lewis, G.D., et al., Cancer Research 56 (1996) 1457-1465; и Schaefer, G., et al., Oncogene 15 (1997) 1385-1394.
Рекомбинантная гуманизированная версия мышиного антитела против HER2 4D5 (huMAb4D5-8, rhuMab HER2, трастузумаб или Герцептин®; см. US 5,821,337) является клинически активной у пациентов с оверэкспрессирующим HER2 метастатическим раком молочной железы, которые получили обширную предшествующую противораковую терапию (Baselga, J., et al., J. Clin. Oncol. 14 (1996) 737-744). Трастузумаб получил предпродажное одобрение Food and Drug Administration (FDA) 25 сентября 1998 для лечения пациентов с метастатическим раком молочной железы, у которых опухоль оверрэкспрессировала белок HER2.
Гуманизированные анти-ErbB2 антитела включают huMAb4D5-1, huMAb4D5-2, huMAb4D5-3, huMAb4D5-4, huMAb4D5-5, huMAb4D5-6, huMAb4D5-7 и huMAb4D5-8 (Герцептин®), как описано в Таблице 3 патента US 5,821,337, специально включенного в данный документ в качестве ссылки; гуманизированные 520C9 (WO 93/21319) и гуманизированные антитела 2C4, как описано в WO 01/000245, специально включены в данный документ в качестве ссылки.
Другие HER2 антитела с различными свойствами описаны в Tagliabue, Е., et al., Int. J. Cancer 47 (1991) 933-937; McKenzie, S.J., et al., Oncogene 4 (1989) 543-548; Maier, L.A., et al., Cancer Res. 51 (1991) 5361-5369; Bacus, S.S., et al., Molecular Carcinogenesis 3 (1990) 350-362; Stancovski, I., et al., PNAS USA 88 (1991) 8691-8695; Bacus, S.S., et al., Cancer Research 52 (1992) 2580-2589; Xu, F., et al., Int. J. Cancer 53 (1993) 401-408; WO 94/00136; Kasprzyk, P.G., et al., Cancer Research 52 (1992) 2771-2776; Hancock, M.C., et al., Cancer Res. 51 (1991) 4575-4580; Shawver, L.K., et al., Cancer Res. 54 (1994) 1367-1373; Arteaga, C.L., et al., Cancer Res. 54 (1994) 3758-3765; Harwerth, I.M., et al., J. Biol. Chem. 267 (1992) 15160-15167; US 5,783,186; и Klapper, L.N., et al., Oncogene 14 (1997) 2099-2109.
Пертузумаб (см., например, WO 01/000245) является первым из нового класса агентов, известных как ингибиторы димеризации HER (HER dimerization inhibitors (HDIs)). Пертузумаб связывается с HER2 в его домене димеризации, тем самым препятствуя его способности образовывать акти