Ингибиторы катехол-о-метилтрансферазы и их применение при лечении психотических расстройств
Иллюстрации
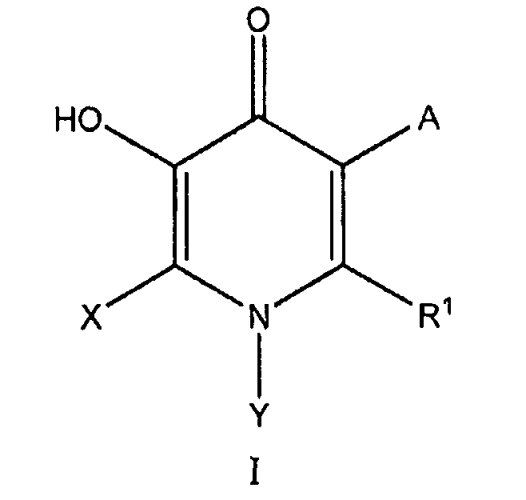
Показать всеИзобретение относится области органической химии, а именно к производным 4-пиридинона формулы I или к их фармацевтически приемлемым солям, где А представляет собой водород, В(ОН)2, галоген, C(O)NH(CH2)nC(O)N(R3)2; X представляет собой водород или галоген; Y представляет собой фенил, бензимидазолил, бензтиазолил, бензоксазолил, бензпиперидинил, хинолил, индолил, индазолил или пиридил, каждый из которых необязательно замещен 1-3 группами Ra, при условии, что Y представляет собой фенил, то по меньшей мере один из указанного Ra выбирают из OCF3, О(СН2)nC3-6циклоалкила, NR2C(O)R2, C(O)R2, N(R2)2, (СН2)nC(О)OR2, OR2, (CH2)nгетероциклила, NH(СН2)nгетероциклила, (СН2)nC6-10арила, О(СН2)nC6-10арила или О(СН2)nгетероциклила, где указанные гетероциклил и арил необязательно замещены 1-3 группами Rb; R1 представляет собой водород, NR2R3, Si(CH3)3, (CH2)nC6-10арил, С2алкенил или С1-4алкил, причем указанные алкил и алкенил необязательно замещены 1-3 группами из галогена, ОН, С1-6алкила, O-С1-6алкила, NR2R3, SOR2, NHSO2R2, CF3, С6-10арила, гетероциклила, -С≡С-С6-10арила, C(O)NR2R3, причем указанные арил и гетероциклил необязательно замещены 1-2 группами Ra; R2 и R3 независимо представляют собой Н, С1-6алкил, (СН2)nгетероциклил, (СН2)nC6-10арил, причем указанный арил необязательно замещен группой Ra; или R2 и R3 вместе с атомом азота, к которому они присоединены, образуют 6-членное кольцо, которое содержит кислород; Ra представляет С1-6алкил, галоген, CF3, OCF3, С3-6циклоалкил, O(СН2)nC3-6циклоалкил, NR2C(O)R2, C(O)R2, CN, N(R2)2, (CH2)nC(O)OR2, OR2, (CH2)nгетероциклил, NH(CH2)nгетероциклил, (CH2)nC6-10арил, О(CH2)nC6-10арил или О(CH2)nгетероциклил, причем указанные гетероциклил и арил необязательно замещены 1-3 группами Rb; Rb представляет С1-6алкил, галоген, CHF2, оксо (=O), N(R2)2, CH2OH, S(O)2NR2R3, (СН2)nC6-10арил, (СН2)nгетероциклил, NH(СН2)nгетероциклил, OR2, С3-6циклоалкил, CF3 или CN; и n равно 0-3; и где гетероцикл представляет собой ароматическое или насыщенное, или частично насыщенное моноциклическое или бициклическое кольцо, содержащее 5-10 атомов, среди которых 1-4 атома являются гетероатомами, выбранными из азота, кислорода и серы. Также изобретение относится к фармацевтической композиции на основе соединения формулы I, способу лечения и/или предотвращения неврологических и психиатрических заболеваний и способу усиления действия антипсихотического средства, основанных на использовании соединения формулы I. Технический результат: получены новые соединения, полезные при лечении заболеваний, связанных с катехол-О-метилтрансферазой (СОМТ). 6 н. и 46 з.п. ф-лы, 1 табл., 17 пр.
Реферат
Уровень техники изобретения
Симптомы шизофрении обычно делят на три категории; позитивные, негативные и когнитивные. Позитивные симптомы включают в себя галлюцинации, бред и неадекватное поведение, в то время как негативные симптомы характеризуются отсутствием удовольствий и желаний и/или интереса к жизни. Когнитивные симптомы или нарушение познавательной способности включает в себя трудности в организации процесса мышления и установлении приоритета задач. У пациентов с биполярным расстройством обычно проявляются круговые изменения настроения от глубокой депрессии до тяжелой мании с психотическими особенностями или без них. Шизофрения и биполярное расстройство являются одними из наиболее тяжелых форм психиатрических расстройств, которые вызывают перекрывание нарушений познавательной способности (когнитивных нарушений) (Tasman et al., Psychiatry, West Sussex, John Wiley & Sons, Ltd., Second Edition, Volume 1, 2003, pp 254-272; и Sadock and Sadock, Kaplan and Sadock's Comprehensive Textbook of Psychiatry, 7 ed., Vol. 1, 2005, Philadelphia, Pa.; Lippincott Williams & Wilkins, pp 236-272 и 1330-1395), и они имеют тенденцию становиться хроническими/прогрессирующими. В отличие от позитивных симптомов, негативные и когнитивные симптомы шизофрении, как полагают, оказывают огромное влияние на инвалидизацию, результат лечения и функциональное восстановление (Addington and Addington, 1993; Green, 1996). Неудовлетворенность терапией шизофрении относят к отсутствию эффективности такой терапии или невыносимым и нежелательным побочным действиям. Побочные действия были связаны со значительными метаболическими, экстрапирамидными, пролактиновыми и сердечными побочными явлениями. См. Lieberman et al., N. Engl. J. Med. (2005) 353:1209-1223.
Хотя считается, что множество путей принимают участие в патогенезе шизофрении, приводящей к негативным и когнитивным симптомам, основное внимание было направлено на снижение нейротрансмиссии допамина в префронтальной коре головного мозга (Weinberger, 1987; Weinberger et al., 1988; Akil et al., 1999). Доказательство пониженной нейротрансмиссии допамина в префронтальной коре головного мозга подкрепляется пониженным региональным мозговым кровотоком или гипоактивацией дорсолатеральной префронтальной коры головного мозга у пациентов, страдающих шизофренией (Weinberger et al., 1988; Daniel et al., 1991; Okubo et al., 1997; Abi-Dargham et al., 2002). Связанные с шизофренией префронтальные недостаточности, независимо от лечения или психотического состояния, коррелировали с низкой результативностью при заданиях исполнительной функции (например, при испытаниях n-back или Wisconsin Card Sorting Test), которая оценивает участие префронтальной коры головного мозга (Weinberger et al., 1986, 1988; Carter et al., 1998; Callicott et al., 2000; Barch et al., 2001). Помимо этих недостатков в исполнительной функции, пониженная нейротрансмиссия допамина в префронтальной коре головного мозга оказывает влияние на несколько активностей головного мозга, включающих в себя внимание, гедонические действия, природные подкрепления и биологические активности, такие как клеточная передача сигналов. Таким образом, соединения, которые селективно повышают нейротрансмиссию допамина в префронтальной коре головного мозга, могут иметь терапевтический потенциал для лечения когнитивных и негативных симптомов.
Уровни допамина в головном мозге определяются его биосинтезом и секрецией, а также скоростью его диффузии, обратного поглощения и деградации. Катехол-О-метилтрансфераза (СОМТ) является важным ферментом, принимающим участие в расщеплении допамина в коре головного мозга. COMT превращает допамин в 3-метокситирамин и превращает метаболит допамина дигидроксифенилуксусную кислоту (DOPAC) в гомованилиновую кислоту (HVA) (Boulton and Eisenhofer, 1998). Фактически, COMT воздействует на различные биогенные катехинамины, а также катехинэстрогены, питательные фитохимикаты и аскорбиновую кислоту. В подкорковых структурах (например, полосатом теле), допаминергическая передача сигнала регулируется, главным образом, удалением допамина из синаптической щели посредством быстрого поглощения переносчиком допамина (DAT) и/или переносчиком норадреналина (NET). Регулирование передачи допамина в префронтальной коре головного мозга заметно отличается от указанного выше. DAT менее интенсивно экспрессируется в синапсах в префронтальной коре головного мозга, где допамин удаляется поглощением посредством NET, диффузией или метаболизмом посредством СОМТ и моноаминоксидазы (Mazei et al., 2002; Moron et al., 2002; Lewis et al., 2001; Sesack et al., 1998; Smiley et al., 1994). Поэтому можно предсказать применение ингибиторов СОМТ для селективного усиления передачи кортикального допаминергического сигнала и тем самым улучшения когнитивной функции.
Ген COMT расположен в районе хромосомы 22q11.21, которая связана с шизофренией, биполярным расстройством, ADHD и зависимостью от психоактивного вещества (Williams, et al., 2003 and Takahashi et al., 2003). Существуют две основные изоформы COMT, связанная с мембраной COMT (MB-COMT) является преобладающей формой, участвующей в деградации допамина синаптической фронтальной доли в головном мозге человека (Lachman et al., Pharmacogenetics (1996), 6(3):243-250). Другой формой является растворимая COMT (S-COMT), которая транскрибируется из промотора, отличного от промотора MB-COMT, и в остальном идентична человеческой MB-COMT минус 50 аминокислот у N-конца белка. У человека активность COMT модулируется полиморфизмом одного нуклеотида у Val158Met (MB-COMT). Из-за различий в термостабильности ферментов, гомозиготные Met-носители имеют более низкую активность СОМТ, гетерозиготы проявляют промежуточную активность и гомозиготные Val-носители имеют более высокую ферментативную активность (Chen et al., 2004). Несмотря на различия, наблюдаемые в активности на основе генотипа, только умеренную связь между Val158Met-генотипом и когнитивной активностью демонстрировали мета-анализом у здоровых индивидуумов, тогда как никакого эффекта не наблюдали при шизофрении. На основании обратной U-образной зависимости считали, что существует связь между активацией рецепторов допамина и функционированием префронтальной коры головного мозга, эти данные могут быть согласованы с тем фактом, что патологическое состояние, а также многочисленные экологические и генетические факторы ухудшают префронтальную эффективность и снижают уровни допамина (см. обзор в публикации Tunbridge et al., Biol Psych, 2006).
Хотя клозапин, зипрекса, риспердал и другие антипсихотические лекарственные средства были применимы для лечения позитивных и, возможно, негативных симптомов шизофрении и биполярного расстройства, они не были лишены побочных действий, таких как агранулоцитоз, седативное действие, увеличение массы тела, гиперлипидемия и гипергликемия, все из которых ограничивают их применение (Tasman et al., 2003; Sadock and Sadock 2005). Таким образом, остается потребность в лекарственных средствах, которые эффективно лечат негативные симптомы и нарушение познавательной способности, не имеют серьезных побочных действий и являются эффективными при лечении шизофрении, биполярного расстройства, депрессии, зависимости от психоактивных веществ и ADD/ADHD и т.д. Такие лекарственные средства можно также применять для ослабления таких симптомов, когда они имеют место как часть другого психиатрического синдрома или когда они сопутствуют неврологическому расстройству.
Сущность изобретения
Настоящее изобретение относится к производным 4-пиридинона, которые являются ингибиторами фермента катехол-О-метилтрансферазы (СОМТ) и применимы при лечении и предотвращении неврологических и психиатрических нарушений и заболеваний, в которых участвует СОМТ.
Настоящее изобретение относится также к фармацевтическим композициям, содержащим эти соединения, и применению этих соединений и композиций при предотвращении или лечении таких заболеваний, в которых участвует фермент COMT.
Настоящее изобретение также относится к способу лечения симптомов, связанных с психиатрическим нарушением, включающему введение фармакологически эффективной дозы композиции, содержащей 4-пиридинон в качестве ингибитора COMT или его фармацевтически приемлемую соль, пациенту.
Кроме того, настоящее изобретение относится к улучшению негативных симптомов и симптомов нарушений познавательной способности, связанных с шизофренией, усилению действий антипсихотических средств при лечении позитивных симптомов шизофрении, при лечении тяжелой депрессии, депрессивной фазы биполярного расстройства, связанных с недостаточностью DA заболеваний, таких как ADD/ADHD, и зависимости от психоактивного вещества (в борьбе с болезненными пристрастиями, связанными с аддикцией и/или злоупотреблением алкоголем, опиатами, кокаином, марихуаной, амфетамином, табаком). Настоящее изобретение также относится к способу лечения табачной зависимости и увеличения массы тела/тяги к пищевым продуктам, связанной с отказом от курения или применением антипсихотических средств.
Настоящее изобретение также относится к способу повышения познавательной способности при травмах головы и деменции.
Эти и другие аспекты изобретения будут реализованы при более подробном рассмотрении описания изобретения в целом.
Подробное описание изобретения
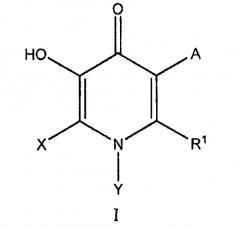
Настоящее изобретение относится к являющимся ингибиторами COMT новым соединениям формулы I
или их фармацевтически приемлемым солям и индивидуальным энантиомерам и диастереомерам,
где
А представляет собой водород, B(OH)2, NO2, галоген, OH, C(О)NH(CH2)nC(О)N(R3)2, C3-10циклоалкил или С1-6алкил;
X представляет собой водород, галоген, C1-6алкил, (CH2)nC5-10гетероциклил, причем указанный алкил, гетероциклил необязательно замещен 1-3 группами Ra;
Y представляет собой фенил, бензимидазолил, бензтиазолил, бензоксазолил, бензпиперидинил, хинолил, индолил, индазолил или пиридил, каждый из которых необязательно замещен 1-3 группами Ra;
R1 представляет собой водород, NR2R3, Si(CH3)3, (CH2)nC6-10арил, (CH2)nC5-10гетероциклил, С2-10алкенил, С1-10алкил, причем указанные алкил и алкенил необязательно замещены 1-3 группами из галогена, OH, С1-6алкила, О-С1-6алкила, NR2R3, SOR2, NHSO2R2, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra;
R2 и R3 независимо представляют собой H, OH, C1-6алкил, N(CH3)2, (CH2)nC5-10гетероциклил, (CH2)nC6-10арил, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra;
R2 и R3 вместе с атомом азота, к которому они присоединены, образуют 5-10-членное кольцо, которое необязательно замещено 1-3 группами из галогена, OH, C2-6алкенила, (CH2)nC5-10гетероциклила или (CH2)nC6-10арила;
Ra представляет C1-6алкил, галоген, гидроксил, (CH2)nCF3, OCHF2, OCF3, C3-6циклоалкил, O(CH2)nC3-6циклоалкил, NR2C(О)R2, C(О)N(R2)2, C(R2)2OR2, C(О)R2, NO2, CN, N(R2)2, (CH2)nC(О)OR2, SO2R2, OR2, (CH2)nC5-10гетероциклил, NH(CH2)nC5-10гетероциклил, (CH2)nC6-10арил, O(CH2)nC6-10арил или O(CH2)nC5-10гетероциклил, причем указанные циклоалкил, гетероциклил и арил необязательно замещены 1-3 группами Rb;
Rb представляет C1-6алкил, галоген, CHF2, -O-, N(R2)2 , CH2OH, S(O)2NR2R3, (CH2)nC6-10арил, (CH2)nC5-10гетероциклил, C(O)(CH2)nC5-10гетероциклил, NH(CH2)nC5-10гетероциклил, С(О)NHC3-6циклоалкил, OR2, C3-6циклоалкил, (CH2)nCF3 или CN; и
n равно 0-5.
Вариант осуществления настоящего изобретения реализуется, когда Y представляет собой фенил, причем указанный фенил необязательно замещен 1-3 группами Ra и все другие символы имеют значения, указанные ранее. Подвариант осуществления данного изобретения реализуется, когда по меньшей мере один из Ra выбран из группы, состоящей из C6-10арила и C5-10гетероциклила, причем указанный арил и гетероциклил необязательно замещены 1-3 группами Rb. Другой подвариант осуществления данного изобретения реализуется, когда арил и гетероциклил Ra выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина, 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-а]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-a]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Следующий подвариант осуществления этого изобретения реализуется, когда Ra выбран из группы, состоящей из индолила, пиридила, фенила и индазолила, каждый из которых необязательно замещен 1-3 группами Rb. Еще один дополнительный подвариант осуществления этого изобретения реализуется, когда Rb выбран из группы, состоящей из С1-6алкила, галогена, CHF2, N(R2)2, CH2OH, OR2, C3-6циклоалкила, (CH2)nCF3 или CN.
Другой вариант этого изобретения реализуется, когда Y представляет собой пиридил, причем указанный пиридил необязательно замещен 1-3 группами Ra и все другие символы имеют значения, описанные ранее. Подвариант осуществления этого изобретения реализуется, когда по меньшей мере один из Ra выбран из группы, состоящей из C6-10арила и C5-10гетероциклила, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Rb. Другой подвариант осуществления данного изобретения реализуется, когда арил и гетероциклил Ra выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-а]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина, имидазо[1,2-a]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Следующий подвариант осуществления этого изобретения реализуется, когда Ra выбран из группы, состоящей из индолила, пиридила, фенила и индазолила, каждый из которых необязательно замещен 1-3 группами Rb. Еще один дополнительный подвариант осуществления этого изобретения реализуется, когда Ra выбран из группы, состоящей из С1-6алкила, галогена, CHF2, N(R2)2, CH2OH, OR2, C3-6циклоалкила, (CH2)nCF3 или CN.
Еще один вариант осуществления этого изобретения реализуется, когда Y представляет собой индолил, причем указанный индолил замещен 1-3 группами Ra и все другие символы имеют значения, указанные ранее. Подвариант осуществления этого изобретения реализуется, когда по меньшей мере один из Ra выбран из группы, состоящей из C6-10арила и C5-10гетероциклила, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Rb. Другой подвариант осуществления данного изобретения реализуется, когда арил и гетероциклил Ra выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола; 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-а]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-a]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Следующий подвариант осуществления данного изобретения реализуется, когда Ra выбран из группы, состоящей из индолила, пиридила, фенила и индазолила, каждый из которых необязательно замещен 1-3 группами Rb. Еще один дополнительный подвариант осуществления данного изобретения реализуется, когда Rb выбран из группы, состоящей из С1-6алкила, галогена, CHF2, N(R2)2, CH2OH, OR2, C3-6циклоалкила, (CH2)nCF3 или CN.
Другой вариант данного изобретения реализуется, когда Y представляет собой бензимидазолил, причем указанный бензимидазолил необязательно замещен 1-3 группами Ra и все другие символы имеют значения, указанные ранее. Подвариант осуществления данного изобретения реализуется, когда по меньшей мере один из Ra выбран из группы, состоящей из C6-10арила и C5-10гетероциклила, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Rb. Другой подвариант осуществления данного изобретения реализуется, когда арил и гетероциклил Ra выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-а]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-a]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Следующий подвариант осуществления данного изобретения реализуется, когда Ra выбран из группы, состоящей из индолила, пиридила, фенила и индазолила, каждый из которых необязательно замещен 1-3 группами Rb. Еще один дополнительный подвариант осуществления данного изобретения реализуется, когда Rb выбран из группы, состоящей из С1-6алкила, галогена, CHF2, N(R2)2, CH2OH, OR2, C3-6циклоалкила, (CH2)nCF3 или CN.
Еще один вариант осуществления данного изобретения реализуется, когда Y представляет собой индазолил, причем указанный индазолил необязательно замещен 1-3 группами Ra и все другие символы имеют значения, указанные ранее. Подвариант осуществления данного изобретения реализуется, когда по меньшей мере один из Ra выбран из группы, состоящей из C6-10арила и C5-10гетероциклила, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Rb. Другой подвариант осуществления данного изобретения реализуется, когда арил и гетероциклил Ra выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина, 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-а]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина, имидазо[1,2-a]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Следующий подвариант осуществления данного изобретения реализуется, когда Ra выбран из группы, состоящей из индолила, пиридила, фенила и индазолила, каждый из которых необязательно замещен 1-3 группами Rb. Еще один дополнительный подвариант осуществления данного изобретения реализуется, когда Rb выбран из группы, состоящей из С1-6алкила, галогена, CHF2, N(R2)2, CH2OH, OR2, C3-6циклоалкила, (CH2)nCF3 и CN.
Другой вариант данного изобретения реализуется, когда R1 представляет собой водород и все другие символы имеют значения, описанные ранее.
Еще один вариант данного изобретения реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, описанные ранее.
Еще один вариант данного изобретения реализуется, когда R1 представляет собой С1-10алкил, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, O-С1-6алкила, NR2R3, CF3, С6-10арила, С5-10гетероциклила, ОС6-10арила, С1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡C-С6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra.
Другой вариант этого изобретения реализуется, когда R1 представляет собой водород, CH(OH)CH3, NH2, NHCH3, (CHR2)nC6-10арил и (CHR2)nC6-10гетероциклил, где указанные арил и гетероарил необязательно замещены 1-3 группами Ra. Другой вариант осуществления данного изобретения реализуется, когда R1 представляет собой водород или CH(OH)CH3.
Другой вариант данного изобретения реализуется, когда А представляет собой водород и все другие символы имеют значения, описанные ранее.
Другой вариант данного изобретения реализуется, когда Х представляет собой водород и все другие символы имеют значения, описанные ранее.
Еще один вариант осуществления данного изобретения реализуется, когда Х представляет собой галоген и все другие символы имеют значения, описанные ранее.
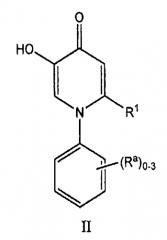
Другой вариант этого изобретения реализуется соединениями структурной формулы II
или их фармацевтически приемлемыми солями и индивидуальными энантиомерами и диастереомерами, где R1 и Ra имеют значения, указанные ранее. Подвариант осуществления соединений формулы II реализуется, когда R1 представляет собой водород и все другие символы имеют значения, указанные выше. Другой подвариант осуществления соединений формулы II реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, указанные выше. Еще один подвариант осуществления соединений формулы II реализуется, когда R1 представляет собой С1-10алкил и все другие символы имеют значения, указанные выше, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, О-С1-6алкила, NR2R3, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формулы II реализуется, когда R1 представляет собой водород, NH2, NHCH3 и замещенный алкил, выбранный из СН(ОН)СН3, (CHR2)nC6-10арила и (CHR2)nC6-10гетероциклила, где указанные арил и гетероарил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формулы II реализуется, когда R1 представляет собой водород или СН(ОН)СН3. Еще один вариант осуществления соединений формулы II реализуется, когда Ra представляет собой С1-6алкил, галоген, (СН2)nCF3, OR2, (СН2)nC5-10гетероциклил, (СН2)nC6-10арил, О(СН2)nC6-10арил или О(СН2)nC5-10гетероциклил, причем указанные алкил, гетероциклил и арил необязательно замещены 1-3 группами Rb. Другой вариант осуществления Ra формулы II реализуется, когда арил и гетероциклил выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина, 1H-пирроло[3,2-с]пиридина, 2,1,3-бензоксадиазола; 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-a]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-а]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb. Другой вариант осуществления соединений изобретения формулы II реализуется, когда по меньшей мере один из Ra представляет собой арил или гетероциклил, необязательно замещенный 1-3 группами Rb.
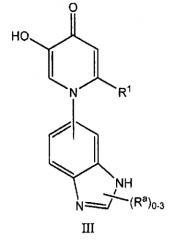
Другой вариант данного изобретения осуществляется соединениями структурной формулы III
или их фармацевтически приемлемыми солями и индивидуальными энантиомерами и диастереомерами, где R1 и Ra имеют значения, указанные ранее. Подвариант осуществления соединений формулы III реализуется, когда R1 представляет собой водород и все другие символы имеют значения, указанные выше. Другой подвариант осуществления соединений формулы III реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, указанные выше. Еще один подвариант осуществления соединений формулы III реализуется, когда R1 представляет собой С1-10алкил и все другие символы имеют значения, указанные выше, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, О-С1-6алкила, NR2R3, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формулы III реализуется, когда R1 представляет собой водород, NH2, NHCH3 и замещенный алкил, выбранный из СН(ОН)СН3, (CHR2)nC6-10арила и (CHR2)nC6-10гетероциклила, где указанные арил и гетероарил необязательно замещены 1-3 группами Ra. Другой подвариант осуществления соединений формулы III реализуется, когда R1 представляет собой водород или СН(ОН)СН3. Еще один вариант осуществления соединений формулы III реализуется, когда Ra представляет собой С1-6алкил, галоген, (СН2)nCF3, OR2, (СН2)nC5-10гетероциклил, (СН2)nC6-10арил, О(СН2)nC6-10арил или О(СН2)nC5-10гетероциклил, причем указанные алкил, гетероциклил и арил необязательно замещены 1-3 группами Rb. Еще один вариант осуществления Ra формулы III реализуется, когда арил и гетероциклил выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина, 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина, 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-a]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-а]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb.
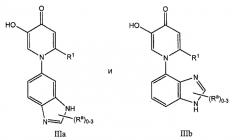
Подвариант осуществления соединений формулы III по данному изобретению реализуется соединениями структурной формулы IIIa и IIIb
или их фармацевтически приемлемыми солями и индивидуальными энантиомерами и диастереомерами, где R1 и Ra имеют значения, указанные ранее. Другой подвариант осуществления соединений формул IIIa и IIIb реализуется, когда R1 представляет собой водород и все другие символы имеют значения, указанные выше. Другой подвариант осуществления соединений формул IIIa и IIIb реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, указанные выше. Еще один подвариант осуществления соединений формул IIIa и IIIb реализуется, когда R1 представляет собой С1-10алкил и все другие символы имеют значения, указанные выше, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, О-С1-6алкила, NR2R3, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формул IIIa и IIIb реализуется, когда R1 представляет собой водород, NH2, NHCH3 и замещенный алкил, выбранный из СН(ОН)СН3, (CHR2)nC6-10арила и (CHR2)nC6-10гетероциклила, где указанные арил и гетероарил необязательно замещены 1-3 группами Ra. Другой подвариант осуществления соединений формул IIIa и IIIb реализуется, когда R1 представляет собой водород или СН(ОН)СН3. Еще один вариант осуществления соединений формул IIIa и IIIb реализуется, когда Ra представляет собой С1-6алкил, галоген, (СН2)nCF3, OR2, (СН2)nC5-10гетероциклил, (СН2)nC6-10арил, О(СН2)nC6-10арил или О(СН2)nC5-10гетероциклил, причем указанные алкил, гетероциклил и арил необязательно замещены 1-3 группами Rb. Другой вариант осуществления Ra формул IIIa и IIIb реализуется, когда арил и гетероциклил выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила, пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола, 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-a]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-а]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb.
Другой вариант осуществления данного изобретения реализуется соединениями структурной формулы IV
или их фармацевтически приемлемыми солями и индивидуальными энантиомерами и диастереомерами, где R1 и Ra имеют значения, указанные ранее. Подвариант осуществления соединений формулы IV реализуется, когда R1 представляет собой водород и все другие символы имеют значения, указанные выше. Другой подвариант осуществления соединений формулы IV реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, указанные выше. Еще один подвариант осуществления соединений формулы IV реализуется, когда R1 представляет собой С1-10алкил и все другие символы имеют значения, указанные выше, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, О-С1-6алкила, NR2R3, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формулы IV реализуется, когда R1 представляет собой водород, NH2, NHCH3 и замещенный алкил, выбранный из СН(ОН)СН3, (CHR2)nC6-10арила и (CHR2)nC6-10гетероциклила, где указанные арил и гетероарил необязательно замещены 1-3 группами Ra. Другой подвариант осуществления соединений формулы IV реализуется, когда R1 представляет собой водород или СН(ОН)СН3. Еще один вариант осуществления соединений формулы IV изобретения реализуется, когда Ra представляет собой С1-6алкил, галоген, (СН2)nCF3, OR2, (СН2)nC5-10гетероциклил, (СН)nC6-10арил, О(СН2)nC6-10арил или О(СН2)nC5-10гетероциклил, причем указанные алкил, гетероциклил и арил необязательно замещены 1-3 группами Rb. Другой вариант осуществления Ra формулы IV реализуется, когда арил и гетероциклил выбраны из группы, состоящей из нафтиридина, индолила, пиразолила, бензодиоксазолила пиридила, фуропиридинила, изоиндолила, пиридооксазинила, имидазолила, пирролила, пирролопиридинила, тиофенила, изоксазолила, пиримидинила, хиноксалинила, хиназолинила, хинолинила, изохинолинила, фенила, индазолила, [1,2,4]триазоло[1,5-а]пиридина; 1,2,3,4-тетрагидроизохинолина; 1,3-бензодиоксола; 1-бензотиофена; 1H-индазола; 1H-пирроло[2,3-b]пиридина; 1H-пирроло[2,3-с]пиридина; 1H-пирроло[3,2-b]пиридина; 1H-пирроло[3,2-с]пиридина; 2,1,3-бензоксадиазола; 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазина; 3Н-имидазо[4,5-b]пиридина; 4,5,6,7-тетрагидропиразоло[1,5-a]пиридина; фуро[2,3-с]пиридина; фуро[3,2-b]пиридина; имидазо[1,2-а]пиридина; изоксазола; хиназолина и тиено[3,2-с]пиридин-4(5Н)-она, каждый из которых необязательно замещен 1-3 группами Rb.
Другой вариант осуществления данного изобретения реализуется соединениями структурной формулы V
или их фармацевтически приемлемыми солями и индивидуальными энантиомерами и диастереомерами, где R1 и Ra имеют значения, указанные ранее. Подвариант осуществления соединений формулы V реализуется, когда R1 представляет собой водород и все другие символы имеют значения, указанные выше. Другой подвариант осуществления соединений формулы V реализуется, когда R1 представляет собой NR2R3 и все другие символы имеют значения, указанные выше. Еще один подвариант осуществления соединений формулы V реализуется, когда R1 представляет собой С1-10алкил и все другие символы имеют значения, указанные выше, причем указанный алкил необязательно замещен 1-3 группами, выбранными из галогена, OH, О-С1-6алкила, NR2R3, CF3, C6-10арила, C5-10гетероциклила, OC6-10арила, C1-6алкенила, С3-6циклоалкила, С1-6алкинила, -C≡С-C6-10арила, C(О)NR2R3, NHSO2C6-10арила, COOR2, C(О)R2, циано, причем указанные арил и гетероциклил необязательно замещены 1-3 группами Ra. Другой вариант осуществления соединений формулы V реализуется, когда R1 представляет собой водород, NH2, NHCH3 и замещен