Лечение заболеваний, связанных с альфа-субъединицей потенциалзависимого натриевого канала (scna), путем ингибирования природного антисмыслового транскрипта гена scna
Иллюстрации
Показать всеИзобретение относится к биохимии. Описаны антисмысловые олигонуклеотиды, которые увеличивают экспрессию указанного гена альфа-субъединицы потенциалзависимого натриевого канала (SCNA) in vivo или in vitro по сравнению с нормальным контролем. Олигонуклеотиды представляют собой фосфотиоатные аналоги длиной от 11 до 30 нуклеотидов, содержащие по меньшей мере одну модификацию, выбранную из: модифицированного остатка сахара; модифицированной межнуклеотидной связи; модифицированного нуклеотида и их комбинаций; при этом указанные олигонуклеотиды представляют собой соединения, которые специфически гибридизуются с комплементарной областью природного антисмыслового олигонуклеотида гена альфа-субъединицы потенциалзависимого натриевого канала (SCNA). Изобретение также относится к применению указанных олигонуклеотидов для лечения заболеваний и расстройств, ассоциированных с экспрессией гена SCNA. 6 н. и 27 з.п. ф-лы, 22 ил., 2 табл., 21 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
[0001] Данная заявка испрашивает приоритет на основании предварительной заявки на патент США № 61/357774, поданной 23 июня 2010 года, полное содержание которой включено в настоящее описание посредством ссылки.
[0002] Варианты реализации изобретения включают олигонуклеотиды, модулирующие экспрессию и/или функцию гена альфа-субъединицы потенциалзависимого натриевого канала (SCNA) и связанных с ним молекул.
УРОВЕНЬ ТЕХНИКИ
[0003] Гибридизация ДНК-РНК и РНК-РНК важна для многих аспектов функционирования нуклеиновых кислот, включая репликацию ДНК, транскрипцию и трансляцию. Процесс гибридизации также является основным во множестве технологий, которые позволяют либо обнаруживать конкретную нуклеиновую кислоту, либо изменять ее экспрессию. Антисмысловые нуклеотиды, например, нарушают экспрессию генов за счет гибридизации с РНК-мишенью, таким образом препятствуя сплайсингу РНК, транскрипции, трансляции и репликации. Антисмысловая ДНК обладает дополнительной особенностью, заключающейся в том, что гибриды ДНК-РНК выступают в качестве субстрата для ферментативного расщепления рибонуклеазой Н, активность которой присутствует в большинстве типов клеток. Антисмысловые молекулы могут быть доставлены в клетки, как в случае для олигодезоксинуклеотидов (ОДН), или они могут представлять собой продукты экспрессии эндогенных генов в виде молекул РНК. Недавно Федеральное агентство по контролю за лекарственными средствами США (FDA) одобрило антисмысловое лекарственное средство, Витравен (VITRAVENETM) (для лечения цитомегаловирусного ретинита), что отражает возможность применения антисмысловых соединений для терапевтических целей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Настоящее Краткое описание предлагает краткое описание настоящего изобретения, предназначенное для того, чтобы в сжатой форме обозначить предмет и сущность изобретения. Краткое описание представляют с пониманием того, что его не следует применять для толкования или ограничения объема или смыслового содержания формулы изобретения.
[0005] В одном варианте реализации согласно изобретению предложены способы для ингибирования действия природного антисмыслового транскрипта путем применения антисмыслового олигонуклеотида (олигонуклеотидов), нацеленного на любую область природного антисмыслового транскрипта, приводящего к увеличению экспрессии соответствующего смыслового гена. Согласно настоящему изобретению также предполагается, что ингибирование природного антисмыслового транскрипта может быть достигнуто с помощью малых интерферирующих РНК (ммРНК), рибозимов и малых молекул, рассматриваемых в рамках настоящего изобретения.
[0006] Согласно одному варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента in vivo или in vitro, включающий осуществление контакта указанных клеток или тканей с антисмысловым олигонуклеотидом длиной от 5 до 30 нуклеотидов, при этом указанный олигонуклеотид имеет по меньшей мере 50 % идентичность последовательности с последовательностью, которая представляет собой обратный комплемент полинуклеотида, содержащего от 5 до 30 последовательных нуклеотидов в пределах нуклеотидов 1-1123, последовательности SEQ ID NO: 12, и 1-2352, последовательности SEQ ID NO:13, 1-267, последовательности SEQ ID NO: 14, 1-1080, последовательности SEQ ID NO: 15, 1-173, последовательности SEQ ID NO: 16, 1-618, последовательности SEQ ID NO: 17, 1-871, последовательности SEQ ID NO: 18, 1-304, последовательности SEQ ID NO: 19, 1-293, последовательности SEQ ID NO: 20, 1-892, последовательности SEQ ID NO: 21, 1-260, последовательности SEQ ID NO: 22, 1-982, последовательности SEQ ID NO: 23, 1-906, последовательности SEQ ID NO: 24, 1-476, последовательности SEQ ID NO: 25, 1-285, последовательности SEQ ID NO: 26, 1-162, последовательности SEQ ID NO: 27, и 1-94, последовательности SEQ ID NO: 28, что приводит к модулированию функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента in vivo или in vitro.
[0007] В одном варианте реализации олигонуклеотид нацелен на природную антисмысловую последовательность для полинуклеотидов SCNA, например, на нуклеотиды, указанные в последовательностях, соответствующих SEQ ID NOS: 12-28, и любые их варианты, аллели, гомологи, мутанты, производные, фрагменты и последовательности, которые представляют собой их комплемент. Примеры антисмысловых олигонуклеотидов указаны в виде последовательностей, соответствующих SEQ ID NOS: 29-94.
[0008] Согласно другому варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента т vivo или in vitro, включающий осуществление контакта указанных клеток или тканей с антисмысловым олигонуклеотидом длиной от 5 до 30 нуклеотидов, при этом указанный олигонуклеотид имеет по меньшей мере 50% идентичность последовательности с последовательностью, которая представляет собой обратный комплемент антисмысловой последовательности для полинуклеотида SCNA; что приводит к модулированию функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента in vivo или in vitro.
[0009] Согласно другому варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента in vivo или in vitro, включающий осуществление контакта указанных клеток или тканей с антисмысловым олигонуклеотидом длиной от 5 до 30 нуклеотидов, при этом указанный олигонуклеотид имеет по меньшей мере 50% идентичность последовательности с антисмысловым олигонуклеотидом для антисмыслового полинуклеотида гена SCNA; что приводит к модулированию функции и/или экспрессии полинуклеотида SCNA в клетках или тканях пациента in vivo или in vitro.
[0010] В одном варианте реализации композиция содержит один или более антисмысловых олигонуклеотидов, которые связываются со смысловыми и/или антисмысловыми полинуклеотидами гена SCNA, при этом указанные полинуклеотиды выбраны из группы, состоящей из SCNA-SCN12A и их вариантов. В предпочтительном варианте реализации полинуклеотид-мишень выбран из SCNA.
[0011] В одном варианте реализации указанные олигонуклеотиды содержат один или более модифицированных или замещенных нуклеотидов.
[0012] В другом предпочтительном варианте реализации указанные олигонуклеотиды содержат одну или более модифицированных связей.
[0013] В еще одном варианте реализации указанные модифицированные нуклеотиды содержат модифицированные основания, включая молекулы фосфотиоатных, метилфосфонатных производных нуклеиновых кислот, пептидо-нуклеиновых кислот, 2'-О-метил-, фтор- или углерод-, метилен- или других закрытых нуклеиновых кислот (ЗНК; locked nucleic acids, LNA). Предпочтительно, указанные модифицированные нуклеотиды представляют собой молекулы закрытых нуклеиновых кислот, включая ЗНК с α-L-рибо-конфигурацией (α-L-ЗНК).
[0014] В другом предпочтительном варианте реализации указанные олигонуклеотиды вводят пациенту подкожно, внутримышечно, внутривенно или внутрибрюшинно.
[0015] В другом предпочтительном варианте реализации указанные олигонуклеотиды вводят в составе фармацевтической композиции. Схема лечения включает по меньшей мере однократное введение указанных антисмысловых соединений пациенту; однако, это лечение может быть модифицировано до введения многократных доз в течение некоторого периода времени. Указанное лечение может быть объединено с одним или более другими типами терапии.
[0016] В другом предпочтительном варианте реализации указанные олигонуклеотиды инкапсулируют в липосому или присоединяют к молекуле-носителю (например, холестерину, ТАТ-пептиду).
[0017] Другие аспекты описаны ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0018] Фигура 1 представляет собой графическое изображение результатов полимеразной цепной реакции (ПНР) в режиме реального времени, иллюстрирующее кратность изменения ± стандартное отклонение числа копий мРНК гена SCN1A после обработки клеток HepG2 фосфотиоатными олигонуклеотидами, вводимыми с применением агента для трансфекции Липофектамин 2000 (Lipofectamine 2000), по сравнению с контролем. Результаты ПЦР в режиме реального времени свидетельствуют о том, что уровни мРНК гена SCN1A в клетках HepG2 достоверно повышаются через 48 ч после обработки одним из антисмысловых олигонуклеотидов, нацеленным на антисмысловую последовательность BG724147 для гена SCN1A. Столбцы диаграммы, обозначенные как CUR-1624 - CUR-1627, соответствуют образцам, обработанным олигонуклеотидами SEQ ID NOS: 30-33, соответственно.
[0019] Фигура 2 представляет собой графическое изображение результатов ПЦР в режиме реального времени, иллюстрирующее кратность изменения ± стандартное отклонение числа копий мРНК гена SCN1A после обработки клеток HepG2 фосфотиоатными олигонуклеотидами, вводимыми с применением Липофектамина 2000, по сравнению с контролем. Столбцы диаграммы, обозначенные как CUR-1628 - CUR-1631, соответствуют образцам, обработанным олигонуклеотидами SEQ ID NOS: 34-37, соответственно.
[0020] Фигура 3 представляет собой графическое изображение результатов ПЦР в режиме реального времени, иллюстрирующее кратность изменения ± стандартное отклонение числа копий мРНК гена SCN1A после обработки клеток HepG2 фосфотиоатными олигонуклеотидами, вводимыми с применением Липофектамина 2000, по сравнению с контролем. Столбцы диаграммы, обозначенные как CUR-1632 - CUR-1636, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 38-42, соответственно.
[0021] Фигура 4 иллюстрирует дозозависимое увеличение экспрессии мРНК гена SCN1A в первичных фибробластах кожи человека, несущих мутацию, ассоциированную с синдромом Драве. Обозначения CUR-1916, CUR-1740, CUR-1764 и CUR-1770 соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 70, 45, 52 и 57, соответственно.
[0022] Фигура 5 иллюстрирует дозозависимое увеличение экспрессии мРНК гена SCN1A в клетках SK-N-AS. Обозначения CUR-1916, CUR-1740, CUR-1764 и CUR-1770 соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 70, 45, 52 и 57, соответственно.
[0023] Фигура 6 иллюстрирует дозозависимое увеличение экспрессии мРНК гена SCN1A в клетках Vero 76. Обозначения CUR-1916, CUR-1740, CUR-1764 и CUR-1770 соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 70, 45, 52 и 57, соответственно.
[0024] Фигура 7 иллюстрирует, что увеличение экспрессии мРНК гена SCN1A не вызвано неспецифической токсичностью антисмысловых олигонуклеотидов. А - увеличение экспрессии при обработке олигонуклеотидом CUR-1916; В - увеличение экспрессии при обработке олигонуклеотидом CUR-1770. Олигонуклеотид CUR-1462 представляет собой неактивный контрольный олигонуклеотид, характеризующийся сходной химической структурой.
[0025] Фигура 8 иллюстрирует, что обработка антисмысловыми олигонуклеотидами, нацеленными на природный антисмысловой транскрипт гена SCN1A, не оказывает существенного влияния на экспрессию каналов SCN8A и SCN9A в фибробластах человека, несущих мутацию, ассоциированную с синдромом Драве. А - обработка олигонуклеотидом CUR-1770; В - обработка олигонуклеотидом CUR-1916.
[0026] Фигура 9 иллюстрирует стабильность антисмысловых олигонуклеотидов, нацеленных на SCN1A-специфичный природный антисмысловой транскрипт. Клетки Vero 76 обрабатывали в соответствии с описанием, приведенным в Примере 2, двумя разными партиями олигонуклеотида CUR-1916, синтезированного в августе 2010 года и марте 2011 года. Олигонуклеотид, синтезированный в августе 2010 года, хранили в виде водного раствора с концентрацией 1 мМ при температуре 4°С. Олигонуклеотид, синтезированный в марте 2011 года, был отправлен в лиофилизированной форме и проверен сразу после доставки.
[0027] Фигура 10 иллюстрирует увеличение экспрессии белка SCN1A в фибробластах, несущих мутацию, ассоциированную с синдромом Драве, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Фибробласты выращивали в 24-луночных планшетах и обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрации 20 нМ (панель с: CUR-1740; d: CUR-1770; e: CUR-1916) и 0 нМ (b). Клетки окрашивали на белок SCN1A (b-е) посредством непрямого иммуногистохимического метода с применением антител к белку SCN1A (Abeam cat#ab24820) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat#PK-6101; Vector Laboratories cat#SK-4105); панель а - отрицательный контроль, кроличьи антимышиные антитела применяли в качестве первичных антител с той же последующей процедурой окрашивания, как и на панелях b-е.
[0028] Фигура 11 иллюстрирует увеличение экспрессии белка SCN1A в клетках SK-N-AS, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Клетки SK-N-AS выращивали в 24-луночных планшетах и обрабатывали олигонуклеотидами в концентрации 20 нМ (с: CUR-1740; d: CUR-1764; e: CUR-1770; f: CUR-1916) и (b: 0 нМ). Клетки SK-N-AS окрашивали на белок SCN1A (b-f) посредством непрямого иммуногистохимического метода с применением антител к белку SCN1A (Abeam cat#ab24820) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat#PK-6101; Vector Laboratories cat#SK-4105); в качестве отрицательного контроля применяли кроличьи антимышиные антитела в качестве первичных антител с той же последующей процедурой окрашивания, как и на панелях b-f (панель а).
[0029] Фигура 12 иллюстрирует увеличение экспрессии белка SCN1A в клетках Vero 76, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Клетки Vero 76 выращивали в 24-луночных планшетах и обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрации 20 нМ (с: CUR-1740; d: CUR-1945; e: CUR-1770; f: CUR-1916; g: CUR-1924) и 0 нМ (b). Клетки Vero 76 окрашивали на белок SCN1A (b-g) посредством непрямого иммуногистохимического метода с применением антител к белку SCN1A (Abeam cat#ab24820) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat# РК-6101; Vector Laboratories cat#SK-4105); панель а - в качестве отрицательного контроля применяли кроличьи антимышиные антитела в качестве первичных антител с той же последующей процедурой окрашивания, как и на панелях b-g.
[0030] Фигура 13 иллюстрирует, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, увеличивающие экспрессию мРНК гена SCN1A, не увеличивают экспрессию гена актина в клетках Vero 76. Те же самые антисмысловые олигонуклеотиды (CUR-1740, CUR-1838, CUR-1924), нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, которые, как было показано в Примерах 5 и 12, увеличивают экспрессию мРНК и белка SCN1A, исследовали на их влияние на экспрессию мРНК гена бета-актина в клетках Vero 76. Данные эксперимента подтверждают, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, не увеличивают экспрессию неродственного гена, такого как ген актина. Столбцы диаграммы, обозначенные как CUR-1740, CUR-1838 и CUR-1924, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 45, 62 и 78, соответственно.
[0031] Фигура 14 иллюстрирует, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, которые, как было показано, увеличивают экспрессию мРНК и белка SCN1A, не увеличивают экспрессию гена актина в фибробластах, несущих мутацию, ассоциированную с синдромом Драве. Олигонуклеотиды (CUR-1916, CUR-1945), нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, которые, как было показано в Примерах 2 и 7, увеличивают экспрессию мРНК и белка SCN1A, исследовали на их влияние на экспрессию мРНК гена актина в фибробластах, несущих мутацию, ассоциированную с синдромом Драве. Приведенные ниже данные подтверждают, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, не увеличивают экспрессию неродственного гена, такого как ген актина. Столбцы диаграммы, обозначенные как CUR-1916 и CUR-1945, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 70 и 93, соответственно.
[0032] Фигура 15 иллюстрирует, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, которые, как было показано, увеличивают экспрессию мРНК и белка SCN1A, не увеличивают экспрессию гена актина в клетках SK-N-AS. Те же самые антисмысловые олигонуклеотиды (CUR-1740, CUR-1770, CUR-1916, CUR-1764, CUR-1838), которые, как было показано в Примерах, увеличивают экспрессию мРНК и белка SCN1A, исследовали на их влияние на экспрессию мРНК гена актина в клетках SK-N-AS. Данные эксперимента подтверждают, что олигонуклеотиды, нацеленные на SCN1A-специфичный природный антисмысловой транскрипт, не увеличивают экспрессию неродственного гена, такого как ген актина. Столбцы диаграммы, обозначенные как CUR-1740, CUR-1770, CUR-1916, CUR-1764, CUR-1838, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 45, 57, 70, 52 и 62, соответственно.
[0033] Фигура 16 иллюстрирует окрашивание белка актина в клетках SK-N-AS, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Клетки SK-N-AS выращивали в 24-луночных планшетах и обрабатывали олигонуклеотидами в концентрации 20 нМ (b: CUR-1740; с: CUR-1764; d: CUR-1770; e: CUR-1916) и 0 нМ (а). Клетки SK-N-AS окрашивали на актин (a-е) посредством непрямого иммуногистохимического метода с применением антител к актину (Abeam cat#ab1801) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat#PK-6101; Vector Laboratories cat#SK-4105).
[0034] Фигура 17 иллюстрирует окрашивание белка актина в клетках Vero 76, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Клетки Vero 76 выращивали в 24-луночных планшетах и обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрации 20 нМ (b: CUR-1740; с: CUR-1770; d: CUR-1916; e: CUR-1924; f: CUR-1945) и 0 нМ (а). Клетки Vero 76 окрашивали на актин (b-f) посредством непрямого иммуногистохимического метода с применением антител к актину (Abeam cat#abl801) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat# PK-6101; Vector Laboratories cat#SK-4105); панель а - отрицательный контроль, кроличьи антимышиные антитела применяли в качестве первичных антител с той же последующей процедурой окрашивания, как и на панелях b-g.
[0035] Фигура 18 иллюстрирует увеличение экспрессии белка актина в фибробластах, несущих мутацию, ассоциированную с синдромом Драве, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A. Фибробласты выращивали в 24-луночных планшетах и обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрации 20 нМ (панель b: CUR-1740; с: CUR-1764; d: CUR-1770; e: CUR-1838 и f: CUR-1916) и 0 нМ (а). Клетки окрашивали на актин (a-f) посредством непрямого иммуногистохимического метода с применением антител к актину (Abeam cat#ab1801) и окрашивания/усиления сигнала вторичными антителами, основанного на взаимодействии авидин/биотин (Vector Laboratories cat#SP-2001; Vector Laboratories cat#PK-6101; Vector Laboratories cat#SK-4105).
[0036] Фигура 19 иллюстрирует увеличение экспрессии белка SCN1A в фибробластах, несущих мутацию, ассоциированную с синдромом Драве, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, количественно определенное с применением иммуноферментного анализа (ИФА; enzyme-linked immunosorbent assay, ELISA). Фибробласты обрабатывали олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрациях 0 или 80 нМ. Через 48 ч клетки переносили в 96-луночный планшет на 24 ч перед фиксацией и исследованием с помощью ИФА-систем для определения белка SCN1A и актина. Показания оптической плотности (ОП) для сигнала белка SCN1A нормализовывали к сигналу актина для одних и тех же условий проведения эксперимента. Нормализованный сигнал белка SCN1A в клетках, обработанных олигонуклеотидами в концентрации 0 нМ, применяли в качестве точки отсчета (100%). Столбцы диаграммы, обозначенные как CUR-1740, CUR-1770 и CUR-1916, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 45, 57 и 70, соответственно.
[0037] Фигура 20 иллюстрирует увеличение экспрессии белка SCN1A в клетках Vero 76, обработанных антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, количественно определенное с применением ИФА. Клетки Vero 76 обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрациях 0 или 80 нМ. Через 48 ч клетки переносили в 96-луночный планшет на 24 ч перед фиксацией и исследованием с помощью ИФА-систем для определения белка SCN1A и актина. Показания ОП для сигнала белка SCN1A нормализовывали к сигналу актина для одних и тех же условий проведения эксперимента. Нормализованный сигнал белка SCN1A в клетках, обработанных олигонуклеотидами в концентрации 0 нМ, применяли в качестве точки отсчета (100 %). Столбцы диаграммы, обозначенные как CUR-1740, CUR-1770, CUR-1916, CUR-1924, CUR-1945, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 45, 57, 70, 78 и 93, соответственно.
[0038] Фигура 21 иллюстрирует увеличение экспрессии белка SCN1A в клетках SK-N-AS, обработанных олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, количественно определенное с применением ИФА. Клетки SK-N-AS обрабатывали антисмысловыми олигонуклеотидами, комплементарными природной антисмысловой последовательности для гена SCN1A, в концентрациях 0 или 20 нМ. Через 48 ч клетки переносили в 96-луночный планшет на 24 ч перед фиксацией и исследованием с помощью ИФА-систем для определения белка SCN1A и актина. Показания ОП для сигнала белка SCN1A нормализовывали к сигналу актина для одних и тех же условий проведения эксперимента. Нормализованный сигнал белка SCN1A в клетках, обработанных олигонуклеотидами в концентрации 0 нМ, применяли в качестве точки отсчета (100 %). Столбцы диаграммы, обозначенные как CUR-1740, CUR-1770, CUR-1924, CUR-1945, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 45, 57, 78 и 93, соответственно.
[0039] На Фигуре 22 показаны продукты после второго раунда ПЦР с быстрой амплификацией 3'-концевого фрагмента кДНК (3'-rapid amplification of cDNA ends, 3'-RACE) природного антисмыслового транскрипта BG724147 гена SCN1A. 3'-RACE была проведена с применением: а) тотальной РНК из клеток HepG2 с добавлением аденозина; b - РНК, содержащей поли(А)-последовательность, выделенной из клеток HepG2; с - с применением тотальной РНК из первичных фибробластов человека, несущих мутацию, ассоциированную с синдромом Драве, с добавлением аденозина; d - с применением РНК, содержащей поли(А)-последовательность, выделенной из первичных фибробластов человека, несущих мутацию, ассоциированную с синдромом Драве. Фигура представляет собой негатив электрофореграммы, полученной в результате проведения электрофореза в 1% агарозном геле/lx буфере ТАЕ (смесь трис/уксусная кислота/ЭДТА) с окрашиванием геля красителем GelRed (GenScript, cat#M00120). Стрелки указывают на зоны, общие для клеток HepG2 и первичных фибробластов человека, несущих мутацию, ассоциированную с синдромом Драве, что свидетельствует о наличии природного антисмыслового транскрипта BG724147 в этих клетках.
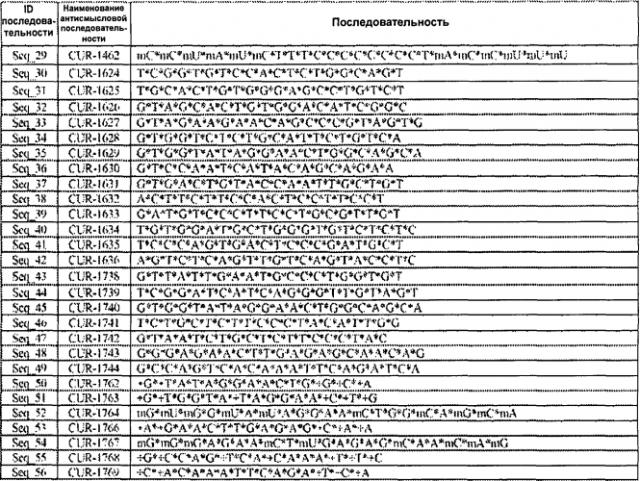
[0040] Описание Перечня последовательностей - SEQ ID NO: 1: Альфа-субъединица потенциалзависимого натриевого канала типа I (SCN1A) человека, транскриптный вариант 1, мРНК (номер последовательности в базе данных NCBI (Национального центра биотехнологической информации США): NM_001165963); SEQ ID NO: 2: Альфа-субъединица потенциалзависимого натриевого канала типа II (SCN2A) человека, транскриптный вариант 1, мРНК (номер последовательности в базе данных NCBI: NM_021007); SEQ ID NO: 3: Альфа-субъединица потенциалзависимого натриевого канала типа III (SCN3A) человека, транскриптный вариант 1, мРНК (номер последовательности в базе данных NCBI: NM_006922); SEQ ID NO: 4: Альфа-субъединица потенциалзависимого натриевого канала типа IV (SCN4A) человека, мРНК (номер последовательности в базе данных NCBI: NM_000334); SEQ ID NO: 5: Альфа-субъединица потенциалзависимого натриевого канала типа V (SCN5A) человека, транскриптный вариант 1, мРНК (номер последовательности в базе данных NCBI: NM_198056); SEQ ID NO: 6: Альфа-субъединица потенциалзависимого натриевого канала типа VII (SCN7A) человека, мРНК (номер последовательности в базе данных NCBI: NM_002976); SEQ ID NO: 7: Альфа-субъединица потенциалзависимого натриевого канала типа VIII (SCN8A) человека, транскриптный вариант 1, мРНК (номер последовательности в базе данных NCBI: NM_014191); SEQ ID NO: 8: Альфа-субъединица потенциалзависимого натриевого канала типа IX (SCN9A) человека, мРНК (номер последовательности в базе данных NCBI: NM_002977); SEQ ID NO: 9: Альфа-субъединица потенциалзависимого натриевого канала типа Х (SCN10A) человека, мРНК (номер последовательности в базе данных NCBI: NM_006514); SEQ ID NO: 10: Альфа-субъединица потенциалзависимого натриевого канала типа XI (SCN11A) человека, мРНК (номер последовательности в базе данных NCBI: NM_014139); SEQ ID NO: 11: Альфа-субъединица потенциалзависимого натриевого канала SCN12A (SCN12A) человека, мРНК, полная кодирующая последовательность (номер последовательности в базе данных NCBI: AF109737); SEQ ID NO: 12: Природная антисмысловая последовательность для гена SCN1A (BG724147 расширенная); SEQ ID NO: 13: Природная антисмысловая последовательность для гена SCN1A (Hs.662210); SEQ ID NO: 14: Природная антисмысловая последовательность для гена SCN1A (АА383040); SEQ ID NO: 15: Природная антисмысловая последовательность для гена SCN1A (ВС029452); SEQ ID NO: 16: Природная антисмысловая последовательность для гена SCN1A (АА630035); SEQ ID NO: 17: Природная антисмысловая последовательность для гена SCN1A (ВЕ566126); SEQ ID NO: 18: Природная антисмысловая последовательность для гена SCN1A (BF673100); SEQ ID NO: 19: Природная антисмысловая последовательность для гена SCN1A (BG181807); SEQ ID NO: 20: Природная антисмысловая последовательность для гена SCN1A (BG183871); SEQ ID NO: 21: Природная антисмысловая последовательность для гена SCN1A (BG215777); SEQ ID NO:22: Природная антисмысловая последовательность для гена SCN1A (BG227970); SEQ ID NO: 23: Природная антисмысловая последовательность для гена SCN1A (ВМ905527); SEQ ID NO: 24: Природная антисмысловая последовательность для гена SCN1A (BU180772); SEQ ID NO: 25: Природная антисмысловая последовательность для гена SCN1A мыши (BG724147 ExtMouse); SEQ ID NO: 26: Природная антисмысловая последовательность для гена SCN1A мыши (Hs.662210mouseAS1); SEQ ID NO: 27: Природная антисмысловая последовательность для гена SCN1A мыши (Hs.662210mouseAS2); SEQ ID NO: 28: Природная антисмысловая последовательность для гена SCN1A мыши (Hs.662210mouseAS3); SEQ ID NOS: 29-94: Антисмысловые олигонуклеотиды. SEQ ID NO: 95 и 96 являются последовательностями, представляющими собой обратные комплементы антисмысловых олигонуклеотидов, соответствующих SEQ ID N0:58 и 59, соответственно. Символ "*" обозначает фосфотиоатную связь, "+" обозначает ЗНК, "r" обозначает РНК, а "m" указывает на наличие метильной группы на 2'-атоме кислорода в обозначенном сахарном остатке олигонуклеотида.
ПОДРОБНОЕ ОПИСАНИЕ
[0041] Некоторые аспекты изобретения описаны ниже со ссылкой на примеры применения для иллюстрации. Следует понимать, что многочисленные конкретные детали, связи и способы приведены с целью обеспечения полного понимания изобретения. Однако для специалиста в данной области техники будет очевидно, что изобретение может быть применено на практике без одной или более конкретных деталей или с применением других способов. Настоящее изобретение не ограничивается указанным порядком действий или процессов, так как некоторые действия могут быть осуществлены в разных порядках и/или одновременно с другими действиями или процессами. Кроме того, не все представленные в качестве примеров действия или процессы необходимы для реализации методологии в соответствии с настоящим изобретением.
[0042] Все гены, названия генов и продукты генов, описанные в настоящей заявке, соответствуют гомологам из организмов любых видов, для которых применимы композиции и способы, предложенные в настоящей заявке. Таким образом, данные термины включают, но не ограничиваются перечисленными, гены и генные продукты из организмов людей и мышей. Следует понимать, что, когда предложен ген или продукт гена из организма конкретного вида, этот элемент изобретения представлен исключительно в качестве примера, и его не следует истолковывать как ограничение, если контекст, в котором он появляется, ясно не предписывает иное. Соответственно, например, гены, описанные в настоящей заявке, которые в некоторых вариантах реализации относятся к нуклеотидным и аминокислотным последовательностям млекопитающих, охватывают гомологичные и/или ортологичные гены и продукты генов из организмов других животных, включая, но не ограничиваясь перечисленными, других млекопитающих, рыб, земноводных, пресмыкающихся и птиц. В предпочтительных вариантах реализации гены или нуклеотидные последовательности представляют собой гены или последовательности человека.
Определения
[0043] Терминология, применяемая в настоящей заявке, служит исключительно для описания конкретных вариантов реализации и не ограничивает изобретение. В настоящей заявке неопределенная и определенная формы единственного числа также включают множественные формы, если контекст ясно не предписывает иное. Кроме того, в той мере, в какой термины "включающий", "включает", "имеющий", "имеет", "с" или их варианты применяют в подробном описании и/или формуле изобретения, такие термины подразумевают включение в себя подобно термину "содержащий".
[0044] Термин "примерно" или "приблизительно" обозначает нахождение внутри диапазона приемлемой погрешности для конкретной величины, определенного специалистом в данной области техники, который будет зависеть отчасти от того, каким образом величину измеряют или определяют, т.е. от ограничений измерительной системы. Например, термин "примерно" может означать, что величина находится в пределах 1 или более чем 1 стандартного отклонения, как показывает практика в данной области техники. Альтернативно, термин "примерно" может означать диапазон погрешности, составляющий вплоть до 20%, предпочтительно вплоть до 10%, более предпочтительно вплоть до 5% и еще более предпочтительно вплоть до 1% от заданной величины. Альтернативно, применительно к биологическим системам или процессам, термин может означать нахождение в пределах порядка величины, предпочтительно в пределах пятикратного значения и более предпочтительно в пределах двукратного значения величины. В тех случаях, когда в заявке и формуле изобретения приведены конкретные значения, то, если не указано иное, следует считать, что термин "примерно" обозначает нахождение внутри диапазона приемлемой погрешности для конкретной величины.
[0045] В настоящей заявке термин "мРНК" обозначает известный на настоящий момент мРНК-транскрипт(ы) гена-мишени и любые дополнительные транскрипты, происхождение которых может быть объяснено.
[0046] С помощью терминов "антисмысловые олигонуклеотиды" или "антисмысловое соединение" обозначают молекулу РНК или ДНК, которая связывается с другой РНК или ДНК (РНК-, ДНК-мишенью). Например, если антисмысловое соединение представляет собой олигорибонуклеотид, оно связывается с другой РНК-мишенью за счет РНК-РНК-взаимодействий и изменяет активность РНК-мишени. Антисмысловой олигонуклеотид может увеличивать или подавлять экспрессию и/или функцию конкретного полинуклеотида. Определение включает любую чужеродную молекулу ДНК или РНК, подходящую с терапевтической, диагностической или другой точки зрения. Такие молекулы включают, например, молекулы антисмысловых ДНК или РНК, молекулы интерферирующих РНК (РНКи), микроРНК, ложных РНК, ммРНК, ферментативные РНК, РНК, применяемые в исправляющей терапии, и РНК, имеющие свойства агонистов и антагонистов, антисмысловые олигомерные соединения, антисмысловые олигонуклеотиды, олигонуклеотиды внешней направляющей последовательности (external guide sequence, EGS), сплайс-варианты, праймеры, зонды и другие олигомерные соединения, которые гибридизуются с по меньшей мере частью нуклеиновой кислоты-мишени. В связи с этим данные соединения могут быть введены в форме одноцепочечных, двухцепочечных, частично одноцепочечных или кольцевых олигомерных соединений.
[0047] В контексте настоящего изобретения термин "олигонуклеотид" относится к олигомеру или полимеру рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или их миметикам. Термин "олигонуклеотид" также включает линейные или кольцевые олигомеры природных и/или модифицированных мономеров или связей, включая дезоксирибонуклеозиды, рибонуклеозиды, их замещенные и альфа-аномерные формы, пептидо-нуклеиновые кислоты (ПНК), закрытые нуклеиновые кислоты (ЗНК; locked nucleic acids, LNA), фосфотиоатные, метилфосфонатные производные и т.п. Олигонуклеотиды способны к специфическому связыванию с полинуклеотидом-мишенью за счет регулярных взаимодействий между мономерными звеньями, такими как Уотсон-Криковский тип спаривания оснований, Хугстиновский или обратный Хугстиновский типы спаривания оснований и т.п.
[0048] Олигонуклеотид может быть "химерным", то есть составленным из разных областей. В контексте настоящего изобретения "химерные" соединения представляют собой олигонуклеотиды, которые содержат две или более химически отличные области, например, область (области) ДНК, область (области) РНК, область (области) ПНК и т.д. Каждая химически отличная область состоит из по меньшей мере одной мономерной единицы, т.е. нуклеотида в случае олигонуклеотидного соединения. Эти олигонуклеотиды, как правило, содержат по меньшей мере одну область, в которой олигонуклеотид модифицирован с целью проявления одного или более желаемых свойств. Желаемые свойства олигонуклеотида включают, но не ограничиваются перечисленными, например, повышенную устойчивость к деградации нуклеазами, повышенное клеточное поглощение и/или повышенную способность к связыванию с нуклеиновой кислотой-мишенью. Разные области олигонуклеотида могут, таким образом, обладать разными свойствами. Химерные олигонуклеотиды согласно настоящему изобретению могут быть образованы в виде смешанных структур из двух или более олигонуклеотидов, модифицированных олигонуклеотидов, олигонуклеозидов и/или аналогов олигонуклеотидов, описанных выше.
[0049] Олигонуклеотид может быть составлен из областей, которые могут быть соединены в "ряд", то есть когда мономеры соединены последовательно, как в нативной ДНК, или соединены посредством спейсеров. Спейсеры формируют ковалентный "мостик" между областями и имеют в предпочтительных случаях длину, не превышающую примерно 100 углеродных атомов. Спейсеры могут иметь разные функциональные характеристики, например, нести положительный или отрицательный заряд, обладать свойствами специфичного связывания нуклеиновых кислот (интеркаляторы, вещества, связывающиеся с бороздками, токсины, флуорофоры и т.д.), быть липофильными, индуцировать образование специфических вторичных структур, как, например, аланинсодержащие пептиды, которые индуцируют образование альфа-спиралей.
[0050] В настоящей заявке термины "ген SCN1A" и "альфа-субъединица потенциалзависимото натриевого канала типа I" включают все члены семейства, мутанты, аллели, фрагменты, виды, кодирующие и некодирующие последовательности, смысловые и антисмысловые полинуклеотидные цепи и т.д. Аналогично, гены SCN2A-SCN12A включают все мутанты, аллели, фрагменты и т.д.
[0051] В настоящем описании слова "альфа-субъединица потенциалзависимого натриевого канала типа I", SCN1A, FEB3, FEB3A, GEFSP2, HBSCI, NaCl, Nav1.1, SCN1, SMEI, альфа-субъединица белка натриевого канала мозга I, альфа-субъединица белка натриевого канала типа 1, альфа-субъединица белка натриевого канала типа I и альфа-субъединица потенциалзависимого натриевого канала Nav1.1 рассматривают как имеющие одно и то же значение в литературе и применяют взаимозаменяемо в настоящей заявке.
[0052] В настоящей заявке термин "олигонуклеотид, специфичный к" или "олигонуклеотид, нацеленный на" относится к олигонуклеотиду, содержащему последовательность, (i) способную образовывать стабильный комплекс с частью гена-мишени или (ii) способную образовывать стабильный дуплекс с частью мРНК-транскрипта гена-мишени. Стабильность комплексов и дуплексов может бы