Продукты питания, содержащие олигосахариды человеческого молока, и способы их получения
Иллюстрации
Показать всеИзобретение относится к продукту питания для грудных детей или детским смесям и способу их производства. Способ включает обработку посредством каталитического гидрогенолиза для удаления групп R смеси по меньшей мере двух соединений, выбранных из группы, содержащей соединения общих формул 1 и 2 и их соли, посредством каталитического гидрогенолиза для удаления группы R.
R1 независимо является фукозилом или H; R2 выбран из N-ацетил-лактозаминильной и лакто-N-биозильной групп, где N-ацетил-лактозаминильная группа может нести гликозильный остаток, содержащий одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп. R3 является H или N-ацетил-лактозаминильной группой. Любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками. R4 независимо является сиалилом или H. По меньшей мере один из R1 или R4 не является H в общей формуле 2. Количество смеси вышеуказанных соединений выбирают так, чтобы указанная смесь олигосахаридов человеческого молока имела олигосахаридный профиль, по существу подобный профилю молозива, переходного грудного молока и зрелого грудного молока. 2 н. и 19 з.п. ф-лы, 1 ил., 6 табл., 6 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способам получения продуктов питания для грудных детей или детских смесей, содержащих олигосахариды, в частности олигосахариды человеческого молока. Кроме того, настоящее изобретение относится к питательным композициям, содержащим такие олигосахариды человеческого молока.
Уровень техники
Олигосахариды человеческого молока (ОЧМ) являются углеводами, интерес к которым сильно возрос за последние годы. В частности, синтез ОЧМ существенно возрос, благодаря роли ОЧМ в многочисленных биологических процессах человека. ОЧМ играют важную роль в раннем развитии детей младшего возраста. Кроме того, важность ОЧМ определяется также их ролью в созревании иммунной системы и их прогнозируемая активность в качестве иммуномодуляторов.
Природным источником ОЧМ является молоко млекопитающих. Молоко млекопитающих содержит до 10% ОЧМ. На сегодняшний день определена структура по меньшей мере 115 ОЧМ, в то время как данные масс-спектрометрии (МС) позволяют предположить наличие почти что 130 ОЧМ (Newburg and Neubauer, 1995, «Carbohydrates in milks: Analysis, quantities and significance)) в Handbook of Milk Composition (R.G. Jensen, ed.), стр.273-249, Academic Press, San Diego, USA).
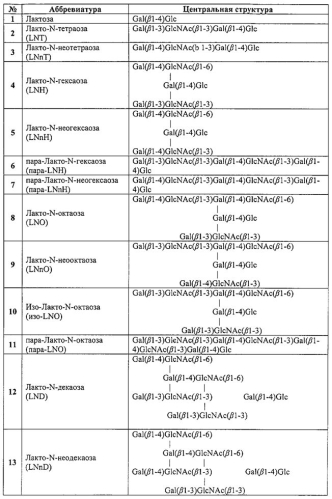
115 олигосахаридов человеческого молока, структура которых определена к настоящему времени, можно разделить на 13 категорий, основываясь на различиях в их центральных структурах. Эти 13 категорий структур проиллюстрированы в таблице 1 ниже (см. также Urashima et al., Advanced Dairy Chemistry, Volume 3: «Lactose, Water, Salts and Minor Constituents)), 2009, стр.295-349; и Tadasu Urashima et al., «Milk oligosaccharides)), Nova Biomedical Books, New York, 2011, ISBN: 978-1-61122-831-1).
| Таблица 1. | |
| Различные центральные структуры олигосахаридов человеческого молока (ОЧМ). |
Из-за большого количества различных ОЧМ и их низких концентраций в молоке млекопитающих выделение ОЧМ из молока млекопитающих является трудной задачей. Таким образом, трудно обеспечить подходящую замену ОЧМ в продуктах питания, в частности в детских смесях, содержащую по меньшей часть из полного спектра ОЧМ.
Хотя известны химические и ферментативные способы получения ОЧМ, такие способы получения не позволяют получать смеси ОЧМ. Кроме того, приготовление таких смесей ОЧМ на основе индивидуально разработанных методов синтеза отдельных ОЧМ является дорогостоящим и не может обеспечить большого разнообразия ОЧМ, сколько-нибудь близкого к ОЧМ природного происхождения.
Таким образом, имеется потребность в способе производства смесей ОЧМ, обладающих профилем, подобным смеси ОЧМ человеческого молока.
Также имеется потребность в способе производства ОЧМ в относительно большом масштабе без применения сложных и дорогостоящих способов, подобных биотехнологическим способам.
Имеется потребность в способе, позволяющем получать смеси ОЧМ в большом масштабе производства.
Раскрытие изобретения
В одном аспекте настоящего изобретения раскрывается способ производства детских смесей или продуктов питания для грудных детей, содержащих смесь олигосахаридов человеческого молока (ОЧМ). Этот способ включает обработку смеси по меньшей мере двух соединений, выбранных из группы, содержащей соединения общей формулы 1 и 2, посредством каталитического гидрогенолиза для удаления группы R.
R является группой, удаляемой в результате каталитического гидрогенолиза;
R1 независимо является фукозилом или H;
R2 выбран из N-ацетил-лактозаминильной и лакто-N-биозильной групп, где N-ацетил-лактозаминильная группа может нести гликозильный остаток, содержащий одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками;
R3 является H или N-ацетил-лактозаминильной группой, необязательно замещенной гликозильным остатком, содержащим одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками;
R4 независимо является сиалилом или H;
и их соли,
с тем условием, что по меньшей мере один из R1 или R4 не является H в общей формуле 2.
Конкретный профиль олигосахаридов, или конкретное отношение олигосахаридов выбирается таким образом, чтобы они наилучшим образом соответствовали аналогичным профилю или отношению грудного молока человека.
В другом аспекте изобретения раскрывается продукт питания для грудных детей или детская смесь. Продукт питания для грудных детей или детская смесь содержат смесь олигосахаридов человеческого молока, полученную способом по настоящему изобретению.
Краткое описание чертежей
На фиг.1 показан состав, включающий смесь по меньшей мере двух соединений, выбранных из группы, содержащей соединения общих формул 1 и 2.
Подробное описание изобретения
Для полного понимания сути настоящего изобретения и его преимуществ следует обратиться к следующему подробному описанию.
Необходимо понимать, что различные варианты осуществления настоящего изобретения можно объединять с другими вариантами осуществления изобретения, и что они являются просто иллюстрациями конкретных путей осуществления и использования настоящего изобретения, но не ограничивают объем изобретения, если рассматривать формулу изобретения и следующее подробное описание.
Предпочтительно задача, лежащая в основе настоящего изобретения, решается путем получения композиции, содержащей смесь по меньшей мере двух соединений, выбранных из группы, содержащей соединения общих формул 1 и 2, как показано на фиг.1.
где R является группой, удаляемой в результате каталитического гидрогенолиза;
R1 независимо является фукозилом или H;
R2 выбран из N-ацетил-лактозаминильной и лакто-N-биозильной групп, где N-ацетил-лактозаминильная группа может нести гликозильный остаток, содержащий одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками;
R3 является H или N-ацетил-лактозаминильной группой, необязательно замещенной гликозильным остатком, содержащим одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками;
R4 независимо является сиалилом или H;
и их соли,
с тем условием, что по меньшей мере один из R1 или R4 не является H в общей формуле 2.
Смесь ОЧМ получают путем каталитического гидрогенолиза соединений общих формул 1 и 2.
В контексте настоящего изобретения выражение «группа, удаляемая каталитическим гидрогенолизом» относится к группам, в которых C-O связь расщепляется в результате присоединения водорода в присутствии катализатора гидрогенолиза. Катализатор гидрогенолиза используется в присутствии газообразного водорода под давлением при нагревании. Катализатором гидрогенолиза может быть, например, палладий, никель Ренея, палладиевый катализатор на угольном носителе или палладиевая чернь, или другой подходящий металлический катализатор, используемый при гидрогенолизе. Таким образом, применение катализатора гидрогенолиза в настоящем изобретении приводит к регенерации - OH группы из R группы соединений общих формул 1 и 2. R группы такого типа известны (см., например, P.G.M. Wuts и T.W. Greene: «Protective Groups in Organic Synthesis», John Wiley & Sons (2007). Подходящие R группы включают бензильную, дифенилметильную (бензгидрильную), 1-нафтилметильную, 2-нафтилметильную или трифенилметильную (тритильную) группы, каждая из которых может быть необязательно замещена одной или несколькими группами, выбранными из: алкильной, алкокси, фенильной, амино, ациламино, алкиламино, диалкиламино, нитро, карбоксильной, алкоксикарбонильной, карбамоильной, N-алкилкарбамоильной, N,N-диалкилкарбамоильной, азидо, галогеналкильной или галогеновой группы. Предпочтительно такое замещение, если оно присутствует, осуществляется на ароматическом кольце (кольцах). Особо предпочтительной защитной группой является бензильная, необязательно замещенная одной или несколькими группами, выбранными ил алкила или галогена. Более предпочтительно защитная группа выбрана из ненасыщенной бензильной, 4-хлоробензильной и 4-метилбензильной. Эти особо предпочтительные и наиболее предпочтительные защитные группы обладают тем преимуществом, что побочными продуктами гидрогенолиза в таком случае являются исключительно толуол или замещенный толуол. Такие побочные продукты легко удалить, даже в многотонном масштабе, из водорастворимых олигосахаридных продуктов с использованием способов выпаривания и/или экстракции.
Кроме того, термин «фукозил» в контексте настоящего изобретения предпочтительно означает L-фукопиранозильную группу, присоединенную к олигосахариду из соединений общих формул 1 и 2 посредством α-интергликозидной связи, такую как:
.
«N-ацетил-лактозаминильная» группа в контексте настоящего изобретения предпочтительно означает гликозильный остаток N-ацетил-лактозамина (LacNAc, Galpβ1-4GlcNAcp) из соединений общих формул 1 и 2, соединенный β-связью, такой как:
.
Далее, термин «лакто-N-биозильная» группа в контексте настоящего изобретения предпочтительно означает гликозильный остаток лакто-N-биозы (LNB, Galpβ1-3GlcNAcp) соединений общих формул 1 и 2, связанный β-связью, такой как:
.
Термин «сиалильный» в контексте настоящего изобретения предпочтительно означает гликозильный остаток сиаловой кислоты (N-ацетил-нейраминовой кислоты, Neu5Ac) соединений общих формул 1 и 2, соединенный β-связью, такой как:
.
Термин «гликозильный остаток, содержащий одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных единиц» в контексте настоящего изобретения предпочтительно означает линейную или разветвленную структуру, содержащую указанные единицы, связанные друг с другом интергликозидными связями.
В соответствии с упомянутым выше способом берутся по меньшей мере два соединения, выбранные из группы, включающей соединения общих формул 1 и 2, в которых R является группой, удаляемой при каталитическом гидрогенолизе. Такая смесь соединений, как уже упоминалось, предпочтительно является смесью по меньшей мере двух, однако возможно и трех, четырех, пяти, двух-пяти, пяти-десяти, двух-десяти, двух-двадцати, трех-двадцати, четырех(или даже пяти)-двадцати или еще большего числа соединений, выбранных из группы, содержащей соединения общих формул 1 и 2.
Заявленный способ основан на использовании по меньшей мере двух соединений, выбранных из группы, включающей соединения, характеризующиеся общими формулами 1 и 2, определенными выше, в процессе каталитическом гидрогенолизе. Данная реакция типично осуществляется в протонном растворителе или в смеси протонных растворителей. Протонный растворитель может быть выбран из группы, состоящей из воды, уксусной кислоты или C1-C6 спиртов. Можно также использовать смесь одного или нескольких протонных растворителей с одним или несколькими подходящими апротонными органическими растворителями, частично или полностью смешиваемыми с протонным растворителем(ями) (такими как ТГФ, диоксан, этилацетат или ацетон). Воду, один или несколько C1-C6 спиртов или смесь воды и одного или нескольких C1-C6 спиртов предпочтительно используют в качестве системы растворителей. Также можно использовать растворы, содержащие производные углеводов в любой концентрации, или суспензии производных углеводов в используемом растворителе(ях). Реакционную смесь перемешивают при температуре в диапазоне 10-100°C, предпочтительно 20-50°C, в водородной атмосфере с абсолютным давлением 1-50 бар (100-5000 кПа) в присутствии такого катализатора, как палладий, никель Ренея или любой другой подходящий металлический катализатор, предпочтительно палладий на угольном носителе или палладиевая чернь, до завершения реакции. Можно также использовать трансферную гидрогенизацию, когда водород генерируется in situ из циклогексена, циклогексадиена, муравьиной кислоты или формиата аммония. Также для улучшения кинетики гидрогенолиза можно добавлять органические или неорганические основания или кислоты и/или основные и/или кислотные ионообменные смолы. Применение основных веществ особенно предпочтительно, когда на замешенных бензильных компонентах предшественников присутствуют галогеновые заместители и/или необходимо формирование маннозаминового основания. Предпочтительные органические основания включают триэтиламин, диизопропилэтиламин, аммиак, карбамат аммония и диэтиламин, но не ограничиваются только ими. В случаях, когда целевыми продуктами являются маннозаминовые соли, в качестве со-растворителя или добавки предпочтительно используют органическую или неорганическую кислоту. Предпочтительные кислоты включают муравьиную кислоту, уксусную кислоту, пропионовую кислоту, хлоруксусную кислоту, дихлоруксусную кислоту, трифторуксусную кислоту, HCl и HBr, но не ограничиваются только ими. Вышеприведенные условия обеспечивают простое, удобное и мягкое удаление растворителя(ей) с получением чистой смеси ОЧМ.
В предпочтительном варианте осуществления изобретения по меньшей мере два соединения, выбранных из группы, включающей соединения, характеризующиеся определенными выше общими формулами 1 и 2, подвергаются каталитическому гидрогенолизу с получением по меньшей мере двух ОЧМ. Каталитический гидрогенолиз можно проводить в воде или водном растворе спирта, предпочтительно в воде, смеси вода/метанол или вода/этанол (содержание спирта 10-50 об.%). Каталитический гидрогенолиз осуществляют при температуре 15-65°C, предпочтительно 40-60°C. Концентрация катализатора может быть в диапазоне от 0,4% до 1,2% (по массе металлического компонента в расчете на массу исходной углеводной смеси).
Соединения общей формулы 1 определены общими формулами 1a, 1b. Соединения общей формулы 2 определены общей формулой 2, приведенной ниже,
где R, R1 и R4 являются такими, как определено выше,
R2a является N-ацетил-лактозаминильной группой, необязательно замещенной гликозильным остатком, содержащим одну N-ацетил-лактозаминильную и/или одну лакто-N-биозильную группу; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками,
R3a является H или N-ацетил-лактозаминильной группой, необязательно замещенной лакто-N-биозильной группой; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками,
R2b является лакто-N-биозильной группой, необязательно замещенной сиалильным и/или фукозильным остатком,
Такие соединения берутся для гидрогенолиза.
В предпочтительном варианте
- N-ацетил-лактозаминильная группа в гликозильном остатке R2a в общей формуле 1a присоединена к другой N-ацетил-лактозаминильной группе 1-3 интергликозидной связью;
- лакто-N-биозильная группа в гликозильном остатке R2a в общей формуле 1a присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью,
- лакто-N-биозильная группа в гликозильном остатке R3a в общей формуле 1a присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью,
- N-ацетил-лактозаминильная группа в гликозильном остатке R3b в общей формуле 1b присоединена к другой N-ацетил-лактозаминильной группе 1-3 или 1-6 интергликозидной связью,
- лактон-N-биозильная группа в гликозильном остатке R3b в общей формуле 1b присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью.
Кроме того, предпочтительными являются соединения общей формулы 1a и 1b, где общая формула 1a представлена R-гликозидами лакто-N-неотетраозы, пара-лакто-N-гексаозы, пара-лакто-N-неогексаозы, лакто-N-неогексаозы, пара-лакто-N-октаозы и лакто-N-неооктаозы, необязательно замещенными одним или несколькими сиалильными и/или фукозильными остатками, а общая формула 1b представлена R-гликозидами лакто-N-тетраозы, лакто-N-гексаозы, лакто-N-октаозы, изо-лакто-N-октаозы, лакто-N-декаозы и лакто-N-неодекаозы, необязательно замещенными одним или несколькими сиалильными и/или фукозильными остатками.
Особенно предпочтительными соединениями для гидрогенолиза общей формулы 1 и 2 являются соединения, в которых:
- фукозильный остаток, присоединенный к N-ацетил-лактозаминильной и/или лакто-N-биозильной группе, связан с:
- галактозой из лакто-N-биозильной группы 1-2 интергликозидной связью и/или
- N-ацетил-глюкозамином из лакто-N-биозильной группы 1-4 интергликозидной связью и/или
- N-ацетил-глюкозамином из N-ацетил-лактозаминильной группы 1-3 интергликозидной связью,
- сиалильный остаток, присоединенный к N-ацетил-лактозаминильной и/или лакто-N-биозильной группе, связан с:
- галактозой из лакто-N-биозильной группы 2-3 интергликозидной связью и/или
- N-ацетил-глюкозамином из лакто-N-биозильной группы 2-6 интергликозидной связью и/или
- галактозой из N-ацетил-лактозаминильной группы 2-6 интергликозидной связью.
Наиболее предпочтительные R-гликозиды для гидрогенолиза соответствуют ОЧМ натурального происхождения, содержащим лактозный, LNT или LNnT центральный фрагмент, и выбраны из группы из: R-гликозидов 2′-фукозиллактозы, 3-фукозиллактозы, 2′,3-дифукозиллактозы, 3′-сиалиллактозы, 6′-сиалиллактозы, 3′-сиалил-3-фукозиллактозы, лакто-N-тетраозы, лакто-N-неотетраозы, LNFP-I, LNFP-II, LNFP-III, LNFP-V, LST-a, LST-b, LST-c, FLST-a, FLST-b, FLST-c, LNDFH-I, LNDFH-II, LNDFH-III, DS-LNT, FDS-LNT I и FDS-LNT II.
В соответствии с другим предпочтительным вариантом осуществления изобретения указанные выше соединения, используемые в гидрогенолизе, являются β-гликозидами, более предпочтительно агликон является бензилом.
Индивидуальные соединения, содержащиеся в смеси, предназначенной для гидрогенолиза, могут быть синтезированы химическим, ферментативным или химико-ферментативным путем. Например, получение 1-O-бензила/замещенного бензил-LNnT описано в Ponpipom et al. Tetrahedron Lett. 20, 1717 (1978) и в международной заявке PCT/DK2011/050053; 1-O-бензил/замещенный бензил-6′-SL и его соли описаны в международной заявке PCT/DK2011/050052; получение 1-O-бензил-LNT описано в Liu et al. Bioorg. Med. Chem. 17, 4910 (2009); 1-O-бензил-3′-SL натриевая соль описана в международной заявке WO 96/32492 A1.
Смесь соединений общей формулы 1 и 2 можно получить следующим путем. Выполняют способ, включающий этапы:
(a) получения по меньшей мере одного фукозильного, сиалильного, N-ацетил-лактозаминильного или лакто-N-биозильного донора;
(b) получения по меньшей мере одного акцептора, выбранного из лактозы R-гликозида, LNT R-гликозида и LNT R-гликозида, где R имеет такие значения, как указано выше;
(c) получения смеси из соединений с этапов (a) и (b);
(d) добавления по меньшей мере одного фермента, обладающего трансгликозидазной активностью и/или гликосинтазной активностью, к смеси с этапа (c), с получением соответствующей смеси;
(e) инкубации смеси, полученной на этапе (d); и
(f) необязательно, повторения любого из этапов (a)-(d), предпочтительно со смесью, полученной на этапе (e).
В соответствии с этапом (a) получают по меньшей мере один фукозильный, сиалильный, N-ацетил-лактозаминильный или лакто-N-биозильный донор, а на этапе (b) получают по меньшей мере один акцептор. В контексте настоящего изобретения термин «фукозильный, сиалильный, N-ацетил-лактозаминильный или лакто-N-биозильный донор» предпочтительно подразумевает соединения, обеспечивающие перенос фукозильного, сиалильного, N-ацетил-лактозаминильного или лакто-N-биозильного компонента в химической реакции, например, ферментативного гликозилирования, к другому соединению, предпочтительно к акцептору. Такие «фукозильные, сиалильные, N-ацетил-лактозаминильные или лакто-N-биозильные доноры» являются усовершенствованными или активированными гликозильными соединениями, например такими, как гликозилфториды, гликозил азиды, необязательно замещенные фенилгликозиды, необязательно замещенные пиридинилгликозиды, необязательно замещенные 3-оксо-(2H)-фуран-4ил-гликозиды, необязательно замещенные 1,3,5-триазинилгликозиды или 4-метилумбеллиферилгликозиды.
В соответствии с этапом (c), готовят смесь из соединений с этапов (a) и (b). Предпочтительно, такая смесь, в соответствии с этапом (c), представляет собой смесь из одного, двух, трех, четырех, пяти, одного-пяти, трех-десяти, пяти-десяти или еще большего числа предпочтительно различных соединений, как они определены для этапа (a), и одного, двух, трех, четырех, пяти, одного-пяти, трех-десяти, пяти-десяти или еще большего числа предпочтительно различных соединений, как они определены для этапа (b).
На этапе (d) способа по настоящему изобретению для получения олигосахаридов человеческого молока (ОЧМ) к смеси, полученной в соответствии с этапом (c) способа по настоящему изобретению, добавляют по меньшей мере один фермент, обладающий трансгликозидазной активностью и/или гликосинтазной активностью, с получением соответствующей смеси.
На этапе (d) добавляют по меньшей мере один фермент, обладающий трансгликозидазной активностью и/или гликосинтазной активностью, предпочтительно по меньшей мере два (предпочтительно различных), три (предпочтительно различных), четыре (предпочтительно различных), пять (предпочтительно различных), от двух до пяти (предпочтительно различных), от двух до десяти (предпочтительно различных), от двух до двадцати (предпочтительно различных), от пяти до десяти (предпочтительно различных) или еще большее число предпочтительно различных ферментов, обладающих трангликозидазной активностью и/или гликосинтазной активностью.
Ферменты, подходящие для использования на этапе (d), предпочтительно включают по меньшей мере один фермент, обладающий трангликозидазной активностью и/или гликосинтазной активностью, предпочтительно выбранный из ферментов, обладающих, например, трангликозидазной активностью и/или гликосинтазной активностью, например обладающих фукозидазной или транс-фукозидазной, сиалидазной (нейраминидазной) или транс-сиалидазной (транс-нейраминидазной), лакто-N-биозидазной или транс-лакто-N-биозидазной и/или N-биозидазной и/или N-ацетил-лактозаминидазной или транс-N-ацетил-лактозаминидазной активностью, или любым другим ферментом, обладающим такой активностью. Еще более предпочтительно ферменты, подходящие для использования на этапе (d), могут быть выбраны из группы, включающий гликозидазы или трансгликозидазы дикого типа или мутантные, предпочтительно гликозидазы или трансгликозидазы дикого типа или мутантные, обладающие фукозидазной или транс-фукозидазной, сиалидазной (нейраминидазной) или транс-сиалидазной (транснейраминидазной), лакто-N-биозидазной или транс-лакто-N-биозидазной и/или N-ацетил-лактозаминидазной или транс-N-ацетил-лактозаминидазной активностью, или предпочтительно обладающие α-транс-фукозидазной, α-транс-сиалидазной, β-транс-лакто-N-биозидазной и/или β-транс-N-ацетил-лактозаминидазной активностью.
Ферменты, подходящие для использования на этапе (d) могут быть выбраны из любого рода, который, как известно специалистам в данной области техники, способен к экспрессии или секреции по меньшей мере одного фермента, как указано выше, например фермента, обладающего трансгликозидазной активностью и/или гликосинтазной активностью, предпочтительно фермента, обладающего фукозидазной или транс-фукозидазной, сиалидазной (нейраминидазной) или транс-сиалидазной (транснейраминидазной), лакто-N-биозидазной или транс-лакто-N-биозидазной и/или N-ацетил-лактозаминидазной или транс-N-ацетил-лактозаминидазной активностью, или предпочтительно обладающего α-транс-фукозидазной, α-транс-сиалидазной, β-транс-лакто-N-биозидазной и/или β-транс-N-ацетил-лактозаминидазной активностью, или любого другого фермента, обладающего такой активностью. Еще более предпочтительно такие ферменты, подходящие для использования на этапе (d), могут быть выбраны из бактерий, выбранных из Bacillus, Bifidobacterium, Lactobacillus, Leuconostoc, Lactococcus, Streptococcus, Streptomyces, Sulfolobus, Thermotoga или Trypanosoma.
Полученную смесь инкубируют на следующем этапе (e). Такая инкубация выгодным образом обеспечивает образование множества различных соединений, характеризующихся указанной выше общей формулой 1 и 2. Образование такого множества различных соединений основано на использовании во время этапа (d) ферментов с различной активностью, а также на применении различных доноров и акцепторов в соответствии с этапами (a) и (b), предпочтительно в виде смеси, как уже было указано для этапа (c). При использовании такого подхода способ по изобретению выгодным образом позволяет варьировать число и тип олигосахаридов, получаемых в ходе синтеза, простым и дешевым образом. Использование ферментов дополнительно позволяет получать различные производные стереоселективным способом. Образование соединений предпочтительно осуществляется в результате переноса N-ацетил-лактозаминильных компонентов, лакто-N-биозильных компонентов, фукозильных компонентов, сиалильных компонентов, с образованием новых связей в желаемых положениях молекулы и т.д., точно определенным образом с получением смеси различных R-гликозидов олигосахаридов человеческого молока.
Инкубацию в соответствии с этапом (e) осуществляют при концентрации (каждого из) ферментов от 1 мЕд/л до 1,000 Ед/л, предпочтительно от 10 мЕд/л до 100 Ед/л, где активность, обеспечивающая образование 1 мкмоль специфического продукта для определенного белка, из определенного исходного продукта, определяется как 1 единица (Ед), например для гликотрансферазы получение гликозо-содержащего комплексного углевода при 37°C за 1 минуту. Активность каждого фермента, как она определена здесь, может оцениваться по отношению к натуральному или искусственному субстрату.
Инкубация в соответствии с этапом (e) может осуществляться в реакционной среде, предпочтительно в водной среде, содержащей смесь, полученную на этапе (d), и, необязательно, воду; буферный раствор, такой как фосфатный буферный раствор, карбонатный буферный раствор, ацетатный буферный раствор, боратный буферный раствор, цитратный буферный раствор и трис-буферный раствор, или их комбинации; спирт, такой как метанол и этанол; сложный эфир, такой как этилацетат; кетон, такой как ацетон; амид, такой как ацетамид; и тому подобное.
Далее, инкубацию в соответствии с этапом (e) можно осуществлять в реакционной среде, как описано выше, в которую необязательно можно добавить сурфактант или органический растворитель; если это необходимо. В качестве сурфактанта можно использовать любой сурфактант, способный ускорить формирование комплексного углевода, определенного в настоящем изобретении, в качестве возможного продукта по настоящему изобретению. Примеры включают не-ионные сурфактанты, такие как полиоксиэтилен октадециламин (например, Nymeen S-215, производимый Nippon Oil & Fats); катионные сурфактанты, такие как цетилтриметиламмоний бромид и алкилдиметил бензиламмоний-хлорид (например, Cation F2-40E, производимый Nippon Oil & Fats); анионные сурфактанты, такие как лауроил-саркозинат; третичные амины, такие как алкилдиметиламин (например, третичный амин FB, производимый Nippon Oil & Fats); и тому подобные, которые используются либо по отдельности, либо в виде смеси двух или большего числа сурфактантов. Сурфактант можно использовать, как правило, в концентрации от 0,1 до 50 г/л. Органический растворитель может включать ксилол, толуол, жирнокислотный спирт, ацетон, этилацетат и тому подобное, и его можно использовать в концентрации, как правило, от 0,1 до 50 мл/л.
Инкубацию в соответствии с этапом (e) можно, кроме того, осуществлять в реакционной среде, как описано выше, предпочтительно при pH от 3 до 10, от 5 до 10, предпочтительно от 6 до 8.
Инкубацию в соответствии с этапом (е) можно, кроме того, осуществлять при температуре от примерно 0°C до примерно 100°C, предпочтительно при температуре от примерно 10°C до примерно 50°C, например при температуре от примерно 20°C до примерно 50°C. В реакционную среду при необходимости можно добавлять неорганические соли, такие как MnCl2 и MgCl2.
Инкубацию в соответствии с этапом (e) можно осуществлять в биореакторе. Биореактор предпочтительно является биореактором, подходящим для работы в непрерывном режиме или периодическом режиме.
Способ каталитического гидрогенолиза соединений общей формулы 1 и 2 обеспечивает смесь олигосахаридов человеческого молока (ОЧМ), отдельные соединения из которых характеризуются общей формулой 3 и 4, соответственно.
где R1 независимо является фукозилом или H,
R2 выбран из N-ацетил-лактозаминильной и лакто-N-биозильной групп, где N-ацетил-лактозаминильная группа может нести гликозильный остаток, содержащий одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками;
R3 является H или N-ацетил-лактозаминильной группой, необязательно замещенной гликозильным остатком, содержащим одну или несколько N-ацетил-лактозаминильных и/или одну или несколько лакто-N-биозильных групп; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками,
R4 независимо является сиалилом или H,
и их соли,
с тем условием, что по меньшей мере один из R1 или R4 не является H в общей формуле 4.
Компоненты ОЧМ, полученные путем гидрогенолиза, как описано выше, в частности компоненты, характеризующиеся общими формулами 3a, 3b и 4
где R1 и R4 являются такими, как определено выше,
R2a является N-ацетил-лактозаминильной группой, необязательно замещенной гликозильным остатком, содержащим одну N-ацетил-лактозаминильную и/или одну лакто-N-биозильную группу; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками,
R3a является Н или N-ацетил-лактозаминильной группой, необязательно замещенной лакто-N-биозильной группой; любая N-ацетил-лактозаминильная и лакто-N-биозильная группа может быть замещена одним или несколькими сиалильными и/или фукозильными остатками,
R2b является лакто-N-биозильной группой, необязательно замещенной сиалильным и/или фукозильным остатком.
Более предпочтительно, соединения получают в результате гидрогенолиза, где
- N-ацетил-лактозаминильная группа в гликозильном остатке из R2a в общей формуле 3a присоединена к другой N-ацетил-лактозаминильной группе 1-3 интергликозидной связью,
- лакто-N-биозильная группа в гликозидном остатке из R2a в общей формуле 3a присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью,
- лакто-N-биозильная группа в гликозильном остатке из R3a в общей формуле 3a присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью;
- N-ацетил-лактозаминильная группа в гликозильном остатке из R3b в общей формуле 3b присоединена к другой N-ацетил-лактозаминильной группе 1-3 или 1-6 интергликозидной связью,
- лакто-N-биозильная группа в гликозильном остатке из R3b в общей формуле 3b присоединена к N-ацетил-лактозаминильной группе 1-3 интергликозидной связью.
Еще более предпочтительными соединениями, полученными после гидрогенолиза, являются соединения общей формулы 3a и 3b, где общая формула 3a представляет лакто-N-неотетраозу, пара-лакто-N-гексаозу, пара-лакто-N-неогексаозу, лакто-N-неогексаозу, пара-лакто-N-октаозу и лакто-N-неооктаозу, необязательно замещенные одним или несколькими сиалильными и/или фукозильными остатками, а общая формула 3b представляет лакто-N-тетраозу, лакто-N-гексаозу, лакто-N-октаозу, изо-лакто-N-октаозу, лакто-N-декаозу и лакто-N-неодекаозу, необязательно замещенные одним или несколькими сиалильными и/или фукозильными остатками.
Особо предпочтительными соединениями в качестве продуктов гидрогенолиза являются соединения, в которых:
- фукозильный остаток, присоединенный к N-ацетил-лактозаминильной и/или лакто-N-биозильной группе, связан с:
- галактозой из лакто-N-биозильной группы 1-2 интергликозидной связью, и/или
- N-ацетил-глюкозамином из лакто-N-биозильной группы 1-4 интергликозидной связью, и/или
- N-ацетил-глюкозамином из N-ацетил-лактозаминильной группы 1-3 интергликозидной связью,
- сиалильный остаток, присоединенный к N-ацетил-лактозаминильной и/или лакто-N-биозильной группе, связан с:
- галактозой из лакто-N-биозильной группы 2-3 интергликозидной связью, и/или
- N-ацетилглюкозамином из лакто-N-биозильной группы 2-6 интергликозидной связью, и/или
- галактозой из N-ацетил-лактозаминильной группы 2-6 интергликозидной связью.
Наиболее предпочтительные соединения, полученные при гидрогенолизе, представляют собой природные ОЧМ, содержащие лактозный, LNT или LNnT центральный фрагмент, и выбраны из группы: 2′-фукозиллактозы, 3-фукозиллактозы, 2′,3-дифукозиллактозы, 3′-сиалиллактозы, 6′-сиалиллактозы, 3′-сиалил-3-фукозиллактозы, лакто-N-тетраозы, лакто-N-неотетраозы, LNFP-I, LNFP-II, LNFP-III, LNFP-V, LST-a, LST-b, LST-c, FLST-a, FLST-b, FLST-c, LNDFH-I, LNDFH-II, LNDFH-III, DS-LNT, FDS-LNT I и FDS-LNT II.
Преимущество настоящего изобретения состоит в том, что его можно применять для получения смеси ОЧМ, состав которой по существу схож с составом натурального человеческого молока. Другими словами, количество исходной смеси, содержащей соединения общей формулы 1, 1a, 1b и 2, можно выбрать так, чтобы при каталитическом гидрогенолизе получаемая в итоге смесь ОЧМ в соответствии с общими формулами 3 и 4 имела профиль ОЧМ, который по существу подобен профилю натурального человеческого молока. Далее, поскольку каталитический гидрогенолиз проходит практически без образования побочных продуктов и почти количественно, состав исходной смеси, содержащей соединения общей формулы 1, 1a, 1b и 2, прямо пропорционален смеси ОЧМ в готовом продукте. Таким образом, тщательная регулировка исходных материалов приводит к композициям, аналогичным человеческому молоку.
Для целей настоящего изобретения «по существу подобный профиль олигосахаридов» означает профиль олигосахаридов, в котором количество всех рассматриваемых олигосахаридов отличается менее чем на 25%, предпочтительно менее чем на 15%, более предпочтительно менее чем на 5%, наиболее предпочтительно менее чем на 1%, от количества соответствующих олигосахаридов в контрольном образце. Для целей настоящего изобретения контрольный образец для определения количества олигосахаридов должен быть получен из молока матерей со схожим генотипом в отношении ферментов, ответственных за естественное формирование указанных олигосахаридов в молочных железах.
Например, если рассматриваемая смесь содержит 2 олигосахарида A и B, и оценивается по отношению к человеческому молоку, олигосахаридный профиль смеси считается «по существу подобным» человеческому молоку, если количество каждого из A и B отли