Новые 4-амино-n-гидроксибензамиды в качестве ингибиторов hdac для лечения рака
Иллюстрации
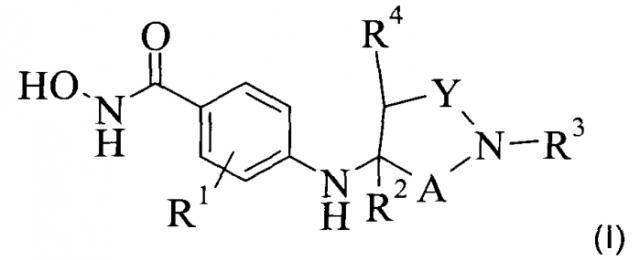
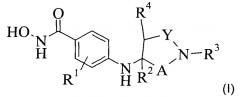
Показать всеИзобретение относится к ингибиторам HDAC формулы (I) или их фармацевтически приемлемым солям, эфирам или стереоизомерам, где R1 представляет собой водород или галоген; R2 представляет собой водород, C1-4-алкил; R3 представляет собой фенил, незамещенный или замещенный один, или два, или три раза галогеном, C1-4-алкилом, C1-4-алкокси, C1-4-алкилсульфонилом, циано, трифторметилом, фенилом, фенокси, пирролилом, имидазонилом, оксазолилом или ди C1-4-алкиламино-C1-4-алкокси; нафталинил; хинолинил; C3-7-циклоалкил; фенилалкил, где фенил может быть не замещен или один или два раза замещен галогеном, C1-4-алкокси, фенилом; нафталинилалкил; фенилциклоалкил; пиримидинил; фенилсульфонил, где фенил может быть не замещен или один или два раза замещен галогеном, фенилом; или фенилкарбонил, где фенил может быть не замещен или один или два раза замещен галогеном, C1-4-алкокси; R4 представляет собой водород или C1-4-алкил; Y представляет собой -СН2- или -С=O; или R4 и Y вместе с атомом углерода, к которому R4 присоединен, могут образовывать фенильное кольцо или пиридиновое кольцо, которое может быть не замещено или дополнительно замещено галогеном; при условии, что R2 представляет собой C1-4алкил; А представляет собой -С=O, -СН2- или -СН-алкил, при условии, что А и Y одновременно не представляют собой -С=O. Также предложены фармацевтические композиции этих соединений и их применение в качестве лекарства для лечения рака. 3 н. и 11 з.п. ф-лы, 3 табл., 101 пр.
Реферат
Изобретение относится к новым противоопухолевым агентам и их фармацевтически приемлемым солям, способам получения этих новых соединений и лекарствам, содержащим их. Соединения по изобретению обладают антипролиферативной и вызывающей дифференцировку активностью, что приводит к ингибированию пролиферации опухолевых клеток и вызывает апоптоз. Изобретение также относится к применению этих соединений для лечения заболеваний, таких как рак, и для изготовления соответствующих лекарств.
В частности изобретение относится к (i) соединению формулы (I)
где
R1 представляет собой водород, алкил или галоген;
R2 представляет собой водород, алкил, гидроксиалкил, алкоксиалкил, аминоалкил, алкиламиноалкил или диалкиламиноалкил;
R3 представляет собой фенил, незамещенный или замещенный один, или два, или три раза галогеном, алкилом, алкокси, алкилсульфонилом, циано, трифторметилом, фенилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
нафталинил, незамещенный или один или два раза замещенный галогеном, алкилом, алкокси, алкилсульфонилом, циано, трифторметилом, диалкиламино или диалкиламиноалкилом;
хинолинил, незамещенный или один или два раза замещенный алкилом, алкокси, алкилсульфонилом, циано, трифторметилом, диалкиламино или диалкиламиноалкилом;
циклоалкил;
фенилалкил, где фенил может быть не замещен или один или два раза замещен галогеном, алкокси, фенилом, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
нафталинилалкил, где нафталинил может быть не замещен или один или два раза замещен галогеном, алкокси, фенилом, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
фенилциклоалкил, где фенил может быть не замещен или один или два раза замещен галогеном, алкокси, фенилом, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
пиримидинил, где пиримидинил может быть не замещен или один или два раза замещен алкокси, фенилом, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
фенилсульфонил, где фенил может быть не замещен или один или два раза замещен галогеном, фенилом, алкокси, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси; или
фенилкарбонил, где фенил может быть не замещен или один или два раза замещен галогеном, алкокси, фенилом, алкилом, циано, алкилсульфонилом, трифторметилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
R4 представляет собой водород или алкил;
Y представляет собой -CH2- или -C=O;
или
R4 и Y вместе с атомом углерода, к которому R4 присоединен, могут образовывать фенильное кольцо или пиридиновое кольцо, которое может быть не замещено или дополнительно замещено галогеном; при условии, что R2 представляет собой алкил;
А представляет собой -C=O, -CH2- или -СН-алкил, при условии, что А и Y одновременно не представляют собой -C=O;
или его фармацевтически приемлемой соли, эфиру или стереоизомерам.
Изобретение также относится к способу изготовления этих новых соединений и лекарств, содержащих их.
Гистондеацетилазы (HDACs от histone deacetylases) являются одним из основных классов посттрансляционных регуляторов и выполняют развивающую, антиапоптическую и антидифференцирующую роль при разных видах рака. В качестве ключевых ферментативных компонентов мультипротеиновых комплексов гистондеацетилазы (HDACs) отвечают за деацетилирование лизиновых остатков в гистоновых и негистоновых белковых субстратах. Недавно было установлено, что ингибиторы HDAC задерживают рост и вызывают апоптоз некоторых видов раковых клеток, включая раковые клетки толстой кишки, клетки Т-клеточной лимфомы и эритролейкемические клетки. Учитывая, что апоптоз является определяющим фактором в развитии рака, ингибиторы HDAC являются перспективными реагентами в терапии рака в качестве эффективных стимуляторов апоптоза (Koyama, Y., et al., Blood 2000, 96, 1490-1495).
Белки HDAC включают семейство из 18 членов у людей с гомологией до дрожжевых HDACs, Rpd3, Hda1 и Sir2. Исходя из сходства их последовательности, тенденции клеточного расположения, особенностей экспрессии в тканях и ферментативных механизмов, HDACs, таким образом, можно разделить на четыре класса. HDACs класса I (HDACs 1, 2, 3 и 8), гомологичны с Rpd3, преимущественно распространены в ядрах клеток и, по-видимому, повсеместно экспрессированы в большинстве тканях. HDACs класса II (HDACs 4, 5, 6, 7, 9, 10), гомологичны с Hda1, способны перемещаться между ядрами клеток и цитоплазмой в зависимости от ряда регулирующих сигналов и клеточного состояния и экспрессированы в более ограниченном количестве видов клеток. Эти HDACs, кроме того, можно разделить на класс IIa (HDACs 4, 5, 7, 9) и класс IIb (HDACs 6, 10). HDAC11 является единственным членом гистондеацетилазы класса IV. HDACs классов I, II и IV являются полностью цинк-зависимыми деацетилазами. Напротив HDACs класса III, гомологичны с Sir2, представляет собой NAD+-зависимые деацетилазы, которые механистически отличаются от HDACs классов I и II и не ингибируются классическими ингибиторами HDAC, такими как трихостатин А, трапоксин В или MS-275.
Учитывая их связь с образованием рака, белки HDAC классов I и II оказываются привлекательными мишенями в противоопухолевой терапии. В частности HDACs класса I тесно связаны с антипролиферативными эффектами против опухолевых клеток. Например, фармакологическое ингибирование HDACs 1-3 приводит к индукции ингибитора циклинзависимой киназы р21 и сопутствующей остановке клеточного цикла. Некоторые лекарства ингибиторы HDAC (HDACi) находятся на разных стадиях клинических испытаний, SAHA (субероиланилид гидроксамовой кислоты, вориностат) и ромидепсин (FK228), получившие одобрение FDA в 2006 и 2009, соответственно, для лечения кожной Т-клеточной лимфомы (CTCL от cutaneous T-cell lymphoma). Недавно было показано, что экспрессия HDAC8 (а не другие изоформы HDAC) значительно и независимо соотносится со стадией заболевания и недостаточной продолжительностью существования нейробластомы (НБ), являющейся неоплазмой периферической вегетативной нервной системы, которая представляет вторую наиболее распространенную злокачественную опухоль в детском возрасте. Кроме того, снижение HDAC8 под действием миРНК приводит к клеточной дифференцировке НБ и ингибирует клеточный рост, при этом ее сверхэкспрессия блокирует дифференцировку МБ, вызванную ретиноевой кислотой (Clinical Cancer Research 2009, 15, 91-99). Следовательно, HDAC8 является потенциальной лекарственной мишенью при дифференцирующей терапии минимального остаточного заболевания в НБ. Кроме того, также предполагается возможное соответствие между HDAC8 и острым миелобластным лейкозом (AML от acute myeloid leukemia) (Bioorg. Med. Chem. Lett. 2007, 17, 2874).
В отличие от HDACs класса I, которые являются преимущественно ферментами клеточных ядер, ферменты класса IIа двигаются между ядрами и цитоплазмой, и, как известно, связаны с комплексом HDACS/SMRT/N-CoR и MEF2, и по существу играют важную роль в регулировании экспрессии генов мышечных клеток (рассмотрено в Oncogene 2007, 26, 5450-5467) и иммунной реакции (Biochemical Pharmacology 2007, 74, 465-476). Ферменты подкласса IIb уникально представляют собой два домена деацетилазы и являются главным образом цитоплазматическими. Важно отметить, что HDAC6 влияет на ряд субстратов за исключением гистоновых белков, и участвует в процессировании Lys40 митотического веретенообразного белка α-тубулин. Также HDAC6 имеет двигательный связывающий домен динеина, что позволяет HDAC6 двигать груз вдоль микроканальца, и «цинковый палец» убиквитин-связывающий домен на С-конце. Посредством своей убиквитин-сязывающей активности HDAC6 способен опосредовать восстановление аутофагического вещества до агресом для разрушения, таким образом, уменьшая цитотоксические эффекты этих агрегатов (Cell 2003, 115, 727-738). Ингибирование активности HDAC6 под действием специфичного ингибитора, тубацина, может увеличивать накопление ацетилированного α-тубулина и ингибировать клеточную подвижность, не воздействуя на стабильность микроканальца по существу (J. Am. Chem. Soc. 2003, 125, 5586-5587, Proc. Nat. Acad. Sci. USA 2003, 4389-4394).
Множественная миелома (ММ) является злокачественной опухолью плазматических клеток, характеризуемой сложными гетерогенными цитогенетическими нарушениями и проникновением злокачественных клеток в костный мозг, что приводит к заболеванию костей, гиперкальцемии, цитопении, почечной дисфункции, повышенной вязкости и периферической невропатии. Стандартные методы лечения, основанные на ингибиторе протеасом, достигли замечательного быстродействия при ММ, однако комбинированные методы лечения с новыми нацеленными препаратами до сих пор необходимы вследствие развития устойчивости к лекарственным препаратам и плохой продолжительности существования. Недавно было продемонстрировано, что одновременное ингибирование протеасомы и HDAC6 может приводить к синергическим антипролиферативым эффектам в клетках ММ, наиболее вероятно из-за роли HDAC6 в опосредовании функции агресом, и последующему напряжению неправильно свернутого белка, которое развивается в результате двойного ингибирования протеасомы / агресомы (Proc. Nat. Acad. Sci. USA 2005, 102, 8567-8572). Следовательно, HDAC6 является привлекательной новой мишенью для развития новых комбинированных методов лечения ММ.
Соединения согласно данному изобретению являются ингибиторами HDAC6 или HDAC8 и, следовательно, демонстрируют антипролиферативную и вызывающую дифференцировку активности, которые приводят к ингибированию пролиферации опухолевых клеток и вызывают апоптоз. Ингибиторы pan HDAC обладают преклинической активностью широкого спектра против большого числа форм рака, также еще обладают неспецифической цитотоксичностью, которая может ограничить их клиническое применение. Наоборот ингибиторы HDAC, воздействующие на конкретные изоформы, особенно HDAC6 и HDAC8, обычно демонстрируют низкую неспецифическую цитотоксичность и могут быть пригодны для лечения определенных подтипов рака. Соединения по настоящему изобретению показывают увеличенную селективность относительно HDAC6 или HDAC8 по сравнению с ингибитором pan HDAC SAHA, как оценено в ходе и ферментативного, и клеточного анализов.
Исходя из разных цинк-связывающих групп, в литературе широко описаны четыре основных класса ингибиторов HDAC: (1) гидроксамовые кислоты; (2) орто-аминоанилиды; (3) тиолы или их пролекарства; (4) карбоновые кислоты и их аналоги (рассмотрено в J. Med. Chem. 2003, 46, 5097-5116). В общем, гидроксамовые кислоты, такие как SAHA, LBH589, PXD101, JNJ26481585 и ITF2357, демонстрируют широкую ингибирующую активность против большинства изоформ HDAC в субмикромолярном диапазоне (J. Med. Chem. 2007, 50, 4405). С другой стороны, орто-аминоанилиды, примерами которых являются MS275 и его арильный замещенный аналог, показывают высокую эффективность и активность класса I, ограниченную прежде всего подтипами HDAC 1, 2, 3. Тиольное пролекарство FK228 (депсипептид/ромидепсин) также, как сообщалось, обладает похожей селективностью класса I, хотя разработчик препарата, Gloucester pharmaceuticals, заявлял, что молекула является ингибитором pan-HDAC (Mitchell Keegan, Discovery On Target HDAC Inhibitor Conference 2007). Напротив жирные кислоты являются наименее мощными ингибиторами HDAC с ферментативными ингибирующими значениями в высоких микромолярных диапазонах.
Ограниченные сообщения, ограничивающиеся областью молекул на основе гидроксамовой кислоты, были опубликованы при описании соединений с селективностью к HDAC6 и/или HDAC8. Тубацин является селективным ингибитором прототипа HDAC6 с большой блокирующей группой, связывающейся с периферийной областью HDAC6. Kozikowski и др. описали эффективные HDAC6-селективные триазолилфенильные блокированные гидроксаматы и родственные фенилизоксазольные блокированные гидроксаматные ингибиторы с более чем 50-кратной селективностью относительно HDAC1 и HDAC3 (J. Meet. Chem. 2008, 51, 3437 и J. Med. Chem. 2008, 51, 4370). Во все случаях ингибиторы имеют жесткие и большие блокирующие группы в качестве элементов селективности, и эти блокирующие группы связаны с цинк-связывающими гидроксамовыми кислотами посредством гибких алифатических цепей. В другом подходе Envivo Pharmaceuticals раскрыл 1,2,3,4-тетрагидроизохинолиновые гидроксаматы для возможного лечения нейродегенеративных заболеваний (WO 2005/108367), но селективность их изоформы HDAC еще требует разъяснения. Совсем недавно Smil и др. из MethylGene Inc. сообщили о хиральных 3,4-дигидрохиноксалин-2(1H)-онных и пиперазин-2,5-дионных арильных гидроксаматах с селективностью (до 40-кратной) к HDAC6 человека относительно других HDACs класса I/IIa. В соединениях по настоящему изобретению применяются жесткие тетрагидронафтилен, 1,2,3,4-тетрагидрохинолин и хроман в качестве связующего звена между цинк-связывающей группой гидроксамовой кислоты и край-связывающими блокирующими группами. Они демонстрируют субмикромолярное до микромолярного ингибирование HDAC6 или HDAC8, основанное на их клеточной индукционной активности ацетилирования тубулина (клеточный анализ HDAC6) и ферментативном ингибировании HDAC8. Соединения по настоящему изобретению способны вызывать заметную клеточную дифференцировку НБ. Также соединения по настоящему изобретению демонстрируют синергизм в сочетании с бортезомибом при ингибировании роста клеток клеточных линий ММ. В качестве заменителя для клеточного ингибирования HDAC1/2/3 применяли индукцию р21 в виде обратного скрининга, чтобы оценить селективность соединений по настоящему изобретению относительно HDAC6 или HDAC8 сверх HDACs 1, 2 и 3. В отличие от положительного контроля MS275 и SAHA, ни одно из соединений по настоящему изобретению не показало значительную или сопоставимую индукционную активность р21 при 3 мкМ, 10 мкМ и 30 мкМ концентрациях. Соединения по настоящему изобретению являются эффективными и селективными ингибиторами HDAC6 или HDAC8, которые могут особенно подойти для лечения множественной миеломы и нейробластомы, исходя из перспективной биологии HDAC6 и HDAC8 при этих двух формах рака.
Было установлено, что соединения по настоящему изобретению представляют собой ингибиторы HDAC6 или HDAC8, которые обладают антипролиферативной и вызывающей дифференцировку активностью, что приводит к ингибированию пролиферации опухолевых клеток и вызывает апоптоз. Следовательно, эти соединения полезны для лечения заболеваний, таких как нейробластома и множественная миелома, у людей и животных.
Как используется здесь, термин «алкил», отдельно или в сочетании, обозначает насыщенный, линейный или разветвленный, моно- или двухвалентный углеводород, содержащий от 1 до 8, предпочтительно от 1 до 6, более предпочтительно от 1 до 4 атомов углерода, например метил, этил, пропил, изопропил, 1-бутил, 2-бутил и трет-бутил. Предпочтительными «алкильными» группами являются метил, этил, пропил и бутил, более предпочтительны метил, этил, изопропил и трет-бутил.
Термин «алкокси», отдельно или в сочетании, обозначает группу алкил-O-, где «алкил» является таким, как определено выше; например метокси, этокси, пропокси, изопропокси, н-бутокси, изобутокси, 2-бутокси и трет-бутокси. Предпочтительными «алкокси» группами являются метокси и этокси, и более предпочтителен метокси.
Термин «циклоалкил», отдельно или в сочетании, относится к насыщенному, моно- или двухвалентному циклическому углеводороду, содержащему от 3 до 7 атомов углерода, предпочтительно от 3 до 6 атомов углерода, например, циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Предпочтительными «циклоалкильными» группами являются циклопропил, циклопентил и циклогексил.
Термин «галоген» означает фтор, хлор, бром или йод. «Галоген» предпочтительно является фтором, хлором или бромом.
Термин «карбонил», отдельно или в сочетании, относится к группе -С(O)-.
Термин «амино», отдельно или в сочетании, относится к первичному (-NH2), вторичному (-NH-) или третичному амину (-N-).
Термин «гидрокси», отдельно или в сочетании, относится к группе -ОН.
Термин «сульфонил», отдельно или в сочетании, относится к группе -S(O)2-.
Термины «фенилалкил», «нафталинилалкил», «фенилциклоалкил», «фенилсульфонил» или «фенилкарбонил» означают, что ароматические группы, т.е. фенил или нафталинил, присоединены посредством алкила, циклоалкила, сульфонила или карбонильной группы в качестве соединяющей группы, где термины «алкил» и «циклоалкил» имеют вышеприведенные значения.
Соединения по настоящему изобретению могут существовать в форме их фармацевтически приемлемых солей. Термин «фармацевтически приемлемая соль» относится к обычным солям присоединения кислоты или солям присоединения основания, которые сохраняют биологическую эффективность и свойства соединений формулы (I) и образуются из подходящих нетоксичных органических или неорганических кислот или органических или неорганических оснований. Соли присоединения кислоты включают, например те, что получены из неорганических кислот, таких как соляная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота и азотная кислота, и те, что получены из органических кислот, таких как п-толуолсульфоновая кислота, салициловая кислота, метансульфоновая кислота, щавелевая кислота, янтарная кислота, лимонная кислота, яблочная кислота, молочная кислота, фумаровая кислота и подобные. Соли присоединения основания включают те, что получены из гидроксидов аммония, калия, натрия и четвертичного аммония, таких как, например, гидроксид тетраметиламмония. Модификация химической структуры фармацевтического соединения в соль является известной химикам-фармацевтам методикой для получения улучшенной физической и химической стабильности, гигроскопичности, текучести и растворимости соединений. Она, например описана у Bastin R.J., et. al., Organic Process Research & Development 2000, 4, 427-435; или in Ansel, H., et. al., In: Фармацевтических Dosage Forms и Drug Delivery Systems, 6th ed. (1995), pp.196 и 1456-1457. Предпочтительными являются соли натрия соединений формулы (I).
«Фармацевтически приемлемые эфиры» означает, что соединения общей формулы (I) могут быть преобразованы по функциональным группам с целью получения производных, которые способны превращаться назад в исходные соединения in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически подвижные эфирные производные, такие как ацетаты, пропионаты, бензоаты и пивалаты. Кроме того, любые физиологически приемлемые эквиваленты соединений общей формулы (I), подобные метаболически подвижным эфирам, которые способны давать исходные соединения общей формулы (I) in vivo, находятся в объеме данного изобретения. Предпочтительными являются ацетильные, пропионильные и бензоильные эфиры соединений формулы (I).
Соединения общей формулы (I), которые содержат один или несколько хиральных центров, могут находиться в виде либо рацематов, диастереомерных смесей, либо оптически активных отдельных изомеров. Рацематы могут быть разделены известными способами на энантиомеры. Предпочтительно диастереомерные соли, которые могут быть разделены в ходе кристаллизации, образуются из рацемических смесей в результате реакции с оптически активной кислотой, такой как, например D- или L-винная кислота, миндальная кислота, яблочная кислота, молочная кислота или камфорсульфоновая кислота.
Другим воплощением настоящего изобретения является (ii) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где
R1 представляет собой водород или галоген;
R2 представляет собой водород или алкил;
R3 представляет собой фенил, незамещенный или замещенный один, или два, или три раза галогеном, алкилом, алкокси, алкилсульфонилом, циано, трифторметилом, фенилом, фенокси, пирролилом, имидазонилом, оксазолилом или диалкиламиноалкокси;
нафталинил;
хинолинил;
циклоалкил;
фенилалкил, где фенил может быть не замещен или один или два раза замещен галогеном, алкокси или фенилом;
нафталинилалкил;
фенилциклоалкил;
пиримидинил;
фенилсульфонил, где фенил может быть не замещен или один или два раза замещен галогеном или фенилом; или
фенилкарбонил, где фенил может быть не замещен или один или два раза замещен галогеном или алкокси;
R4 представляет собой водород или алкил; и все остальные заместители имеют приведенные выше значения.
Другим особым воплощением изобретения является (iii) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R1 представляет собой водород, фтор или хлор; и все остальные заместители имеют приведенные выше значения.
Другим особым воплощением изобретения является (iv) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R2 представляет собой водород, метил или этил; и все остальные заместители имеют приведенные выше значения.
Дополнительным особым воплощением изобретения является (v) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R2 представляет собой водород или метил; и все остальные заместители имеют приведенные выше значения.
Другим особым воплощением изобретения является (vi) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R3 представляет собой фенил, незамещенный или замещенный один, или два, или три раза фтором, хлором, метокси, метилом, изопропилом, изопропокси, бутилом, трет-бутилом, метилсульфонилом, циано, трифторметилом, фенокси, фенилом, пирролилом, имидазонилом, оксазолилом или диметиламиноэтокси; нафталинил; хинолинил; циклогексил; фенилметил; фенилэтил; фенилизопропил; хлорфенилметил; метоксифенилметил; хлорфенилизопропил; фенилфенилизопропил; нафталинилизопропил; фенилциклобутил; фенилциклопентанил; фенилциклогексил; пиримидинил; фенилсульфонил; фторфенилсульфонил, хлорфенилсульфонил, фенилфенилсульфонил, фенилкарбонил; фторфенилкарбонил или метоксифенилкарбонил; и все остальные заместители имеют приведенные выше значения.
Дополнительным особым воплощением изобретения является (vii) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R3 представляет собой фенил, незамещенный или один раз замещенный диметиламиноэтокси, один или два раза замещенный фтором, хлором или циано; хинолинил; фенилметил; фенилэтил; фенилизопропил; хлорфенилизопропил; фенилциклобутил; фенилциклогексил; пиримидинил; фторфенилсульфонил; фторфенилкарбонил или хлорфенилметил; и все остальные заместители имеют приведенные выше значения.
Другим особым воплощением изобретения является (viii) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R4 представляет собой водород или метил; и все остальные заместители имеют приведенные выше значения.
Дополнительным воплощением изобретения является (ix) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где Y представляет собой -СН2- или -C=O; и все остальные заместители имеют приведенные выше значения.
Дополнительным особым воплощением изобретения является (x) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где R4 и Y вместе с атомом углерода, к которому R4 присоединен, образуют фенильное кольцо или пиридиновое кольцо, которое может быть не замещено или замещено фтором, при условии, что R2 представляет собой алкил; и все остальные заместители имеют приведенные выше значения.
Другим особым воплощением изобретения является (xi) соединение формулы (I) или его фармацевтически приемлемая соль, эфир или стереоизомеры, где А представляет собой -C=O, -CH2- или -СН-CH3; при условии, что А и Y одновременно не представляют собой -C=O; и все остальные заместители имеют приведенные выше значения.
Особые соединения формулы (I) или их фармацевтически приемлемые соли, эфиры или стереоизомеры по изобретению могут быть выбраны из
N-Гидрокси-4-(5-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(2-Фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2-Хлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(3-метокси-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(3-изопропокси-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(4-изопропокси-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(3-трифторметил-фенил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(4-трифторметил-фенил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(3-изопропил-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(4-изопропил-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-[1-(4-Бутил-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-трет-Бутил-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(4-метансульфонил-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-[1-(3-Циано-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Циано-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-4-фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-5-фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(5-Хлор-2-фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,4-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,3-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3,4-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3,5-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,6-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Фтор-2,6-диметил-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-3-гидроксиметил-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[2-оксо-1-(3-фенокси-фенил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(4-фенокси-фенил)-пирролидин-3-иламино]-бензамида;
4-(1-Бифенил-3-ил-2-оксо-пирролидин-3-иламино)-N-гидрокси-бензамида;
N-Гидрокси-4-[2-оксо-1-(3-пиррол-1-ил-фенил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(4-имидазол-1-ил-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(3-оксазол-5-ил-фенил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-{1-[3-(2-Диметиламино-этокси)-фенил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
N-Гидрокси-4-(1-нафталин-1-ил-2-оксо-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(1-нафталин-2-ил-2-оксо-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(2-оксо-1-хинолин-8-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(2-оксо-1-хинолин-5-ил-пирролидин-3-иламино)-бензамида;
4-(1-Циклогексил-2-оксо-пирролидин-3-иламино)-N-гидрокси-бензамида;
4-(1-Бензил-5-оксо-пирролидин-3-иламино)-N-гидрокси-бензамида;
N-Гидрокси-4-(2-оксо-1-фенэтил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-[5-оксо-1-(R-1-фенил-этил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[5-оксо-1-(R-1-фенил-этил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(4-метокси-бензил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(1-метил-1-фенил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-{1-[1-(2-Хлор-фенил)-1-метил-этил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
4-{1-[1-(3-Хлор-фенил)-1-метил-этил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
4-{1-[1-(4-Хлор-фенил)-1-метил-этил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
4-[1-(1-Бифенил-4-ил-1-метил-этил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(1-метил-1-нафталин-1-ил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(1-метил-1-нафталин-2-ил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(1-фенил-циклобутил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(1-фенил-циклопентил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(1-фенил-циклогексил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(3-Фтор-фенил)-3-метил-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-фенил)-3-метил-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-3-метил-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-3-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-8-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-6-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-[3-метил-1-(1-метил-1-фенил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-[3-Этил-1-(1-метил-1-фенил-этил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
2-Фтор-N-гидрокси-4-(2-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(3-Хлор-фенил)-2-оксо-пирролидин-3-иламино]-2-фтор-N-гидрокси-бензамида;
4-[1-(3,4-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-2-фтор-N-гидрокси-бензамида;
3-Хлор-N-гидрокси-4-(2-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(4-Фтор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2-Хлор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(3-метокси-фенил)-5-оксо-пирролидин-3-иламино]-бензамида;
4-(1-Бензил-5-оксо-пирролидин-3-иламино)-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(1-метил-1-фенил-этил)-5-оксо-пирролидин-3-иламино]-бензамида;
транс-4-[1-(4-Хлор-фенил)-2-метил-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-4-метил-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-(1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(4-Хлор-фенил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,6-Дихлор-фенил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,4-Дихлор-фенил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-(1-пиримидин-2-ил-пирролидин-3-иламино)-бензамида;
4-(1-Бензолсульфонил-пирролидин-3-иламино)-N-гидрокси-бензамида;
4-[1-(4-Фтор-бензолсульфонил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-бензолсульфонил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(Бифенил-4-сульфонил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-(1-Бензоил-пирролидин-3-иламино)-N-гидрокси-бензамида;
4-[1-(4-Фтор-бензоил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-[1-(4-метокси-бензоил)-пирролидин-3-иламино]-бензамида;
4-(1-Бензил-3-метил-2-оксо-2,3-дигидро-1Н-индол-3-иламино)-N-гидрокси-бензамида;
4-[1-(2-Хлор-бензил)-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино)-N-гидрокси-бензамида;
4-[1-(3-Хлор-бензил)-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино)-N-гидрокси-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-фенэтил-2,3-дигидро-1H-индол-3-иламино)-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-фенил-2,3-дигидро-1H-индол-3-иламино)-бензамида;
4-[1-(3-Хлор-фенил)-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино)-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-5-фтор-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-фенил)-5-фтор-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино]-N-гидрокси-бензамида;
4-[1-(2-Хлор-бензил)-5-фтор-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино]-N-гидрокси-бензамида; и
4-[1-(3-Хлор-фенил)-3-метил-2-оксо-2,3-дигидро-1H-пирроло[3,2-с]пиридин-3-иламино]-N-гидрокси-бензамида.
Дополнительные особые соединения формулы (I) или их фармацевтически приемлемые соли, эфиры или стереоизомеры по изобретению могут быть выбраны из:
4-[1-(3-Фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Циано-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Циано-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-4-фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(3-Хлор-5-фтор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,6-Дихлор-фенил)-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-{1-[3-(2-Диметиламино-этокси)-фенил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
N-Гидрокси-4-(2-оксо-1-хинолин-5-ил-пирролидин-3-иламино)-бензамида;
4-(1-Бензил-5-оксо-пирролидин-3-иламино)-N-гидрокси-бензамида;
N-Гидрокси-4-[5-оксо-1-(R-1-фенил-этил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[1-(1-метил-1-фенил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
4-{1-[1-(3-Хлор-фенил)-1-метил-этил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
4-{1-[1-(4-Хлор-фенил)-1-метил-этил]-2-оксо-пирролидин-3-иламино}-N-гидрокси-бензамида;
N-Гидрокси-4-[2-оксо-1-(1-фенил-циклобутил)-пирролидин-3-иламино]-бензамида;
N-Гидрокси-4-[2-оксо-1-(1-фенил-циклогексил)-пирролидин-3-иламино]-бензамида;
4-[1-(4-Хлор-фенил)-3-метил-2-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-3-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-8-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-(3-метил-2-оксо-1-хинолин-6-ил-пирролидин-3-иламино)-бензамида;
N-Гидрокси-4-[3-метил-1-(1-метил-1-фенил-этил)-2-оксо-пирролидин-3-иламино]-бензамида;
2-Фтор-N-гидрокси-4-(2-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
3-Хлор-N-гидрокси-4-(2-оксо-1-фенил-пирролидин-3-иламино)-бензамида;
4-[1-(4-Фтор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
транс-4-[1-(4-Хлор-фенил)-2-метил-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Хлор-фенил)-4-метил-5-оксо-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2,6-Дихлор-фенил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
N-Гидрокси-4-(1-пиримидин-2-ил-пирролидин-3-иламино)-бензамида;
4-[1-(4-Фтор-бензолсульфонил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(4-Фтор-бензоил)-пирролидин-3-иламино]-N-гидрокси-бензамида;
4-[1-(2-Хлор-бензил)-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино)-N-гидрокси-бензамида;
4-[1-(3-Хлор-фенил)-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино)-N-гидрокси-бензамида;
4-[1-(2-Хлор-бензил)-5-фтор-3-метил-2-оксо-2,3-дигидро-1H-индол-3-иламино]-N-гидрокси-бензамида и
4-[1-(3-Хлор-фенил)-3-метил-2-оксо-2,3-дигидро-1H-пирроло[3,2-с]пиридин-3-иламино]-N-гидрокси-бензамида.
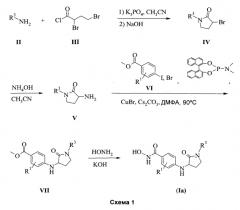
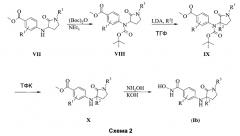
Соединения по настоящему изобретению могут быть получены обычными способами. Подходящие способы синтеза этих соединений, а также исходных веществ приведены на схемах ниже и в Примерах. Все заместители, в частности от R1 до R4, Y и А являются такими, как определено выше, если не указано иное. Кроме того, и если особо не указано иное, все реакции, реакционные условия, аббревиатуры и символы имеют значения, известные специалисту в органической химии.
| Аббревиатуры: | |
| Boc: | трет-бутоксикарбонил |
| д: | день |
| ДИПЭА: | диизопропилэтиламин |
| ДМАП: | 4-N,N-диметиламинопиридин |
| ДМФА: | диметилформамид |
| ДМСО: | диметилсульфоксид |
| ECL: | усиленная хемилюминесценция |
| EDCI: | 1-этил-3-(3-диметиламинопропил)карбодиимид |
| ИФА: | иммуноферментный твердофазный анализ |
| EtOAc: | этилацетат |
| эксп.: | экпериментальный |
| ФБС: | фетальная бычья сыворотка |
| г: | г |
| ЕС50: | концентрация, необходимая для 50% индукции ацетилированного тубулина |
| ИК50: | концентрация, необходимая для 50% ферментативного ингибирования HDAC8 |
| ч: | час |
| HDAC: | гистондеацетилаза |
| ВЭЖХ: | высокоэффективная жидкостная хроматография |
| HRP: | пероксидаза хрена |
| Гц: | герц |
| KOH: | гидроксид калия |
| LDA: | диизопропиламид лития |
| MeOD: | дейтерированный метанол |
| MeOH: | метанол |
| мг: | миллиграмм |
| МГц: | мегагерц |
| мл: | миллилитр |
| ММ: | множественная миелома |
| ммоль: | миллимоль |
| НАД: | никотинамидадениндинуклеотид |
| NaOH: | гидроксид натрия |
| НБ: | не |