Замороженные кондитерские изделия, содержащие пробиотические микроорганизмы
Иллюстрации
Показать всеИзобретение относится к композиции замороженного йогурта для укрепления иммунной системы и/или с противовоспалительным действием. Композиция содержит нереплицирующиеся пробиотические микроорганизмы в количестве от около 106 до 1012 КОЕ на одну порцию, в которой нереплицирующиеся пробиотические микроорганизмы приведены в нереплицирующееся состояние тепловой обработкой при 71,5-150ºС в течение 1-120 с. Изобретение обеспечивает получение композиций, обладающих новыми и улучшенными противовоспалительными и иммуногенными свойствами по сравнению с исходными живыми штаммами. 12 з.п. ф-лы, 18 ил., 2 табл., 5 пр.
Реферат
Настоящее изобретение относится к области замороженных йогуртов. В частности, настоящее изобретение обеспечивает замороженные композиции йогурта, содержащие нереплицирующиеся пробиотические микроорганизмы. Эти нереплицирующиеся пробиотические микроорганизмы могут быть, например, биологически активными пробиотическими микроорганизмами, подвергнутыми тепловой обработке, или все еще биологически активными пробиотическими микроорганизмами, экструдированными при низких температурах. Настоящее изобретение также относится к обеспечиваемой этими нереплицирующимися пробиотическими микроорганизмами пользе для здоровья.
При этом полезные для здоровья эффекты пробиотиков широко используются в данной области и в обобщенном виде представлены, например, Blum и др. в Curr Issues Intest Microbiol. 2003 сентябрь; 4(2):53-60. Часто пробиотики применяются в симбиотических рецептурах совместно с пребиотиками, которые могут даже увеличивать пользу для здоровья.
Обычно пробиотики в настоящее время предлагаются в продаже в составе, например, йогурта и йогуртных напитков.
Однако пробиотики могут обеспечивать свои полезные для здоровья эффекты, только когда они действительно употребляются потребителями. Другими словами, предоставление пробиотиков в продуктах, которые обычно любимы всеми, сделает пользу для здоровья пробиотиков доступной для широкого круга потребителей. Замороженный йогурт является таким продуктом, который любим почти всеми, в частности, детьми и подростками. Помимо этого, замороженный йогурт в целом видится в качестве низкокалорийной альтернативы мороженому.
Что касается мороженого, то M.W. Modler и др. сообщают, что мороженое, содержащее бифидобактерии и фруктоолигосахариды, представляет значительный интерес для здоровья человека (Cult. Dairy Prod. J., 25, стр.4-9, 1990; Canadian Dairy, 75, стр.10, 1996). Аналогичным образом в ЕР307523 (японский био-йогурт Honsha КК) сообщается, что кисломолочный продукт, содержащий волокна пребиотика, может фасоваться в форме мороженого, и таким образом использоваться для терапии некоторых желудочно-кишечных нарушений.
Применение этой концепции к замороженному йогурту дало бы возможность расширить данный подход на замороженные йогурты.
Однако приведение пищевых волокон в контакт с молочнокислыми бактериями имеет значительные недостатки. Эти недостатки имеют различные типы и относятся, в частности, к преждевременной деструкции волокон в ходе приготовления и хранения десерта и к неблагоприятным условиям in vivo, при которых, например, развивается биологическая активность этих волокон.
В патенте US 6399124 ставится цель преодоления этих недостатков посредством разъединения пищевых волокон и пробиотиков в замороженном десерте, обеспечивая съедобный барьер между содержащей волокно основой и содержащим пробиотик мороженым.
Пробиотические бактерии, как известно, способны прилипать к клеткам кишечника человека и вытеснять патогенные бактерии с клеток кишечника человека. Для того чтобы обладать такой активностью, Пробиотические бактерии должны оставаться жизнеспособными в продукте до момента его употребления. Это является задачей для промышленности, и способ ее решения предлагает, например, US 4308287.
Было бы желательно располагать композицией замороженного йогурта, способной обеспечивать полезное пробиотическое действие даже после длительных сроков хранения в критических для пробиотиков условиях и являющейся при этом простой в приготовлении. Было бы предпочтительным достичь этого посредством применения натуральных ингредиентов, которые являются безопасными для употребления, не обладая при этом побочными эффектами, и которые легко вводятся в композиции замороженных йогуртов с использованием промышленных технологий существующего уровня техники.
Также для таких препаратов было бы желательным дальнейшее улучшение укрепляющего иммунную систему действия пробиотиков.
Помимо этого, было бы желательным дальнейшее улучшение противовоспалительного эффекта пробиотиков в таких препаратах.
Настоящее изобретение обращается именно к этой потребности. То есть цель настоящего изобретения состоит в улучшении существующего уровня техники и предоставлении композиций замороженного йогурта, которые отвечали бы обозначенной выше потребности.
Авторы настоящего изобретения неожиданно обнаружили, что они могут достигнуть этого с помощью объектов независимых пунктов формулы изобретения. Основную идею настоящего изобретения развивают дополнительные пункты формулы изобретения.
Соответственно, настоящее изобретение предлагает обеспечить композиции замороженного йогурта, содержащие нереплицирующиеся пробиотические микроорганизмы.
Замороженные йогурты являются замороженными молочными продуктами, изготавливаемыми или содержащими йогурт. Замороженные йогурты могут подаваться, например, как десерт или закуска.
Авторы настоящего изобретения смогли показать, что нереплицирующиеся пробиотики также могут приносить здоровью ту пользу, которую обеспечивают пробиотики, и, возможно, даже в еще большей степени.
Следовательно, представляются излишними усложненные меры по сохранению пробиотиков в живом состоянии в конечном продукте и обеспечении их поступления в живом состоянии в кишечник. Кроме того, использование в замороженном йогуртном продукте нереплицирующихся пробиотиков позволяет иметь вместе в одном препарате и пробиотики, и пребиотики без риска протекания в ходе приготовления и хранения продукта нежелательной преждевременной деструкции волокон.
Количество нереплицирующихся микроорганизмов в композиции мороженого настоящего изобретения может соответствовать от около 106 до 1012 КОЕ на одну порцию.
Очевидно, что нереплицирующиеся микроорганизмы не образуют колоний, поэтому этот термин следует понимать как количество нереплицирующихся микроорганизмов, которое получается из от 104 до 1012 КОЕ/г реплицирующихся бактерий. Они включают микроорганизмы, которые являются инактивированными, мертвыми, нежизнеспособными и/или присутствуют в виде фрагментов, таких как ДНК или цитоплазматические соединения. Другими словами, количество микроорганизмов, которое содержит данная композиция, вне зависимости от того, являются ли они на самом деле живыми, инактивированными, мертвыми или фрагментированными, или же представляют собой смесь любых из этих состояний, выражается в терминах способности данного количества микроорганизмов образовывать колонии (КОЕ), как если бы все эти микроорганизмы являлись бы живыми.
Для целей настоящего изобретения может применяться любая композиция замороженного йогурта. Примеры представлены обычными замороженными йогуртами, обезжиренными замороженными йогуртами, замороженными йогуртами без добавления сахара или обезжиренными замороженными йогуртами без добавления сахара.
Например, такая замороженная композиция йогурта может содержать около 0-12 мас.% жира, около 5-15 мас.% обезжиренного сухого молока, около 5-32 мас.% углеводов, около 1-5 мас.% белка и имеет общее содержание сухого остатка около 30-45 мас.%.
Разумеется, могут добавляться фрукты, шоколад, ваниль, карамель, кофе, орехи, злаки, мед и/или другие вкусоароматические компоненты.
Композиция замороженного йогурта может, кроме того, содержать около 1-25 мас.% добавленного сахара.
Замороженный йогурт может также содержать пребиотики.
Под «пребиотиком» подразумеваются пищевые продукты, которые поддерживают рост пробиотиков в кишечнике. Они не подвергаются расщеплению в желудке и/или верхних отделах кишечника и не всасываются желудочно-кишечным трактом принимающего их человека, но они ферментируются желудочно-кишечной микрофлорой и/или пробиотиками. Пребиотики, например, определяются публикацией Glenn R. Gibson and Marcel B. Roberfroid Dietary Modulation of the Human Colonic Microbiota: Introducing the Concept of Prebiotics (Диетическое модифицирование толстокишечной микробиоты человека: представление концепции пребиотиков), J. Nutr. 1995 125: 1401-1412.
Пребиотики, которые могут использоваться в соответствии с настоящим изобретением, специальным образом не ограничиваются и включают все пищевые продукты, которые способствуют росту пробиотиков в кишечнике. Предпочтительно они могут выбираться из группы, состоящей из олигосахаридов, необязательно содержащих фруктозу, галактозу, маннозу; пищевых волокон, в частности, растворимых волокон, волокон сои; инулина или их смесей. Предпочтительные пребиотики являются фруктоолигосахаридами (FOS), галактоолигосахаридами (IOS), изомальтоолигосахаридами, ксилоолигосахаридами, олигосахаридами сои, гликозилсахарозой (GS), лактосахарозой (LS), лактулозой (LA), палатинозоолигосахаридами (РАО), мальтоолигосахаридами (MOS), камедями и/или их гидролизатами, пектинами и/или их гидролизатами.
Типичные примеры пребиотиков представляют олигофруктоза и инулин.
Композиция замороженного йогурта в соответствии с настоящим изобретением может, кроме того, содержать пищевую основу, связанную с замороженным йогуртом, основу, являющуюся съедобной для людей и содержащей пребиотики.
Эти пребиотики могут иметь белковую или сахаридную природу, выбираясь, например, из растительных пектинов, хито-, фрукто-, гентио-, галакто-, изомальто-, манно- или ксилоолигосахаридов, или олигосахаридов сои, Polymnia sonchifolia (якон), артишока, лука или спаржи, или резистентных крахмалов, или продуктов с высоким содержанием [бета]-глюканов, таких как, например, концентрат овса (Playne и др.; Fukai и др., Soil Sci. Plant Nutr., 39, 567-571, 1993).
Предпочтительные пектины являются полимерами [альфа]-1,4-D-галактуроновой кислоты, имеющей молекулярную массу порядка 10-400 кДа, которые могут быть выделены, например, из моркови или томатов (JP 60164432). Предпочтительные галактоолигосахариды содержат сахаридную часть, состоящую из 2-5 повторяющихся структурных звеньев {-[альфа]-D-Glu-(1->4)-[бета]-D-Gal-(1->6)-} (Yakult Honsa Co., Япония). Предпочтительными фруктоолигосахаридами являются извлекаемые из цикория инулин-олигофруктозы, которые могут содержать, например, 1-9 повторяющихся структурных звеньев {-[бета]-D-Fru-(1->2)-[бета]-D-Fru-(1->2)-} (WO 94/12541; Raffinerie Tirlemontoise S.A., Бельгия), или олигосахариды, синтезируемые из звеньев сахарозы, которые могут содержать, например, сахарозную часть, состоящую из 2-9 повторяющихся структурных звеньев {-[альфа]-D-Glu-(1->2)-[бета]-D-Fru-(1->2)-} (Meiji Seika Kasiha Co., Япония). Предпочтительные мальтоолигосахариды содержат сахаридную часть, состоящую из 2-7 повторяющихся структурных звеньев {-[альфа]-D-Gal-(1->4)-} (Yakult Honsa Co., Япония). Предпочтительные изомальтозы содержат сахаридную часть, состоящую из 2-6 повторяющихся структурных звеньев {-[альфа]-D-Glu-(1->6)-} (Showa Sangyo Co., Япония). Предпочтительные гентиоолигосахариды содержат сахаридную часть, состоящую из 2-5 повторяющихся структурных звеньев {-бета]-D-Glu-(1->6)-} (Nihon Shokuhin Kako Co., Япония). Наконец, предпочтительные ксилоолигосахариды содержат сахаридную часть, состоящую из 2-9 повторяющихся структурных звеньев, например, {-[бета]-ху1-(1->4)-} (Suntory Co., Япония).
Количество пребиотиков в композиции замороженного йогурта согласно изобретению зависит от их способности поддерживать развитие молочнокислых бактерий. Как общее правило, основа может содержать от 0,1 до 20% таких пребиотиков (мас.% по отношению к содержанию сухого вещества).
Композиция замороженного йогурта может содержать нереплицирующиеся пробиотики в количестве, соответствующем количеству по меньшей мере 103 КОЕ на 1 г пребиотика, предпочтительно от 104 до 107 КОЕ/г пребиотика, например.
Авторы данного изобретения неожиданно обнаружили, что, например, в отношении укрепления иммунной системы и/или с точки зрения противовоспалительного действия нереплицирующиеся пробиотические микроорганизмы могут быть даже более эффективными, чем реплицирующиеся пробиотические микроорганизмы.
Это является удивительным, так как пробиотики часто определяются как «живые микроорганизмы, которые при введении в надлежащих количествах приносят пользу здоровью организма» (Руководящие принципы FAO/WHO). Огромное большинство литературных публикаций касается живых пробиотиков. При этом в нескольких исследованиях изучалась полезность для здоровья снабжения нереплицирующимися бактериями, и большинство из них показало, что инактивация пробиотиков, например, тепловой обработкой приводит к потере их подразумеваемой пользы для здоровья (Rachmilewitz, D. и др., 2004, Gastroenterology 126:520-528; Castagliuolo и др., 2005, FEMS Immunol. Med. Microbiol. 43:197-204; Gill, H.S. и K.J. Rutherfurd, 2001, Br. J. Nutr. 86:285-289; Kaila, M. и др., 1995, Arch. Dis. Child 72:51-53.). Некоторые исследования показали, что мертвые пробиотики могут сохранять некоторую способность влиять на состояние здоровья (Rachmilewitz, D., и др., 2004, Gastroenterology 126:520-528; Gill, H.S. и K.J. Rutherfurd, 2001, Br. J. Nutr. 86:285-289), но очевидно, живые пробиотики с этой точки зрения были оценены как намного более эффективные.
«Нереплицирующиеся» пробиотические микроорганизмы включают пробиотические бактерии, подвергнутые тепловой обработке, и пробиотические бактерии, подвергнутые экструдированию. Они включают микроорганизмы, которые являются инактивированными, мертвыми, нежизнеспособными и/или присутствующими в виде фрагментов, таких как ДНК, метаболиты, цитоплазматические соединения или материалы клеточной оболочки.
«Нереплицирующиеся» означает, что никаких жизнеспособных клеток и/или колониеобразующих единиц классическими методами культивирования обнаружено быть не может. Такие классические методы культивирования сведены воедино в книге по микробиологии James Monroe Jay, Martin J. Loessner, David A. Golden. 2005. Modem food microbiology («Современная микробиология пищевых продуктов»). 7 издание, Springer Science, Нью-Йорк, N.Y. 790 стр. Как правило, отсутствие жизнеспособных клеток может быть показано следующим образом: отсутствие каких-либо видимых колоний на чашках с агаровой средой или отсутствие увеличивающегося помутнения в жидкой среде для выращивания после засева бактериальными препаратами в различных концентрациях («Нереплицирующиеся» образцы) и выдерживания в подходящих условиях (аэробная и/или анаэробная атмосфера на протяжении по меньшей мере 24 час).
Пробиотики для целей настоящего изобретения определяются как «препараты микробиологических клеток или компоненты микробиологических клеток, обладающие благотворным воздействием на состояние здоровья или самочувствие организма». (C Salminen, Ouwehand A. Benno Y. и др. “Probiotics: how should they be defined” («Пробиотики: как их следует определять») Trends Food Sci. Technol. 1999:10 107-10).
Композиции настоящего изобретения содержат пробиотические микроорганизмы и/или нереплицирующиеся пробиотические микроорганизмы в количестве, достаточном для по меньшей мере частичного обеспечения благотворного воздействия на здоровье. Подходящее для обеспечения такого действия количество определяется как «терапевтически эффективная доза». Эффективные для этих целей количества зависят от многих известных специалистам в данной области факторов, таких как масса тела и общее состояние здоровья потребителя, а также от эффекта, оказываемого матрицей пищевого продукта.
При профилактических применениях композиции согласно изобретению назначаются восприимчивым или иным образом подверженным риску развития определенного заболевания потребителям в количестве, которое является достаточным для по меньшей мере частичного снижения риска развития такого заболевания. Такое количество определяется как представляющее собой «профилактически эффективную дозу». Аналогично, точные количества зависят от ряда таких факторов, как состояние здоровья и масса потребителя, а также от эффекта, оказываемого матрицей пищевого продукта.
Специалисты в данной области смогут отрегулировать терапевтически эффективную дозу и/или, соответственно, профилактически эффективную дозу.
В целом композиция настоящего изобретения содержит нереплицирующиеся пробиотические микроорганизмы в терапевтически эффективной дозе и/или в профилактически эффективной дозе.
Как правило, терапевтически эффективная доза и/или профилактически эффективная доза находится в диапазоне около 0,005 мг - 1000 мг нереплицирующихся пробиотических микроорганизмов в сутки.
Предпочтительно нереплицирующиеся микроорганизмы присутствуют в количестве, эквивалентном величине между 104 и 109 КОЕ/г сухой композиции, еще более предпочтительно в количестве, эквивалентном величине между 105 и 109 КОЕ/г сухой композиции.
Пробиотики могут быть приведены в нереплицирующееся состояние любым известным в данной области способом.
Имеющиеся в настоящее время технологии, пригодные для приведения пробиотика в нереплицирующееся состояние, обычно представлены тепловой обработкой, γ-облучением, ультрафиолетовым светом или применением химических реагентов (формалин, параформальдегид).
Также обнаружено, что пробиотик может стать нереплицирующимся биологически активным посредством применения некоторой сдвиговой обработки, такой как используется при низкотемпературной экструзии. Поэтому согласно другому воплощению пробиотики приводятся в нереплицирующееся состояние с помощью низкотемпературной экструзии. Низкотемпературная экструзия широко используется в области замороженных кондитерских изделий и определяется как экструзия при отрицательных температурах, обычно при температуре ниже -11°C.
В численном выражении, например, подвергнутые «кратковременной высокотемпературной» обработке нереплицирующиеся микроорганизмы могут присутствовать в композиции в количествах, эквивалентно соответствующих между 104 и 1012 КОЕ/г сухой композиции.
Предпочтительной для приведения пробиотика в нереплицирующееся состояние была бы технология, которая является относительно простой в применении в производственных условиях пищевой промышленности.
Большинство представленных в настоящее время на рынке продуктов содержат пробиотики, подвергнутые в процессе их изготовления тепловой обработке. Поэтому было бы удобным иметь возможность обрабатывать пробиотики нагреванием либо вместе с вырабатываемым продуктом, либо по меньшей мере подобным способом, при том, чтобы пробиотики сохраняли или улучшали свои полезные качества, или даже приобретали бы новые полезные для потребителя свойства.
Однако инактивация пробиотических микроорганизмов тепловой обработкой или высокосдвиговой обработкой, такой, как применяется при низкотемпературной экструзии, по литературным данным, как правило, связана с по меньшей мере частичной потерей активности пробиотика.
Авторы настоящего изобретения в настоящее время неожиданно обнаружили, что приведение пробиотических микроорганизмов в нереплицирующееся состояние, например, тепловой обработкой или низкотемпературной экструзией не приводит к потере полезных для здоровья качеств пробиотика, но, наоборот, может усиливать имеющийся благотворный эффект и даже приводить к созданию новых благоприятствующих здоровью свойств.
Соответственно, одно воплощение настоящего изобретения является композицией замороженного йогурта, в которой нереплицирующиеся пробиотические микроорганизмы приводятся в нереплицирующееся состояние тепловой обработкой, и второе воплощение изобретения является замороженной композицией йогурта, в которой нереплицирующиеся пробиотические микроорганизмы приводятся в нереплицирующееся состояние низкотемпературной экструзией.
Что касается тепловой обработки, то предпочтительно тепловая обработка микроорганизмов выполняется независимо, а затем полученные нереплицирующиеся пробиотические микроорганизмы могут добавляться к замороженной йогуртной смеси.
Такая тепловая обработка может выполняться при по меньшей мере 71,5°C в течение по меньшей мере 1 секунды.
Может применяться как длительная тепловая обработка, так и кратковременная тепловая обработка.
В промышленных масштабах в настоящее время предпочтительными обычно являются способы кратковременной тепловой обработки, такие как пастеризация. Этот вид тепловой обработки снижает бактериальную нагрузку и сокращает продолжительность обработки, тем самым ослабляя ухудшение качества питательных веществ.
Авторы данного изобретения впервые продемонстрировали, что пробиотические микроорганизмы, подвергнутые тепловой обработке при высоких температурах в течение непродолжительного времени, демонстрируют противовоспалительные иммунные профили независимо от своих исходных свойств. В частности, либо вырабатывается новой противовоспалительный профиль, либо существующий противовоспалительный профиль в результате такой тепловой обработки усиливается.
Поэтому теперь оказывается возможным вырабатывать нереплицирующиеся пробиотические микроорганизмы с противовоспалительными иммунными профилями, применяя специальные параметры тепловой обработки, которые соответствуют типичным применяемым при тепловой обработке в промышленности, даже если их живые аналоги не являются штаммами, обладающими противовоспалительной активностью.
Поэтому тепловая обработка может представлять собой, например, высокотемпературную обработку при около 71,5-150°C в течение около 1-120 секунд. Высокотемпературная обработка может являться высокотемпературной/кратковременной (HTST) обработкой, обработкой с повышенной температурой и сокращенным временем пастеризации (HHST) или ультравысокотемпературной (UHT) обработкой.
Пробиотические микроорганизмы могут быть подвергнуты высокотемпературной обработке при около 71,5-150°C в течение короткого времени около 1-120 секунд.
Более предпочтительно микроорганизмы могут быть подвергнуты высокотемпературной обработке при около 90-140°C, например при 90-120°C, в течение короткого времени около 1-30 секунд.
Эта высокотемпературная обработка переводит микроорганизмы, по меньшей мере частично, в нереплицирующееся состояние.
Высокотемпературная обработка может проводиться при нормальном атмосферном давлении, но также может быть выполнена под повышенным давлением. Типичные диапазоны давлений составляют от 1 до 50 бар, предпочтительно от 1 до 10 бар, еще более предпочтительно от 2 до 5 бар. Очевидно, что предпочтительным будет, если пробиотики подвергаются тепловой обработке в питательной среде, которая при приложении теплоты является жидкостью или твердым веществом. Поэтому идеальная величина прикладываемого давления будет зависеть от природы композиции, которая обеспечивается микроорганизмами, и от используемой температуры.
Высокотемпературная обработка может выполняться в интервале температур около 71,5-150°C, предпочтительно около 90-120°C, еще более предпочтительно около 120-140°C.
Высокотемпературная обработка может выполняться в течение короткого времени около 1-120 секунд, предпочтительно около 1-30 секунд, еще более предпочтительно около 5-15 секунд.
Данный временной интервал относится ко времени, в течение которого пробиотические микроорганизмы подвергаются воздействию данной температуры. Следует заметить, что в зависимости от природы и количества обеспечиваемой микроорганизмами композиции, а также в зависимости от конструкции применяемого нагревательного устройства, продолжительность применяемого нагревания может изменяться.
Однако, как правило, композиция настоящего изобретения и/или микроорганизмы подвергаются высокотемпературной кратковременной (HTST) обработке, мгновенной пастеризации или ультравысокотемпературной (UHT) обработке.
Обработка является ультравысокотемпературной обработкой или ультратепловой обработкой (обе сокращаются аббревиатурой UHT), включающей по меньшей мере частичную стерилизацию композиции при нагревании ее в течение короткого времени, приблизительно 1-10 секунд, при температуре, превышающей 135°C (275°F), которая является температурой, необходимой для уничтожения в молоке спор бактерий. Например, такая обработка молока с помощью температур, превышающих 135°C, делает возможным снижение величины бактериальной нагрузки при таком обязательным времени пребывания (до 2-5 с), которое позволяет использовать режим непрерывного потока.
Есть два основных типа UHT-систем: прямые и непрямые системы. В прямой системе продукты обрабатываются впрыскиванием пара или нагнетанием пара, тогда как в непрямой системе продукты подвергаются тепловой обработке с помощью пластинчатого теплообменника, трубчатого теплообменника или скребкового теплообменника. В процессе обработки продукта комбинации UHT-систем могут применяться на любом этапе или на ряде этапов.
Обработка HTST определяется следующим образом (высокая температура / короткое время): способ пастеризации, предназначенный для пятикратного по логарифмической шкале снижения количества жизнеспособных микроорганизмов в молоке с уничтожением 99,9999% их общего содержания. Это считается подходящим для истребления почти всех дрожжей, плесневых грибков и обычных вызывающих порчу бактерий, а также для обеспечения надлежащего уничтожения обычных патогенных теплоустойчивых организмов. При способе HTST молоко на 15-20 секунд нагревается до 71,7°C (161°F).
Мгновенная пастеризация является способом тепловой пастеризации скоропортящихся напитков, таких как фруктовые и овощные соки, пиво и молочные продукты. Это выполняется перед расфасовкой в контейнеры для уничтожения вызывающих порчу микроорганизмов, придания продуктам большей безопасности и увеличения продолжительности их хранения. Жидкость двигается в контролируемом непрерывном потоке и при этом в течение около 15-30 секунд подвергается воздействию температур от 71,5°C (160°F) до 74°C (165°F).
Для целей настоящего изобретения термин «кратковременная высокотемпературная обработка» включает, например, кратковременную обработку при высокой температуре (HTST), UHT-обработку и мгновенную пастеризацию.
Так как такая тепловая обработка придает нереплицирующимся пробиотикам улучшенный противовоспалительный профиль, композиция настоящего изобретения может быть применена в профилактике или терапии воспалительных нарушений.
Воспалительные нарушения, которые могут быть излечены или предупреждены с помощью композиции настоящего изобретения, специальным образом не ограничивается. Например, они могут быть выбраны из группы, состоящей из острых воспалений, таких как сепсис; ожогов; хронических воспалений, таких как воспалительные заболевания кишечника, например, болезнь Крона, неспецифический язвенный колит, паучит; некротизирующего энтероколита; кожных воспалений, таких как УФ- или химически индуцированное воспаление кожи, экзема, реактивная кожа; синдрома раздраженного кишечника; воспалений глаз; аллергии, астмы и их комбинаций.
Если для приведения пробиотических микроорганизмов в нереплицирующееся состояние применяется длительная тепловая обработка, такая тепловая обработка может осуществляться в интервале температур около 70-150°C в течение около 3 минут - 2 часов, предпочтительно в диапазоне 80-140°C от 5 минут до 40 минут.
В то время как существующий уровень техники в основном указывает, что бактерии, приведенные в нереплицирующееся состояние с помощью длительной тепловой обработки, обычно менее эффективны, чем живые клетки, в отношении проявления их пробиотических качеств, авторы настоящего изобретения смогли продемонстрировать, что подвергнутые тепловой обработке пробиотики превосходят свои живые аналоги в способности стимулировать иммунную систему.
Настоящее изобретение также относится к композиции, содержащей пробиотические микроорганизмы, приведенные в нереплицирующееся состояние тепловой обработкой в течение по меньшей мере около 3 минут при по меньшей мере около 70°C.
Усиливающее иммунную систему действие нереплицирующихся пробиотиков было подтверждено in vitro иммунным профилем. В применяемой in vitro модели используется цитокиновый профиль человеческих мононуклеаров периферической крови (РВМС) и хорошо принимается в данной области в качестве стандартной модели для исследования иммуномодулирующих соединений (Schultz и др., 2003, Journal of Dairy Research 70, 165-173; Taylor и др., 2006, Clinical and Experimental Allergy, 36, 1227-1235; Kekkonen и др., 2008, World Journal of Gastroenterology, 14, 1192-1203).
Испытания РВМС in vitro применялись несколькими авторами / исследовательскими группами, например, для классифицирования пробиотиков согласно их иммунным профилям, то есть по их анти- или провоспалительным показателям (Kekkonen и др., 2008, World Journal of Gastroenterology, 14, 1192-1203). Было показано, например, что такие испытания позволяют прогнозировать противовоспалительное действие исследуемых пробиотиков в отношении кишечного колита в моделях на мышах (Foligne В. и др., 2007, World J. Gastroenterol. 13:236-243). Более того, это испытание регулярно применяется в качестве показательного в клинических исследованиях и была продемонстрирована его способность представлять результаты, согласующиеся с клиническими данными (Schultz и др., 2003, Journal of Dairy Research 70, 165-173; Taylor и др., 2006, Clinical and Experimental Allergy, 36, 1227-1235).
За последние десятилетия непрерывно увеличивается распространенность аллергических заболеваний и в настоящее время они рассматриваются ВОЗ в качестве эпидемических. В общих чертах, аллергия, как полагают, является следствием дисбаланса между иммунными ответами Th1 и Th2, приводящего к сильному сдвигу в сторону продуцирования медиаторов Th2. Поэтому аллергия может быть смягчена, подавлена или предотвращена посредством восстановления надлежащего соответствия между Th1 и Th2 компонентами иммунной системы. Это подразумевает необходимость в снижении ТП2-ответов или усилении, по меньшей мере временном, ответа Th1. Последнее было бы показателем укрепления иммунной системы, часто сопровождаемого высокими уровнями, например, IFN-γ, TNF-α и IL-12 (World Journal of Gastroenterology, 14, 1192-1203; Viljanen M. и др., 2005, Allergy, 60, 494-500).
Композиция замороженного йогурта настоящего изобретения позволяет поэтому излечивать или предупреждать нарушения, связанные с повреждениями иммунной защиты.
Соответственно, нарушения, связанные с повреждениями иммунной защиты, которые могут быть излечены или предупреждены с помощью композиции настоящего изобретения, специальным образом не ограничивается.
Например, они могут выбираться из группы, состоящей из инфекций, в частности, бактериальных, вирусных, грибковых и/или паразитарных инфекций; фагоцитарного дефицита; угнетения иммунитета слабой или тяжелой степени, вызванного стрессом или действием иммунодепрессивных лекарственных препаратов, химиотерапии или лучевой терапии; натуральных состояний сниженной иммунокомпетентности иммунной системы, например, у новорожденных; аллергий и их комбинаций.
Описанная в настоящем изобретении композиция замороженного йогурта позволяет также усиливать реакцию ребенка на вакцины, в частности, на пероральные вакцины.
Согласно второму воплощению нереплицирующиеся микроорганизмы приводятся в нереплицирующееся состояние посредством приложения высокосдвиговой обработки, такой как низкотемпературная экструзия. Низкотемпературная экструзия, также именуемая в области замороженных кондитерских изделий замораживанием при низких температурах, описывается, например, в патенте US 7261913, содержание которого включено здесь посредством ссылки. Эта обработка состоит в применении, например, сдвиговой обработки со скоростями сдвига в диапазоне от 1 до 50 л/с или в развитии сдвигового напряжения в диапазоне от 2500 до 75000 Па при поддержании критической температуры в шнековом экструдере. Шнековый экструдер может быть таким, как описывается в заявке WO 2005/070225. Экструзия может выполняться в одно- или двухшнековом экструдере.
В частности, нереплицирующиеся микроорганизмы, приведенные в нереплицирующееся состояние низкотемпературной экструзией, показывают такое же благоприятное противовоспалительное действие, как и подвергнутые тепловой обработке. Эффективными могут быть любые количества нереплицирующихся микроорганизмов. Однако предпочтительно, чтобы в целом по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, идеально по меньшей мере 99,9%, наиболее идеально все пробиотики являлись бы нереплицирующимися.
В одном воплощении настоящего изобретения все микроорганизмы являются нереплицирующимися.
Соответственно, в композиции настоящего изобретения по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, идеально по меньшей мере 99,9%, наиболее идеально все пробиотики могут быть нереплицирующимися.
Для целей настоящего изобретения могут применяться любые пробиотические микроорганизмы.
Например, пробиотические микроорганизмы могут выбираться из группы, состоящей из бифидобактерий, молочнокислых бактерий, пропионовокислых бактерий или их комбинаций, например, Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus fermentum, Lactococcus lactis. Streptococcus thermophilus, Lactococcus lactis, Lactococcus diacetylactis, Lactococcus cremoris, Lactobacillus bulgaricus, Lactobacillus helveticus, Lactobacillus delbrueckii, Escherichia coli и/или их смесей.
Композиция в соответствии с настоящим изобретением может, например, содержать пробиотические микроорганизмы, выбранные из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus johnsonii La1, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Lactobacillus reuteri DSM 17983, Lactobacillus reuteri ATCC 55730, Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus casei NCC 4006, Lactobacillus acidophilus NCC 3009, Lactobacillus casei ACA-DC 6002 (NCC 1825), Escherichia coli Nissle, Lactobacillus bulgaricus NCC 15, Lactococcus lactis NCC 2287 или их комбинаций.
Все эти штаммы были или депонированы согласно Будапештскому договору, и/или являются предлагаемыми в продаже.
Депонированными согласно Будапештскому договору являются следующие штаммы:
| Bifidobacterium longum NCC 3001: | ATCC BAA-999 |
| Bifidobacterium longum NCC 2705: | CNCM I-2618 |
| Bifidobacterium breve NCC 2950 | CNCM I-3865 |
| Bifidobacterium lactis NCC 2818: | CNCM I-3446 |
| Lactobacillus paracasei NCC 2461: | CNCM I-2116 |
| Lactobacillus rhamnosus NCC 4007: | CGMCC 1.3724 |
| Streptococcus themophilus NCC 2019: | CNCM I-1422 |
| Streptococcus themophilus NCC 2059: | CNCM 1-4153 |
| Lactococcus lactis NCC 2287: | CNCM I-4154 |
| Lactobacillus casei NCC 4006: | CNCM I-1518 |
| Lactobacillus casei NCC 1825: | ACA-DC 6002 |
| Lactobacillus acidophilus NCC 3009: | ATCC 700396 |
| Lactobacillus bulgaricus NCC 15: | CNCM I-1198 |
| Lactobacillus johnsonii La1 | CNCM I-1225 |
| Lactobacillus reuteri DSM17983 | DSM 17983 |
| Lactobacillus reuteri ATCC 55730 | ATCC 55730 |
| Escherichia coli Nissle 1917: | DSM 6601 |
Штаммы, именуемые ATCC, были депонированы в Американской коллекции типовых культур (ATCC Patent Depository), 10801 University Blvd., Manassas, VA 20110, США.
Штаммы, именуемые CNCM, были депонированы в COLLECTION NATIONALE DE CULTURES DE MICROORGANISMES (CNCM), 25 rue du Docteur Roux, F-75724 PARIS Cedex 15, Франция.
Штаммы, именуемые CGMCC, были депонированы в Китайском главном коллекционном центре микробиологических культур, Институт микробиологии Академии наук Китая, Zhongguancun, P.O. Box 2714, Пекин 100080, Китай.
Штаммы, именуемые ACA-DC, были депонированы в Греческом координационном центре коллекций микроорганизмов. Лаборатория молочных продуктов, Отдел теоретических основ и технологии пищевых продуктов, Сельскохозяйственный университет Афин, 75, Iera odos, Botanikos, Афины, 118 55, Греции.
Штаммы, именуемые DSM, были депонированы в DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstr., 7 B, 38124 Braunschweig, Германия.
Специалистам в данной области ясно, что они могут свободно объединять все описанные здесь признаки настоящего изобретения без отступления от его раскрываемого здесь объема.
Дальнейшие признаки и преимущества настоящего изобретения будут очевидны из следующих далее Фигур и Примеров.
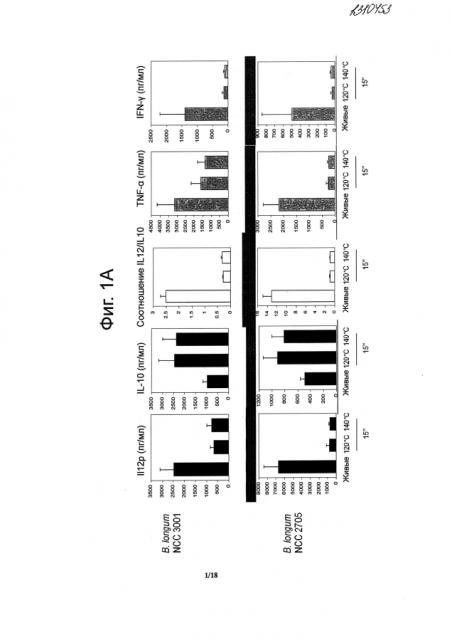
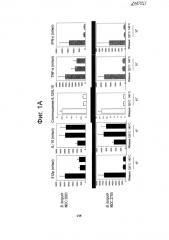
Фигуры 1A и B показывают усиление противовоспалительных иммунных профилей пробиотиков, подвергнутых «кратковременной высокотемпературной» обработке.
Фигура 2 показывает штаммы пробиотиков, не обладающие противовоспалительными качествами, которые становились противовоспалительными, то есть демонстрирующими выраженный противовоспалительный профиль in vitro после «кратковременной высокотемпературной» обработки.
Фигуры 3A и B показывают штаммы пробиотиков, применяемые в коммерчески доступных продуктах, которые демонстрируют усиленные или новоприобрет