Средства, вызывающие апоптоз, для лечения злокачественных новообразований и иммунных и аутоиммунных заболеваний
Иллюстрации
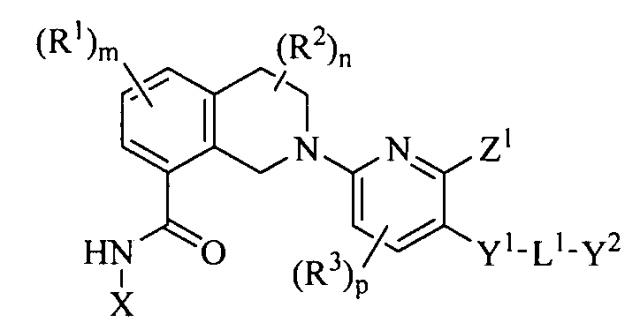
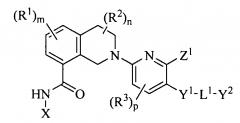
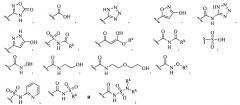
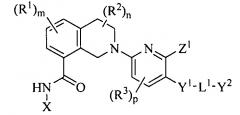
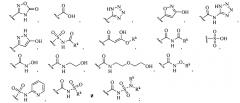
Показать всеИзобретение относится к гетероциклическим соединениям формулы (I) или к его терапевтически приемлемой соли, где X представляет собой бензо[d]тиазолил, необязательно замещен одним или двумя R4; Y1 представляет собой пирролил, пиразолил, триазолил или пиридинил; где Y1 необязательно замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из R5, CO(O)R5, СО(O)Н и CN; L1 выбран из группы, состоящей из (CR6R7)q, (CR6R7)s-O-(CR6R7)r, (CR6R7)s-C(O)-(CR6R7)r, (CR6R7)s-S(О)2-(CR6R7)r и (CR6R7)s-NR6A-(CR6R7)r; и Y2 выбран из группы, состоящей из C3-4 алкила с разветвленной цепью, C5-7 циклоалкила, C6-7 циклоалкенила, фенила, пиперидинила, морфолинила и тетрагидропиранила; где фенил необязательно конденсирован с бензолом; где Y2 необязательно замещен одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из R8, OR8, SO2R8, CO(O)R8, NHR8, N(R8)2, C(O)H, OH, CN, NO2, F, Cl, Br и I; или L1 представляет собой связь; и Y2 выбран из группы, состоящей из С5 циклоалкила, фенила, тетрагидропиранила и пиперидинила; где С5 циклоалкил и тетрагидропиранил, представленные Y2, необязательно конденсированы с бензолом; Z1 выбран из группы, состоящей из или ; R1, R2 и R3 отсутствуют; R4, в каждом случае, независимо выбран из группы, состоящей из OR12 и галогена; R5, в каждом случае, независимо выбран из группы, состоящей из C1-6 алкила, C1-6 гидроксиалкила, фенила и циклопропила; R6A представляет собой C1-6 алкил; каждый R6 и R7, в каждом случае, независимо выбран из группы, состоящей из водорода, R15 и CO(O)R15; R8, в каждом случае, независимо выбран из группы, состоящей из C1-6 алкила, C2-6 алкинила, фенила, пиперидинила и морфолинила; где R8 C1-6 алкил и C2-6 алкинил необязательно замещены одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из R16, OR16, SO2R16, C(O)R16, NHR16, N(R16)2, ОН и F; где R8 фенил необязательно замещен одним Cl; Rk, в каждом случае, представляет собой C1-6 алкил; R12 представляет собой C1-4 алкил; R15, в каждом случае, независимо выбран из группы, состоящей из C1-4 алкила и фенила; где R15 C1-4 алкил необязательно замещен одним заместителем, выбранным из группы, состоящей из C1-4 алкокси, морфолинила и С6циклоалкила; R16, в каждом случае, независимо выбран из группы, состоящей из C1-4 алкила, C1-4 гидроксиалкила, фенила, тетрагидропиранила, морфолинила, 1,4-диоксанила, диоксидотиоморфолинила и пиридинила; q равно 1, 2 или 3; s, r, m, n и p равно 0; или где соединение выбрано из группы, указанной в п.1. Также изобретение относится к фармацевтической композиции на основе описанных соединений и способу лечения рака. Технический результат: получены новые гетероциклические соединения, полезные при лечении рака. 5 н. и 4 з.п. ф-лы, 3 табл., 188 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям, которые ингибируют активность антиапоптотических белков Bcl-xL, к композициям, содержащим эти соединения, и к способам лечения заболеваний, при которых экспрессируются антиапоптотические белки Bcl-xL.
УРОВЕНЬ ТЕХНИКИ, ПРЕДШЕСТВУЮЩИЙ ИЗОБРЕТЕНИЮ
Известно, что апоптоз является основным биологическим процессом для тканевого гомеостаза у всех живых организмов. У млекопитающих, в частности, было показано, что апоптоз регулирует ранние стадии эмбрионального развития. Остальную часть жизни гибель клеток является механизмом по умолчанию, при котором удаляются потенциально опасные клетки (например, клетки, несущие раковые повреждения). Было обнаружено несколько путей апоптоза, и один из самых важных путей включает в себя белки семейства Bcl-2, которые являются ключевыми регуляторами митохондриального (также называемого «внутренним») пути апоптоза. См., Danial, N.N. and Korsmeyer, S.J. Cell (2004) 116, 205-219. Структурно гомологичные домены BH1, BH2, ВН3 и BH4 являются характерными для этого семейства белков. Семейство белков Bcl-2 может быть дополнительно классифицировано на три подсемейства в зависимости от того, сколько каждый белок содержит гомологичных доменов и от их биологической активности (т.е. обладает ли он про- или антиапоптотической функцией).
Первая подгруппа содержит белки, имеющие все 4 гомологичных домена, то есть BH1, ВН2, BH3 и BH4. Их общим эффектом является антиапоптотический эффект, то есть эффект предохранения клетки от запуска процесса гибели клетки. Белки, такие как, например, Bcl-2, Bcl-w, Bcl-xL, Mcl-1 и Bfl-1/A1, являются членами этой первой подгруппы. Белки, принадлежащие второй подгруппе, содержат три гомологичных домена BH1, BH2 и BH3, и обладают проапоптотическим эффектом. Двумя главными представителями белков этой второй подгруппы являются Вах и Bak. Наконец, третья подгруппа состоит из белков, содержащих только домен BH3, а члены этой подгруппы обычно называют белками «BH3-only». Их биологическим эффектом на клетки является проапоптотическим. Bim, Bid, Bad, Bik, Noxa, Hrk, Bmf и Puma являются примерами этого третьего подсемейства белков. Точный механизм, с помощью которого семейство белков Bcl-2 регулируют гибель клеток, пока не совсем известен, и в рамках научного сообщества ведутся активные исследования в попытках понять этот механизм. По одной из гипотез регуляции гибели клеток белками семейства Bcl-2 белки «BH3-only» дополнительно разделяют на белки «активаторы» (например, Bim и Bid) или «сенсибилизаторы» (например, Bad, Bik, Noxa, Hrk, Bmf и Puma) в зависимости от их регуляторной функции.
Ключом к тканевому гомеостазу является достижение хрупкого баланса во взаимодействии трех подгрупп белков в клетке. В недавних исследованиях были сделаны попытки выяснить механизмы, с помощью которых взаимодействуют проапоптотические и антиапоптотические подгруппы семейства белков Bcl-2, обеспечивая программируемую гибель клеток. После получения внутриклеточных или внеклеточных сигналов в клетки возникает посттрансляционная или транскрипционная активность «BH3-only» белков. «BH3-only» белки являются первичными индукторами апоптотического каскада, который включает, как одну стадию, активацию проапоптотических белков Bax и Bak на мембране митохондрий в клетках. После активации Вах и/или Bak, которые либо уже прикреплены к мембране митохондрий, либо мигрируют к мембране, Вах и/или Bak олигомеризуются, что приводит к пермеабилизации наружной митохондриальной мембраны (MOMP), высвобождению цитохрома С и активации эффекторных каспаз далее в сигнальном пути, что в конечном счете приводит к апоптозу клетки. Некоторые исследователи предполагают, что некоторые белки «BH3-only» (например, Puma, Bim, Bid) являются «активаторами» в том плане, что эти белки непосредственно вовлекают проапоптотические белки Bax и Bak в инициацию MOMP, тогда как другие белки «ВН3-only» (например, Bad, Bik и Noxa) являются «сенсибилизаторами» и вовлекают Вах и Bak в олигомеризацию косвенно, путем связывания антиапоптотических белков (например, Bcl-2, Bcl-xL, Bcl-w, Mcl-1) и вытеснения и «освобождения места» для «активаторных» белков «ВН3-only», которые затем связываются с проапоптотическими белками и активируют их (например, Вах, Bak), вызывая гибель клеток. Другие исследователи предполагают, что антиапоптотические белки напрямую влияют на Bax и Bak и опосредуют их действие, и все белки «BH3-only» регулируют это взаимодействие путем связывания с антиапоптотическими белками (например, Bcl-2, Bcl-xL, Bcl-w, Mcl-1), что приводит к высвобождению Вах и Bak. См., Adams, J.M. и Cory S. Oncogene (2007) 26, 1324-1337; Willis, S.N. et al. Science (2007) 315, 856-859. Хотя детали взаимодействий посредством которых анти- и проапоптотические белки семейства Bcl-2 регулируют апоптоз остаются на стадии обсуждения, есть большое количество научных доказательств того, что соединения, которые ингибируют связывание белков «BH3-only» с антиапоптотическими белками Bcl-2 способствуют апоптозу в клетках.
Апоптотические пути с нарушенным контролем вовлечены в патологию большого числа различных заболеваний, таких как нейродегенеративные нарушения (повышенная активация апоптоза), такие как, например, болезнь Альцгеймера; и пролиферативные заболевания (ингибирование апоптоза), такие как, например, злокачественные опухоли, аутоиммунные заболевания и про-тромботические состояния.
В одном из аспектов подразумевается, что подавление апоптоза (и, более конкретно, белков семейства Bcl-2), которое вовлечено в возникновение злокачественных новообразований, является новым подходом, направленным на это до сих пор неизлечимое заболевание. Исследования показали, например, что антиапоптотические белки, Bcl-2 и Bcl-xL, сверхэкспрессируются во многих типах злокачественных клеток. См., Zhang J.Y., Nature Reviews/Drugs Discovery, (2002) 1, 101; Kirkin, V. et al. Biochimica et Biophysica Acta (2004) 1644, 229-249; и Amundson, S.A. et al. Cancer Research (2000) 60, 6101-6110. Эффектом этого нарушения является жизнеспособность измененных клеток, которые в нормальных условиях подверглись бы апоптозу. Повторение этой неисправности, связанной с нерегулируемой пролиферацией, как полагают, является отправной точкой развития раковых новообразований. Кроме того, исследования показали, что белки “BH3-only” могут действовать как опухолевые супрессоры при экспрессии в организме больных животных.
Эти обнаружения, наряду с другими многочисленными данными, сделали возможным появление новых подходов в поисках лекарственных средств, нацеленных на злокачественные опухоли. Если низкомолекулярные соединения, которые могут имитировать эффект белков «BH3-only», могли бы войти в клетку и устранить сверхэкспрессию антиапоптотических белков, то можно было бы перезапустить процесс апоптоза. Преимуществом этого подхода могло бы быть решение проблемы лекарственной устойчивости, которая, как правило, является следствием нарушенной регуляции апоптоза (патологичная жизнеспособность).
Кроме того, исследования показали, что тромбоциты также содержат необходимую машину для апоптоза (например, Вах, Bak, Bcl-xL, Bcl-2, цитохром с, каспаза-9, каспаза-3 и APAF-1) для выполнения программируемой гибели клеток посредством присущего пути апоптоза. Хотя продукция циркулирующих тромбоцитов является нормальным физиологическим процессом, при ряде заболеваний происходит или усугубляется увеличение, или нежелательная активность, тромбоцитов. Вышеуказанное позволяет сделать предположение о том, что терапевтические средства, способные ингибировать антиапоптотические белки в тромбоцитах и уменьшающие количество тромбоцитов у млекопитающих, могут быть эффективны для лечения протромботических состояний и заболеваний, которые характеризуются избытком, или нежелательной активацией, тромбоцитов.
Авторы разработали класс низкомолекулярных миметиков белков «BH3-only», т.е. ABT-737 и ABT-263, которые высокоэффективно связываются с различными антиапоптотическими белками Bcl-2, в том числе Bcl-2, Bcl-w и Bcl-xL, и крайне слабо связываются с Mcl-1 и A1, и демонстрируют основанную на механизме цитотоксичность. Эти соединения тестировали в исследованиях на животных и они показали цитотоксическую активность на некоторых моделях ксенотрансплантатов как самостоятельные средства, так и повышенные эффекты ряда химиотерапевтических средств на других моделях ксенотрансплантатов, в которых их использовали в комбинации. См., Tse, C. et al. Cancer Res (2008) 68, 3421-3428; и van Delft, M.F. et al. Cancer Cell (2006) 10, 389-399. Эти in vivo исследования предполагают возможную эффективность ингибиторов из антиапоптотических белков семейства Bcl-2 для лечения заболеваний, которые связаны с нарушением регуляции апоптоза.
Природные уровни экспрессии представителей антиапоптотических белков семейства Bcl-2 различаются в зависимости от типов клеток. Например, в недавно образованных тромбоцитах белок Bcl-xL экспрессируется на высоком уровне и играет важную роль в регулировании клеточной гибели (продолжительности жизни) тромбоцитов. Кроме того, в некоторых типах злокачественных клеток, жизнеспособность злокачественных клеток связана с нарушением регуляции пути апоптоза, вызванного сверхэкспрессией одного или нескольких антиапоптотических белков, представителей семейства Bcl-2. Ввиду важной роли белков семейства Bcl-2 в регуляции апоптоза как в злокачественных, так и в нормальных (т.е. нераковых) клетках, и известной изменчивости экспрессии белков семейства Bcl-2 типа в зависимости от типа клетки, предпочтительно иметь низкомолекулярный ингибитор, который избирательно нацеливается и предпочтительно связывается с одним типом или с подмножеством антиапоптотических белков Bcl-2, например, с антиапоптотическим представителем семейства Bcl-2, который сверхэкспрессирован в определенных типах злокачественных опухолей. Такое селективное соединение также может обеспечивать определенные преимущества в клинических условиях, предоставляя возможность, например, гибкого режима дозирования, уменьшая нацеленный токсический эффект на нормальные клетки, наряду с другими (например, у мышей с дефицитом Bcl-2 наблюдалась лимфопения). См., Nakayama, K. et al. PNAS (1994) 91, 3700-3704.
В связи с указанным выше, в данной области существует необходимость в низкомолекулярных терапевтических средствах, которые могут селективно ингибировать активность одного типа или подмножества антиапоптотических белков Bcl-2, например, антиапоптотическего белка Bcl-xL. Настоящее изобретение решает по меньшей мере эту потребность.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Один из вариантов осуществления настоящего изобретения, таким образом, относится к соединениям или их терапевтически приемлемым солям, которые могут использоваться в качестве ингибиторов антиапоптотических белков Bcl-xL, к соединениям, имеющим формулу (I)
Формула (I)
или к их терапевтически приемлемой соли, где
Х представляет собой гетероарил; где гетероарил, представленный Х, необязательно замещен один, двумя, тремя или четырьмя R4;
Y1 представляет собой фенилен или C5-6 гетероарилен; необязательно конденсированный с одним или двумя кольцами, выбранными из группы, состоящей из C3-8 циклоалкана, C3-8 циклоалкена, бензола, C5-6 гетероарена, C3-8 гетероциклоалкана и C3-8 гетероциклоалкена; где Y1 необязательно замещен одним, двумя, тремя или четырьмя заместителями, независимо выбранными из группы, состоящей из R5, OR5, SR5, S(O)R5, SO2R5, C(O)R5, CO(O)R5, OC(O)R5, OC(O)OR5, NH2, NHR5, N(R5)2, NHC(O)R5, NR5C(O)R5, NHS(O)2R5, NR5S(O)2R5, NHC(O)OR5, NR5C(O)OR5, NHC(O)NH2, NHC(O)NHR5, NHC(O)N(R5)2, NR5C(O)NHR5, NR5C(O)N(R5)2, C(O)NH2, C(O)NHR5, C(O)N(R5)2, C(O)NHOH, C(O)NHOR5, C(O)NHSO2R5, C(O)NR5SO2R5, SO2NH2, SO2NHR5, SO2N(R5)2, CO(O)H, C(O)H, OH, CN, N3, NO2, F, Cl, Br и I;
L1 выбран из группы, состоящей из (CR6R7)q, (CR6R7)s-O-(CR6R7)r, (CR6R7)s-C(O)-(CR6R7)r, (CR6R7)s-S-(CR6R7)r, (CR6R7)s-S(O)2-(CR6R7)r, (CR6R7)s-NR6AC(O)-(CR6R7)r, (CR6R7)s-C(O)NR6A-(CR6R7)r, (CR6R7)s-NR6A-(CR6R7)r, (CR6R7)s-S(O)2NR6A-(CR6R7)r и (CR6R7)s-NR6AS(O)2-(CR6R7)r; и
Y2 выбран из группы, состоящей из C3-11 алкила с разветвленной цепью, C3-7 циклоалкила, C4-7 циклоалкенила, фенила и C3-7 гетероциклила; где C3-7 циклоалкил, C4-7 циклоалкенил, фенил и C3-7 гетероциклил необязательно конденсированы с одним или двумя кольцами, выбранными из группы, состоящей из C3-8 циклоалкана, C3-8 циклоалкена, бензола, C5-6 гетероарена, C3-8 гетероциклоалкана и C3-8 гетероциклоалкена; где Y2 необязательно замещен одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из группы, состоящей из R8, OR8, SR8, S(O)R8, SO2R8, C(O)R8, CO(O)R8, OC(O)R8, OC(O)OR8, NH2, NHR8, N(R8)2, NHC(O)R8, NR8C(O)R8, NHS(O)2R8, NR8S(O)2R8, NHC(O)OR8, NR8C(O)OR8, NHC(O)NH2, NHC(O)NHR8, NHC(O)N(R8)2, NR8C(O)NHR8, NR8C(O)N(R8)2, C(O)NH2, C(O)NHR8, C(O)N(R8)2, C(O)NHOH, C(O)NHOR8, C(O)NHSO2R8, C(O)NR8SO2R8, SO2NH2, SO2NHR8, SO2N(R8)2, CO(O)H, C(O)H, OH, CN, N3, NO2, F, Cl, Br и I; или
L1 представляет собой связь; и
Y2 выбран из группы, состоящей из C3-7 циклоалкила, C4-7 циклоалкенила, фенила и C3-7 гетероциклила; где C3-7 циклоалкил, C4-7 циклоалкенил, фенил и C3-7 гетероциклил, представленный Y2, необязательно конденсированы с одним или двумя кольцами, выбранными из группы, состоящей из C3-8 циклоалкана, C3-8 циклоалкена, бензола, C5-6 гетероарена, C3-8 гетероциклоалкана и C3-8 гетероциклоалкена; где каждый Y2 и каждое кольцо, конденсированное с Y2, необязательно замещены одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранным из группы, состоящей из R8, OR8, SR8, S(O)R8, SO2R8, C(O)R8, CO(O)R8, OC(O)R8, OC(O)OR8, NH2, NHR8, N(R8)2, NHC(O)R8, NR8C(O)R8, NHS(O)2R8, NR8S(O)2R8, NHC(O)OR8, NR8C(O)OR8, NHC(O)NH2, NHC(O)NHR8, NHC(O)N(R8)2, NR8C(O)NHR8, NR8C(O)N(R8)2, C(O)NH2, C(O)NHR8, C(O)N(R8)2, C(O)NHOH, C(O)NHOR8, C(O)NHSO2R8, C(O)NR8SO2R8, SO2NH2, SO2NHR8, SO2N(R8)2, CO(O)H, C(O)H, OH, CN, N3, NO2, F, Cl, Br и I;
Z1 выбран из группы, состоящей из C(O)OR9, C(O)NR10R11, C(O)R11, NR10C(O)R11, NR10C(O)NR10R11, OC(O)NR10R11, NR10C(O)OR9, C(=NOR10)NR10R11, NR10C(=NCN)NR10R11, NR10S(O)2NR10R11, S(O)2R9, S(O)2NR10R11, N(R10)S(O)2R11, NR10C(=NR11)NR10R11, C(=S)NR10R11, C(=NR10)NR10R11, галоген, NO2 и CN; или
Z1 выбран из группы, состоящей из
R1, в каждом случае, независимо выбран из группы, состоящей из галогена, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C1-6 галогеналкила;
R2, в каждом случае, независимо выбран из группы, состоящей из дейтерия, галогена, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C1-6 галогеналкила;
два R2, которые присоединены к одному и тому же атому углерода, вместе с указанным атомом углерода, необязательно образуют кольцо, выбранное из группы, состоящей из гетероциклоалкила, гетероциклоалкенила, циклоалкила и циклоалкенила;
R3, в каждом случае, независимо выбран из группы, состоящей из галогена, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C1-6 галогеналкила;
R4, в каждом случае, независимо выбран из группы, состоящей из NR12R13, OR12, CN, NO2, галогена, C(O)OR12, C(O)NR12R13, NR12C(O)R13, NR12S(O)2R14, NR12S(O)R14, S(O)2R14, S(O)R14 и R14;
R5, в каждом случае, независимо выбран из группы, состоящей из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, C1-6 гидроксиалкила, арила, гетероциклила, циклоалкила и циклоалкенила;
R6A независимо выбран из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C1-6 галогеналкила;
каждый R6 и R7, в каждом случае, независимо выбран из группы, состоящей из водорода, R15, OR15, SR15, S(O)R15, SO2R15, C(O)R15, CO(O)R15, OC(O)R15, OC(O)OR15, NH2, NHR15, N(R15)2, NHC(O)R15, NR15C(O)R15, NHS(O)2R15, NR15S(O)2R15, NHC(O)OR15, NR15C(O)OR15, NHC(O)NH2, NHC(O)NHR15, NHC(O)N(R15)2, NR15C(O)NHR15, NR15C(O)N(R15)2, C(O)NH2, C(O)NHR15, C(O)N(R15)2, C(O)NHOH, C(O)NHOR15, C(O)NHSO2R15, C(O)NR15SO2R15, SO2NH2, SO2NHR15, SO2N(R15)2, CO(O)H, C(O)H, OH, CN, N3, NO2, F, Cl, Br и I;
R8, в каждом случае, независимо выбран из группы, состоящей из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, арила, гетероциклила, циклоалкила и циклоалкенила; где R8 C1-6 алкил, C2-6 алкенил, C2-6 алкинил и C1-6 галогеналкил необязательно замещены одним, двумя, тремя, четырьмя, пятью или шестью заместителями, независимо выбранными из группы, состоящей из R16, OR16, SR16, S(O)R16, SO2R16, C(O)R16, CO(O)R16, OC(O)R16, OC(O)OR16, NH2, NHR16, N(R16)2, NHC(O)R16, NR16C(O)R16, NHS(O)2R16, NR16S(O)2R16, NHC(O)OR16, NR16C(O)OR16, NHC(O)NH2, NHC(O)NHR16, NHC(O)N(R16)2, NR16C(O)NHR16, NR16C(O)N(R16)2, C(O)NH2, C(O)NHR16, C(O)N(R16)2, C(O)NHOH, C(O)NHOR16, C(O)NHSO2R16, C(O)NR16SO2R16, SO2NH2, SO2NHR16, SO2N(R16)2, CO(O)H, C(O)H, OH, CN, N3, NO2, F, Cl, Br и I; где R8 арил, гетероциклил, циклоалкил и циклоалкенил необязательно замещены одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, NH2, C(O)NH2, SO2NH2, C(O)H, (O), OH, CN, NO2, OCF3, OCF2CF3, F, Cl, Br и I;
R9 выбран из группы, состоящей из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, циклоалкила, фенила и (CH2)1-4 фенила; и
R10 и R11, в каждом случае, независимо выбраны из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, C1-6 галогеналкила, фенила и (CH2)1-4-фенила; или
R10 и R11, или R10 и R9, вместе с атомом, к которому каждый присоединен, объединены с образованием гетероциклила;
Rk, в каждом случае, независимо выбран из группы, состоящей из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-7 гетероциклоалкила, C3-7 циклоалкила и C1-6 галогеналкила; где Rk C1-6 алкил, C2-6 алкенил и C2-6 алкинил необязательно замещены арилом, гетероциклилом, циклоалкилом или циклоалкенилом;
R12 и R13, в каждом случае, независимо выбраны из группы, состоящей из водорода, C1-4 алкила, C2-4 алкенила, C2-4 алкинила, C1-4 галогеналкила и (CH2)1-4 фенила;
R14, в каждом случае, независимо выбран из группы, состоящей из C1-4 алкила, C2-4 алкенила, C2-4 алкинила и C1-4 галогеналкила;
R12 и R13, или R12 и R14, в каждом случае, вместе с атомом вместе с атомом, к которому каждый присоединен, необязательно объединены с образованием гетероциклила;
R15, в каждом случае, независимо выбран из группы, состоящей из C1-4 алкила, C2-4 алкенила, C2-4 алкинила, C1-4 галогеналкила, C1-4 гидроксиалкила, арила, гетероциклила, циклоалкила и циклоалкенила; где R15 C1-4 алкил, C2-4 алкенил, C2-4 алкинил, C1-4 галогеналкил и C1-4 гидроксиалкил необязательно замещены одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из C1-4 алкила, C2-4 алкенила, C2-4 алкинила, C1-4 галогеналкила, C1-4 гидроксиалкила, C1-4 алкокси, арила, гетероциклоалкила, гетероциклоалкенила, гетероарила, циклоалкила и циклоалкенила, NH2, C(O)NH2, SO2NH2, C(O)H, C(O)OH, (O), OH, CN, NO2, OCF3, OCF2CF3, F, Cl, Br и I;
R16, в каждом случае, независимо выбран из группы, состоящей из C1-4 алкила, C2-4 алкенила, C2-4 алкинила, C1-4 галогеналкила, C1-4 гидроксиалкила, арила, гетероциклоалкила, гетероциклоалкенила, гетероарила, циклоалкила и циклоалкенила; где R16 C1-4 алкил, C2-4 алкенил, C2-4 алкинил, C1-4 галогеналкил и C1-4 гидроксиалкил необязательно замещены одним заместителем, независимо выбранным из группы, состоящей из OCH3, OCH2CH2OCH3 и OCH2CH2NHCH3;
q равно 1, 2 или 3;
s равно 0, 1, 2 или 3;
r равно 0, 1, 2 или 3;
где сумма s и r равна 0, 1 или 2;
m равно 0, 1, 2 или 3;
n равно 0, 1, 2, 3, 4, 5 или 6; и
p равно 0, 1 или 2.
В другом варианте осуществления формулы (I) Y1 представляет собой пирролил, пиразолил или триазолил.
В другом варианте осуществления формулы (I) Y1 представляет собой пиридинил или фенил.
В другом варианте осуществления формулы (I) Х представляет собой бензо[d]тиазолил; который необязательно замещен одним, двумя, тремя или четырьмя R4. В другом варианте осуществления формулы (I) Y1 представляет собой пирролил, пиразолил или триазолил, и Х представляет собой бензо[d]тиазолил; который необязательно замещен одним, двумя, тремя или четырьмя R4. В другом варианте осуществления формулы (I) Y1 представляет собой пиридинил или фенил, и Х представляет собой бензо[d]тиазолил; который необязательно замещен одним, двумя, тремя или четырьмя R4.
В другом варианте осуществления формулы (I), Y1 представляет собой пирролил, пиразолил или триазолил; и Z1 представляет собой , или .
В другом варианте осуществления формулы (I) Y1 представляет собой пиридинил или фенил; и Z1 представляет собой или .
В другом варианте осуществления формулы (I) Y1 представляет собой пирролил, пиразолил или триазолил; L1 представляет собой (CR6R7)q; и Y2 выбран из группы, состоящей из C3-7 циклоалкила, C4-7 циклоалкенила, фенила, C5-6 гетероарила и C3-7 гетероциклоалкила; где R6 и R7, в каждом случае, представляет собой R15 или водород; и q равно 1, 2 или 3. В другом варианте осуществления формулы (I) Y1 представляет собой пиридинил или фенил; L1 представляет собой (CR6R7)q; и Y2 выбран из группы, состоящей из C3-7 циклоалкила, C4-7 циклоалкенила, фенила, C5-6 гетероарила и C3-7 гетероциклоалкила; где R6 и R7, в каждом случае, представляет собой R15 или водород; и q равно 1, 2 или 3.
В другом варианте осуществления формулы (I) Y1 представляет собой пирролил, пиразолил или триазолил; L1 выбран из группы, состоящей из (CR6R7)s-C(O)NR6A-(CR6R7)r и (CR6R7)s-S(O)2NR6A -(CR6R7)r; s равно 0; r равно 0 или 1; R6A независимо выбран из группы, состоящей из водорода и C1-6 алкила; и R6 и R7, в каждом случае, представляют собой водород. В другом варианте осуществления формулы (I) Y1 представляет собой пиридинил или фенил; L1 выбран из группы, состоящей из (CR6R7)s-NR6AC(O)-(CR6R7)r, (CR6R7)s-C(O)NR6A-(CR6R7)r, (CR6R7)s-NR6A-(CR6R7)r, (CR6R7)s-S(O)2NR6A -(CR6R7)r и (CR6R7)s-NR6AS(O)2-(CR6R7)r; s равно 0; r равно 0 или 1; R6A независимо выбран из группы, состоящей из водорода и C1-6 алкила; и R6 и R7, в каждом случае, представляют собой водород.
Еще один вариант осуществления относится к соединению формулы (I), выбранному из группы, состоящей из
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(пиридин-4-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(пиридин-3-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(4-гидроксибензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(1-фенилэтил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{4-[2-(диметиламино)этокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
3-(1-бензил-1H-пиразол-4-ил)-6-{8-[(5,6-дифтор-1,3-бензотиазол-2-ил)карбамоил]-3,4-дигидроизохинолин-2(1H)-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(4-фторфенил)этил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-хлорбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
3-(1-бензил-1H-пиразол-4-ил)-6-{8-[(6-фтор-1,3-бензотиазол-2-ил)карбамоил]-3,4-дигидроизохинолин-2(1H)-ил}пиридин-2-карбоновой кислоты;
3-(1-бензил-1H-пиразол-4-ил)-6-{8-[(6-метокси-1,3-бензотиазол-2-ил)карбамоил]-3,4-дигидроизохинолин-2(1H)-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-3,5-диметил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-метилбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-метоксибензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(4-хлорбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(бензилокси)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-гидроксибензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{3-[2-(диметиламино)этокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-3-метил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-5-метил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
3-(1-бензил-1H-пиразол-4-ил)-6-{8-[(7-хлор-1,3-бензотиазол-2-ил)карбамоил]-3,4-дигидроизохинолин-2(1H)-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{[6-(пирролидин-1-ил)пиридин-2-ил]метил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-фенил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-цианобензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-хлорбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(пиридин-2-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-3-циано-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(нафтален-2-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(3-метил-1,2,4-оксадиазол-5-ил)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-бензил-3-(гидроксиметил)-5-метил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(бензилокси)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(5-метил-1-{[6-(пирролидин-1-ил)пиридин-2-ил]метил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-бензил-3-(этоксикарбонил)-5-метил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(диметиламино)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-3-карбокси-5-метил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-гидроксибензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2,3-дигидро-1H-инден-1-ил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-фенилэтил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3,4-дигидро-2H-хромен-4-ил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{2-[2-(диметиламино)этокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-фторбензил)-5-метил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(циклогексилметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(циклогексилметил)-5-метил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(4-{[3-(диметиламино)пропил]амино}-3-нитробензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(4-фтор-3-нитробензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{2-[2-(морфолин-4-ил)этокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{2-[3-(диметиламино)пропокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(пиридин-4-илметокси)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{2-[2-(диметиламино)этокси]бензил}-5-метил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(тетрагидро-2H-пиран-4-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{2-[3-(диметиламино)проп-1-ин-1-ил]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2,3-дифторбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3,5-дифторбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2,5-дифторбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2,6-дифторбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(тетрагидро-2H-пиран-3-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-нитробензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(бифенил-3-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2,2-диметилпропил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(2-циклогексилэтил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(трифторметил)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(бифенил-2-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(циклопентилметил)-5-метил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3-формилбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-бензил-5-фенил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[5-метил-1-(тетрагидро-2H-пиран-3-илметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[(1-фенилциклогексил)метил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{3-[(диметиламино)метил]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(метилсульфонил)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(циклогексилметил)-5-циклопропил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(3,5-ди-трет-бутилбензил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(морфолин-4-илсульфонил)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[(4,4-дифторциклогексил)метил]-5-метил-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{[1-(трифторметил)циклогексил]метил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(дифенилметил)-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(морфолин-4-ил)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[3-(морфолин-4-ил)-1-фенилпропил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{[1-(трет-бутоксикарбонил)пиперидин-4-ил]метил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(5-метил-1-{2-[2-(морфолин-4-ил)этокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{1-[2-(диметиламино)бензил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(5-метил-1-{2-[3-(морфолин-4-ил)пропокси]бензил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-{5-метил-1-[(1-метилциклогексил)метил]-1H-пиразол-4-ил}пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-[1-(циклогексилметил)-5-этил-1H-пиразол-4-ил]пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-дигидроизохинолин-2(1H)-ил]-3-(1-{[(1R,2R,5R)-6,6-диметилбицикло[3.1.1]гепт-2-ил]метил}-5-метил-1H-пиразол-4-ил)пиридин-2-карбоновой кислоты;
6-[8-(1,3-бензотиазол-2-илкарбамоил)-3,4-