Хроменоновые соединения в качестве ингибиторов рi3-киназы для лечения рака
Иллюстрации
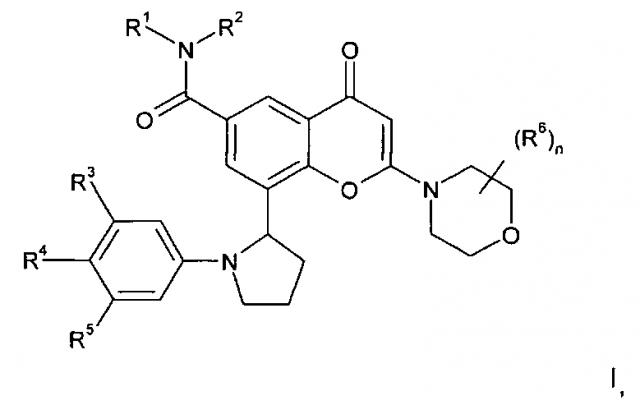
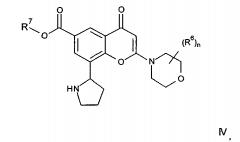
Показать всеИзобретение относится к хроменоновым соединениям формулы I, обладающим свойствами ингибитора ферментов PI3-киназ, или его фармацевтически приемлемым солям, фармацевтическим композициям на их основе и способу лечения или профилактики опухолей, чувствительных к ингибированию ферментов PI3-киназ, с их использованием. В общей формуле I R1 представляет собой С1-4алкил, возможно замещенный гидрокси; R2 представляет собой С1-4алкил; или R1 и R2 вместе образуют 4-6-членную азотсодержащую гетероциклильную кольцевую систему, которая возможно содержит 1 дополнительный гетероатом, выбранный из кислорода и серы, где кольцевой атом серы возможно окислен с образованием S-оксида(ов), где указанное кольцо возможно замещено гидрокси; R3 и R5 независимо выбраны из Н, галогена, C1-3алкокси и циано; R4 представляет собой Н или фтор; n равен 0 или 1. 4 н. и 11 з.п. ф-лы, 4 ил., 3 пр., 1 табл.
Реферат
Изобретение относится к некоторым новым хроменоновым соединениям или их фармацевтически приемлемым солям, которые обладают противоопухолевой активностью и соответственно полезны в способах лечения организма человека или животного. Изобретение также относится к способам получения указанных хроменоновых соединений, содержащим их фармацевтическим композициям и их применению в терапевтических способах, например в изготовлении лекарственных средств для использования в профилактике или лечении злокачественных новообразований у теплокровного животного, такого как человек, включая использование в профилактике или лечении рака.
Настоящее изобретение также относится к хроменоновым соединениям, которые являются избирательными ингибиторами фосфоинозитид-3-киназы (PI3-киназы) β и полезны, например, для противоопухолевой терапии. Кроме того, настоящее изобретение также относится к применению хроменоновых соединений по изобретению, которые являются избирательными ингибиторами фосфоинозитид-3-киназы (PI3-киназы) β, в противоопухолевой терапии. Ингибиторы PI3-киназы β могут быть эффективными в лечении опухолей, которые имеют дефект в гене PTEN (фосфатаза и гомолог тензина с делецией на 10-й хромосоме), что составляет дополнительный аспект изобретения.
Настоящее изобретение также относится к хроменоновым соединениям, которые являются избирательными ингибиторами фосфоинозитид-3-киназы (PI3-киназы) δ, и полезны, например, для противоопухолевой терапии; а также к хроменоновым соединениям, которые являются избирательными ингибиторами как в отношении PI3-киназы β, так и в отношении PI3-киназы δ. Такие двойные ингибиторы PI3-киназы β/δ также полезны в лечении опухолей.
В области рака в последние годы было обнаружено, что клетки могут становиться злокачественными в результате трансформации части ее ДНК в онкоген, то есть ген, приводящий при его активации к образованию злокачественных опухолевых клеток (Bradshaw, Mutagenesis, 1986, 1, 91). Некоторые такие онкогены вызывают продуцирование пептидов, которые являются рецепторами факторов роста. Активация комплекса рецепторов факторов роста впоследствии приводит к увеличению пролиферации клеток. Известно, например, что некоторые онкогены кодируют ферменты тирозинкиназы и что некоторые рецепторы факторов роста также являются ферментами тирозинкиназами (Yarden etal., Ann. Rev. Biochem., 1988, 57, 443; Larsen et al., Ann. Reports in Med. Chem., 1989, Chpt. 13). Первая группа тирозинкиназ, подлежащая идентификации, возникла от таких вирусных онкогенов, как, например, тирозинкиназа pp60v-Src (также известная как v-Src), и соответствующих тирозинкиназ в нормальных клетках, например, тирозинкиназа pp60c-Src (также известная как c-Src).
Рецепторные тирозинкиназы являются важными в передаче биохимических сигналов, которые инициируют клеточную репликацию. Они представляют собой крупные ферменты, которые охватывают клеточную мембрану и имеют домен внеклеточного связывания для факторов роста, таких как эпидермальный фактор роста (EGF), и внутриклеточную область, которая функционирует как киназа для фосфорилирования тирозиновых аминокислот в белках и поэтому влияет на клеточную пролиферацию. Известны различные классы рецепторных тирозинкиназ (Wilks, Advances in Cancer Research, 1993, 60, 43-73), основанные на семействах факторов роста, которые связываются с разными рецепторными тирозинкиназами. Классификация включает рецепторные тирозинкиназы класса I, содержащие EGF семейство рецепторных тирозинкиназ, таких как рецепторы EGF, TGFα (трансформирующий фактор роста альфа), Neu и erbB.
Известно также, что некоторые тирозинкиназы относятся к классу нерецепторных тирозинкиназ, которые локализованы внутри клетки и вовлечены в передачу биохимических сигналов, таких как сигналы, влияющие на подвижность опухолевой клетки, распространение и инвазивность и впоследствии метастатический рост опухоли. Известны разные классы нерецепторных тирозинкиназ, включая Src семейство, такие как тирозинкиназы Src, Lyn, Fyn и Yes.
Кроме того, известно также, что некоторые тирозинкиназы относятся к классу серин/треонинкиназ, которые локализованы внутри клетки и по ходу транскрипции активации тирозинкиназы и вовлечены в передачу биохимических сигналов, таких как сигналы, влияющие на рост опухолевой клетки. Такие сериновые/треониновые пути передачи сигнала включают каскад Raf-MEK-ERK и те, которые расположены по ходу транскрипции PI3-киназы, например PDK-1, АКТ и mTOR (Blume-Jensen и Hunter, Nature, 2001, 411, 355).
Также известно, что некоторые другие киназы относятся к классу липидкиназ, которые локализованы внутри клетки и также вовлечены в передачу биохимических сигналов, таких как сигналы, влияющие на рост и инвазивность опухолевой клетки. Известны разные классы липидкиназ, включая вышеупомянутое семейство PI3-киназ, которое альтернативно известно как семейство фосфатидилинозитол-3-киназ.
В настоящее время хорошо понятно, что нарушение регуляции онкогенов и генов-супрессоров опухолевого роста вносит вклад в образование злокачественных опухолей, например посредством увеличенной клеточной пролиферации или повышенного клеточного выживания. Также в настоящее время известно, что пути передачи сигналов, опосредованные семейством PI3-киназ, имеют центральную роль в ряде клеточных процессов, включая пролиферацию и выживание, и разрегулирование этих путей является причинным фактором широкого спектра злокачественных новообразований и других заболеваний человека (Katso ef al., Annual Rev. Cell Dev. Biol., 2001, 17: 615-617 и Foster et al., J. Cell Science. 2003, 116: 3037-3040).
PI3-киназное семейство липидкиназ представляет собой группу ферментов, которые фосфорилируют третье положение инозитолового кольца фосфатидилинозитола (PI). Известны три основных группы ферментов PI3-киназ, которые классифицируют согласно их физиологической субстратной специфичности (Vanhaesebroeck et al., Trends in Biol. Sci., 1997, 22, 267). Ферменты PI3-киназы класса III фосфорилируют только PI. В противоположность этому, ферменты PI3-киназы класса II фосфорилируют и PI, и PI-4-фосфат [сокращенный ниже как PI(4)P]. Ферменты PI3-киназы класса I фосфорилируют PI, PI(4)P и PI-4,5-бисфосфат [сокращенный ниже как PI(4,5)P2], хотя, как полагают, только PI(4,5)P2 является физиологическим клеточным субстратом. Фосфорилирование PI(4,5)P2 продуцирует липидный вторичный мессенджер PI-3,4,5-трифосфат [сокращенный ниже как PI(3,4,5)P3]. Более отдаленные родственные члены этого суперсемейства представляют собой киназы класса IV, такие как mTOR и DNA-зависимая киназа, которые фосфорилируют остатки серина/треонина в белковых субстратах. Наиболее изученные и понятные из этих липидкиназ представляют собой ферменты PI3-киназы класса I.
PI3-киназа класса I представляет собой гетеродимер, состоящий из каталитической субъединицы p110 и регуляторной субъединицы, и это семейство дополнительно разделено на ферменты класса Ia и класса Ib на основе регуляторных партнеров и механизма регуляции. Ферменты класса Ia включают PI3-киназу β и состоят из трех отдельных каталитических субъединиц (р110α, р110β и р110δ), которые димеризуются с пятью отдельными регуляторными субъединицами (р85α, р55α, р50α, р85β и р55γ), причем все каталитические субъединицы способны взаимодействовать со всеми регуляторными субъединицами с образованием широкого ряда гетеродимеров. Ферменты PI3-киназы класса Ia в общем активируются в ответ на стимуляцию рецепторных тирозинкиназ фактором роста посредством взаимодействия SH2 доменов регуляторной субъединицы со специфическими фосфо-тирозиновыми остатками активированного рецептора или адаптерных белков, таких как IRS-1. И р110α, и р110β конститутивно экспрессируются во всех типах клеток, в то время как экспрессия р110δ более ограничена популяциями лейкоцитов и, некоторыми эпителиальными клетками. В противоположность этому, единственный фермент класса Ib состоит из каталитической субъединицы р110γ, которая взаимодействует с регуляторной субъединицей р101. Кроме того, ферменты класса Ib активируются в ответ на системы рецептора, сопряженного с G-белком (GPCR), а также посредством описанных выше механизмов.
В настоящее время имеются существенные свидетельства в пользу того, что ферменты PI3-киназы класса Ia, которые включают PI3-киназу β, вносят вклад в онкогенез в широком разнообразии человеческих раковых опухолей, либо непосредственно, либо опосредованно (Vivanco и Sawyers, Nature Reviews Cancer, 2002, 2, 489-501), например, субъединица р110α распространена при некоторых опухолях, таких как опухоли яичника (Shayesteh et al., Nature Genetics. 1999, 21: 99-102) и шейки матки (Ma et al., Oncogene. 2000, 19: 2739-2744). Активирующие мутации в пределах каталитического сайта р110α ассоциированы с различными другими опухолями, такими как опухоли колоректальной области, а также груди и легкого (Samuels et al., Science, 2004, 304, 554). Связанные с опухолями мутации в р85α также были идентифицированы при злокачественных новообразованиях, таких как рак яичника и толстой кишки (Philp et al., Cancer Research. 2001, 61, 7426-7429). PI3-киназа 5 играет решающую роль в B-клеточной функции, и было показано, что она является медиатором передачи сигнала выживания при разнообразных B-клеточных злокачественных новообразованиях. Это включает в себя хронический лимфоцитарный лейкоз (CLL), острый лимфобластный лейкоз (ALL), фолликулярную лимфому, диффузную крупноклеточную B-клеточную лимфому (DLBCL) и лимфому из клеток мантийной зоны (Ikeda et al., Blood, 2010, 116, 1460-1468; Herman et al., Blood, 2010, 116, 2078-2088; Lannutti et al., Blood, 2011, 117. 591-594; Hoellenriegel et al., Blood, 2011, 118, 3603-3612), но не ограничено ими. В дополнение к прямым эффектам, полагают, что активация PI3-киназы класса Ia вносит вклад в канцерогенные события, которые возникают в путях передачи сигнала против хода транскрипции, например, посредством лиганд-зависимой или лиганд-независимой активации рецепторных тирозинкиназ, GPCR-систем или интегринов (Vara et al., Cancer Treatment Reviews, 2004, 30, 193-204). Примеры таких путей передачи сигнала против хода транскрипции включают сверхэкспрессию рецепторной тирозинкиназы Erb2 при разных видах опухолей, приводящую к активации путей, опосредованных PI3-киназой (Harari et al., Oncogene, 2000, 19, 6102-6114), и сверхэкспрессию онкогена Ras (Kauffmann-Zeh et al., Nature, 1997, 385, 544-548). Кроме того, PI3-киназы класса Ia могут вносить вклад непосредственно в онкогенез, вызванный различными событиями в передаче сигнала по ходу транскрипции. Например, потеря эффекта подавляющей опухоль фосфатазы PTEN, которая катализирует превращение PI(3,4,5)P3 обратно в PI(4,5)P2, ассоциирована с чрезвычайно широким рядом опухолей посредством разрегулирования продуцирования PI(3,4,5)P3, опосредованного PI3-киназой (Simpson и Parsons, Exp. Cell Res., 2001, 264, 29-41). Более того, добавление эффектов от других событий в путях передачи сигнала, опосредованных PI3-киназой, как полагают, вносит вклад в разнообразие злокачественных новообразований, например посредством активации Akt (Nicholson и Anderson, Cellular Signalling, 2002, 14, 381-395).
Помимо роли в опосредовании передачи сигнала пролиферации и выживания в опухолевых клетках, также имеются свидетельства в пользу того, что ферменты PI3-киназы класса Ia вносят вклад в онкогенез посредством ее функции в ассоциированных с опухолями стромальных клетках. Например, известно, что передача сигнала PI3-киназы играет важную роль в опосредовании ангиогенных событий в эндотелиальных клетках в ответ на проангиогенные факторы, такие как VEGF (Abid et al., Arterioscler. Thromb. Vase. Biol., 2004, 24, 294-300). Поскольку ферменты PI3-киназы класса I также вовлечены в подвижность и миграцию (Sawyer, Expert Opinion Investig. Drugs, 2004, 13, 1-19), ингибиторы PI3-киназы обеспечат терапевтический благоприятный эффект посредством ингибирования инвазии и метастазов опухолевой клетки.
Кроме того, ферменты PI3-киназы класса I играют важную роль в регуляции иммунных клеток, причем PI3-киназная активность вносит вклад в проонкогенные эффекты воспалительных клеток (Coussens и Werb, Nature, 2002, 420, 860-867).
Эти обнаружения подтверждают, что фармакологические ингибиторы ферментов PI3-киназ класса I будут терапевтически ценными для лечения разных форм раковых заболеваний, включая солидные опухоли, такие как карциномы и саркомы, а также лейкозы и лимфоидные злокачественные новообразования. В частности, ингибиторы ферментов PI3-киназ класса I будут терапевтически ценными для лечения, например, рака груди, толстой и прямой кишки, легкого (включая мелкоклеточный рак легкого, немелкоклеточный рак легкого и бронхоальвеолярный рак) и предстательной железы, а также рака желчных протоков, кости, мочевого пузыря, головного мозга, головы и шеи, почки, печени, желудочно-кишечной ткани, пищевода, яичника, поджелудочной железы, кожи, семенников, щитовидной железы, матки, шейки матки и вульвы, а также лейкозов (включая ALL, CLL и CML [хронический миелоидный лейкоз]), множественной миеломы и лимфом (включая неходжкинские лимфомы, такие как диффузная крупноклеточная B-клеточная лимфома [DLBCL], фолликулярная лимфома и лимфома из клеток мантийной зоны).
В общем, исследователи изучали физиологические и патологические роли семейства ферментов PI3-киназ, используя вышеупомянутые ингибиторы PI3-киназ LY294002 и вортманнин. Хотя применение этих соединений может подтвердить роль PI3-киназы в клеточном событии, они являются недостаточно избирательными в пределах семейства PI3-киназ для того, чтобы обеспечить разделение на индивидуальные роли членов семейства. По этой причине более эффективные и избирательные фармацевтические ингибиторы PI3-киназ будут полезны для обеспечения более полного понимания функции PI3-киназы и для предложения полезных терапевтических агентов.
В дополнение к онкогенезу, имеются свидетельства в пользу того, что ферменты PI3-киназы класса I играют роль в других заболеваниях (Wymann et al, Trends in Pharmacological Science, 2003, 24, 366-376). Как ферменты PI3-киназы класса Ia, так и индивидуальный фермент класса Ib играют важные роли в клетках иммунной системы (Koyasu, Nature Immunology, 2003, 4, 313-319), и поэтому они являются терапевтическими мишенями для воспалительных и аллергических показаний. Ингибирование PI3-киназы также полезно, как описано ранее, для лечения сердечно-сосудистого заболевания посредством противовоспалительных воздействий или непосредственно путем воздействия на сердечные миоциты (Prasad et al., Trends in Cardiovascular Medicine, 2003, 13, 206-212). Игибирование PI3-киназы также полезно для лечения тромбоза. В WO 2004016607 предложен способ нарушения агрегации тромбоцитов и адгезии, возникающей в условиях высокого сдвига, и способ подавления активации тромбоцитов, вызванной сдвигом, где оба способа включают введение избирательного ингибитора PI3-киназы β. В WO 2004016607 также предложен антитромботический способ, включающий введение эффективного количества избирательного ингибитора PI3-киназы β. Согласно этому способу, специфическое ингибирование тромбоза может быть достигнуто без влияния на нормальный гемостаз благодаря направленному воздействию на PI3-киназу β, которая является важной для активации тромбоцитов, индуцируемой сдвигом. Указанный антитромботический способ, таким образом, не включает побочные эффекты, вызванные нарушением нормального гемостаза, например увеличение времени кровотечения.
Таким образом, ингибиторы ферментов PI3-киназ класса I, включая ингибиторы PI3-киназы β, как ожидают, будут ценными в предупреждении и лечении широкого ряда заболеваний помимо рака.
В настоящее время неожиданно обнаружено, что соединения, а именно хроменоновые соединения, по изобретению обладают сильной противоопухолевой активностью, являясь полезными в ингибировании неконтролируемой клеточной пролиферации, которая обусловлена злокачественным заболеванием. Не подразумевая, что соединения, раскрытые в настоящем изобретении, обладают фармакологической активностью только благодаря влиянию на единый биологический процесс, полагают, что соединения обеспечивают противоопухолевый эффект путем ингибирования ферментов PI3-киназ класса I, в частности путем ингибирования ферментов PI3-киназ класса Ia и/или фермента PI3-киназы класса Ib, более конкретно путем ингибирования ферментов PI3-киназ класса Ia, которые включают ингибирование PI3-киназы β.
Соединения по настоящему изобретению также полезны в ингибировании неконтролируемой клеточной пролиферации, обусловленной незлокачественными заболеваниями, такими как воспалительные заболевания (например ревматоидный артрит и воспалительное заболевание кишечника), фиброзные заболевания (например цирроз печени и фиброз легких), гломерулонефрит, рассеянный склероз, псориаз, доброкачественная гипертрофия простаты (ВРН), реакции гиперчувствительности кожи, заболевания кровяных сосудов (например атеросклероз и рестеноз), аллергическая астма, инсулинзависимый диабет, диабетическая ретинопатия и диабетическая нейропатия.
В общем, соединения по настоящему изобретению обладают сильной ингибирующей активностью в отношении ферментов PI3-киназ класса I, в частности в отношении ферментов PI3-киназ класса Ia, в том числе в отношении PI3-киназы β, в то же время обладая менее сильной ингибирующей активностью в отношении ферментов тирозинкиназ, таких как рецепторные тирозинкиназы, например тирозинкиназа EGF рецептора и/или тирозинкиназа VEGF рецептора, или в отношении нерецепторных тирозинкиназ, таких как Src. Более того, некоторые соединения по настоящему изобретению обладают существенно лучшей эффективностью в отношении ферментов PI3-киназ класса I, в частности в отношении ферментов PI3-киназ класса Ia, в том числе в отношении PI3-киназы β, чем в отношении тирозинкиназы EGF рецептора или тирозинкиназы VEGF рецептора или нерецепторной тирозинкиназы Src. Такие соединения обладают достаточной эффективностью в отношении ферментов PI3-киназ класса I, которые могут быть использованы в количестве, достаточном для ингибирования ферментов PI3-киназ класса I, в частности для ингибирования ферментов PI3-киназ класса Ia, включая PI3-киназу β, в то же время демонстрируя малую активность в отношении тирозинкиназы EGF рецептора или тирозинкиназы VEGF рецептора, или нерецепторной тирозинкиназы Src.
В дополнение, конкретные соединения по изобретению демонстрируют сильную ингибирующую активность в отношении как PI3-киназы β, так и PI3-киназы δ, в то же время обладая менее сильной ингибирующей активностью в отношении ферментов тирозинкиназ, таких как рецепторные тирозинкиназы, например тирозинкиназа EGF рецептора и/или тирозинкиназа VEGF рецептора, или в отношении нерецепторных тирозинкиназ, таких как Src. Более того, некоторые соединения по настоящему изобретению обладают существенно лучшей эффективностью в отношении как PI3-киназы β, так и PI3-киназы δ, чем в отношении тирозинкиназы EGF рецептора или тирозинкиназы VEGF рецептора, или нерецепторной тирозинкиназы Src. Такие соединения обладают достаточной эффективностью в отношении и PI3-киназы β, и PI3-киназы δ, которые могут быть использованы в количестве, достаточном для ингибирования PI3-киназы β и PI3-киназы δ, в то же время демонстрируя незначительную активность в отношении тирозинкиназы EGF рецептора или тирозинкиназы VEGF рецептора, или нерецепторной тирозинкиназы Src.
Согласно одному аспекту изобретения предложено производное хроменона формулы I:
в которой:
R1 представляет собой С1-4алкил, возможно замещенный гидрокси;
R2 представляет собой Н или С1-4алкил; или
R1 и R2 вместе образуют 3-8-членную азотсодержащую гетероциклильную кольцевую систему, которая возможно содержит 1 или 2 дополнительных гетероатома, выбранных из кислорода, азота и серы, где кольцевой атом серы возможно окислен с образованием S-оксида(ов), где указанное кольцо возможно замещено гидрокси;
R3 и R5 независимо выбраны из H, галогена, C1-3алкокси и циано;
R4 представляет собой Н или фтор;
n равен 0 или 1, и когда n равен 1, группа R6 представляет собой метил; или его фармацевтически приемлемая соль.
В данном описании общий термин "C1-4алкил" включает как прямые, так и разветвленные алкильные группы, такие как пропил, изопропил и трет-бутил, а также C3-4циклоалкильные группы, такие как циклопропил и циклобутил, и также группы, такие как циклопропилметил. Однако, ссылки на индивидуальные алкильные группы, такие как "пропил", являются конкретным указанием только на вариант с прямой цепью, ссылки на индивидуальные разветвленные алкильные группы, такие как "изопропил", являются конкретным указанием только на вариант с разветвленной цепью, и ссылки на индивидуальные циклоалкильные группы, такие как "циклопропил", являются конкретным указанием только на 3-членное кольцо.
Специалисту в данной области техники понятно, что термины "C1-4алкил" и "C1-3алкил", как они использованы здесь, относятся к любой из алкильных групп, определенных выше, которые имеют от 1 до 4 и от 1 до 3 атомов углерода, соответственно. То же самое правило применимо в отношении других терминов, использованных здесь, таких как, например, "C1-3алкокси", "C1-10алкоксикарбонил" и "C1-10алканоил".
Следует понимать, что поскольку некоторые из соединений формулы I, определенной выше, могут существовать в оптически активных или рацемических формах благодаря одному или более асимметрическим атомам углерода, изобретение включает в его определении любую такую оптически активную или рацемическую форму, которая обладает ингибирующей активностью в отношении фосфоинозитид-3-киназы (PI3-киназы). Синтез оптически активных форм может быть осуществлен стандартными методиками органической химии, хорошо известными в данной области техники, например, синтезом из оптически активных исходных материалов или разделением рацемической формы. Подобным образом, вышеупомянутая активность может быть оценена с использованием стандартных лабораторных процедур.
Конкретный энантиомер описанных здесь соединений может быть более активным по сравнению с другими энантиомерами соединения. Например, (+)-энантиомер указанного в заголовке соединения Примера 1.03 (то есть, соединения Примера 1.03а, где (+) означает оптическое вращение, измеренное с использованием условий, описанных в Примере 1.03а) является энантиомером, активность которого слабее. Во избежание сомнений, рассматриваемый хиральный центр представляет собой атом углерода по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу.
Соответственно, в дополнительном аспекте изобретения предложено производное хроменона формулы I или его фармацевтически приемлемая соль, где хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (R)-стереохимической конфигурации. В дополнительном аспекте изобретения предложено производное хроменона формулы I или его фармацевтически приемлемая соль, где хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (S)-стереохимической конфигурации.
Согласно еще одному аспекту изобретения предложено производное хроменона формулы I или его фармацевтически приемлемая соль, которое представляет собой индивидуальный энантиомер, находящийся в энантиомерном избытке (%ee) не менее 95%, не менее 98% или не менее 99%. В одном воплощении этого аспекта изобретения хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (R)-стереохимической конфигурации. В еще одном воплощении этого аспекта изобретения хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (S)-стереохимической конфигурации.
Согласно еще одному аспекту изобретения предложена фармацевтическая композиция, содержащая производное хроменона формулы I, которое представляет собой индивидуальный энантиомер, находящийся в энантиомерном избытке (%ее) не менее 95%, не менее 98% или не менее 99%, или его фармацевтически приемлемую соль вместе с фармацевтически приемлемым разбавителем или носителем. Предпочтительно индивидуальный энантиомер присутствует в энантиомерном избытке (%ее) не менее 99%. В одном воплощении этого аспекта изобретения хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (R)-стереохимической конфигурации. В еще одном воплощении этого аспекта изобретения хиральный центр по положению 2 центрального пирролидинового кольца, которое присоединено к хроменоновому бициклическому кольцу, находится в (S)-стереохимической конфигурации.
Некоторые соединения формулы I могут проявлять полиморфизм. Следует понимать, что настоящее изобретение охватывает любую полиморфную форму или их смеси, которые обладают свойствами, полезными в ингибировании активности фосфоинозитид(PI)-3-киназы, причем в данной области хорошо известно как определить эффективность полиморфной формы в отношении ингибирования активности фосфоинозитид(PI)-3-киназы стандартными тестами, описанными ниже в данном описании.
В целом известно, что кристаллические вещества могут быть проанализированы с использованием традиционных методик, таких как анализ дифракции рентгеновских лучей на порошке (ниже XRPD), дифференциальная сканирующая калориметрия (ниже ДСК), термогравиметрический анализ (ниже ТГА), инфракрасная спектроскопия диффузного отражения с Фурье-преобразованием (DRIFT), коротковолновая инфракрасная спектроскопия (NIR), ядерная магнитно-резонансная спектроскопия жидкого и/или твердого состояния. Содержание воды таких кристаллических веществ может быть определено анализом по Карлу Фишеру.
В качестве примера, соединение Примера 1.03b проявляет полиморфизм, и были идентифицированы три кристаллические формы A, B и C. Конкретные кристаллические формы могут проявлять благоприятные свойства, такие как улучшенная стабильность, которая делает их особенно-подходящими для фармацевтических разработок.
Соответственно, в дополнительном аспекте изобретения предложена Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 4,8°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 8,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 4,8° и 8,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета примерно равных 4,8, 6,4, 8,1, 9,6, 15,8, 19,5, 20,3, 22,7, 23,4, 25,9°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке по существу такую же, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг.1.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 4,8° плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 8,1° плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 4,8° и 8,1°, где указанные значения могут отклоняться на плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета примерно равных 4,8, 6,4, 8,1, 9,6, 15,8, 19,5, 20,3, 22,7, 23,4, 25,9°, где указанные значения могут отклоняться на плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета равном 4,8°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета равном 8,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета равных 4,8° и 8,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета равных 4,8, 6,4, 8,1, 9,6, 15,8, 19,5, 20,3, 22,7, 23,4, 25,9°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма А 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке как показано на Фиг.1.
В дополнительном аспекте изобретения предложена Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма B 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 11,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 6,9° и 11,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета примерно равных 6,9, 9,4, 9,8, 11,1, 12,7, 13,1, 13,7, 17,8, 18,7, 19,7°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке по существу такую же, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг.2.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета примерно равном 11,1° плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 6,9 и 11,1°, где указанные значения могут отклоняться на плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета примерно равных 6,9, 9,4, 9,8, 11,1, 12,7, 13,1, 13,7, 17,8, 18,7, 19,7°, где указанные значения могут отклоняться на плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере одним характеристическим пиком при 2-тета равном 11,1°.
Согласно еще одному аспекту настоящего изобретения, предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета равных 6,9° и 11,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета равных 6,9, 9,4, 9,8, 11,1, 12,7, 13,1, 13,7, 17,8, 18,7, 19,7°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма В 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке как показано на Фиг.2.
В дополнительном аспекте изобретения предложена Форма С 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма С 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 5,9 и 12,2°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма С 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с характеристическими пиками при 2-тета примерно равных 5,9, 12,2, 11,8, 13,5, 15,2, 15,4, 17,1°.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма С 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке по существу такую же, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг.4.
Согласно еще одному аспекту настоящего изобретения предложена кристаллическая форма Форма С 8-[(2R)-1-(3,5-дифторфенил)пирролидин-2-ил]-6-(морфолин-4-карбонил)-2-морфолино-хромен-4-она, которая имеет картину дифракции рентгеновских лучей на порошке с по меньшей мере двумя характеристическими пиками при 2-тета примерно равных 5,9 и 12,2°, где указанные значения могут отклоняться на плюс или минус 0,5° 2-тета.
Согласно еще одному аспекту настоящего изобретения предложена к