Способ прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде
Иллюстрации
Показать всеИзобретение относится к области медицинской диагностики и касается прогнозирования интенсивности болевого синдрома в раннем послеоперационном периоде у больных хроническим калькулезным холециститом, русской национальности, являющихся уроженцами Центрального Черноземья России. Способ включает забор крови и выделение ДНК из периферической венозной крови. После выделения ДНК проводят анализ полиморфизмов генов IL-1А -889Т>С, IL-5 -703С>Т и прогнозируют более выраженную боль у больных хроническим калькулезным холециститом в 18 часов и в 22 часа первых суток после холецистэктомии в случае выявления генотипов -889ТТ и -889СТ IL-1A. Прогнозируют интенсивные болевые ощущения в 8 часов вторых суток после операции при выявлении генотипов -703СТ и -703ТТ IL-5. 5 ил.
Реферат
Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде.
Желчнокаменная болезнь (далее ЖКБ) - многофакторное и многостадийное заболевание, характеризующееся нарушением обмена холестерина или билирубина с образованием конкрементов в желчном пузыре или желчных протоках. Заболеваемость ЖКБ в последние десятилетия резко повысилась и продолжает возрастать. ЖКБ занимает 3-е место после сердечно-сосудистых заболеваний и сахарного диабета [Ильченко, А. А. Желчнокаменная болезнь /А. А. Ильченко. - Москва: Анахарсис, 2004. - 200 с.]. Почти 90% всех случаев желчнокаменной болезни составляет хронический калькулезный холецистит (далее ХКХ). У современных жителей Земли желчные камни обнаруживают у 24% женщин и 12% мужчин. По количеству оперативных вмешательств, холецистэктомия занимает второе место после аппендэктомии [Яфаров, А. Р. Применение лазерного излучения на этапах лапароскопической холецистэктомии: дис.… канд. мед. наук: 14.01.17 /А. Р. Яфаров. - Москва, 2010. - 116 с.].
Среди факторов, приводящих к развитию хронического калькулезного холецистита, значимую роль играют генетические факторы. Показана роль отдельных генетических полиморфизмов, участвующих в регуляции воспаления, клеточной пролиферации, метаболизма липидов и желчных кислот в формировании ХКХ [Григорьева, И. Основные факторы риска желчнокаменной болезни /И. Григорьева //Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2007. - Т. 17, №6. - С. 17-21; Lammert, F. Mechanisms of disease: the genetic epidemiology of gallbladder stones /F. Lammert, T. Sauerbruch //Nat. Сlin. Pract. Gastroenterol. Hepatol. - 2005. - Vol. 2, №9. - P. 423-433]. Среди генов-кандитатов, регулирующих преимущественно процессы воспаления, важное значение имеют интерлейкины. Интерлейкины, взаимодействуя со специфическими рецепторами, являются одними из главных звеньев в воспалительном каскаде при ЖКБ, изменяя интенсивность и длительность воспалительных, склеротических и литогенных процессов в желчном пузыре [Царегородцева, Т. М. Цитокины при заболеваниях органов пищеварения [Электронный ресурс] /Т. М. Царегородцева //Регистр лекарственных средств России: энцикл. лекарств и товаров аптечного ассортимента: офиц. сайт /группа компаний РЛС. - Москва, 2009. - 28 апр. - Режим доступа: http://www.rlsnet.ru/articles_426.htm.].
Провоспалительные интерлейкины, взаимодействуя со своими рецепторами, стимулируют возбуждение в сенсорных нейронах, формируют болевую чувствительность при хирургической агрессии [Dray, А. Inflammatory mediators of pаin /А. Dray //Br. J. Anaesth. - 1995. - Vol. 75, №2. - P. 125-131].
Развитию болевого синдрома сопутствует гиперактивация симпатической нервной системы, что приводит к тахикардии, гипертензии, повышению общего периферического сопротивления сосудов. Подобная клиническая картина резко увеличивает вероятность потребности миокарда в кислороде и развития острого инфаркта миокарда у пациентов группы риска. Для профилактики кардиальных осложнений необходимо своевременное лечение выраженной боли и торможение симпатической активности в пред- и послеоперационном периоде [Корячкин, В. А. Анестезия и интенсивная терапия: справ. /В. А. Корячкин, В. И. Страшнов. - Санкт-Петербург: С.-Петерб. мед. изд-во, 2004. - 465 с. - (Б-ка врача анестезиолога)].
IL-1А - белок, кодируемый геном IL-1А, который располагается на второй хромосоме (2q14). IL-1А - провоспалительный цитокин, обладающий широким спектром метаболической, физиологической, кроветворной деятельности, а также играет одну из центральных ролей в регуляции иммунного ответа. После попадания инфекции в организм, IL-1А активизирует множество процессов системы иммунного ответа. В частности: стимулирует распространение фибробластов, индуцирует синтез протеаз и белков острой фазы, влияет на увеличение числа нейтрофилов крови, активизирует распространение лимфоцитов и вызывает лихорадку [Dinarello, С. А. Induction of interleukin-1 and interleukin-1 receptor antagonist /С. А. Dinarello //Semin. Оnсоl. - 1997. - №24, №3, suppl. 9. - P. S981-S993].
Ген IL-1А содержит 7 экзонов и 6 интронов, на 3 и 5 концах он имеет нетранслируемые области. Кроме того, он обладает высокой степенью гомологии интронных последовательностей, что, возможно, регулирует экспрессию этого гена [Громова, А. Ю. Полиморфизм генов семейства IL-1 человека /А. Ю. Громова, А. С. Симбирцев //Цитокины и воспаление. - 2005. - Т. 4, №2. - С. 3-12].
IL-5 - димерный белок, массой 50-60 kDa. Ген IL-5 располагается на пятой хромосоме 5q23 -q31. Продуцируется IL-5 Т-клетками (Th 2). В пептидной части одной цепи IL-5 содержатся 115 аминокислотных остатков. Сходной функциональной активностью обладают его мономерная и димерная формы. IL-5 инициирует продукцию иммуноглобулинов и стимулирует синтез IgA [Murphy, J. M. IL-3, IL-5, and GM-CSF signaling: crystal structure of the human beta-common receptor /J. M. Murphy, I. G. Уоung //Vitam. Horm. - 2006. - Vol. 74. - P. 1-30].
Помимо клеток иммунной системы, данный цитокин оказывает влияние и на миелоидные клетки. IL-5 оказывает избирательное действие на костномозговых предшественников эозинофилов, регулируя их пролиферацию и дифференцировку. Наряду с этим, IL-5 увеличивает продукцию супероксидантов и усиливает хемотаксис данных типов клеток [База знаний по биологии человека /разраб. А. А. Александров. - Москва, 1990-2011. - Режим доступа: http://humbio.ru].
Для оценки сложившейся патентной ситуации был выполнен поиск по охранным документам за период с 1990 по 2014 гг. Анализ документов производился по направлению: способ прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде на основе молекулярно-генетических данных в зависимости от полиморфных маркеров генов интерлейкинов.
Источники информации: сайты Федерального института промышленной собственности http://fips.ru.
Известен способ по патенту РФ №2067768 «Способ прогнозирования течения послеоперационного периода у хирургических больных», в котором для повышения точности прогнозирования течения послеоперационного периода в ранние сроки у хирургических больных до операции и в первые 4-5 суток после нее в крови исследуют содержание миоглобина и по результатам 2-3 исследований прогнозируют развитие послеоперационного осложнения. Недостатком данного способа является необходимость неоднократных заборов крови и то, что способ решает задачу прогноза послеоперационных осложнений, а не прогнозирования послеоперационного болевого синдрома после видеолапароскопической холецистэктомии до проведения операции.
За прототип был выбран патент RU №2461830 «Способ прогнозирования интенсивности и резистентности болевого синдрома после операции видеолапароскопической холецистэктомии у больных хроническим калькулезным холециститом». Сущность способа заключается в том, что выделяют ДНК из периферической венозной крови, проводят анализ полиморфизма -308 G/A гена фактора некроза опухоли α. При выявлении генотипов -308 АА и -308 AG TNFα прогнозируют наибольшую выраженность и стойкость болевого синдрома и рекомендуют проведение мультимодальной послеоперационной анальгезии. При выявлении генотипа -308 GG TNFα прогнозируют более слабый болевой синдром и рекомендуют мономодальную послеоперационную анальгезию. Недостаток данного способа заключается в ассоциации с интенсивным болевым синдромом только одного генетического полиморфизма -308 G/A гена фактора некроза опухоли α.
Задачей настоящего изобретения является создание способа прогнозирования интенсивности болевого синдрома в раннем послеоперационном периоде у больных ХКХ.
Технический результат использования изобретения - получение критериев оценки интенсивности болевого синдрома в раннем послеоперационном периоде у больных ХКХ русской национальности, являющихся уроженцами Центрального Черноземья России в зависимости от наличия генетических вариантов полиморфных маркеров IL-1А -889Т>С, IL-5 -703С>Т, что будет способствовать своевременной профилактике выраженного болевого синдрома у пациентов с ХКХ после видеолапароскопической холецистэктомии.
В соответствии с поставленной задачей был разработан способ прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде, включающий:
- выделение ДНК из периферической венозной крови методом фенольно-хлороформной эстракции;
- генотипирование образцов ДНК с использованием стандартных олигонуклеотидных праймеров;
- прогнозирование более выраженной боли в 18 часов и в 22 часа первых суток после холецистэктомии в случае выявления генотипов -889ТТ и -889СТ IL-1A у больных ХКХ, прогнозирование интенсивных болевых ощущений в 8 часов вторых суток после операции при выявлении генотипов -703СТ и -703ТТ IL-5 у больных ХКХ.
Новизна и изобретательский уровень заключается в том, что из уровня техники не известна возможность прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде по наличию генетических вариантов полиморфных маркеров IL-1А -889Т>С, IL-5 -703С>Т.
Изобретение охарактеризовано на следующих фигурах
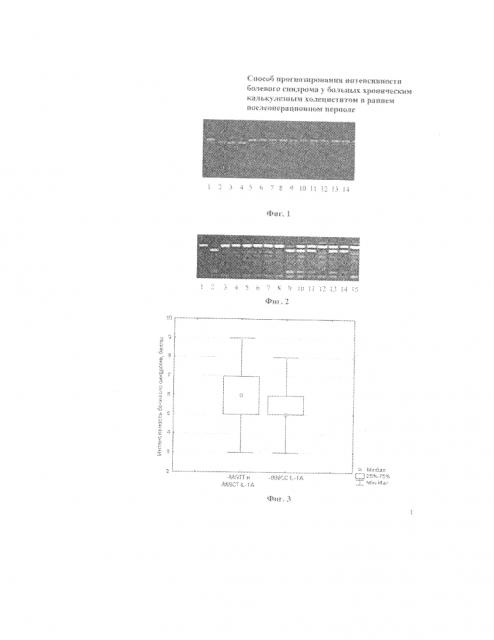
На фиг. 1 представлена дискриминация аллелей по локусу IL-1А -889 Т>С (rs 1800587), где 2,3,4 - -889ТТ IL-1А; 5,6,10 - -889СС IL-1А; 1, 7-9, 11-14 - -889СТ IL-1А.
На фиг. 2 представлена дискриминация аллелей по локусу IL-5 -703С>Т (rs12704795), где 1, 3-8, 12, 15 - гомозиготы -703СС; 10, 11, 13, 14 - гетерозиготы -703СТ; 2, 9 - гомозиготы -703ТТ.
На фиг. 3 представлены ассоциации генетических вариантов локуса IL-1А -889Т>С с интенсивностью послеоперационного болевого синдрома у больных ХКХ, время измерения 18 ч.
На фиг. 4 представлена связь генетических вариантов локуса IL-1А -889Т>С с уровнем болевых ощущений после холецистэктомии у больных ХКХ,
время измерения 22 ч.
На фиг. 5 представлен уровень болевых ощущений после холецистэктомии у больных ХКХ в зависимости от генетических вариантов локуса IL-5 -703С>Т, время измерения вторые сутки 8 ч.
Способ осуществляют следующим образом:
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции в два этапа. На первом этапе к 4 мл крови добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4ºС, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10 мг/мл) и инкубируют образец при 37ºС в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. Сформированную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -200С. Выделенную ДНК используют для проведения полимеразной цепной реакции синтеза ДНК.
Анализ всех генетических полиморфизмов интерлейкинов проводят методом полимеразной цепной реакции (ПЦР) синтеза ДНК. Для ПЦР используют: ДНК-полимераза Thermus aquaticus производства фирмы «Силекс-М», олигонуклеотидные праймеры и зонды, синтезированные фирмой «Синтол». Полимеразную цепную реакцию выполняют на амплификаторах «Терцик-МС4» (ДНК-технология) и IQ5 (Bio-Rad).
Генотипирование ДНК-маркеров производят методом полиморфизма длин рестрикционных фрагментов с помощью соответствующих эндонуклеаз. Реакция протекала в присутствии буферов и при температурных условиях, рекомендованных производителями эндонуклеаз - ООО «Сибэнзим» (Новосибирск). Продукты рестрикции фракционируют с помощью электрофореза в агарозных гелях различной концентрации и окрашивают в этидиум бромиде (фиг. 1, 2).
Возможность использования предложенного способа для прогнозирования интенсивности болевого синдрома у больных хроническим калькулезным холециститом в раннем послеоперационном периоде подтверждает анализ результатов наблюдений 249 больных хроническим калькулезным холециститом и 294 человек популяционного контроля. Общий объем исследуемой выборки составил 543 человека. Среди больных ХКХ 16,80% составили мужчины (41 человек), 83,20% - женщины (208 человек). В контрольной выборке (n=294) процентное соотношение было аналогичным: мужчины - 17,00% (50 человек), женщины - 83,00% (244 человек) (p>0,05).
В выборки больных и контроля включали индивидуумы русской национальности Центрального Черноземья России, не связанные между собой родственными связями. Пациентов относили к соответствующей группе больных ХКХ после подтверждения установленного диагноза с помощью клинических и лабораторно-инструментальных методов обследования, в соответствии с обязательными диагностическими стандартами. Контрольная группа была сформирована при экспедиционном обследовании населения областей Центрально - Черноземного региона России: Красненского и Прохоровского районов Белгородской области, Репьевского района Воронежской области и Черемисиновского района Курской области.
Типирование молекулярно-генетических маркеров осуществляли в лаборатории «Молекулярной генетики человека» медицинского института Белгородского государственного национального исследовательского университета.
Формирование базы данных и статистические расчеты осуществляли с использованием программы «STATISTICA 6.0».
Характер болевого синдрома определяли при помощи визуально-аналоговых и цифровых шкал боли [Корячкин, В. А. Анестезия и интенсивная терапия: справ. /В. А. Корячкин, В. И. Страшнов. - Санкт-Петербург: С.-Пб. мед. изд-во, 2004. - 465 с. - (Б-ка врача анестезиолога)]. Для оценки интенсивности болевых ощущений пациентов использовали десятибалльную шкалу (от 0 - слабая боль, до 10 - невыносимая боль). Мониторинг проводили каждые 4 часа в первые и вторые сутки после операции.
Изучение анализируемых количественных признаков показало, что их распределение в исследуемой группе больных не соответствует закону нормального распределения: значения критерия Шапиро-Уилка составили W=0,83-0,94; c уровнем их статистической значимости p<0,001. Таким образом, для описания рассматриваемых количественных показателей нами применялась медиана (Ме) и интерквартильный размах (Q25-Q75), а при сравнении пациентов с разными генотипами по анализируемым показателям использовался непараметрический метод - критерий Манна-Уитни [Реброва, О. Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA /О. Ю. Реброва. - [3-е изд.]. - Москва: Медиа Сфера, 2006. - 305 с.].
Установлено, что у индивидуумов с генотипами -889ТТ и -889СТ IL-1А боль была более выражена в 18 часов первых суток (Ме=6 баллов), чем у пациентов с генотипом -889СС (Ме=5 баллов). В 22 часа первых суток боль была более выражена у пациентов с генотипами -889ТТ и -889СТ IL-1А (Ме=5 баллов), чем у пациентов с генотипом -889СС (Ме=4 балла) (фиг. 3 и 4). Пациенты с ХКХ, имеющие генотипы -703СТ и -703ТТ локуса IL-5 -703С>Т, испытывали более резкую боль в 8 часов вторых суток (Ме=4 балла) по сравнению с индивидуумами с генотипом -703СС (Ме=3 балла,) (фиг. 5).
Таким образом, полученные данные указывают на важную роль полиморфных маркеров IL-1А -889Т>С и IL-5 -703С>Т в формировании послеоперационного болевого синдрома у пациентов с ХКХ.
Примеры, подтверждающие осуществимость предложенного изобретения.
1. Генотипы -889ТТ и -889СТ IL-1А были выявлены у пациента Т. При дальнейшем наблюдении у данного пациента в 18 часов первых суток после холецистэктомии отмечался уровень боли, равный 6 баллам.
2. Генотипы -889ТТ и -889СТ IL-1А были выявлены у пациентки Н. При дальнейшем наблюдении у данной пациентки в 22 часа первых суток после холецистэктомии отмечался уровень боли, равный 5 баллам.
3. У пациента С. были выявлены генотипы -703СТ и -703ТТ локуса IL-5 -703С>Т. При дальнейшем наблюдении удалось установить, что данный пациент испытывал резкую боль в 8 часов вторых суток, равную 4 баллам.
4. У пациента С. был выявлен генотип -703СС локуса IL-5 -703С>Т. При дальнейшем наблюдении удалось установить, что данный пациент испытывал в 8 часов вторых суток боль, уровень которой был равен 3 баллам.
Использование данного способа позволяет прогнозировать интенсивность болевого синдрома в раннем послеоперационном периоде у больных хроническим калькулезным холециститом, русской национальности, являющихся уроженцами Центрального Черноземья России, что будет способствовать своевременной профилактике выраженного болевого синдрома у пациентов с ХКХ после видеолапароскопической холецистэктомии, что крайне важно для пациентов, имеющих в анамнезе сердечно-сосудистую патологию.
Способ прогнозирования интенсивности болевого синдрома в раннем послеоперационном периоде у больных хроническим калькулезным холециститом, русской национальности, являющихся уроженцами Центрального Черноземья России, включающий забор крови и выделение ДНК из периферической венозной крови, отличающийся тем, что после выделения ДНК, проводят анализ полиморфизмов генов IL-1А -889Т>С, IL-5 -703С>Т и прогнозируют более выраженную боль у больных хроническим калькулезным холециститом в 18 часов и в 22 часа первых суток после холецистэктомии в случае выявления генотипов -889ТТ и -889СТ IL-1A, прогнозируют интенсивные болевые ощущения в 8 часов вторых суток после операции при выявлении генотипов -703СТ и -703ТТ IL-5.