Новая полиморфная форма кальцимиметического соединения
Иллюстрации
Показать всеИзобретение относится к кристаллической форме X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, которая может найти применение для лечения, ослабления или профилактики физиологических расстройств или заболеваний, связанных с нарушениями активности CaSR, таких как гиперпаратиреоз. Данная форма имеет рентгеновскую порошковую дифрактограмму, которая демонстрирует характеристические пики, выраженные при 2θ, равном приблизительно , , 11,4, 15,0, 18,2 и/или 21,5 градусов (±0,05 градусов) (подчеркнутый является первичным). Изобретение относится также к фармацевтической композиции, содержащей кристаллическую форму X, и способам ее получения. 5 н. и 14 з.п. ф-лы, 10 ил., 6 табл., 5 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новой полиморфной форме {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, способам ее получения и ее применению.
Предпосылки создания изобретения
Настоящее изобретение относится к новой полиморфной форме {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, ранее описанной в WO 2009/065406. Указанное соединение можно применять для лечения ряда расстройств или заболеваний, связанных с нарушениями активности кальций-чувствительного рецептора (CaSR).
Кальцимиметики представляют собой небольшие молекулы, являющиеся аллостерическими активаторами (CaSR) [Urena, P.; Frazao, J. M. Calcimimetic agents: Review and perspectives. Kidney International (2003), 63, pp.s91-s96; Soudijn, W. et al. Allosteric modulation of G protein-coupled receptors: perspectives and recent developments. DDT (2004), 9, 752-758].
Кальцимиметики, как уже было показано, можно коммерчески применять для лечения гиперпаратиреоза (HPT): недавно было начато применение цинакалцета (Cinacalcet®), представляющего собой кальцимиметическое соединение, для лечения вторичного НРТ у пациентов с хронической болезнью почек, находящихся на диализе, и для лечения первичного НРТ у пациентов с карциномой околощитовидной железы [Balfour, J. A. B. et al. Drugs (2005) 65(2), 271-281; Linberg et. al. J. Am. Soc. Nephrol (2005), 16, 800-807, Clinical Therapeutics (2005), 27 (11), 1725-1751]. Таким образом, доказана справедливость концепции о роли активаторов кальций-чувствительных рецепторов (CaSR) у человека и уже хорошо установлено их клиническое значение. Другие кальцимиметические соединения были описаны, например, в WO 94/018959, WO 98/001417, WO 05/065050, WO 03/099814, WO 03/099776, WO 00/21910, WO 01/34562, WO 01/090069, WO 97/41090, US 6001884, WO 96/12697, EP 1203761, WO 95/11221, WO 93/04373, EP 1281702, WO 02/12181, WO 04/069793, US 2004242602, WO 04/106296 и WO 05/115975.
{4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусная кислота представляет собой часть нового перспективного класса (WO 2009/065406) соединений, демонстрирующих кальцимиметическую активность. Одним из важных аспектов фармацевтического производства является вопрос о физической форме активного фармацевтического ингредиента (API). Физическая форма (например, кристаллическая форма) лекарственного вещества или API, применяемого в фармацевтическом препарате или в лекарственном средстве, является важной, поскольку разные физические формы часто демонстрируют разные основные свойства - такие как растворимость, скорость растворения, гигроскопичность, биодоступность, технологичность и стабильность. Существование разнообразных твердых форм (таких как, полиморфизм или псевдополиморфизм) может тем самым влиять на свойства лекарственного продукта.
Поэтому одни конкретные кристаллические формы, включая сольваты и гидраты, могут быть более предпочтительными, чем другие. Кроме того, определенные формы могут быть более предпочтительными в зависимости от конкретного состава препарата и/или способа применения. Например, свойства лекарственного средства, такие как скорость растворения активного ингредиента, можно регулировать, соответствующим образом выбирая конкретную кристаллическую форму или смесь кристаллических форм, комбинируемых в специфических соотношениях.
В готовом лекарственном препарате или при его химическом производстве кристаллическая форма API, благодаря ее предсказуемым свойствам, обычно является более предпочтительной, чем некристаллическая (например, аморфная). Наряду с прочими качествами, кристаллические формы имеют преимущество, заключающееся в большей химической стабильности (при воздействии повышенного давления, тепла и света), более легкой обрабатываемости и технологичности. В частности, предоставление кристаллической формы является важным преимуществом при химическом синтезе лекарственного средства, особенно в промышленном масштабе, поскольку кристаллы, как правило, легче выделяются из реакционной смеси.
Кроме того, известно, что результатом кристаллизации конкретной кристаллической формы некоторого соединения в конкретном растворителе может быть эффективная очистка указанного соединения, недостижимая при кристаллизации другой формы в другом растворителе (частично вследствие разной растворимости загрязняющих примесей в разных растворителях). В отличие от этого, аморфные соединения невозможно очищать посредством кристаллизации, и часто для их очистки требуется применение способов, связанных с большими затратами, таких как, например, препаративная хроматография. Разные кристаллические формы имеют также разные точки плавления, плотность, твердость, способность к измельчению и т.п., и поэтому, в зависимости от конкретного применения, одна конкретная полиморфная форма оказывается более предпочтительной, чем другая. Разные кристаллические формы имеют разную стабильность в готовых фармацевтических формах, что зависит от природы эксципиентов, носителей и других добавочных компонентов, присутствующих в дозированной форме. В частности, нестабильность аморфных соединений или полиморфных форм, не являющихся наиболее стабильными, представляет собой проблему, свойственную суспензиям лекарственных веществ.
Соответственно, хотя кристаллические формы лекарственного вещества, как правило, являются более предпочтительными, чем его некристаллические формы, конкретная кристаллическая форма соединения будет более предпочтительной в зависимости от многих обстоятельств, таких как область ее применения или процесс, в котором ее применяют.
Иногда термодинамически более стабильная форма является более предпочтительной, чем метастабильная форма, а иногда предпочитают метастабильную форму, которая может быть более быстрорастворимой.
WO 2009/065406 описывает синтез {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, но не раскрывает сведений о кристаллических формах этого соединения или о получении таких форм. Указанная заявка умалчивает и о полиморфизме {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, и о способе получения ее стабильной полиморфной формы.
WO 2010/021351 описывает синтез производных {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, но не раскрывает информации о кристаллических формах указанных производных.
Сущность изобретения
Настоящее изобретение неожиданно предоставляет стабильный полиморф {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
В первом аспекте настоящее изобретение, таким образом, относится к {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоте в кристаллической форме.
В предпочтительном аспекте настоящее изобретение относится к {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоте как к кристаллическому полиморфу, демонстрирующему один или более из отличительных признаков или характеристических линий, форм или образов, представленных на графиках 2b, 4b, 6b, 8b, в формуле 2 и/или в таблицах 1-6; или имеющему одно или более из значений, перечисленных в них, например, волновые числа, выраженные в см-1 (±3 или ±4 см-1 в зависимости от использованного способа), или углы рефлексов в градусах 2θ (±0,1); или представленному спектром или дифрактограммой, по существу подобных тем, что показаны на указанных графиках или в указанных таблицах; далее в настоящем документе указанный кристаллический полиморф {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты упоминается под названием «форма Х» или «полиморф Х».
Форму Х можно отличить от других полиморфных форм несколькими аналитическими способами, такими как рентгеновская порошковая дифрактометрия (XRPD). График 1 показывает наложение XRPD-дифрактограмм двух полиморфных форм С и Х, которое ясно указывает области сходства и различия.
В варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, таким образом, характеризуется тем, что она имеет XRPD-дифрактограмму по существу такую же, как дифрактограмма, показанная на графике 2b, которая представляет собой XRPD-дифрактограмму, записанную с чистой полиморфной формой Х.
В другом варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризована XRPD-дифрактограммой, демонстрирующей один или более пиков отражения, находящихся приблизительно при 2θ=8,0, 11,3, 11,4, 15,0, 18,2 и/или 21,5° (±0,05°) (подчеркнутый является первичным), соответственно.
Форму X можно также отличить от других полиморфных форм посредством дифференциальной сканирующей калориметрии (DSC). График 3 показывает наложение термограмм форм С и Х, при котором видны эндотермические эффекты, характерные для двух полиморфных форм и начинающиеся примерно при 240°C и примерно при 255°C (±2°C).
В варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, таким образом, охарактеризована тем, что она имеет кривую дифференциальной сканирующей калориметрии (DSC), по существу такую же, как кривая, показанная на графике 4b, содержащая эндотермический эффект, начинающийся примерно при 255°C (±2°C). Кроме того, на графике 4b имеется запись TGA (термогравиметрического анализа), которая указывает, что при температурах ниже 255°C (±2°C) {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусная кислота является устойчивой к разрушению.
Форму X можно также отличить от других полиморфных форм посредством инфракрасной спектроскопии нарушенного полного внутреннего отражения с Фурье-преобразованием (ATR-FTIR). График 5 показывает наложение спектров ATR-FTIR двух полиморфных форм С и Х, которое ясно указывает области сходства и различия.
В одном варианте осуществления настоящего изобретения форма X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризована тем, что она имеет спектр ATR-FTIR, по существу такой же, как спектр, показанный на графике 6b, который представляет собой спектр ATR-FTIR, записанный с чистой полиморфной формой Х.
В другом варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризована спектром ATR-FTIR, демонстрирующим один или более пиков нарушенного полного внутреннего отражения приблизительно при 1409, 1113, 1061, 939, 841 и/или 701 см-1 (±3 см-1) (подчеркнутый является первичным), соответственно.
Форму X можно также отличить от других полиморфных форм посредством твердотельной спектроскопии ядерного магнитного резонанса (SS-NMR). График 7 показывает наложение спектров 13C-SS-NMR двух полиморфных форм С и Х, которое ясно указывает области сходства и различия.
Поэтому в одном варианте осуществления настоящего изобретения форма X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризована тем, что она имеет спектр 13C-SS-NMR, по существу такой же, как спектр, показанный на графике 8b, который представляет собой спектр 13C-SS-NMR, записанный с чистой полиморфной формой Х.
В другом варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризована спектром 13C-SS-NMR, демонстрирующим один или более резонансных пиков при следующих значениях δ 13C: 172,7, 155,8, 140,5, 68,5, 52,6, 34,0, 29,6 м.д. (±1 м.д.) (подчеркнутый является первичным), соответственно.
В другом варианте осуществления настоящего изобретения форма С и форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты охарактеризованы тем, что они имеют параметры монокристаллов, по существу такие же, как параметры, приведенные в таблице 1.
| Таблица 1Параметры монокристаллов формы С и формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты | ||
| Форма X | Форма C | |
| Кристаллографическая система: | Орторомбическая | Тетрагональная |
| Описание кристалла | Куб | Пирамида |
| Пространственная группа: | P212121 | P41212 |
| Размеры элементарной ячейки (Å) | a=8,7299(17)b=14,822(3)c=16,353(3) | a=10,2289(16)b=10,2289(16)c=41,492(13) |
| Объем (Å3): | 2116,0(7) | 4341,3(16) |
| Число молекул в элементарной ячейке (Z) | 4 | 8 |
Во всем тексте настоящей заявки параметры кристаллов, такие как размеры элементарной ячейки, атомные координаты и тому подобные, даны в стандартной кристаллографической системе обозначений, так что стандартная неопределенность конкретного значения указана в скобках. Например, значение по оси «а» в таблице 1, представленное в виде выражения «a=8,7299(17)», означает, что имеется 95%-ная вероятность того, что значение «а» составляет 8,7299±0,0017 Å, т.е. находится между 8,7282 Å и 8,7316 Å.
| Таблица 2Кристаллографические данные и подробности методики определения тонкой монокристаллической структуры формы X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты | |
| Полиморф X | |
| Кристаллографические данные | |
| Химическая формула | C25H27NO3 |
| Mr | 389,48 |
| Кристаллографическая система, пространственная группа | Орторомбическая, P212121 |
| Температура (K) | 120(2) |
| a, b, c (Å) | 8,7299(17), 14,822(3), 16,353(3) |
| α, β, γ (°) | 90,00, 90,00, 90,00 |
| V(Å3) | 2116,0(7) |
| Z | 4 |
| Тип излучения | Mo Kα |
| μ (мм-1) | 0,08 |
| Описание кристалла | куб |
| Цвет кристалла | бесцветный |
| Размер кристалла (мм) | 0,18×0,15×0,15 |
| Сбор данных | |
| Дифрактометр | Дифрактометр Bruker SMART на платформе ccd |
| Поправка на поглощение | - |
| Число измеренных, независимых и наблюдавшихся рефлексов [I>2σ(I)] | 14231, 2719, 1946 |
| Rint | 0,326 |
| Тонкая структура | |
| R[F2>2σ(F2)], wR(F2), S | 0,079, 0,211, 0,76 |
| Число рефлексов | 5113 |
| Число параметров | 262 |
| Число ограничений | 0 |
| Обработка атома H | Параметры атома H ограничены |
| Δρmax, Δρmin (e Å-3) | 0,30, -0,52 |
| Абсолютная структура | Flack H D (1983), Acta Cryst. A39, 876-881 |
| Параметр Флэка | 4(3) |
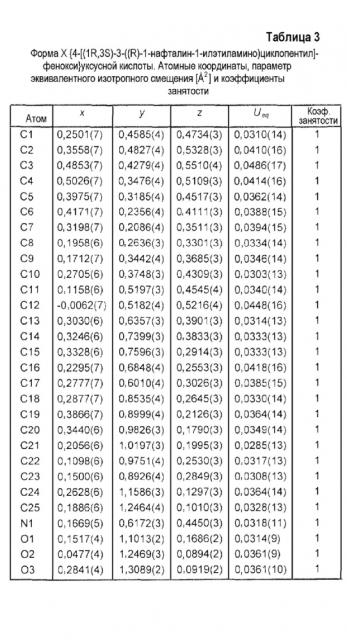
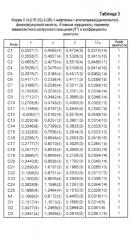
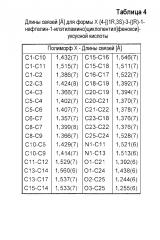
В предпочтительном в настоящее время варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты содержит атомы с такими же атомными координатами относительно начала координат элементарной ячейки, как представлено ниже в таблице 3, длины связей, как представлено ниже в таблице 4, а углы между связями, как представлено ниже в таблице 5.
В другом предпочтительном в настоящее время варианте осуществления настоящего изобретения форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты имеет структуру, полученную посредством рентгеновской кристаллографии (XRC) монокристалла, как показано в формуле 2.
В следующем аспекте настоящее изобретение относится к конкретной полиморфной форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты и способам ее получения.
В еще одном другом аспекте настоящее изобретение относится к изготовлению формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты с применением в качестве исходного материала аморфной формы {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
В дальнейшем аспекте настоящее изобретение относится к изготовлению формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты с использованием C1-C6-алкилового сложного эфира, такого как метиловый сложный эфир или этиловый сложный эфир {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, в качестве исходного материала по двухстадийной однореакторной производственной процедуре, где C1-C6-алкиловый сложный эфир гидролизуют в щелочных условиях в растворе C1-C6-алкилового спирта, а продукт, полученный в результате этого, кристаллизуют прямо из смеси реакции омыления посредством концентрирования, нейтрализации и разбавления водой.
В дополнительных аспектах настоящее изобретение направлено на фармацевтические композиции, содержащие эту полиморфную форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, и на способы ее получения и применения.
Определения
Термин «линейные или разветвленные C1-C6-алкиловые спирты» охватывает метанол, этанол, 1-пропанол, 2-пропанол, 1-бутанол, трет-бутанол и 2-бутанол.
Краткое описание графиков, фигур и таблиц
Вышеуказанный график 1 показывает наложение XRPD-дифрактограмм формы С и формы Х.
График 2a показывает типичную XRPD-дифрактограмму формы C.
График 2b показывает типичную XRPD-дифрактограмму формы X.
График 3 показывает сравнение термограмм DSC для формы C и формы X, которые демонстрируют эндотермические эффекты для двух полиморфных форм, начинающиеся примерно при 240°C и примерно при 255°C (±2°C), соответственно.
График 4a показывает типичную термограмму DSC+TGA для формы C.
График 4b показывает типичную термограмму DSC+TGA для формы X.
Вышеуказанный график 5 показывает наложение спектров ATR-FTIR формы C и формы X.
График 6a показывает спектр ATR-FTIR, записанный с чистой формой С.
График 6b показывает спектр ATR-FTIR, записанный с чистой формой Х.
График 7 показывает наложение спектров твердотельного ЯМР формы С и формы Х.
График 8a показывает спектр твердотельного ЯМР чистой формы С.
График 8b показывает спектр твердотельного ЯМР чистой формы X.
Формула 1 показывает монокристаллическую конфигурацию кристаллической формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Формула 2 показывает монокристаллическую конфигурацию кристаллической формы X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 1 представляет монокристаллические параметры кристаллической формы С и кристаллической формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 2 представляет экспериментальные подробности, относящиеся к определению монокристаллической структуры формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 3 представляет избранные атомные координаты и изотропные термические параметры для монокристаллической конфигурации формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 4 и таблица 5 представляют длины связей и углы между связями, соответственно, для монокристаллической конфигурации формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
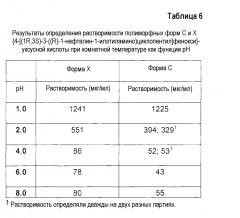
Таблица 6 представляет значения растворимости при разных рН для формы X и формы C {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты. Можно сделать вывод о том, что при комнатной температуре растворимость формы Х является более высокой, чем растворимость формы С.
Подробное описание изобретения
{4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусная кислота представляет собой цвиттерионную молекулу со значениями рКа, равными 2,9 и 9,3. Соли указанного соединения нестабильны в препаратах с рН между двумя значениями рКа, поэтому были предприняты поиски стабильных кристаллических форм этой цвиттерионной формы. Были найдены многие метастабильные формы или сольваты {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, но до сих пор были идентифицированы только два стабильных полиморфа (форма C и форма X). Эти две формы относятся друг к другу как энантиомеры.
В настоящее время полагают, что форма X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, в том виде, как описано выше, при комнатной температуре представляет собой несольватированную и безводную полиморфную кристаллическую форму.
Для характеризации полиморфов применяют целый ряд способов (H. G. Brittain (ed.) Polymorphism in Pharmaceutical Solids. Marcel Dekker, Inc., New York, 1999, p.227-278). Полезными инструментальными средствами, как было доказано, являются оптическая микроскопия и термомикроскопия. Для получения дополнительной информации (включая обнаружение фазовых переходов и выяснение того, не является ли каждая выделенная форма сольватом или ангидратом) можно применять процедуры термического анализа, такие как дифференциальная сканирующая калориметрия (DSC), термогравиметрический анализ (TGA). Эти термические методологии применяют для различения энантиотропных и монотропных систем, поскольку полиморфы относят к категориям двух типов (монотропов и энантиотропов), в зависимости от их стабильности в разных диапазонах температур и давлений.
Как правило, монотропы можно отличить от энантиотропов по их теплоте плавления. Эндотермический полиморфный переход свидетельствует об энантиотропах, тогда как экзотермический переход указывает на монотропы. Как обсуждалось выше в настоящем документе, имеется целый ряд эффективных способов характеризации полиморфов и нахождения отличий одного полиморфа от другого, отличных от анализа с использованием дифференциальной сканирующей калориметрии (DSC).
Кристаллизация является хорошо известным техническим средством для очистки химических соединений и для получения желаемых кристаллических форм химических соединений. Однако известно, что на кристаллизацию полиморфов влияют многие факторы, механизм которых неизвестен, а количественные взаимосвязи между операционными факторами и характеристиками кристаллизации полиморфов изучены недостаточно.
Процесс кристаллизации полиморфных кристаллов состоит из конкурентного зародышеобразования, роста и трансформации из метастабильной формы в стабильную. Для того чтобы полиморфы кристаллизовались избирательно, необходимо, чтобы механизм каждой элементарной стадии в процессе кристаллизации был четко связан с операционными условиями и с ключевыми регуляторными факторами [Crystal Growth & Design, 2004, Vol.4, № 6, 1153-1159].
Получение кристаллической {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты оказалось неожиданно сложной задачей. Одним из препятствий при этом является относительная стабильность аморфной формы, обусловленная высокой температурой стеклования (значительно выше комнатной температуры). Поэтому при попытке слишком быстрого осаждения {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты часто получают аморфный продукт. Кроме того, {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусная кислота кристаллизуется в виде многих метастабильных формах или сольватов. Во многих случаях твердый материал, полученный осаждением из некоторого растворителя, оказывался сольватом.
Форму X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты можно кристаллизовать из чистого профильтрованного раствора в подходящем растворителе, таком как линейный или разветвленный C1-C6-алкиловый спирт, подобный метанолу, без добавления затравочных кристаллов, что делает крупномасштабное производство формы Х более простым, чем производство других кристаллических форм {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Кроме того, было обнаружено, что {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусную кислоту можно подходящим образом получать омылением ее C1-C6-алкилового сложного эфира в растворе C1-C6-алкилового спирта водным щелочным гидроксидом, таким как гидроксид натрия. Было также обнаружено, что форму X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты удобно кристаллизовать из реакционной смеси омыления посредством концентрирования, регулирования рН (например, 50%-ной уксусной кислотой) и разбавления водой, которая инициирует кристаллизацию формы Х.
В еще одном другом аспекте настоящее изобретение относится к выделенной форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, как определено в настоящем документе, которая имеет полиморфную чистоту не менее 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%).
В еще одном другом аспекте настоящее изобретение относится к выделенной форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, как определено в настоящем документе, которая имеет степень кристалличности не менее 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%).
В еще одном другом аспекте настоящее изобретение относится к смеси или композиции кристаллических форм {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, включая псевдополиморфы {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, содержащие кристаллическую форму {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, такие как, например, смесь формы X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты с другой полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты.
Предпочтительная в настоящее время форма Х согласно настоящему изобретению обладает физическими свойствами, которые облегчают производство указанного соединения; особенно важна легкость, с которой этот конкретный кристаллический полиморф можно выделять в чистой форме без необходимости добавлять зародышевые кристаллы формы Х. Кроме того, форма Х также хорошо подходит для долгосрочного хранения дозированных форм соединения благодаря ее стабильности в отношении преобразования в другие твердые формы {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, которые обычно имеют плотность и внешнюю форму кристаллов, отличные от формы Х. Полиморфные преобразования API в твердых дозированных формах, таких как таблетки, могут приводить к их растрескиванию.
Взаимное преобразование между полиморфными формами в твердых дозированных формах является весьма существенным осложнением и поэтому его следует по возможности избегать, что достигается применением стабильной полиморфной формы Х. Это доказано в испытаниях на стабильность, при которых форма C, форма X и смеси двух полиморфных форм Х+С выдержали 4-недельные испытания стабильности в стрессовых условиях при 60°С, при 60°С и 75%-ной относительной влажности и при 80°С и 75%-ной относительной влажности без какой-либо трансформации твердого состояния.
Поэтому в еще одном другом варианте осуществления настоящее изобретение относится к выделенной форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, которая не претерпевает никакой трансформации твердого состояния в течение 4-недельного испытания стабильности в стрессовых условиях при 60°С, при 60°С и 75%-ной относительной влажности и при 80°С и 75%-ной относительной влажности.
В еще одном другом варианте осуществления настоящее изобретение относится к кристаллической форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или к ее смесям с другой стабильной кристаллической полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, для применения в терапии.
В конкретном варианте осуществления настоящее изобретение относится к кристаллической форме Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или к ее смесям с аморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты или с кристаллической формой С {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, для применения в терапии.
В еще одном другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей кристаллическую форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, или к ее смесям с другой стабильной кристаллической полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, вместе с фармацевтически приемлемым эксципиентом или носителем.
В конкретном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей кристаллическую форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению, или к ее смесям с кристаллической формой С {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты или с аморфной {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислотой, как определено в настоящем документе, или с их смесями, вместе с фармацевтически приемлемым эксципиентом или носителем.
В конкретном варианте осуществления настоящее изобретение предоставляет форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или ее смеси с кристаллической формой С или с аморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, для применения для лечения, ослабления или профилактики физиологических расстройств или заболеваний, связанных с нарушениями активности CaSR, таких как гиперпаратиреоз.
В другом конкретном варианте осуществления настоящее изобретение предоставляет форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или ее смеси с кристаллической формой С {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, для применения для лечения, предупреждения или ослабления физиологических расстройств или заболеваний, связанных с нарушениями активности CaSR, таких как гиперпаратиреоз.
В следующем варианте осуществления настоящее изобретение направлено на применение предпочтительной формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или ее смесей с кристаллической формой С 4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, для изготовления медикамента для профилактики, лечения или ослабления физиологических расстройств или заболеваний, связанных с нарушениями активности CaSR, таких как гиперпаратиреоз.
В еще одном дополнительном варианте осуществления настоящее изобретение направлено на фармацевтическую композицию, содержащую предпочтительную форму Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или ее смеси с кристаллической формой С 4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено, вместе с фармацевтически приемлемым носителем или эксципиентом.
Настоящее изобретение также предоставляет способ предупреждения, лечения или облегчения карциномы паращитовидной железы, аденомы паращитовидной железы, первичной гиперплазии паращитовидной железы, дисфункций сердца, почек или кишечника, заболеваний центральной нервной системы, хронической почечной недостаточности, хронической болезни почек, подоцитарных заболеваний, первичного гиперпаратиреоза, вторичного гиперпаратиреоза, третичного гиперпаратиреоза, анемии, сердечнососудистых заболеваний, фиброзного остита, адинамической болезни кости, остеопороза, индуцированного стероидами остеопороза, старческого остеопороза, постменопаузного остеопороза, остеомаляции и связанных с ней заболеваний костей, остеопороза после трансплантации почки, желудочно-кишечных заболеваний, эндокринных и нейродегенеративных заболеваний, рака, болезни Альцгеймера, гиперкальциемии или почечной остеодистрофии, причем указанный способ включает в себя введение пациенту, нуждающемуся в этом, эффективного количества формы X {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты согласно настоящему изобретению или ее смесей с кристаллической формой С {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты, как определено в настоящем документе, необязательно, в комбинации или в качестве дополнения к активному стероидному витамину D или к производному витамина D, такому как 1-α-гидроксихолекальциферол, эргокальциферол, холекальциферол, 25-гидроксихолекальциферол, 1-α-25-дигидроксихолекальциферол, или в комбинации или в качестве дополнения к веществам, связывающим фосфат, эстрогенам, кальцитонину или бифосфонатам.
Таким образом, предпочтительный в настоящее время полиморф {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты представляет собой кристаллическую форму Х, характеризуемую ее рентгеновской порошковой дифрактограммой (XRPD) (график 2b), ее инфракрасным спектром нарушенного полного внутреннего отражения с Фурье-преобразованием (ATR-FTIR) (график 6b), ее кривой дифференциальной сканирующей калориметрии (DSC) (график 4b), ее спектром твердотельного ЯМР (SS-NMR) (график 8b), параметрами ее монокристалла, как определено в таблице 1, и ее кристаллической структурой (формула 2), полученной посредством рентгеноструктурного анализа ее монокристаллов (XRC).
Другой конкретный полиморф {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты представляет собой форму С, характеризуемую ее рентгеновской порошковой дифрактограммой (XRPD) (график 2a), ее инфракрасным спектром нарушенного полного внутреннего отражения с Фурье-преобразованием (ATR-FTIR) (график 6a), ее кривой дифференциальной сканирующей калориметрии (DSC) (график 4a), ее спектром твердотельного ЯМР (SS-NMR) (график 8a), параметрами ее монокристалла, как определено в таблице 1, и ее кристаллической структурой (формула 1), полученной посредством рентгеноструктурного анализа ее монокристаллов (XRC).
Как обсуждалось выше в настоящем документе, кристаллическая композиция вещества, раскрытого в настоящем документе, может быть получена из аморфной (т.е. некристаллической) {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты. Получение аморфной {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты раскрыто в WO 2009/065406, которая включена в настоящий документ посредством ссылки.
Конкретный способ образования кристаллической формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты включает в себя растворение аморфного соединения в сухом растворителе или смеси растворителей. К предпочтительным растворителям относятся линейные или разветвленные С1-С6-алкиловые спирты, такие как метанол и этанол.
Предпочтительно, растворитель нагревают, аморфное соединения растворяют в нем до концентрации, приблизительно соответствующей насыщению, и раствор, полученный в результате этого, фильтруют, после чего ему дают возможность охлаждаться до температуры, при которой полное количество растворенного вещества больше не является растворимым в указанном растворителе и начинается кристаллизация. Затем кристаллизации дают возможность продолжаться (необязательно, с охлаждением суспензии) до предполагаемого завершения. Кристаллы отфильтровывают и сушат (необязательно, в вакууме при повышенной температуре).
Другой конкретный двухстадийный однореакторный способ образования кристаллической формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-илэтиламино)циклопентил]фенокси}уксусной кислоты включает в себя растворение C1-C6-алкилового сложного эфира указанного соединения (такого как метиловый или этиловый сложный эфир) в C1-C6-алкиловом спирте (таком как этанол) с последующим добавлением, по меньшей мере, молярного э