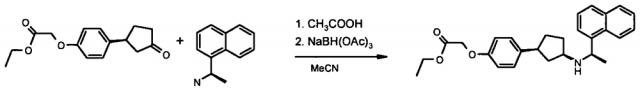
Новая полиморфная форма кальцимиметического соединения
Иллюстрации
Показать всеИзобретение относится к кристаллической форме {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, которая может найти применение для лечения, уменьшения интенсивности симптомов или профилактики физиологических расстройств или заболеваний, связанных с нарушениями активности кальцийчувствительных рецепторов (CaSR), таких как гиперпаратиреоидизм. Данная кристаллическая форма имеет рентгеновскую порошковую дифрактограмму, которая показывает характеристические пики, выраженные в углах 2θ, при приблизительно , , 12,3, 16,0, , 19,1 и/или 20,2 (±0,1 градуса) (подчеркнутое является основным). Изобретение относится также к фармацевтической композиции, содержащей указанную кристаллическую форму, и способам ее получения. 5 н. и 10 з.п. ф-лы, 12 ил., 2 ф-лы, 6 табл., 6 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к новой полиморфной форме {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, к способам ее получения и к ее применению.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Изобретение относится к новой полиморфной форме {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, ранее описанной в международной публикации WO09/065406. Соединение может быть использовано в лечении ряда расстройств или заболеваний, связанных с нарушениями активности кальцийчувствительных рецепторов (CaSR).
Кальцимиметики представляют собой низкомолекулярные аллостерические активаторы кальцийчувствительного рецептора (CaSR) [Urena, P.; Frazao, J.M. Calcimimetic agents: Review and perspectives. Kidney International (2003), 63, pp. s91-s96; Soudijn, W. et al. Allosteric modulation of G protein-coupled receptors: perspectives and recent developments. DDT (2004), 9, 752-758].
Кальцимиметики, как уже было показано, являются коммерчески полезными в лечении гиперпаратиреоидизма (HPT): Кальцимиметическое соединение Cinacalcet® [Balfour, J.A. B. et al. Drugs (2005) 65(2), 271-281; Linberg et al. J. Am. Soc. Nephrol (2005), 16, 800-807, Clinical Therapeutics (2005), 27(11), 1725-1751] недавно выпущен на рынок для лечения вторичного HPT у пациентов с хроническим заболеванием почек на диализе и для лечения первичного HPT у пациентов с паратиреоидной карциномой. Таким образом, получено доказательство обоснованности концепции в отношении активаторов кальцийчувствительного рецептора (CaSR) у людей, и уже хорошо установлена клиническая значимость. Другие кальцимиметические соединения были описаны, например, в международных публикациях: WO 94/018959, WO 98/001417, WO 05/065050, WO 03/099814, WO 03/099776, WO 00/21910, WO 01/34562, WO 01/090069, WO 97/41090, в патенте США US6001884, в международной публикации WO96/12697, в европейском патенте EP1203761, в международных публикациях: WO95/11221, WO93/04373, в европейском патенте EP1281702, в международных публикациях: WO02/12181, WO04/069793, в патенте США US2004/242602, в международных публикациях: WO04/106296 и WO05/115975.
{4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусная кислота представляет собой новый перспективный класс (WO2009/065406) соединений, проявляющих кальцимиметическую активность.
Одним важным аспектом фармацевтического производства является физическая форма Активного Фармацевтического Ингредиента (API=АФИ). Физическая форма, как, например, кристаллическая форма, лекарственного вещества или API, используемого в фармацевтическом составе или в лекарственном препарате, важна, так как различные физические формы часто проявляют различные фундаментальные свойства, такие как растворимость, скорость растворения, гигроскопичность, биодоступность, перерабатываемость и стабильность. Наличие различных твердых форм, как например полиморфизм или псевдополиморфизм, таким образом, может оказывать влияние на свойства лекарственного продукта.
Следовательно, конкретная кристаллическая форма, включая сольваты и гидраты, могла бы быть предпочтительной по сравнению с другой формой. Кроме того, некоторые формы могут быть предпочтительны в зависимости от конкретного состава и/или применения. Например, свойство лекарственного средства, такое как скорость растворения активного ингредиента, может быть отрегулировано соответствующим подбором некоторой кристаллической формы, или смесей кристаллических форм в особых соотношениях.
Кристаллическая форма для API обычно предпочтительна в сравнении с некристаллической формой, например, в сравнении с аморфной формой, и в приготовлении состава лекарственного средства и во время химической переработки благодаря ее предсказуемым свойствам. Кристаллические формы имеют, в том числе, преимущество, проявляющееся в большей химической стабильности (при действии давления, нагревания и света), в более легкой перерабатываемости и в более хорошей технологичности. В частности, обеспечение кристаллической формы является важным преимуществом во время синтеза лекарственного средства, в особенности в промышленном масштабе, так как кристаллы, как правило, легче выделяются из реакционной смеси. Кроме того, известно, что кристаллизация конкретной кристаллической формы соединения в конкретном растворителе может приводить к преимущественной очистке соединения, которая не могла быть достигнута кристаллизацией другой формы в другом растворителе (отчасти вследствие различий характеристик растворимости примесей в различных растворителях). Аморфные соединения, в противоположность тому, не могут быть очищены перекристаллизацией, но будут часто требовать более дорогих способов очистки, таких как, например, препаративная хроматография.
Различные кристаллические формы также отличаются температурой плавления, плотностью, твердостью, характеристиками измельчения/обрабатываемостью шлифованием, и так далее, и, как следствие, конкретная полиморфная форма предпочтительна в сравнении с другой формой в зависимости от конкретного применения. Различные кристаллические формы имеют различные характеристики стабильности в фармацевтических составах, которые зависят от эксципиентов, составов среды для лекарства, и других добавок, присутствующих в лекарственной форме. Нестабильность аморфных соединений или полиморфных форм, которые не являются наиболее стабильными формами, отражает, в частности, проблему, имеющую место, когда лекарственное средство находится в суспензии.
В соответствии с вышеизложенным, хотя кристаллические формы, как правило, являются предпочтительными в сравнении с некристаллическими формами лекарственного вещества, конкретная кристаллическая форма соединения будет предпочтительна в зависимости от различных обстоятельств, таких как ее применение или способ, которым ее используют.
Иногда термодинамически более стабильная форма предпочтительна в сравнении с метастабильной формой, иногда метастабильная форма, которая может иметь повышенную скорость растворения, является предпочтительной.
Международная публикация WO2009/065406 описывает синтез {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, но не раскрывает кристаллические формы соединения или получение таких форм. Заявка умалчивает в отношении полиморфизма и в отношении того, как получить стабильную полиморфную форму {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Международная публикация WO2010/021351 описывает синтез производных {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, но не раскрывает кристаллические формы вышеупомянутых производных.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение неожиданно обеспечивает стабильную кристаллическую полиморфную модификацию {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
В первом аспекте, настоящее изобретение, таким образом, относится к {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоте, в кристаллической форме.
В предпочтительном аспекте, настоящее изобретение относится к {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоте в виде кристаллической полиморфной модификации, проявляющей один или более признаков, или характеристических линий, форм, или конкретных комбинаций линий, отраженных на Фиг. 2а, 4а, 6а, 8а, в Формуле 1 и/или в Таблице 1-6; или имеющей одно или более значений, перечисленных там, например, волновых чисел в см-1 (±3 или ±4 см-1 в зависимости от используемого способа), или углов отражения в градусах угла 2θ (±0,1); или представляемой спектром/дифрактограммой, в значительной мере похожим(ей) на спектр/дифрактограмму, показанный(ую) на упомянутых Фигурах или в Таблицах, где упомянутая кристаллическая полиморфная модификация {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты в дальнейшем в этом документе называется «Форма С» или «полиморфная модификация С».
Форму С можно отличить от других полиморфных форм с помощью нескольких аналитических методов, таких как рентгеновская порошковая дифрактометрия. Фиг. 1 показывает наложенную дифрактограмму, полученную методом рентгеновской порошковой дифрактометрии (XRPD), для двух полиморфных форм С и Х, которая ясно показывает как зоны сходства, так и различия.
Так, в варианте осуществления настоящего изобретения Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется наличием XRPD-дифрактограммы, в значительной мере совпадающей с XRPD-дифрактограммой, показанной на Фиг. 2а, которая представляет собой XRPD-дифрактограмму, записанную для чистой полиморфной Формы С.
В другом варианте осуществления Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется XRPD-дифрактограммой, показывающей один или более пиков отражения при приблизительном значении 2θ= 8,8, 9,5, 12,3, 16,0, 18,3, 19,1 и/или 20,2 (±0,1 градуса) (подчеркнутое является основным), соответственно.
Форму С также можно отличить от других полиморфных форм с помощью дифференциальной сканирующей калориметрии (DSC). Фиг. 3 показывает наложенную термограмму форм С и Х, которая указывает на эндотермические переходы для двух полиморфных форм, имеющих температуры начала эндотермического перехода при приблизительно 240°С и приблизительно 255°С (±2°С), соответственно.
Так, в варианте осуществления Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется наличием кривой, полученной методом дифференциальной сканирующей калориметрии (DSC), в значительной мере совпадающей с DSC-кривой, показанной на Фиг. 4а, содержащей эндотермический переход с температурой начала перехода при приблизительно 240°С (±2°С).
DSC-кривая на Фиг. 4а также содержит экзотермический переход при температуре приблизительно 245°С, которая благодаря кристаллизации Формы Х из расплавленной {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты превышает температуру плавления Формы С. Таким образом полученные кристаллы Формы Х впоследствии плавятся при дальнейшем повышении температуры, признаком чего служит другой эндотермический переход при температуре приблизительно 255°С (±2°С). Фиг. 4а, кроме того, включает траекторию, полученную методом термогравиметрического анализа (TGA), которая показывает, что {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусная кислота является стабильной, то есть не разлагается при температуре ниже 255°С (±2°С).
Форму С также можно отличить от других полиморфных форм с помощью инфракрасной спектроскопии нарушенного полного внутреннего отражения с преобразованием Фурье (ATR-FTIR). Фиг. 5 показывает наложенный ATR-FTIR-спектр двух полиморфных форм С и Х, который ясно показывает как зоны сходства, так и различие.
В одном варианте осуществления настоящего изобретения Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется наличием ATR-FTIR-спектра, в значительной мере совпадающего с показанным ATR-FTIR-спектром на Фиг. 6а, который представляет собой ATR-FTIR-спектр, записанный для чистой полиморфной Формы С.
В другом варианте осуществления Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется ATR-FTIR-спектром, показывающим один или более пиков нарушенного полного внутреннего отражения при приблизительно 1636, 1298, 1225, 822, 811 и/или 786 (± 3 см-1) (подчеркнутое является основным), соответственно.
Форму С также можно отличить от других полиморфных форм с помощью метода твердотельной спектроскопии ядерного магнитного резонанса (SS-NMR). Фиг. 7 показывает наложенный 13С-SS-NMR-спектр двух полиморфных форм С и Х, который ясно показывает как области сходства, так и различие.
В одном варианте осуществления настоящего изобретения Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется наличием 13С-SS-NMR-спектра, в основном совпадающего с показанным спектром на Фиг. 8а, который представляет собой 13С-SS-NMR-спектр, записанный для чистой полиморфной Формы С.
В еще одном варианте осуществления Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется 13С-SS-NMR-спектром, показывающим один или более резонансных пиков при δ 13С: 173,4, 157,6, 132,6, 117,0, 67,8, 48,9, 35,6 и/или 27,0 (±1 м.д. (ppm)) (подчеркнутое является основным), соответственно.
В другом варианте осуществления настоящего изобретения Форма С и Форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты характеризуется наличием параметров монокристалла, которые в значительной мере сходны с параметрами монокристалла, которые представлены в Таблице 1:
| Таблица 1Параметры монокристалла для Формы С и Формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты | ||
| Форма Х | Форма С | |
| Кристаллическая система: | Орторомбическая | Тетрагональная |
| Описание кристалла | Куб | Пирамида |
| Пространственная группа (группа симметрии кристаллической решетки): | P212121 | P41212 |
| Размеры элементарной ячейки кристалла (Ǻ) | а=8,7299(17)b=14,822(3)c=16,353(3) | a=10,2289(16)b=10,2289(16)c=41,492(13) |
| Объем (Ǻ3): | 2116,0(7) | 4341,3(16) |
| Количество молекул на элементарную ячейку (Z) | 4 | 8 |
На всем протяжении настоящей заявки параметры кристаллов, такие как размеры элементарных ячеек, атомные координаты, и так далее, даны в стандартном кристаллографическом представлении, в котором стандартная неопределенность для конкретного значения показана в скобках. Например, значение по оси а в Таблице 1, «а=10,2289(16)» означает, что существует 95%-ная вероятность того, что значение равно 10,2289±0,0016 Ǻ, то есть, лежит между 10,2273 Ǻ и 10,2305 Ǻ.
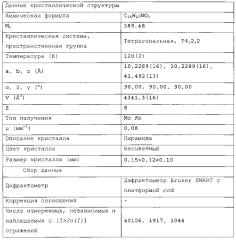
| Таблица 2Данные кристаллической структуры и подробности уточнения структуры, касающиеся определения структуры Монокристалла Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты | |
| Форма С | |
| Данные кристаллической структуры | |
| Химическая формула | C25H27NO3 |
| Mr | 389,48 |
| Кристаллическая система,пространственная группа | Тетрагональная, Р41212 |
| Температура (К) | 120(2) |
| a, b, c (Ǻ) | 10,2289(16), 10,2289(16), 41,492(13) |
| α, β, γ (°) | 90,00, 90,00, 90,00 |
| V (Ǻ3) | 4341,3(16) |
| Z | 8 |
| Тип излучения | Mo Kα |
| μ (мм-1) | 0,08 |
| Описание кристалла | Пирамида |
| Цвет кристалла | Бесцветный |
| Размер кристалла (мм) | 0,15×0,12×0,10 |
| Сбор данных | |
| Дифрактометр | Дифрактометр Bruker SMART c платформой ccd |
| Коррекция поглощения | - |
| Число измеренных, независимых инаблюдаемых с [I>2σ(I)] отражений | 40106, 1917, 1044 |
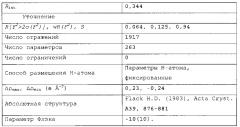
| Rint | 0,344 |
| Уточнение | |
| R[F2>2σ(F2)], wR(F2), S | 0,064, 0,125, 0,94 |
| Число отражений | 1917 |
| Число параметров | 263 |
| Число ограничений | 0 |
| Способ размещения Н-атома | Параметры Н-атома, фиксированные |
| ∆ρmax, ∆ρmin (e Ǻ-3) | 0,23, -0,24 |
| Абсолютная структура | Flack H.D. (1983), Acta Cryst. A39, 876-881 |
| Параметр Флэка | -10(10) |
В предпочтительном на настоящий момент варианте осуществления настоящего изобретения Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты содержит атомы в атомных положениях относительно начала координат элементарной ячейки, которые представлены ниже в Таблице 3, с длинами связей, которые изложены ниже в Таблице 4, или с углами между связями, которые приведены ниже в Таблице 5.
| Таблица 3Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты. Атомные координаты, параметр эквивалентного изотропного смещения [Ǻ2] и фактор заселенности того или иного положения в кристаллической решетке | |||||
| Атом | x | y | z | Параметр эквивалентного изотропного смещения (Ueq) | Фактор заселенности того или иного положения в кристаллической решетке (S.o.f.) |
| C1 | 0,7619(4) | 0,8578(6) | 0,36785(18) | 0,0189(8) | 1 |
| C2 | 0,8333(4) | 0,6643(6) | 0,3605(2) | 0,0246(9) | 1 |
| C3 | 0,8834(4) | 0,5170(7) | 0,4205(2) | 0,0297(9) | 1 |
| C4 | 0,8607(4) | 0,5619(7) | 0,4891(2) | 0,0273(9) | 1 |
| C5 | 0,7844(4) | 0,7538(6) | 0,5000(2) | 0,0247(9) | 1 |
| C6 | 0,7569(4) | 0,8021(7) | 0,5706(2) | 0,0328(10) | 1 |
| C7 | 0,6838(4) | 0,9876(8) | 0,5822(2) | 0,0356(10) | 1 |
| C8 | 0,6347(4) | 1,1390(7) | 0,52299(19) | 0,0301(9) | 1 |
| C9 | 0,6599(4) | 1,1023(6) | 0,45443(19) | 0,0241(9) | 1 |
| C10 | 0,7339(3) | 0,9077(6) | 0,43923(19) | 0,0206(8) | 1 |
| C11 | 0,7224(3) | 1,0179(6) | 0,30160(16) | 0,0169(7) | 1 |
| C12 | 0,8486(3) | 1,0709(6) | 0,26906(18) | 0,0223(8) | 1 |
| C13 | 0,4663(3) | 0,8874(6) | 0,25509(19) | 0,0220(8) | 1 |
| C14 | 0,3588(3) | 0,8012(7) | 0,18398(19) | 0,0286(9) | 1 |
| C15 | 0,2273(4) | 0,9483(6) | 0,1715(2) | 0,0271(9) | 1 |
| C16 | 0,2380(4) | 1,0459(8) | 0,24879(19) | 0,0315(9) | 1 |
| C17 | 0,3972(4) | 1,0974(7) | 0,2782(2) | 0,0309(10) | 1 |
| C18 | 0,0870(3) | 0,8398(6) | 0,13484(19) | 0,0220(8) | 1 |
| C19 | -0,0082(4) | 0,9429(6) | 0,07658(19) | 0,0251(9) | 1 |
| C20 | -0,1352(4) | 0,8407(6) | 0,04212(19) | 0,0228(8) | 1 |
| C21 | -0,1719(3) | 0,6313(6) | 0,06428(17) | 0,0186(8) | 1 |
| C22 | -0,0780(3) | 0,5261(6) | 0,12344(18) | 0,0230(8) | 1 |
| C23 | 0,0495(4) | 0,6305(6) | 0,1591(2) | 0,0272(9) | 1 |
| C24 | -0,3108(3) | 0,5214(6) | 0,02492(17) | 0,0217(8) | 1 |
| C25 | -0,4280(3) | 0,5572(6) | 0,06667(17) | 0,0186(8) | 1 |
| C26 | -0,4079(3) | 0,4076(6) | 0,13577(19) | 0,0175(8) | 1 |
| N1 | 0,6060(3) | 0,9270(4) | 0,23889(13) | 0,0156(6) | 1 |
| O1 | -0,3690(2) | 0,4919(4) | 0,19980(12) | 0,0221(6) | 1 |
| O2 | -0,4316(3) | 0,2019(4) | 0,12297(13) | 0,0277(6) | 1 |
| Таблица 4Длины связей [Ǻ] для Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты | |||
| Полиморфная модификация С - длины связей [Ǻ] | |||
| C1-C10 | 1,416(8) | C15-C16 | 1,533(9) |
| C1-C2 | 1,376(8) | C17-C16 | 1,518(9) |
| C2-C3 | 1,411(9) | C18-C15 | 1,505(9) |
| C4-C3 | 1,356(8) | C18-C19 | 1,380(8) |
| C5-C10 | 1,412(9) | C18-C23 | 1,378(9) |
| C5-C4 | 1,408(8) | C20-C19 | 1,390(9) |
| C5-C6 | 1,411(9) | C20-C21 | 1,396(9) |
| C7-C6 | 1,349(9) | C22-C21 | 1,368(8) |
| C8-C7 | 1,405(9) | C22-C23 | 1,406(9) |
| C9-C8 | 1,336(8) | C25-C24 | 1,565(9) |
| C10-C9 | 1,434(9) | N1-C11 | 1,512(8) |
| C11-C1 | 1,520(8) | N1-C13 | 1,476(8) |
| C11-C12 | 1,536(9) | O1-C21 | 1,372(8) |
| C13-C14 | 1,535(8) | O1-C24 | 1,439(7) |
| C13-C17 | 1,524(9) | O2-C25 | 1,244(7) |
| C14-C15 | 1,518(8) | O3-C25 | 1,195(7) |
| Таблица 5Углы между связями [°] для Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты | |||
| Полиморфная модификация С - углы между связями [°] | |||
| C1-C10-C5 | 119,1(6) | C17-C16-C15 | 106,0(6) |
| C1-C10-C9 | 124,2(6) | C18-C15-C14 | 115,5(6) |
| C1-C11-C12 | 114,3(6) | C18-C15-C16 | 114,1(6) |
| C1-C2-C3 | 121,6(7) | C18-C19-C20 | 122,1(7) |
| C2-C1-C10 | 119,1(6) | C18-C23-C22 | 121,1(7) |
| C2-C1-C11 | 119,1(6) | C19-C18-C15 | 120,4(7) |
| C3-C4-C5 | 120,5(7) | C19-C18-C23 | 117,9(7) |
| C4-C3-C2 | 119,8(7) | C19-C20-C21 | 119,1(7) |
| C4-C5-C10 | 120,0(7) | C21-C22-C23 | 119,9(7) |
| C4-C5-C6 | 120,2(7) | C21-01-C24 | 118,7(5) |
| C5-C10-C9 | 116,7(6) | C22-C21-C20 | 119,9(7) |
| C6-C5-C10 | 119,8(7) | C22-C21-01 | 116,1(7) |
| C6-C7-C8 | 119,8(7) | C23-C18-C15 | 121,6(6) |
| C7-C6-C5 | 121,1(7) | N1-C11-C1 | 109,8(6) |
| C8-C9-C10 | 121,8(7) | N1-C11-C12 | 107,5(5) |
| C9-C8-C7 | 120,8(7) | N1-C13-C14 | 110,1(5) |
| С10-С1-С11 | 121,8(6) | N1-C13-C17 | 114,7(6) |
| C13-N1-C11 | 117,0(5) | O1-С21-С20 | 124,0(7) |
| С14-С15-С16 | 101,5(6) | O1-С24-С25 | 114,2(6) |
| С15-С14-С13 | 104,9(5) | O2-С25-С24 | 110,6(7) |
| С16-С17-С13 | 106,4(6) | O3-С25-С24 | 119,9(6) |
| С17-С13-С14 | 105,3(6) | O3-С25-O2 | 129,5(7) |
| Таблица 6Краткие сведения растворимости, определенной при комнатной температуре, полиморфных модификаций: Формы С и Формы Х, {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты в виде функциональной зависимости от рН | ||
| Форма Х | Форма С | |
| рН | Растворимость (мкг/мл) | Растворимость (мкг/мл) |
| 1,0 | 1241 | 1225 |
| 2,0 | 551 | 394; 3291 |
| 4,0 | 86 | 52; 531 |
| 6,0 | 78 | 43 |
| 8,0 | 80 | 55 |
| 1Растворимость была определена дважды на двух различных сериях |
В другом предпочтительном на настоящий момент варианте осуществления настоящего изобретения Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты имеет структуру, полученную с помощью рентгеновской кристаллографии (XRC) монокристалла, которая показана в Формуле 1.
В дополнительном аспекте изобретение относится к конкретной полиморфной Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, и к способам ее получения.
В еще одном аспекте, это изобретение относится к изготовлению Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты с использованием в качестве исходного вещества другой кристаллической полиморфной формы {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, или аморфной формы {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Изобретение в дополнительных аспектах направлено на фармацевтические композиции, содержащие эту полиморфную Форму С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, и на способы получения этого и на применение.
ОПРЕДЕЛЕНИЯ
Термин «линейные или разветвленные С1-С6 алкиловые спирты» включает метанол, этанол, 1-пропанол, 2-пропанол, 1-бутанол, трет-бутанол, и 2-бутанол.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ И ТАБЛИЦ
Вышеупомянутая Фиг. 1 показывает наложенную XRPD-дифрактограмму Формы С и Формы Х.
Фиг. 2а показывает характерную XRPD-дифрактограмму Формы С.
Фиг. 2b показывает характерную XRPD-дифрактограмму Формы Х.
Фиг. 3 показывает сравнение DSC-термограмм для Формы С и Формы Х, которое отражает эндотермические процессы для двух полиморфных форм, имеющих температуры начала эндотермического перехода при приблизительно 240°С и при приблизительно 255°С (±2°С), соответственно.
Фиг. 4а показывает характерную DSC- + TGA-термограмму для Формы С.
Фиг. 4b показывает характерную DSC- + TGA-термограмму для Формы Х.
Вышеупомянутое Фиг. 5 показывает наложенные ATR-FTIR-спектры Формы С и Формы Х.
Фиг. 6а показывает ATR-FTIR-спектр, записанный для чистой Формы С.
Фиг. 6b показывает ATR-FTIR-спектр, записанный для чистой Формы Х.
Фиг. 7 показывает наложенные твердотельные ЯМР-спектры Формы С и Формы Х.
Фиг. 8а показывает твердотельный ЯМР-спектр чистой Формы С.
Фиг. 8b показывает твердотельный ЯМР-спектр чистой Формы Х.
Формула 1 показывает конфигурацию монокристалла кристаллической Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Формула 2 показывает конфигурацию монокристалла кристаллической Формы Х {4-[(1R,3S)-3-((R)-1-Нафталин-1-ил-этиламино)-циклопентил]-фенокси}-уксусной кислоты.
Таблица 1 показывает параметры монокристалла для кристаллической Формы С и Формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 2 обеспечивает экспериментальные подробности, касающиеся определения структуры монокристалла Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 3 обеспечивает выбранные атомные координаты и изотропические тепловые параметры для Конфигурации Монокристалла Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 4 и Таблица 5 обеспечивает длины связей и углы между связями, соответственно, для Конфигурации Монокристалла Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Таблица 6 обеспечивает характеристики растворимости при различных рН для Формы Х и Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты. Может быть сделан вывод, что при комнатной температуре растворимость Формы Х выше по сравнению с растворимостью Формы С.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
{4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусная кислота представляет собой цвиттер-ионную молекулу со значениями рКа 2,9 и 9,3. Соли соединения являются нестабильными в составе с рН между двумя значениями рКа, поэтому сделан запрос на поиск стабильных кристаллических форм цвиттер-ионной формы. Были обнаружены многие метастабильные формы или сольваты {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, но до настоящего времени только две стабильные полиморфные модификации были идентифицированы (Форма С и Форма Х). Эти две формы находятся в состоянии энантиотропного превращения.
В настоящее время полагают, что Форма С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, которая описана выше, представляет собой термодинамически стабильную полиморфную кристаллическую форму при температуре окружающей среды, которая является несольватированной и безводной. Термодинамически стабильные кристаллические формы лекарственных препаратов, как правило, предпочтительны, поскольку они не превращаются в другие кристаллические формы во время производственного процесса или в конечном составе лекарственного средства [Topics in Current Chemistry, Vol. 198, 1998, 164-208].
Для охарактеризовывания полиморфных модификаций в фармацевтических твердых веществах было применено много методов (H.G. Brittain (ed.) Polymorphism in Pharmaceutical Solids. Marcel Dekker, Inc., New York, 1999, pp. 227-278). Было признано, что поляризационная оптическая микроскопия и термомикроскопия являются полезными средствами. Методы термического анализа, такие как дифференциальная сканирующая калориметрия (DSC) и термогравиметрический анализ (TGA), могут быть использованы для получения дополнительной информации, включая фазовые изменения, и для выявления того, является ли каждая выделенная форма сольватом или ангидритом. Эти термические методы исследования применяют для различения энантиотропных и монотропных систем, так как полиморфные модификации подразделены на два типа, монотропы и энантиотропы, в зависимости от их стабильности в отношении диапазона температур и давлений.
Как правило, можно отличить монотропы от энантиотропов по их теплотам плавления. Эндотермический переход, связанный с полиморфными превращениями, указывает на энантиотропы, тогда как экзотермический переход указывает на монотропы. Помимо анализа методом дифференциальной сканирующей калориметрии (DSC), существует ряд эффективных способов для того, чтобы охарактеризовать полиморфные модификации и отличить одну полиморфную модификацию от другой, что рассмотрено в этом документе выше.
Для полиморфных модификаций {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, Форма С имеет более низкую температуру плавления, чем Форма Х, но более высокую энтальпию плавления, что означает то, что она является термодинамически более стабильной при низких температурах в сравнении с Формой Х. Температура перехода Tb, при которой две полиморфные модификации являются одинаково стабильными, превышает выше 110°С, поскольку конкурентный переход в жидкую фазу при этой температуре приводит к превращению Формы Х в Форму С. В результате тщательных измерений энтальпии плавления и температур плавления обоих форм, было установлено, что температура перехода лежит между 120 и 145°С.
Кристаллизация представляет собой общеизвестный метод очистки химических соединений и получения желательной кристаллической формы химических соединений. Однако известно, что на кристаллизацию полиморфных модификаций оказывает влияние ряд эффектов, и механизм влияния этих эффектов не известен, и количественная взаимосвязь между рабочими характеристиками процесса кристаллизации и кристаллизационными характеристиками полиморфных модификаций не вполне понятна.
Процесс кристаллизации полиморфных кристаллов состоит из конкурентного зародышеобразования, роста, и превращения из метастабильной формы в стабильную форму. Для селективной кристаллизации полиморфных модификаций, необходимо, чтобы механизм каждой элементарной стадии в кристаллизационном процессе находился в точной взаимозависимости от рабочих условий процесса и от важнейших регулирующих факторов [Crystal Growth & Design, 2004, Vol. 4, No.6, 1153-1159].
Оказалось, что кристаллическую {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусную кислоту неожиданно трудно получать. Одним затруднением была относительная стабильность аморфной формы в связи с высокой температурой стеклования (значительно превышающей комнатную температуру). По этой причине, если предпринимают попытку осадить {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусную кислоту слишком быстро, то часто получают аморфный продукт.
Кроме того, {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусная кислота кристаллизуется с образованием множества метастабильных форм или сольватов. Во многих случаях оказывается, что твердое вещество, полученное осаждением из растворителя, является сольватом.
Форма С может быть наиболее эффективно получена кристаллизацией из метанола или этанола в присутствии центров кристаллизации Формы С, или, альтернативно, пролонгированным перемешиванием суспензии либо аморфной {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, либо ее другой полиморфной формы (такой как Форма Х) в органическом растворителе, таком как метанол, этанол, толуол и ксилол, необязательно при повышенной температуре или при кипячении с обратным холодильником.
В другом аспекте, это изобретение, таким образом, относится к изготовлению Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты с использованием в качестве исходного вещества другой кристаллической полиморфной формы {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, или ее аморфной формы, в присутствии зародышей кристаллов Формы С.
С другой стороны, кристаллизацией из холостого отфильтрованного раствора без добавления зародышей кристаллов может быть получена Форма Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, посредством чего обеспечивается возможность получения подходящего исходного вещества для предпочтительной Формы С, которая затем, в одном варианте осуществления изобретения, может быть получена превращением в твердом растворе Формы Х в Форму С при перемешивании суспензии Формы Х в течение длительного периода в подходящем растворителе, таком как линейный или разветвленный С1-С6 алкиловый спирт, например, метанол, подходящим образом при повышенной температуре или при кипячении с обратным холодильником.
В конкретном варианте осуществления, это изобретение, таким образом, относится к способу изготовления Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты с использованием в качестве исходного вещества кристаллической полиморфной Формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, где способ включает кипячение суспензии Формы Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты в течение длительного периода в метаноле.
В еще одном аспекте, это изобретение относится к выделенной Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, определяемой в этом документе, которая имеет полиморфную чистоту, по меньшей мере, 80%, такую как 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%.
В еще одном аспекте, это изобретение относится к выделенной Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, определяемой в этом документе, которая имеет степень кристалличности, по меньшей мере, 80%, такую как 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%.
В другом аспекте, это изобретение относится к смеси или к композиции кристаллических форм {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, включающих псевдополиморфные модификации {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, содержащие кристаллическую форму {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, определяемую в этом документе, такой как, например, смесь Формы С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты с другой полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты.
Предпочтительная в настоящий момент Форма С настоящего изобретения обладает физическими свойствами, которые облегчают изготовление и длительное хранение лекарственных форм соединения, в частности своей стабильностью в отношении взаимопревращения с другими формами {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, которые обычно имеют другие плотности и габитусы кристалла, чем Форма С. Полиморфное взаимопревращение активного фармацевтического ингредиента (API) в твердых лекарственных формах, таких как таблетки, может приводить к образованию трещин в таблетках.
Взаимопревращение между полиморфными формами в твердых лекарственных формах является серьезной проблемой, и, следовательно, должно быть, по возможности, устранено, что достигают путем использования стабильной полиморфной модификации, Формы С. Это проверено путем проведения испытания стабильности; так, полиморфные модификации: Форма С, Форма Х и смеси двух полиморфных форм С+Х все прошли 4-недельное испытание стабильности в стрессовых условиях: при 60°С, при 60°С/75%-ной относительной влажности и при 80°С/75%-ной относительной влажности без какой-либо трансформации твердого состояния.
В еще одном варианте осуществления, изобретение, таким образом, относится к выделенной Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, которая не испытывает никакой трансформации твердого состояния во время 4-недельного испытания стабильности в стрессовых условиях: при 60°С, при 60°С/75%-ной относительной влажности и при 80°С/75%-ной относительной влажности.
В другом варианте осуществления, это изобретение относится к кристаллической Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, или к ее смесям с другой стабильной кристаллической полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, определяемой в этом документе, для применения в терапии.
В конкретном варианте осуществления, это изобретение относится к кристаллической Форме С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, или к ее смесям с аморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты или с кристаллической Формой Х {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, определяемой в этом документе, для применения в терапии.
В еще одном аспекте, это изобретение относится к фармацевтической композиции, содержащей кристаллическую Форму С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты настоящего изобретения, или ее смесь с другой стабильной кристаллической полиморфной формой {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}уксусной кислоты, что определено в этом документе, вместе с фармацевтически приемлемым(ой) эксципиентом или средой для лекарства.
В конкретном варианте осуществления, это изобретение относится к фармацевтической композиции, содержащей кристаллическую Форму С {4-[(1R,3S)-3-((R)-1-нафталин-1-ил-этиламино)циклопентил]фенокси}ук