Способ получения пентаоксаспироалканов
Иллюстрации
Показать всеИзобретение относится к области органической химии, в частности к способу получения пентаоксаспироалканов общей формулы (1), заключающегося в том, что 1,1-1,1-бис(гидроперокси)циклоалканы (где циклоалкан - циклопентан, или циклогексан, или циклогептан, или циклооктан, или циклододекан) подвергают взаимодействию с формальдегидом в присутствии катализатора Sm(NO3)3·6H2O, и мольном соотношении 1,1-бис(гидроперокси)циклоалкан : формальдегид : Sm(NO3)3·6H2O = 10:20:(0.3-0.7), при комнатной температуре (20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч. Эти соединения могут найти применение в качестве препаратов, обладающих противомалярийной активностью. Выход пентаоксаспироалканов (1) составляет 65-97%. 1 табл., 1 пр.
Реферат
Предлагаемое изобретение относится к области органической химии, конкретно к способу получения пентаоксаспироалканов общей формулы (1):
Пентаоксаканы применяются в медицине в качестве препаратов, обладающих противомалярийной активностью (Hye-Sook Kim, Yasuharu Shibata, Yusuke Wataya, Kaoru Tsuchiya, Araki Masuyama, Masatomo Nojima // J. Med. Chem. - 1999. - Vol. 42. - p. 2604-2609).
Известен способ (Hye-Sook Kim, Yasuharu Shibata, Yusuke Wataya, Kaoru Tsuchiya, Araki Masuyama, Masatomo Nojima // J. Med. Chem. - 1999. - Vol.42. - p. 2604-2609) получения 1,2,4,5,7-пентаоксаканов формулы (2) с выходом 12% ацидолизом смеси 1-фенилциклопентена с перекисью водорода и бензальдегидом по схеме:
Известный способ не позволяет получать пентаоксаспироалканы общей формулы (1).
Известен способ (Kevin J. McCullough, Yoshihiro Ushigoe, Shogo Tanaka, Shin-ichi Kawamura, Araki Masuyama, Masatomo Nojiama // J. Chem. Soc., Perkin Trans. - 1998 - Vol. 1. - p. 3059-3064) получения производного 1,2,4,6,8-пентаоксакана формулы (3) с выходами 23-34% взаимодействием α-алкоксигидропероксидов с алифатическими альдегидами в условиях кислотного катализа с последующим добавлением формальдегида по схеме:
Известным способом не могут быть получены пентаоксаспироалканы общей формулы (1).
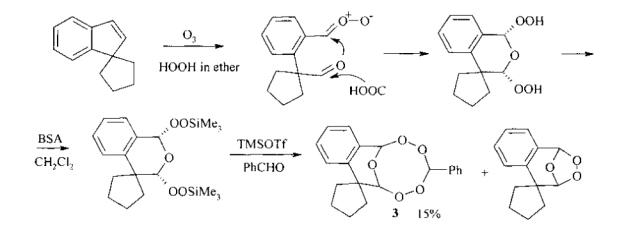
Известен способ (Hye-Sook Kim, Kaoru Tsuchiya, Yasuharu Shibata, Yusuke Wataya, Yoshihiro Ushigoe, Araki Masuyama, Masatomo Nojima, Kevin J. McCullough // J. Chem. Soc., Perkin Trans. - 1999 - Vol. 1. - p. 1867-1870) получения 1,2,4,5,7-пентаоксакана формулы (3) с выходом 15% озонолизом производного индена с образованием бис-гидропероксида, который превращают в бис-силилидизохроман, последний подвергают взаимодействию с бензальдегидом по схеме:
Таким образом, в литературе отсутствуют сведения о селективном получении пентаоксаспироалканов формулы (1).
Предлагается новый способ селективного получения пентаоксаспироалканов общей формулы (1).
Сущность способа заключается во взаимодействии 1,1-бис(гидроперокси)циклоалканов общей формулы (4) (где циклоалкан - циклопентан, или циклогексан, или циклогептан, или циклооктан, или циклододекан) с формальдегидом (CH2O) в присутствии катализатора Sm(NO3)3·6H2O или мольном соотношении 4:CH2O:Sm(NO3)3·6H2O=10:20:(0.3-0.7), предпочтительно 10:20:0.5 при комнатной температуре (~20°C) и атмосферном давлении в тетрагидрофуране (ТГФ) в качестве растворителя в течение 4-6 ч, предпочтительно 5 ч. Выход пентаоксаспироалканов (1) составляет 65-97%. Реакция протекает по схеме:
Пентаоксаспироалканы (1) образуются только лишь с участием формальдегида и 1,1-бис(гидроперокси)циклоалканов. В присутствии других альдегидов (например, уксусный альдегид, бензальдегид) целевые продукты (1) не образуются. Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3·6H2O больше 7 мол. % не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3·6H2O менее 3 мол. % снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°C. При температуре выше 20°C (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°C (например, -10°C) снижается скорость реакции.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве исходных соединений озонида, перекиси водорода, силильных производных, бензальдегида. Известный способ не позволяет получать пентаоксаспироалканы общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются 1,1-бис(гидроперокси)циклоалканы и формальдегид, а Sm(NO3)3·6H2O применяется в каталитических количествах. В отличие от известных способов, предлагаемый способ позволяет синтезировать индивидуальные пентаоксаспироалканы (1).
Способ поясняется следующими примерами
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, при температуре ~20°C помещают 5 мл тетрагидрофурана, 1.46 мл (20 ммоль) водного раствора (37%) формальдегида и 1.48 г (10 ммоль) 1,1-бис(гидроперокси)циклогексана, затем добавляют 0.062 г (0.5 ммоль) Sm(NO3)2·6H2O. Реакционную смесь перемешивают при температуре ~20°C в течение 5 ч, выделяют 7,8,10,12,13-пентаоксаспиро[5.7]тридекан с выходом 95%.
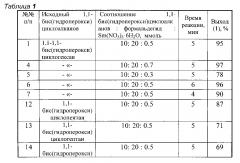
Другие примеры, подтверждающие способ, приведены в табл. 1.
Все опыты проводили в ТГФ при комнатной температуре (~20°C).
Спектральные характеристики 6,7,9,11,12-пентаоксаспиро[4.7]додекана: δН (400 MHz, DMSO-d6, 25°C) 1.62-1.66 (m, 4Н, Н2С), 1.86-1.89 (m, 4Н, Н2С), 5.04 (d, 4Н, J 4 Hz, ОН2СО); δС (100 MHz, CDCl3, 25°C) 24.42 (СН2СН2), 34.01 (СН2СН2), 92.31 (OCH2O), 119.90 (С). MALDI TOF, m/z: 175.165 [М-Н]+ (85%).
Спектральные характеристики 7,8,10,12,13-пентаоксаспиро[5.7]тридекана: δН (400 MHz, CDCl3, 25°C) 1.43-1.44 (m, 4Н, Н2С), 1.54-1.55 (m, 2Н, Н2С), 1.76-1.83 m, 4Н, Н2С), 5.17 (d, 4Н, J 12 Hz, ОН2СО); δС (100 MHz, CDCl3, 25°C) 22.35 (СН2СН2), 25.18 (СН2), 29.98 (СН2СН2), 92.30 (OCH2O), 109.98 (С). MALDI TOF, m/z: 212.387 [M+Na-H]+ (55%), m/z: 250.318 [M+Na+K-2H]+ (19%).
Спектральные характеристики 8,9,11,13,14-пентаоксаспиро[6.7]тетрадекана: δН (400 MHz, DMSO-d6, 25°С) 1.50-1.51 (m, 6Н, Н2С), 1.59-1.63 (m, 6Н, Н2С), 5.03 (d, 4Н, J 4 Hz, ОН2СО); δС (100 MHz, DMSO-d6, 25°C) 24.15 (СН2СН2), 30.14 (СН2СН2), 43.75 (СН2СН2), 92.08 (OCH2O), 113.90 (С). MALDI TOF, m/z: 203.758 [М-Н]+ (56%).
Спектральные характеристики 1,2,4,6,7-пентаоксаспиро[7.7]пентадекана: δН (400 MHz, DMSO-d6, 25°C) 1.45-1.51 (m, 4Н, Н2С), 1.77-1.79 (m, 10Н, Н2С), 5.01 (d, 4Н, J 4 Hz, ОН2СО); δС (100 MHz, DMSO-d6, 25°C) 25.57 (СН2СН2), 27.15 (СН2СН2СН2), 41.48 (СН2СН2), 92.25 (OCH2O), 113.05 (С). MALDI TOF, m/z: 217.245 [М-Н]+ (35%).
Спектральные характеристики 1,2,4,6,7-пентаоксаспиро[7.11]нонадекана: δН (400 MHz, DMSO-d6, 25°C) 1.45-1.51 (m, 22Н, Н2С); 5.03 (d, 4Н, J 4 Hz, ОН2СО); δС (100 MHz, DMSO-d6, 25°C) 24.97 (СН2СН2), 28.13 ((СН2СН2)8), 42.08 (СН2СН2), 92.33 (OCH2O), 113.25 (С). MALDI TOF, m/z: 273.357 [М-Н]+ (64%).
Способ получения пентаоксаспироалканов общей формулы (1): отличающийся тем, что 1,1-1,1-бис(гидроперокси)циклоалканы (где циклоалкан - циклопентан, или циклогексан, или циклогептан, или циклооктан, или циклододекан) подвергают взаимодействию с формальдегидом в присутствии катализатора Sm(NO3)3·6H2O и мольном соотношении 1,1-бис(гидроперокси)циклоалкан : формальдегид : Sm(NO3)3·6H2O = 10:20:(0.3-0.7), при комнатной температуре (20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч.