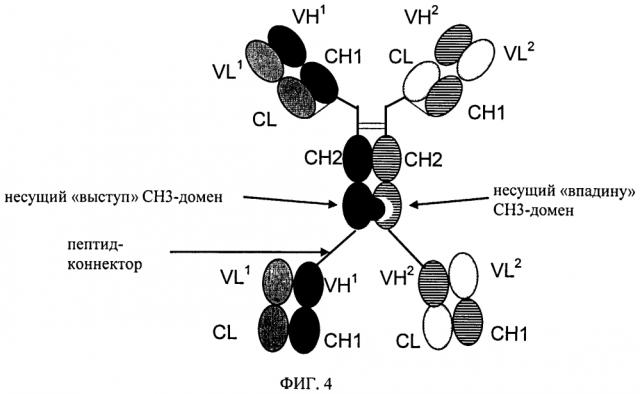
Биспецифические четырехвалентные антигенсвязывающие белки
Иллюстрации
Показать всеНастоящее изобретение относится к области биоинженерии и иммунологии. Предложен способ получения биспецифического антигенсвязывающего белка, включающего модифицированную тяжелую цепь первого антитела, которое специфически связывается с первым антигеном, С-конец которой дополнительно слит с N-концом VH-CH1 доменов первого антитела через пептидный коннектор; две легкие цепи первого антитела; модифицированную тяжелую цепь второго антитела, которое специфически связывается со вторым антигеном, в котором СН1-домен заменен на CL-домен второго антитела и С-конец дополнительно слит с N-концом VH-CL второго антитела через пептидный коннектор; и две модифицированные легкие цепи второго антитела, в которых CL-домен заменен на СН1-домен второго антитела, причем СН3-домены тяжелых цепей соприкасаются друг с другом по принципу "выступ-впадина" ("knobs-into-holes"). Также рассмотрена клетка-хозяин для получения указанного биспецифического антитела. Данное изобретение обеспечивает получение стабильных биспецифических антител с высоким выходом и может найти дальнейшее применение в разработке терапевтических тетравалентных антител. 2 н. и 2 з.п. ф-лы, 4 ил.
Реферат
Настоящее изобретение относится к биспецифическим четырехвалентным антигенсвязывающим белкам, способам их получения, фармацевтическим композициям, которые содержат указанные антитела, и их применению.
Предпосылки создания изобретения
В данной области известны сконструированные белки, такие как би- и мультиспецифические антитела, которые могут связываться с двумя или большим количеством антигенов. Указанные мультиспецифические связывающие белки можно создавать на основе методов клеточного слияния, химической конъюгации или рекомбинантной ДНК.
В последние годы создано широкое разнообразие форматов рекомбинантных мультиспецифических антител, например четырехвалентные биспецифические антитела, полученные путем слияния, например, антитела IgG-формата и одноцепочечных доменов (см., например, Coloma M.J. и др., Nature Biotech 15, 1997, cc.159-163; WO 001/077342 и Morrison S.L., Nature Biotech 25, 2007, cc.1233-1234).
Разработано также несколько других новых форматов, в которых уже не сохранялась основная структура антитела (IgA, IgD, IgE, IgG или IgM), таких как димерные (диабоди), тримерные (триабоди) или тетрамерные (тетрабоди) антитела, миниантитела, несколько одноцепочечных форматов (scFv, бис-scFv), которые могут связываться с двумя или большим количеством антигенов (Holliger Р. и др., Nature Biotech 23, 2005, cc.1126-1136; Fischer N., Léger О., Pathobiology 74, 2007, cc.3-14; Shen J и др., Journal of Immunological Methods 318, 2007, cc.65-74; Wu С. и др., Nature Biotech 25, 2007, cc.1290-1297).
Во всех указанных форматах используют линкеры либо для слияния основной структуры антитела (IgA, IgD, IgE, IgG или IgM) с дополнительным связывающим белком (например, scFv), либо для слияния, например, двух Fab-фрагментов или scFv (Fischer N., Léger О., Pathobiology 74, 2007, cc.3-14). Хотя очевидно, что линкеры дают преимущества при создании биспецифических антител, с ними могут быть связаны также проблемы терапевтического плана. Фактически эти чужеродные пептиды могут вызывать иммунный ответ против самого линкера или области стыка между белком и линкером. Кроме того, гибкая природа этих пептидов делает их более чувствительными к протеолитическому расщеплению, что может приводить к плохой стабильности, агрегации и повышенной иммуногенности антитела. Кроме того, может существовать необходимость в поддержании эффекторных функций, таких, например, как комплементзависимая цитотоксичность (CDC) или антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), которые опосредуются Fc-областью, путем сохранения высокой степени сходства с встречающимися в естественных условиях антителами.
Таким образом, в идеальном варианте необходимо создавать биспецифические антитела, структура которых очень сходна с общей структурой встречающихся в естественных условиях антител (типа IgA, IgD, IgE, IgG или IgM) и имеет минимальное отклонение от человеческих последовательностей.
В соответствии с одним из подходов биспецифические антитела с высокой степенью сходства со встречающимися в естественных условиях антителами создавали с помощью технологии квадром (квадрогибридом) (см. Milstein С. и А.С.Cuello, Nature, 305, 1983, cc.537-540) на основе соматического слияния двух различных клеточных линий гибридом, которые экспрессируют мышиные моноклональные антитела с требуемыми для биспецифического антитела специфичностями. В результате случайного спаривания тяжелых и легких цепей двух различных антител в образующейся линии клеток гибрида-гибридомы (или квадромы) получают вплоть до 10 различных видов антител, из которых только одно представляет собой требуемое функциональное биспецифическое антитело. Из-за присутствия полученных в результате ошибочного спаривания побочных продуктов и в значительной степени сниженного выхода продукта требуются более сложные процедуры очистки (см., например, Morrison S.L., Nature Biotech 25, 2007, cc.1233-1234). В целом эта же проблема, связанная с ошибочно спаренными побочными продуктами, сохраняется и при применении методов рекомбинантной экспрессии.
Подход, с помощью которого можно обойти проблему, связанную с полученными в результате ошибочных спариваний побочными продуктами, известный под названием «knobs-into-holes»-технология (взаимодействие по типу «выступ-впадина»), направлен на усиление спаривания тяжелых цепей двух различных антител путем интродукции мутаций в СН3-домены для модификации поверхности раздела в области контакта. На одной цепи имеющие большие размеры аминокислоты заменяли на аминокислоты с короткими боковыми цепями для создания «впадины». И, наоборот, аминокислоты с более крупными боковыми цепями интродуцировали в другой СН3-домен, создавая «выступ». Путем совместной экспрессии этих двух тяжелых цепей (и двух идентичных легких цепей, которые должны соответствовать обеим тяжелым цепям) достигали высоких выходов гетеродимерной конструкции («выступ-впадина») относительно гомодимерной конструкции («впадина-впадина» или «выступ-выступ») (Ridgway J. В. и др., Protein Eng. 9, 1996, cc.617-621; и WO 1996/027011). Процентное содержание гетеродимера можно дополнительно повышать путем ремоделирования поверхностей раздела двух СН3-доменов с помощью технологии фагового дисплея и интродукции дисульфидного мостика с целью стабилизации гетеродимеров (Merchant A.M и др., Nature Biotech 16, 1998, cc.677-681; Atwell S., Ridgway J.B., Wells J.A., Carter P., J Mol Biol 270, 1997, cc.26-35). Новые подходы к технологии «knobs-into-holes» описаны, например, в ЕР 1870459А1. Хотя указанный формат, вероятно, является очень привлекательным, в настоящее время отсутствуют данные о его усовершенствовании в направлении клинического применения. Одним из важных ограничений этой стратегии является то, что легкие цепи двух родительских антител должны быть идентичными для предупреждения ошибочного спаривания и формирования неактивных молекул. Таким образом, эта технология не пригодна в качестве основы для более легкого создания рекомбинантных биспецифических антител к двум антигенам с использованием в качестве исходных двух антител к первому и второму антигену, поскольку должны быть оптимизированы или тяжелые цепи этих антител, и/или идентичные легкие цепи. Такая же проблема, связанная с ошибочными спариваниями, сохраняется, когда вместо двухвалентных биспецифических антител экспрессируют четырехвалентные биспецифические антитела, например, посредством слияния дополнительных Fab-фрагментов (каждый из которых идентичен Fab-фрагменту соответствующего антитела, которое связывается с первым или вторым антигеном) с С-концом каждой тяжелой цепи гетеродимера (см. фиг.2).
В WO 2006/093794 описаны композиции гетеродимерных связывающих белков. В WO 99/37791 описаны многоцелевые производные антител. У Morrison и др., J. Immunolog, 160, 1998, cc.2802-2808 описано влияние замены вариабельных областей на функциональные свойства IgG.
Краткое изложение сущности изобретения
Настоящее изобретение относится к биспецифическому четырехвалентному антигенсвязывающему белку, содержащему:
а) модифицированную тяжелую цепь первого антитела, которое специфически связывается с первым антигеном, где С-конец указанной тяжелой цепи дополнительно слит с VH-CH1-доменами указанного первого антитела посредством их N-концов;
б) две легкие цепи первого антитела, указанного в подпункте а),
в) модифицированную тяжелую цепь второго антитела, которое специфически связывается со вторым антигеном,
в котором СН1-домен заменен на CL-домен указанного второго антитела,
и где С-конец указанной тяжелой цепи дополнительно слит с VH-CL-доменами указанного второго антитела посредством их N-концов; и
г) две модифицированные легкие цепи второго антитела, указанного в подпункте в),
в которых CL-домен заменен на СН1-домен указанного второго антитела.
Следующим вариантом осуществления изобретения является способ получения антигенсвязывающего белка, предлагаемого в изобретении, заключающийся в том, что
а) трансформируют клетку-хозяина
- векторами, которые содержат молекулы нуклеиновых кислот, кодирующие биспецифический антигенсвязывающий белок, предлагаемый в изобретении,
б) культивируют клетку-хозяина в условиях, которые позволяют синтезировать указанную молекулу антитела, и
в) выделяют молекулу антитела из культуры.
Следующим вариантом осуществления изобретения является клетка-хозяин, содержащая
- векторы, которые содержат молекулы нуклеиновых кислот, кодирующие антигенсвязывающий белок, предлагаемый в изобретении.
Следующим вариантом осуществления изобретения является фармацевтическая композиция, которая содержит антигенсвязывающий белок, предлагаемый в изобретении, и по меньшей мере один фармацевтически приемлемый эксципиент.
Следующим вариантом осуществления изобретения является способ лечения пациента, который нуждается в терапии, отличающийся тем, что вводят пациенту в терапевтически эффективном количестве антигенсвязывающий белок, предлагаемый в изобретении.
Согласно изобретению соотношение требуемого биспецифического четырехвалентного антигенсвязывающего белка и нежелательных побочных продуктов можно повышать путем замены СН1-домена на CL-домен в модифицированной тяжелой цепи, указанной в подпункте в), и в соответствующих двух модифицированных легких цепях, указанных в подпункте г). Таким путем можно снижать нежелательное ошибочное спаривание легких цепей антитела, которое специфически связывается с первым антигеном (указаны в подпункте б) с «несоответствующими» VH-CH1 -доменами модифицированных тяжелых цепей антитела (указаны в подпункте в), которое связывается со вторым антигеном. И аналогичным образом снижать ошибочное спаривание модифицированных легких цепей, указанных в подпункте г), с тяжелыми цепями, указанными в подпункте а), (см. фиг.2, на которой представлен вариант, в котором отсутствуют указанные модификации и присутствует ошибочное спаривание, и фиг.3, на которой представлен вариант, в котором присутствуют замены (или обмены) СН1-CL и отсутствует ошибочное спаривание).
Подробное описание изобретения
Настоящее изобретение относится к биспецифическому четырехвалентному антигенсвязывающему белку, содержащему:
а) модифицированную тяжелую цепь первого антитела, которое специфически связывается с первым антигеном,
где С-конец указанной тяжелой цепи дополнительно слит посредством пептида-коннектора с N-концами VH-CH1-доменов указанного первого антитела;
б) две легкие цепи первого антитела, указанного в подпункте а),
в) модифицированную тяжелую цепь второго антитела, которое специфически связывается со вторым антигеном,
в котором СН1-домен заменен на CL-домен указанного второго антитела, и где С-конец указанной тяжелой цепи дополнительно слит посредством пептида-коннектора с N-концами VH- CL-доменов указанного второго антитела, и
г) две модифицированные легкие цепи второго антитела, указанного в подпункте в),
в которых CL-домен заменен на СН1-домен указанного второго антитела. Согласно изобретению соотношение требуемого биспецифического четырехвалентного антигенсвязывающего белка и нежелательных побочных продуктов (полученных в результате ошибочного спаривания легких цепей антитела и «несоответствующих» тяжелых цепей антитела) можно повышать путем замены СН1-домена на CL-домен в модифицированной тяжелой цепи указанной в подпункте в), и в соответствующих двух модифицированных легких цепях, указанных в подпункте г). В этом плане ошибочное спаривание означает ассоциацию I) легких цепей антитела, которое специфически связывается с первым антигеном, указанных в подпункте б), с модифицированной тяжелой цепью антитела, которое специфически связывается со вторым антигеном; или II) легких цепей антитела, которое специфически связывается со вторым антигеном, указанных в подпункте б), с модифицированной тяжелой цепью антитела, которое специфически связывается с первым антигеном (см. фиг.2), что приводит к образованию нежелательных неактивных или не полностью функциональных побочных продуктов.
Согласно дополнительному объекту изобретения такое улучшенное соотношение между требуемым биспецифическим четырехвалентным антителом и нежелательными побочными продуктами можно еще более улучшать путем осуществления модификаций СН3-доменов указанных антител, которые обладают способностью специфически связываться с первым и вторым антигенами.
Таким образом, в одном из предпочтительных вариантов осуществления изобретения СН3-домены (в модифицированных тяжелых цепях, указанных в подпунктах а) и в)) указанного биспецифического четырехвалентного антигенсвязывающего белка, предлагаемого в изобретении, можно изменять с помощью технологии «knob-into-holes», которая подробно описана на нескольких примерах, например, в WO 96/027011, у Ridgway J.B. и др., Protein Eng 9, 1996, cc.617-621; и у Merchant A.M. и др., Nat Biotechnol 16, 1998, cc.677-681. При использовании этого метода взаимодействующие поверхности двух СН3-доменов изменяют с целью повышения уровня гетеродимеризации обеих тяжелых цепей, содержащих эти два СН3-домена. Каждый из двух СН3-доменов (двух тяжелых цепей) может представлять собой «выступ», а другой представлять собой «впадину». Введение дисульфидного мостика дополнительно стабилизирует гетеродимеры (Merchant A.M, и др., Nature Biotech 16, 1998, cc.677-681; Atwell S. и др., J Mol Biol 270, 1997, cc.26-35) и повышает выход продукта.
Таким образом, согласно одному из объектов изобретения биспецифический четырехвалентный антигенсвязывающий белок дополнительно отличается тем, что
СН3-домен модифицированной тяжелой цепи антитела, указанной в подпункте а), и СН3-домен модифицированной тяжелой цепи антитела, указанной в подпункте б), каждый соприкасается друг с другом на поверхности раздела, которая представляет собой исходную поверхность раздела между СН3-доменами антитела;
- при этом поверхность раздела изменена для стимулирования формирования биспецифического четырехвалентного антигенсвязывающего белка, где изменение отличается тем, что:
I) СН3-домен одной тяжелой цепи изменен
так, что на исходной поверхности раздела СН3-домена одной тяжелой цепи, которая соприкасается с исходной поверхностью раздела СН3-домена другой тяжелой цепи в биспецифическом четырехвалентном антигенсвязывающем белке,
аминокислотный остаток заменен на аминокислотный остаток, который имеет большую по объему боковую цепь, создавая тем самым «выпуклость» на поверхности раздела СН3-домена одной тяжелой цепи, которая может помещаться в «полость» на поверхности раздела СН3-домена другой тяжелой цепи,
и
II) СН3-домен другой тяжелой цепи изменен
так, что на исходной поверхности раздела второго СН3-домена, которая соприкасается с исходной поверхностью раздела первого СН3-домена в биспецифическом четырехвалентном антигенсвязывающем белке,
аминокислотный остаток заменен на аминокислотный остаток, который имеет меньшую по объему боковую цепь, создавая тем самым «полость» на поверхности раздела второго СН3-домена, в которую может помещаться «выпуклость» на поверхности раздела первого СН3-домена.
Предпочтительно указанный аминокислотный остаток, который имеет большую по объему боковую цепь, выбирают из группы, включающей аргинин (R), фенилаланин (F), тирозин (Y), триптофан (W).
Предпочтительно указанный аминокислотный остаток, который имеет меньшую по объему боковую цепь, выбирают из группы, включающей аланин (А), серин (S), треонин (Т), валин (V).
Согласно одному из объектов изобретения оба СН3-домена дополнительно изменяют путем интродукции цистеина (С) в качестве аминокислоты в соответствующие положения каждого СН3-домена таким образом, чтобы мог образоваться дисульфидный мостик между обоими СН3-доменами.
В одном из предпочтительных вариантов осуществления изобретения биспецифический четырехвалентный антигенсвязывающий белок содержит мутацию T366W в СН3-домене имеющей «выступ» цепи («knobs-цепь») и мутации T366S, L368A, Y407V в СН3-домене имеющей «впадину» цепи («hole-цепь»), Можно применять также дополнительный связывающий цепи дисульфидный мостик между СН3-доменами (Merchant A.M. и др., Nature Biotech. 16, 1998, cc.677-681), например, путем интродукции мутации Y349C в СН3-домен имеющей «выступ» или «впадину» цепи и мутации Е356С или мутации S354C в СН3-домен другой цепи. Так, в другом предпочтительном варианте осуществления изобретения указанный биспецифический четырехвалентный антигенсвязывающий белок имеет мутации S354C, T366W в одном из двух СН3-доменов и мутации Y349C, T366S, L368A, Y407V во втором из двух СН3-доменов, или указанный биспецифический четырехвалентный антигенсвязывающий белок имеет мутации Е356С, T366W в одном из двух СН3-доменов и мутации Y349C, T366S, L368A, Y407V во втором из двух СН3-доменов, или указанный биспецифический четырехвалентный антигенсвязывающий белок имеет мутации Y349C, T366W в одном из двух СН3-доменов и мутации Е356С, T366S, L368A, Y407V во втором из двух СН3-доменов, или указанный биспецифический четырехвалентный антигенсвязывающий белок имеет мутации Y349C, T366W в одном из двух СН3-доменов и мутации S354C, T366S, L368A, Y407V во втором из двух СН3-доменов (дополнительная мутация Y349C в одном из СН3-доменов и дополнительная мутация Е356С или S354C во втором СН3-домене образуют расположенный между цепями дисульфидный мостик) (нумерация во всех случаях соответствует нумерации EU по Кэботу). В альтернативном варианте или дополнительно можно применять также и другие технологии «knobs-in-holes»-типа, описанные в ЕР 1870459А1. Предпочтительным примером мутаций для рассматриваемого триспецифического или тетраспецифического антитела являются мутации R409D; К370Е в СН3-домене имеющей «выпуклость» цепи и мутации D399K; Е357К в СН3-домене имеющей «впадину» цепи (нумерация во всех случаях соответствует нумерации EU по Кэботу).
В другом предпочтительном варианте осуществления изобретения триспецифическое или тетраспецифическое антитело содержит мутацию T366W в СН3-домене имеющей «выпуклость» цепи и мутации T366S, L368A, Y407V в СН3-домене имеющей «впадину» цепи и дополнительные мутации R409D; К370Е в СН3-домене имеющей «выпуклость» цепи и мутации D399K; Е357К в СН3-домене имеющей «впадину» цепи.
В следующем предпочтительном варианте осуществления изобретения триспецифическое или тетраспецифическое антитело содержит мутации Y349C, T366W в одном из двух СН3-доменов и мутации S354C, T366S, L368A, Y407V во втором из двух СН3-доменов, или указанное триспецифическое или тетраспецифическое антитело содержит мутации Y349C, T366W в одном из двух СН3-доменов и мутации S354C, T366S, L368A, Y407V во втором из двух СН3-доменов и дополнительно содержит мутации R409D; К370Е в СН3-домене имеющей «выпуклость» цепи и мутации D399K; Е357К в СН3-домене имеющей «впадину» цепи.
В контексте настоящего описания понятие «антитело» относится к полноразмерному антителу, состоящему из двух тяжелых цепей антитела и двух легких цепей антитела (см. фиг.1). Тяжелая цепь полноразмерного антитела представляет собой полипептид, который содержит в направлении от N-конца к С-концу вариабельную область (домен) тяжелой цепи антитела (VH), домен 1 константной области тяжелой цепи антитела (СН1), шарнирную область антитела (HR), домен 2 константной области тяжелой цепи антитела (СН2) и домен 3 константной области тяжелой цепи антитела (СН3), что сокращенно обозначают как VH-CH1-HR-CH2-CH3; и необязательно домен 4 константной области тяжелой цепи антитела (СН4) в случае антитела подкласса IgE. Предпочтительно тяжелая цепь полноразмерного антитела представляет собой полипептид, который содержит в направлении от N-конца к С-концу VH, CH1, HR, СН2 и СН3. Легкая цепь полноразмерного антитела представляет собой полипептид, который содержит в направлении от N-конца к С-концу вариабельную область (домен) легкой цепи антитела (VL) и константную область легкой цепи антитела (CL), что сокращенно обозначают как VL-CL. Константная область легкой цепи антитела (CL) может относиться к κ-(каппа)-типу или λ-(лямбда)-типу. Цепи антитела связаны друг с другом посредством расположенных между полипептидами дисульфидных мостиков, которые находятся между CL-доменом и СН1-доменом (т.е. между легкой и тяжелой цепью) и между шарнирными областями тяжелых цепей полноразмерного антитела. Примерами типичных полноразмерных антител являются встречающиеся в естественных условиях антитела типа IgG (например, IgG1 и IgG2), IgM, IgA, IgD и IgE). Антитела, предлагаемые в изобретении, могут иметь происхождение из одного вида, например человеческие антитела, или они могут представлять собой химерные или гуманизированные антитела. Полноразмерные антитела, предлагаемые в изобретении, содержат два антигенсвязывающих центра, каждый из которых образован парой VH- и VL-областей, которые оба специфически связываются с одним и тем же (первым) антигеном. С-конец тяжелой или легкой цепи указанного полноразмерного антитела обозначает последнюю аминокислоту на С-конце указанной тяжелой или легкой цепи. Указанное антитело содержит два идентичных Fab-фрагмента, которые состоят из VH- и CH1-домена тяжелой цепи и VL- и CL-домена легкой цепи (см. фиг.1).
В антигенсвязывающем белке, предлагаемом в изобретении, СН1- и CL-домены второго антитела, которое специфически связывается со вторым антигеном, заменены друг на друга, что приводит к получению модифицированных легких цепей, указанных в подпункте г), и модифицированных тяжелых цепей, указанных в подпункте в), где С-конец указанной тяжелой цепи дополнительно слит посредством пептида-коннектора с N-концами VH-CL-доменов указанного антитела (которое специфически связывается со вторым антигеном).
Понятие «VH-CH1-домены» указанного антитела (которое специфически связывается с первым антигеном) относится к VH- и СН1-доменам антитела, расположенным в направлении от N-конца к С-концу. А понятие «VH-CL-домены» указанного антитела (которое специфически связывается со вторым антигеном) относится к VH- и СН1-доменам антитела, расположенным в направлении от N-конца к С-концу.
В контексте настоящего изобретения понятие «пептид-коннектор» обозначает пептид, аминокислотные последовательности которого предпочтительно являются синтетическими. Такие пептиды-коннекторы, предлагаемые в изобретении, применяют для слияния антигенсвязывающих пептидов с С- или N-концом цепей полноразмерного и/или модифицированного полноразмерного антитела с образованием биспецифического антигенсвязывающего белка, предлагаемого в изобретении. Предпочтительно пептиды-коннекторы, указанные в подпункте в), представляют собой пептиды, аминокислотная последовательность которых состоит по меньшей мере из 5 аминокислот, предпочтительно состоит из 5-100, более предпочтительно из 10-50 аминокислот.В одном из вариантов осуществления изобретения пептид-коннектор представляет собой конструкцию (GxS)n или (GxS)nGm, где G обозначает глицин, S обозначает серин и (х=3, n=3, 4, 5 или 6 и m=0, 1, 2 или 3) или (х=4, n=2, 3, 4 или 5 и m=0, 1, 2 или 3), предпочтительно х=4 и n=2 или 3, более предпочтительно х=4, n=2. В одном из вариантов осуществления изобретения пептид-коннектор представляет собой конструкцию (G4S)2.
В контексте настоящего описания понятия «сайт связывания» или «антигенсвязывающий центр» обозначают область(и) антигенсвязывающего белка, предлагаемого в изобретении, с которой(ыми) фактически связывается лиганд (например, антиген или фрагмент антигена) и который выведен из молекулы антитела или его фрагмента (например, Fab-фрагмента). Согласно изобретению антигенсвязывающий центр включает вариабельный домен тяжелой цепи антитела (VH) и вариабельный домен легкой цепи антитела (VL) или фрагмента антитела, который специфически связывается с требуемым антигеном.
Антигенсвязывающие центры (т.е. пары VH/VL), обладающие способностью специфически связываться с требуемым антигеном, можно выводить из а) известных антител к антигену или б) новых антител или фрагментов антител, полученных de novo с помощью методов иммунизации с использованием, среди прочего, либо белка, либо нуклеиновой кислоты антигена или его фрагментов, или с помощью метода фагового дисплея.
Антигенсвязывающий центр антигенсвязывающего белка, предлагаемого в изобретении, содержит шесть гипервариабельных участков (CDR), которые вносят различный вклад в аффинность сайта связывания с антигеном. Они представляют собой три вариабельных домена (CDR-участки) тяжелой цепи (CDRH1, CDRH2 и CDRH3) и три вариабельных домена (CDR-участки) легкой цепи (CDRL1, CDRL2 и CDRL3). Размер CDR и каркасных участков (FR) определяют путем сравнения с компилированной базой данных аминокислотных последовательностей, в которых такие участки были определены на основе вариабельности последовательностей.
Специфичность антитела характеризует избирательное распознавание антителом конкретного эпитопа антигена. Например, встречающиеся в естественных условиях антитела являются моноспецифическими. Биспецифические антитела представляют собой антитела, которые обладают специфичностью связывания с двумя различными антигенами. Когда антитело имеет более одной специфичности, то распознаваемые эпитопы могут быть ассоциированы с одним антигеном или с несколькими антигенами.
В контексте настоящего описания понятие «моноспецифическое» антитело или «моноспецифический» антигенсвязывающий белок обозначает антитело или антигенсвязывающий белок, которое/который имеет один или несколько сайтов связывания, каждый из которых связывается с одним и тем же эпитопом одного и того же антигена.
В контексте настоящего описания понятие «валентность» означает наличие определенного количества сайтов связывания в молекуле антитела. Например, встречающееся в естественных условиях антитело или полноразмерное антитело, предлагаемое в изобретении, имеет два сайта связывания и является двухвалентным. Таким образом, понятие «четырехвалентный» означает наличие четырех сайтов связывания в антигенсвязывающем белке. В контексте настоящего описания понятие «биспецифический четырехвалентный» обозначает антигенсвязывающий белок, предлагаемый в изобретении, который имеет четыре антигенсвязывающих центра, два из которых связываются с первым антигеном и два связываются со вторым антигеном (или другим эпитопом антигена). Антигенсвязывающие белки, предлагаемые в настоящем изобретении, имеют четыре сайта связывания и являются четырехвалентными.
Полноразмерные антитела, предлагаемые в изобретении, содержат константные области иммуноглобулина из одного или нескольких классов иммуноглобулинов. Классы иммуноглобулинов включают изотипы IgG, IgM, IgA, IgD и IgE, а в случае IgG и IgA, также их подтипы. В предпочтительном варианте осуществления изобретения полноразмерное антитело, предлагаемое в изобретении, имеет структуру константного домена, которая соответствует структуре антитела IgG-типа.
В контексте настоящего описания понятия «моноклональное антитело» или «композиция моноклонального антитела» относятся к препарату антитела или молекулам антитела или антигенсвязывающего белка одинакового аминокислотного состава.
Понятие «химерное антитело» относится к антителу, содержащему вариабельную область, т.е. связывающую область, полученную из одного и того же источника или из одних и тех же видов, и по меньшей мере часть константной области, полученную из другого источника или других видов, и его, как правило, получают с использованием методов рекомбинантной ДНК. Предпочтительными являются химерные антитела, которые содержат мышиную вариабельную область и человеческую константную область. Другими предпочтительными формами «химерных антител», подпадающих под объем настоящего изобретения, являются антитела, константная область которых модифицирована или изменена по сравнению с исходным антителом с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания Fc-рецептора (FcR). Такие химерные антитела обозначают также как «антитела переключенного класса». Химерные антитела являются продуктом экспрессии генов иммуноглобулинов, содержащих сегменты ДНК, которые кодируют вариабельные области иммуноглобулинов, и сегменты ДНК, которые кодируют константные области иммуноглобулинов. Методы получения химерных антител включают обычные методы рекомбинантной ДНК и генной трансфекции, которые хорошо известны в данной области (см., например, Morrison S.L. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc.6851-6855; US 5202238 и US 5204244).
Понятие «гуманизированное антитело» относится к антителам, в которых каркасные или «гипервариабельные участки» (CDR) модифицированы так, что они содержат CDR иммуноглобулина другой специфичности по сравнению со специфичностью родительского иммуноглобулина. В предпочтительном варианте осуществления изобретения для получения «гуманизированного антитела» мышиный CDR трансплантируют в каркасный участок человеческого антитела (см., например, Riechmann L. и др., Nature 332, 1988, cc.323-327; и Neuberger M.S. и др., Nature 314, 1985, cc.268-270). Наиболее предпочтительные CDR соответствуют участкам, которые имеют последовательности, распознающие антигены, указанные выше для химерных антител. Другими формами «гуманизированных антител», подпадающих под объем настоящего изобретения, являются антитела, константная область которых дополнительно модифицирована или изменена по сравнению с исходным антителом с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания Fc-рецептора (FcR).
Понятие «человеческое антитело» в контексте настоящего описания относится к антителам, вариабельные и константные области которых выведены из последовательностей иммуноглобулина человеческой зародышей линии. Человеческие антитела хорошо известны в данной области (van Dijk M.A. и van de Winkel J.G., Curr. Opin. Chem. Biol. 5, 2001, cc.368-374). Человеческие антитела можно получать также в трансгенных животных (например, мышах), которые в результате иммунизации могут продуцировать полный спектр или определенную часть человеческих антител при отсутствии производства эндогенного иммуноглобулина. Перенос набора генов иммуноглобулинов человеческой зародышевой линии в такую мутантную мышиную зародышевую линию должен приводить к производству человеческих антител после антигенной стимуляции (см., например, Jakobovits А., и др., Proc. Natl. Acad. Sci. USA 90, 1993, cc.2551-2555; Jakobovits А. и др., Nature 362, 1993, cc.255-258; Bruggemann M. и др., Year Immunol. 7, 1993, cc.33-40). Человеческие антитела можно получать также с помощью фаговых дисплейных библиотек (Hoogenboom H.R. и Winter G., J. Mol. Biol. 227, 1992, cc.381-388; Marks J.D. и др., J. Mol. Biol. 222, 1991, cc.581-597). Для получения человеческих моноклональных антител можно использовать также методы, разработанные Cole с соавторами и Boerner с соавторами (Cole и др., Monoclonal Antibodies and Cancer Therapy, под ред. Alan R. Liss, 1985, с.77; и Boerner Р. и др., J. Immunol. 147, 1991, cc.86-95).
Как уже было отмечено для химерных и гуманизированных антител, предлагаемых в изобретении, понятие «человеческое антитело» включает также такие антитела, константная область которых модифицирована с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания FcR, например, путем «переключения класса», т.е. замены или мутации Fc-областей (например, IgG1 на IgG4 и/или IgG1/IgG4-мутация).
Понятие «рекомбинантное человеческое антитело» в контексте настоящего описания относится ко всем человеческим антителам, которые получают, экспрессируют, создают или выделяют с помощью методов рекомбинации, например к антителам, выделенным из клетки-хозяина, такой как NS0- или СНО-клетка, или из животного (например, мыши), которое является трансгенным из-за присутствия человеческих генов иммуноглобулинов или антител, экспрессируемых с использованием рекомбинантного экспрессионного вектора, которым трансфектирована клетка-хозяин. Такие рекомбинантные человеческие антитела имеют вариабельную и константную области, которые находятся в преобразованной форме. Рекомбинантные человеческие антитела, предлагаемые в изобретении, подвергают соматической гипермутации in vivo. Таким образом, аминокислотные последовательности VH- и VL-областей рекомбинантных антител представляют собой последовательности, которые, хотя и выведены из последовательностей VH и VL человеческой зародышевой линии и родственных им линий, могут не существовать в естественных условиях в спектре зародышевой линии человеческих антител in vivo.
Понятие «вариабельная область (домен)» (вариабельный домен легкой цепи (VL), вариабельный домен тяжелой цепи (VH)) в контексте настоящего описания относится к областям каждой из пары легких и тяжелых цепей, которые участвуют непосредственно в связывании антитела с антигеном. Домены вариабельных человеческих легких и тяжелых цепей имеют одинаковую общую структуру, и каждый домен содержит четыре каркасных участка (FR), последовательности которых являются весьма консервативными, связанных тремя «гипервариабельными участками» (или определяющими комплементарность участками, CDR). Каркасные участки адоптированы к β-складчатой конформации, а CDR могут образовывать петли, соединяющие β-складчатую структуру. CDR в каждой цепи сохраняют их трехмерную структуру с помощью каркасных участков и образуют вместе с CDR из других цепей антигенсвязывающий центр. CDR3-участки тяжелых и легких цепей антитела играют особенно важную роль в специфичности связывания/аффинности антител, предлагаемых в изобретении, и поэтому являются дополнительным объектом изобретения.
Понятия «гипервариабельный участок» или «антигенсвязывающий центр антитела» в контексте настоящего описания относятся к аминокислотным остаткам антитела, которые ответственны за связывания антигена. Гипервариабельный участок содержит аминокислотные остатки из «определяющих комплементарность участков» или «CDR». «Каркасные» или «FR»-участки представляют собой участки вариабельной области, отличные от указанных в настоящем описании остатков гипервариабельного участка. Таким образом, легкие и тяжелые цепи антитела содержат в направлении от N- к С-концу участки FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. CDR каждой цепи разделены аминокислотами указанного каркасного участка. В частности, CDR3 тяжелой цепи представляют собой участок, который вносит наибольший вклад в связывание с антигеном. CDR- и FR-участки определяют с помощью стандартной номенклатуры Кэбота (Kabat и др., Sequences of Proteins of Immunological Interest, 5-изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD (1991).
В контексте настоящего описания понятия «связывание», «специфическое связывание» или «который специфически связывается с» относятся к связыванию антитела с эпитопом антигена, что определяют путем анализа in vitro, предпочтительно с помощью анализа резонанса поверхностного плазмона (BIAcore-анализ, фирма GE-Healthcare, Уппсала, Швеция) с использованием очищенного антигена дикого типа. Аффинность связывания характеризуют с помощью понятий ka (константа скорости ассоциации антитела (либо антитела, либо антигенсвязывающего белка) при формировании комплекса антитело/антиген), kD (константа диссоциации) и kD (kD/ka). Наличие связывания или специфического связывания означает, что аффиность связывания (КD) составляет 10-8 моль/л или менее, предпочтительно от 10-9 до 10-13 моль/л. Так, биспецифический антигенсвязывающий белок, предлагаемый в изобретении, специфически связывается с каждым антигеном, в отношении которого он обладает специфичностью, что характеризуется аффинностью связывания (КD), составляющей 10-8 моль/л или менее, предпочтительно от 10-9 до 10-13 моль/л.
Связывание антитела с FcγRIII можно оценивать с помощью BIAcore-анализа (фирма GE-Healthcare, Уппсала, Швеция). Аффинность связывания определяют с помощью понятий ka (константа скорости ассоциации антитела при формировании комплекса антитело/антиген), kD (константа диссоциации) и КD (kD/ka).
Понятие «эпитоп» включает любую полипептидную детерминанту, обладающую способностью специфически связываться с антителом. В некоторых вариантах осуществления изобретения эпитопная детерминанта включает химически активные поверхностные группы молекул, такие как аминокислоты, боковые цепи сахаров, фосфорил или сульфонил, и в некоторых вариантах осуществления изобретения они могут иметь специфические трехмерные структурные характеристики и/или специфические характеристики заряда. Эпитоп представляет собой область антигена, с которой связывается антитело.
В некоторых вариантах осуществления изобретения считается, что антитело специфически связывается с антигеном, когда оно преимущественно распознает свой антиген-мишень в сложной смеси белков и/или макромолекул.
В другом варианте осуществления изобретения б