Пиразолохинолиновое производное
Иллюстрации
Показать всеИзобретение относится к соединению, представленному формулой (I), или к его фармакологически приемлемой соли, где R1 является атомом водорода; R2 является ароматической кольцевой группой, определенной в формуле изобретения, R3 является атомом водорода или фтора, R4 является атомом водорода; R5 является оксепанильной группой и т.д.; R6 является атомом водорода. Заявленное соединение обладает PDE9-ингибирующим действием. Поэтому возможно повышение концентрации внутримозгового cGMP. PDE9-ингибирующее действие и повышение cGMP приводит к улучшению протекания обучения и развития памяти. Соединение формулы (I) может применяться в качестве терапевтического средства от когнитивных дисфункций при болезни Альцгеймера. 12 н. и 7 з.п. ф-лы, 1 ил., 12 табл., 63 пр.
Реферат
Область техники
[0001] Настоящее изобретение относится к пиразолохинолиновым производным, обладающим ингибирующей активностью в отношении фосфодиэстеразы 9 (PDE9), и их фармакологически приемлемым солям, и их фармацевтическим применениям.
Предшествующий уровень техники
[0002] Известно, что циклический гуанозинмонофосфат (далее по тексту называемый cGMP), функционирующий в качестве вторичного мессенджера в клетках, играет важную роль в различных физиологических функциях, в том числе в протекании обучения и развитии памяти.
[0003] На постсинаптическом участке нервных цепей головного мозга монооксид азота (далее по тексту называемый NO), биосинтезируемый синтетазой монооксида азота, активирует гуанилатциклазу, которая является cGMP-синтазой. Активированная гуанилатциклаза биосинтезирует cGMP из гуанозинтрифосфата. cGMP активирует cGMP-зависимую протеинкиназу (далее по тексту называемую PKG), фосфорилирующую различные белки, участвующие в пластичности синапсов. Известно, что активация каскада NO/cGMP/PKG участвует в индукции пластичности синапсов (долговременная потенциация; далее по тексту называемая LTP) гиппокампа, который известен как нейронная основа для протекания обучения и развития памяти (например, см. непатентную литературу 1). Лекарственный препарат, активирующий передачу сигнала по каскаду, известен как улучшающий LTP гиппокампа и протекание обучения у животных, в то же время лекарственный препарат, ингибирующий каскад, известен как оказывающий противоположное действие (непатентная литература 2). Следовательно, исходя из этих фактов, ожидается, что повышение cGMP в головном мозге приведет к улучшению протекания обучения и развитию памяти.
[0004] cGMP метаболизируется до 5′-GMP без PKG-активирующего действия фосфодиэстеразой (далее по тексту называемой PDE). PDE, как известно, имеет 11 семейств, и известно, что PDE9 специфично метаболизирует cGMP и должен экспрессироваться в головном мозге, селезенке, тонком кишечнике и т.п. (например, см. непатентную литературу 3). То есть, ожидается, что ингибирование PDE9 повысит cGMP в головном мозге. Согласно опубликованным данным, ингибитор PDE9 фактически усиливает LTP гиппокампа и улучшает протекание обучения и развитие памяти в тесте по распознанию нового объекта/тесте обучения пассивному избеганию или др. у животных (непатентная литература 4). С клинической точки зрения активность гуанилатциклазы уменьшается, и наблюдают возможность уменьшения уровня cGMP в верхней височной доле у пациентов с болезнью Альцгеймера (непатентная литература 5). Таким образом, есть вероятность, что PDE9 имеет множество тесных взаимосвязей с патологиями нейродегенеративных заболеваний и психиатрических заболеваний, в частности, с патологиями когнитивных дисфункций и др. при болезни Альцгеймера, таких как болезнь Александера, синдром Альперса, болезнь Альцгеймера, латеральный амиотрофический склероз (ALS; известный как болезнь Лу Герига или болезнь двигательного нейрона), атаксия-телеангиэктазия, болезнь Баттена (также известная как болезнь Шпильмайера-Фогта-Баттена), деменция Бинсвангера (субкортикальная ангиосклеротическая энцефалопатия), биполярное расстройство, губчатая энцефалопатия крупного рогатого скота (BSE), болезнь Канавана, индуцированная химиотерапией деменция, синдром Коккейна, кортико-базальная дегенерация, болезнь Крейтцфельда-Якоба, депрессия, синдром Дауна, дегенерация лобно-височной доли (в том числе лобно-височная деменция, семантическая деменция и прогрессирующая экспрессивная афазия), болезнь Герстманна-Штреусслера-Шейнкера, глаукома, болезнь (хорея) Хантингтона, связанная с ВИЧ деменция, гиперкинез, болезнь Кеннеди, корсаковский синдром (конфабуляторный амнестический синдром), болезнь Краббе, деменция с тельцами Леви, прогрессирующая логопеническая афазия, болезнь Мачадо-Джозефа (спинально-церебеллярная атаксия 3 типа), рассеянный склероз, мультисистемная атрофия (оливомостомозжечковая атрофия), тяжелая миастения, болезнь Паркинсона, синдром Пелицеуса-Мерцбахера, синдром Пика, старческий склероз мозга (легкое когнитивное нарушение), первичный латеральный склероз, первичная прогрессирующая афазия, вызванная облучением деменция, синдром Рефсума (заболевание, вызванное накоплением фитановой кислоты), болезнь Сандгоффа, болезнь Шильдера, шизофрения, семантическая деменция, сенильная деменция, синдром Шая-Дрейджера, спинально-церебеллярная атаксия, атрофия остистой мышцы, болезнь Стила-Ричардсона-Ольшевского (прогрессирующий надъядерный паралич), и сосудистый амилоидоз, и сосудистая деменция (мультиинфарктная деменция).
[0005] Недавно стало известно следующее соединение, которое обладает PDE9-ингибирующей активностью и предназначено для предупреждения или терапии болезни Альцгеймера (патентная литература 1).
[0006] Приведенное выше соединение представляет собой пиразолопиримидиновое производное, и при этом соединение имеет структуру, абсолютно отличную от пиразолохинолинового каркаса.
[0007] С другой стороны, в качестве соединения с пиразолохинолиновым каркасом известно следующее описанное в патентной литературе 2 соединение:
,
где кольцо A является бензольным кольцом или т.п.; а R6 является прямой связью или т.п.
Тем не менее, кольцо B в вышеприведенном соединении означает бензольное кольцо или т.п. Хотя сообщают, что вышеупомянутое соединение обладает ингибирующей активностью в отношении PDE4 и его используют при различных типах воспалительных заболеваний, нет ни описания, ни косвенного указания на ингибирующую активность в отношении PDE9 и т.п.
[0008] В качестве соединений, обладающих PDE9-ингибирующей активностью, известны следующие описанные в патентной литературе 3 и патентной литературе 4 соединения.
[0009] Любое из вышеупомянутых соединений является хиноксалиновым производным и является соединением со структурой, абсолютно отличной от пиразолохинолинового каркаса.
[0010] В качестве соединения с пиразолохинолиновым каркасом и PDE9-ингибирующей активностью известно следующее описанное в патентной литературе 5 соединение:
,
где либо R1, либо R2 является группой, представленной формулой
[0011] Структура приведенного выше соединения ограничена по R1 и R2, таким образом, соединение является соединением со структурой, абсолютно отличной от соединения по настоящему изобретению.
Список противопоставленных материалов
Патентная литература
[0012]
[патентная литература 1] WO 2008/139293
[патентная литература 2] WO 2007/032466
[патентная литература 3] WO 2008/072779
[патентная литература 4] WO 2010/101230
[патентная литература 5] WO 2012/033144
Непатентная литература
[0013]
[Непатентная литература 1] Domek-Lopacinska et al., "Cyclic GMP metabolism and its role in brain physiology", J Physiol Pharmacol., vol. 56, Suppl 2: pp. 15-34, 2005;
[Непатентная литература 2] Wang X., "Cyclic GMP-dependent protein kinase and cellular signaling in the nervous system", J. Neurocem., vol. 68, pp. 443-456, 1997;
[Непатентная литература 3] Fisher et al., "Isolation and characterization of PDE9A, a novel human cGMP-specific phosphodiesterase", J. Biol. Chem., vol. 273: pp. 15559-15564, 1998;
[Непатентная литература 4] van der Staay et al., "The novel selective PDE9 inhibitor BAY 73-6691 improves learning and memory in rodents", Neuropharmacology, vol. 55: pp. 908-918, 2008;
[Непатентная литература 5] Bonkale et al., "Reduced nitric oxide responsive soluble guanylyl cyclase activity in the superior temporal cortex of patients with Alzheimer′s disease", Neurosci. Lett., vol 187, pp. 5-8, 1995.
Краткое описание изобретения
Техническая задача
[0014] Целью настоящего изобретения является получение нового соединения, или его фармакологически приемлемой соли, которое обладает PDE9-ингибирующим действием, и содержащей его фармацевтической композиции.
Решение задачи
[0015] В результате всесторонних исследований с целью решения вышеупомянутых задач было обнаружено новое пиразолохинолиновое производное, или его фармакологически приемлемая соль, которое обладает PDE9-ингибирующим действием.
[0016] То есть, настоящее изобретение относится к следующим <1> - <20>.
<1> Соединение, или его фармакологически приемлемая соль, представленное формулой (I):
,
где
R1 является атомом водорода;
R2 является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, пиридинильной группы и пиримидинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A1, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B1;
R3 является атомом водорода или атомом фтора;
R4 является атомом водорода;
R5 является оксепанильной группой, диоксепанильной группой, тетрагидропиранильной группой или тетрагидрофуранильной группой, необязательно замещенной метоксигруппой;
R6 является атомом водорода;
группа A1 состоит из атома галогена, C1-6-алкильной группы, необязательно замещенной 1-3 атомами галогена, и C1-6-алкоксигруппы; и
группа B1 состоит из атома галогена, цианогруппы, C1-6-алкильной группы, необязательно замещенной 1-3 атомами галогена, C1-6-алкокси-C1-6-алкильной группы, C1-6-алкоксигруппы, необязательно замещенной 1-3 атомами галогена, и тетрагидропиранильной группы,
при условии, что если R2 является 3-пиридинильной группой, то заместитель в 4-м положении является атомом галогена или C1-6-алкильной группой, необязательно замещенной 1-3 атомами галогена.
<2> Соединение или его фармакологически приемлемая соль по <1>, где
R2 является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, 3-пиридинильной группы, 4-пиридинильной группы и 5-пиримидинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A2, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B2;
R5 является 4-оксепанильной группой, 1,4-диоксепан-6-ильной группой, 3,4,5,6-тетрагидро-2H-3-пиранильной группой, 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой;
группа A2 состоит из атома хлора и метильной группы, необязательно замещенной 1-2 атомами фтора, этильной группы, метоксигруппы и этоксигруппы; и
группа B2 состоит из атома фтора, атома хлора, цианогруппы, метильной группы, необязательно замещенной 1-3 атомами фтора, этильной группы, метоксиметильной группы, метоксигруппы, необязательно замещенной 1-3 атомами фтора, этоксигруппы, изопропилоксигруппы и 3,4,5,6-тетрагидро-2H-4-пиранильной группы.
<3> Соединение или его фармакологически приемлемая соль по <2>, где R3 является атомом фтора.
<3.1> Соединение или его фармакологически приемлемая соль по <3>, где R5 является 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой.
<4> Соединение или его фармакологически приемлемая соль по <1>, где
R3 является атомом водорода; и
R5 является тетрагидропиранильной группой или тетрагидрофуранильной группой, необязательно замещенной метоксигруппой.
<5> Соединение или его фармакологически приемлемая соль по <2>, где
R3 является атомом водорода; и
R5 является 3,4,5,6-тетрагидро-2H-3-пиранильной группой, 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой.
<6> Соединение или его фармакологически приемлемая соль по <1>, где
R2 является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, 3-пиридинильной группы и 4-пиридинильной группы, где каждый из двух атомов в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A3, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B3;
R3 является атомом водорода;
R4 является атомом водорода;
R5 является 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой;
группа A3 состоит из метильной группы и метоксигруппы; и
группа B3 состоит из метильной группы, метоксигруппы и метоксиметильной группы.
<7> Соединение, или его фармакологически приемлемая соль, выбранное из следующей группы:
1) 7-(6-метокси-2,4-диметилпиридин-3-ил)-1-(тетрагидро-2H-пиран-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
2) 7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидро-2H-пиран-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
3) (S)-7-(6-изопропилокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
4) 8-фтор-7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидро-2H-пиран-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
5) 1-(1,4-диоксепан-6-ил)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
6) 1-(1,4-диоксепан-6-ил)-7-(2-метокси-4,6-диметилпиридин-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
7) (S)-8-фтор-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
8) 7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидро-2H-пиран-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
9) (-)-7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
10) (-)-7-(6-метокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
11) (S)-8-фтор-7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
12) (S)-7-(6-этокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он,
13) (S)-8-фтор-7-(6-метокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он и
14) (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он.
<8> 7-(6-изопропилокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<9> (S)-7-(6-изопропилокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль
<10> 8-фтор-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<11> (S)-8-фтор-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<12> 7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<13> (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<14> 1-(1,4-диоксепан-6-ил)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<14.1> 8-фтор-7-(6-метокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<14.2> (S)-8-фтор-7-(6-метокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<14.3> 8-фтор-7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<14.4> (S)-8-фтор-7-(2-метокси-4,6-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<14.5> 7-(6-этокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль.
<14.6> (S)-7-(6-этокси-2,4-диметилпиридин-3-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармакологически приемлемая соль:
<15> Фармацевтическая композиция, содержащая соединение или его фармакологически приемлемую соль по <1> в качестве активного ингредиента.
<16> Фармацевтическая композиция по <15>, которая является ингибитором PDE9.
<17> Фармацевтическая композиция по <15> для повышения концентрации внутримозгового cGMP.
<18> Средство для облегчения когнитивного нарушения при болезни Альцгеймера, содержащее соединение или его фармакологически приемлемую соль по <1>.
<19> Способ облегчения когнитивного нарушения при болезни Альцгеймера, включающий введение пациенту соединения или его фармакологически приемлемой соли по <1>.
<20> Соединение или его фармакологически приемлемая соль по <1> для применения для облегчения когнитивного нарушения при болезни Альцгеймера.
Полезные эффекты настоящего изобретения
[0017] Пиразолохинолиновое производное (далее по тексту называемое соединение (I)), представленное формулой (I), или его фармакологически приемлемая соль по настоящему изобретению обладают PDE9-ингибирующим действием, как показано в данных по активности в описанном далее примере фармакологического теста. Соединение (I) по настоящему изобретению в основном характеризуется значением IC50, составляющим 1000 нМ или ниже, в качестве PDE9-ингибирующего действия, и предпочтительным является соединение, характеризующееся значением IC50, составляющим 100 нМ или ниже.
[0018] Соединение (I) по настоящему изобретению обладает PDE9-ингибирующим действием, поэтому ожидают повышение концентрации внутримозгового cGMP. PDE9-ингибирующее действие и повышение cGMP приводит к улучшению протекания обучения и развития памяти, и соединение (I) характеризуется возможным применением в качестве терапевтического средства от когнитивных дисфункций и т.п. при болезни Альцгеймера.
Краткое описание графических материалов
[0019] Фиг.1 представляет собой изображение, на котором показана трехмерная структура, полученная в результате рентгеноструктурного анализа соединения, полученного в примере получения 53.
Описание вариантов осуществления
[0020] Далее будет детально описано содержание настоящего изобретения.
[0021] По всему настоящему описанию структурные формулы для соединений для удобства будут демонстрировать только один конкретный изомер, но настоящее изобретение включает все изомеры, такие как геометрические изомеры, оптические изомеры, стереоизомеры и таутомеры, предполагаемые структуры соединения, а также смеси их изомеров, и, таким образом, соединения могут состоять из изомеров и их смесей в любой необходимой пропорции, не ограничиваясь формулами, которые показаны для удобства. Таким образом, например, соединения по настоящему изобретению могут существовать в виде оптически активных форм или рацемических смесей, все из которых включены без ограничения согласно настоящему изобретению, и независимо от того, рацемические ли смеси или оптически активные формы, их можно применять в качестве смесей с оптически активными формами в любой необходимой пропорции. Тем не менее, будет понятно, что некоторые изомеры, или рацематы, или другие смеси изомеров могут проявлять большую активность, чем другие.
[0022] Также могут существовать полиморфные кристаллы, и можно использовать любую кристаллическую форму или их смесь без каких-либо ограничений, а также аморфные формы, и соединения по настоящему изобретению также включают как ангидрат, так и сольват (особенно гидрат).
[0023] Также в настоящее изобретение включены соединения меченного изотопом соединения (I). Меченное изотопом соединение является таким же, как и соединение (I), за исключением того, что один или несколько атомов заменены атомами с атомными массами или массовыми числами, отличными от обычно встречаемых в природе. Изотопы, которые можно включить в соединение по настоящему изобретению, являются изотопами, например, водорода, углерода, азота, кислорода, фтора, фосфора, серы, иода и хлора, и включают 2H, 3H, 11C, 14C, 15N, 18O, 18F, 32P, 35S, 123I и 125I.
[0024] Вышеупомянутые меченные изотопом соединения, например, соединения, в которых включены такие радиоизотопы как 3H и/или 14C, пригодны для анализа распределения в ткани лекарственных препаратов и/или субстратов. Полагают, что 3H и 14C пригодны для облегчения их получения и выявления. Изотопы 11C и 18F считаются пригодными для PET (позитронно-эмиссионной томографии); а изотопы 125I считаются пригодными для SPECT (однофотонной эмиссионной компьютерной томографии); и все они пригодны для получения изображения головного мозга. Замена на более тяжелый изотоп, такой как 2H, послужит причиной для некоторого типа терапевтических преимуществ, включая повышение периода полувыведения in vivo или понижение необходимой дозы вследствие более высокой метаболической стабильности, и, следовательно, считается пригодной в определенной ситуации. Вышеупомянутые меченные изотопами соединения можно аналогично получить путем осуществления процедур, раскрытых в приведенных далее примерах с применением меченных изотопами реагентов, которые можно легко использовать вместо реагентов, которые не мечены изотопом.
[0025] Далее по тексту будут описаны значения терминов, символов и т.п., описываемых в настоящем описании, и будет детально описано настоящее изобретение.
[0026] "Атом галогена" в настоящем описании означает атом фтора, атом хлора, атом брома или атом иода. Подходящие примеры "атома галогена" включают атом фтора и атом хлора.
[0027] "C1-6-алкильная группа" в настоящем описании означает алкильную группу с прямой или разветвленной цепью с 1-6 атомами углерода, и конкретные примеры включают метильную группу, этильную группу, 1-пропильную группу, изопропильную группу, 2-метил-1-пропильную группу, 2-метил-2-пропильную группу, 1-бутильную группу, 2-бутильную группу, 1-пентильную группу, 2-пентильную группу, 3-пентильную группу, 1-гексильную группу, 2-гексильную группу и 3-гексильную группу.
[0028] "C1-6-алкоксигруппа" в настоящем описании означает атом кислорода, к которому прикреплена определенная выше "C1-6-алкильная группа", и конкретные примеры включают метоксигруппу, этоксигруппу, изопропилоксигруппу, 1-пентилоксигруппу и 1-гексилоксигруппу.
[0029] "C1-6-алкокси-C1-6-алкильная группа" в настоящем описании означает определенную выше "C1-6-алкильную группу", к которой прикреплена определенная выше "C1-6-алкоксигруппа", и конкретные примеры включают метоксиметильную группу, 1-метоксиэтильную группу, 2-метоксиэтильную группу, 1-метоксипропильную группу, 2-метоксипропильную группу, 3-метоксипропильную группу, 2-метокси-2-пропильную группу, (1-пропилокси)метильную группу, (изопропилокси)метильную группу, 1-(1-пропилокси)этильную группу, 2-(1-пропилокси)этильную группу, 1-(изопропилокси)этильную группу, 2-(изопропилокси)этильную группу, 1-(1-пропилокси)пропильную группу, 2-(1-пропилокси)пропильную группу, 3-(1-пропилокси)пропильную группу, 2-(1-пропилокси)-2-пропильную группу, 1-(изопропилокси)пропильную группу, 2-(изопропилокси)пропильную группу, 3-(изопропилокси)пропильную группу и 2-(изопропилокси)-2-пропильную группу.
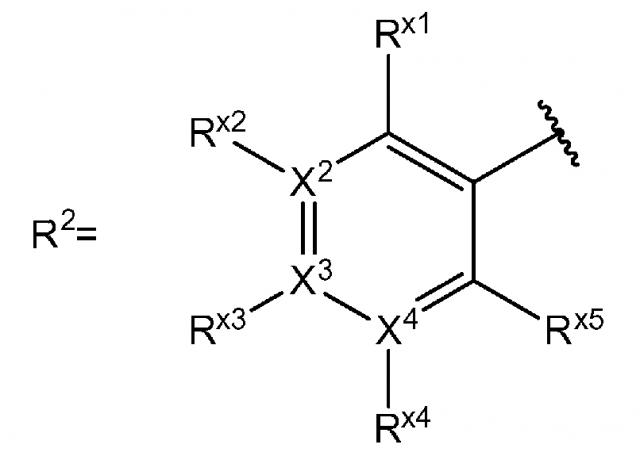
[0030] В определении R2 "ароматическая кольцевая группа, выбранная из группы, состоящей из фенильной группы, пиридинильной группы и пиримидинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A1, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B1" означает:
,
где
X2 - X4 является атомом углерода или атомом азота, образующим фенильную группу, пиридинильную группу или пиримидинильную группу;
если Xn (n = 2-4) является атомом азота, Rxn отсутствует; и если Xn (n=2-4) является атомом углерода, Rxn является атомом водорода или заместителем, выбранным из группы B1, и Rx1 и Rx5 независимо являются заместителем, выбранным из группы A1.
[0031] Далее по тексту будут описаны определения R1 - R6 соединения, представленного формулой (I), и предпочтительные примеры.
R1 является атомом водорода.
R2 является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, пиридинильной группы и пиримидинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A1, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B1.
R2 предпочтительно является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, 3-пиридинильной группы, 4-пиридинильной группы и 5-пиримидинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A2, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B2;
R2 предпочтительнее является ароматической кольцевой группой, выбранной из группы, состоящей из фенильной группы, 3-пиридинильной группы и 4-пиридинильной группы, где каждый из двух атомом в ароматическом кольце, которые находятся рядом с атомом углерода, соединенным с пиразоло[4,3-c]хинолиновым кольцом, независимо имеют заместитель, выбранный из группы A3, а другие атомы в ароматическом кольце независимо необязательно имеют заместитель, выбранный из группы B3.
R3 является атомом водорода или атомом фтора.
R4 является атомом водорода.
R5 является оксепанильной группой, диоксепанильной группой, тетрагидропиранильной группой или тетрагидрофуранильной группой необязательно замещенной метоксигруппой.
R5 предпочтительно является 4-оксепанильной группой, 1,4-диоксепан-6-ильной группой, 3,4,5,6-тетрагидро-2H-3-пиранильной группой, 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой и предпочтительнее является 3,4,5,6-тетрагидро-2H-4-пиранильной группой или 3-тетрагидрофуранильной группой.
R6 является атомом водорода.
Группа A1 состоит из атома галогена, C1-6-алкильной группы, необязательно замещенной 1-3 атомами галогена, и C1-6-алкоксигруппы.
Группа B1 состоит из атома галогена, цианогруппы, C1-6-алкильной группы, необязательно замещенной 1-3 атомами галогена, C1-6-алкокси-C1-6-алкильной группы, C1-6-алкоксигруппы, необязательно замещенной 1-3 атомами галогена, и тетрагидропиранильной группы.
Группа A2 состоит из атома хлора и метильной группы, необязательно замещенной 1-2 атомами фтора, этильной группы, метоксигруппы и этоксигруппы.
Группа B2 состоит из атома фтора, атома хлора, цианогруппы, метильной группы, необязательно замещенной 1-3 атомами фтора, этильной группы, метоксиметильной группы, метоксигруппы, необязательно замещенной 1-3 атомами фтора, этоксигруппы, изопропилоксигруппы и 3,4,5,6-тетрагидро-2H-4-пиранильной группы.
Группа A3 состоит из метильной группы и метоксигруппы.
Группа B3 состоит из метильной группы, метоксигруппы и метоксиметильной группы.
[0032] "Фармакологически приемлемая соль" в настоящем описании конкретно не ограничена при условии, что соль, образованная с соединением по настоящему изобретению, и конкретные примеры включают соли неорганической кислоты, соли органической кислоты, соли неорганического основания, соли органического основания и соли кислых или основных аминокислот.
[0033] Только если "фармакологически приемлемая соль" в настоящем описании является солью, образованной в подходящем соотношении, за исключением любого конкретного ограничивающего описания, то количество молекул кислоты на одну молекулу соединения в образованной соли, даже если конкретно не ограничено, предпочтительно составляет от приблизительно 0,1 до приблизительно 5 молекул, предпочтительнее от приблизительно 0,5 до приблизительно 2 молекул и еще предпочтительнее приблизительно 0,5, приблизительно 1 или приблизительно 2 молекулы на одну молекулу соединения.
[0034] Предпочтительные примеры солей неорганических кислот включают гидрохлориды, гидробромиды, сульфаты, нитраты и фосфаты, и предпочтительные примеры солей органических кислот включают ацетаты, сукцинаты, фумараты, малеаты, тартраты, цитраты, лактаты, стеараты, бензоаты, метансульфонаты, п-толуолсульфонаты и бензолсульфонаты.
[0035] Предпочтительные примеры солей неорганических кислот включают соли щелочных металлов, такие как соли натрия и соли калия, соли щелочноземельных металлов, такие как соли кальция и соли магния, соли алюминия и соли аммония, и предпочтительные примеры солей органических оснований включают соли диэтиламина, соли диэтаноламина, соли меглюмина и соли N,N′-дибензилэталендиамина.
[0036] Предпочтительные примеры кислых солей аминокислот включают аспартаты и глютаматы, и предпочтительные примеры солей основных аминокислот включают соли аргинина, соли лизина и соли орнитина.
[0037] [Общие способы получения]
Соединение по настоящему изобретению можно получить с помощью описанных ниже способов. Тем не менее, способы получения соединения по настоящему изобретению ими не ограничены.
[0038] Соединение (I) по настоящему изобретению можно получить с помощью следующих способов получения A, B, C и D.
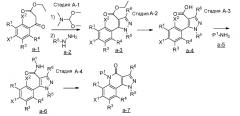
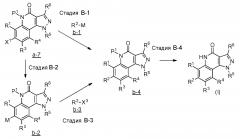
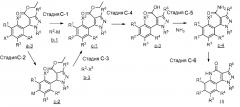
[0039] <Способ получения A>
где каждый из R1, R3, R4, R5 и R6 имеет те же определения, что и приведенные выше определения; P1 означает защитную группу группы NH, такую как 2,4-диметоксибензильная группа; и X1 и X2 обозначают атом галогена.
[0040] Стадия A-1
Данная стадия представляет собой стадию реакции конденсации соединения, представленного формулой a-1 (называемого в некоторых случаях соединением a-1; далее по тексту аналогично) с DMF-DMA, а затем посредством хорошо известного способа, предоставляя возможность полученному продукту прореагировать с гидразиновым производным a-2 с образованием структуры пиразольного кольца, таким образом получая соединение a-3. Настоящую реакцию можно осуществлять в потоке газа или в атмосфере инертного газа, такого как азот или аргон.
Соединение a-1 можно синтезировать согласно хорошо известному способу (например, по описанию в Reuman, Michael et al., "Journal of Medicinal Chemistry", 1995, vol. 38, p. 2531-2540, или Wentland Mark P et al., "Journal of Medicinal Chemistry", 1993, vol. 36, p. 1580-1596).
[0041] Данную стадию можно осуществлять точно согласно способу, предусматривающему определенные реакционные условия, постреакционные процедуры и очистку и т.п., описанному в примерах получения 1, 2, 3, 4, 5, 6, 10 и 11, которые описаны позже, и др.
Поскольку соединение a-2 является коммерчески доступным соединением, то можно использовать его или же его можно синтезировать хорошо известными для специалистов способами. Соединение можно получить путем превращения соответствующего кетонового производного в гидразидимин, и восстановления гидразидимина с помощью боргидрида, цианоборгидрида натрия или др. Соединение a-2 также можно применять в форме соли, такой как гидрохлорид.
[0042] Что касается используемого в настоящей реакции растворителя, то в реакции конденсации соединения a-1 с DMF-DMA, DMF-DMA можно применять в 5-20-кратном молярном эквиваленте в качестве реакционного средства и одновременно растворителя. Растворитель, используемый в последующей реакции образования пиразольного кольца с гидразиновым производным a-2, конкретно не ограничен при условии, что он является растворителем, который до некоторой степени растворяет исходные сырьевые материалы реакции и не подавляет реакцию, но предпочтительно представляет собой метанол, этанол, н-бутанол, трет-бутанол, THF, 1,4-диоксан, воду или смешанный из них растворитель и, предпочтительнее, этанол.
[0043] Температура реакции обычно зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и других реагентов и т.п., используемых в реакции. В реакции конденсации соединения a-1 с DMF-DMA температура реакции предпочтительно составляет от 0°C до температуры кипения растворителя (внутренняя температура реакционного сосуда) и предпочтительнее является комнатной температурой. В последующей реакции образования пиразольного кольца с гидразиновым производным a-2 температура реакции предпочтительно составляет от комнатной температуры до температуры кипения растворителя (внутренней температуры реакционного сосуда) и предпочтительнее от 70°C до температуры кипения растворителя.
[0044] Время реакции обычно зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и других реагентов и т.п., используемых в реакции. В реакции конденсации соединения a-1 с DMF-DMA время реакции предпочтительно составляет от 0,5 до 24 часов, и предпочтительнее от 1 до 3 часов, при вышеуказанной температуре после добавления реагентов. В последующей реакции образования пиразольного кольца с гидразиновым производным a-2 время реакции предпочтительно составляет от 0,5 до 24 часов и предпочтительнее от 1 до 8 часов, при вышеуказанной температуре после добавления реагентов.
[0045] Стадия A-2
Данная стадия является стадией гидролиза соединения a-3 в присутствии основания с получением, таким образом, соединения a-4.
[0046] Растворитель, используемый в настоящей реакции, конкретно не ограничен при условии, что он является растворителем, который до некоторой степени растворяет исходные сырьевые материалы и не подавляет реакцию, но предпочтительно включает метанол, этанол, н-бутанол, трет-бутанол, THF, 1,4-диоксан, воду или смешанные из них растворители.
[0047] Основание зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и др., и конкретно не ограничено, но его примеры включают гидроксид натрия, гидроксид лития, гидроксид калия, карбонат лития, карбонат натрия, карбонат калия, гидрокарбонат натрия, карбонат калия, карбонат цезия, тетраметилсилилоксид лития (TMSOLi). Основание можно использовать в 1-10-кратном молярном эквиваленте по отношению к a-3.
[0048] Температура реакции обычно зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и других реагентов и т.п., используемых в реакции, и предпочтительно составляет от 0°C до температуры кипения растворителя (внутренняя температура реакционного сосуда) и предпочтительнее от комнатной температуры до 50°C.
[0049] Время реакции обычно зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и других реагентов и т.п., используемых в реакции, и предпочтительно составляет от 1 до 48 часов, и предпочтительнее от 2 до 12 часов, при вышеупомянутой температуре после добавления реагентов.
[0050] Стадия A-3
Данная стадия представляет собой стадию предоставления соединению a-4 возможности прореагировать с аминопроизводным a-5 с помощью конденсирующего средства с получением, таким образом, соединения a-6. Настоящую реакцию также можно осуществлять в потоке газа или в атмосфере инертного газа, такого как азот или аргон.
[0051] Данную стадию можно осуществлять точно согласно способу, предусматривающему определенные реакционные условия, постреакционные процедуры и очистку и т.п., описанному в примере получения 1, 2, 4 и 5, которые описаны позже, и др.
[0052] Конденсирующее средство зависит от исходных сырьевых материалов, растворителей, которые необходимо использовать, и др. и оно конкретно не ограничено, но можно использовать DCC, EDC, PYBOP, CDI и др. Конденсирующее средство можно использовать в 1-5-кратном молярном эквиваленте, и предпочтительно 1-2-кратном молярном эквиваленте, по отношению к соединению a-4.
[0053] Растворитель, используемый в настоящей