Композиция гиалуроновой кислоты
Иллюстрации
Показать всеГруппа изобретений относится к медицине, конкретно к инъекционной композиции гиалуроновой кислоты, включающей: гиалуроновую кислоту; местный анестетик, выбранный из группы, состоящей из местных анестетиков амидного и сложноэфирного типов или их сочетания; и производного аскорбиновой кислоты в количестве, которое предотвращает или уменьшает воздействие на вязкость и/или модуль упругости G' композиции, вызванное местным анестетиком при термической стерилизации. Описано применение производного аскорбиновой кислоты, а также описан способ получения композиции. Инъекции геля производного гиалуроновой кислоты восстанавливают кожу и увеличивают мягкие ткани, а также улучшают контур лица или тела. 7 н. и 19 з.п. ф-лы, 22 ил., 22 табл., 22 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к области инъекционных композиций гиалуроновой кислоты и к применению таких композиций в косметических и/или медицинских приложениях.
Уровень техники
Гиалуроновая кислота представляет собой один из наиболее широко применяемых биосовместимых полимеров для медицинского применения. Это встречающийся в природе полисахарид, принадлежащий к группе гликозаминогликанов (GAG). Гиалуроновая кислота и другие GAG содержат отрицательно заряженные гетерополисахаридные цепи, которые обладают способностью абсорбировать большие количества воды. Гиалуроновая кислота и производные продукты, полученные из гиалуроновой кислоты, широко применяют в биомедицинской и косметической областях, например, в процессе вискохирургии и в качестве кожного наполнителя.
Абсорбирующие воду гели или гидрогели широко применяют в биомедицинской области. Их получают, как правило, путем химического сшивания полимеров в бесконечные сетки. Хотя природная гиалуроновая кислота и определенным образом сшитые производные гиалуроновой кислоты абсорбируют воду до тех пор, пока они не оказываются полностью растворенными, сшитые гели гиалуроновой кислоты, как правило, абсорбируют определенное количество воды до тех пор, пока они не оказываются насыщенными, т.е. они обладают конечной способностью удерживания жидкости или степенью набухания.
Поскольку в большинстве живых организмов присутствует гиалуроновая кислота, имеющая одинаковую химическую структуру, за исключением своей молекулярной массы, она вступает в минимальное число реакций, и является пригодной для перспективного применения в медицине. Сшивание и/или другие модификации молекул гиалуроновой кислоты являются необходимыми для увеличения продолжительности ее существования в условиях организма. Кроме того, такие модификации влияют на способность удерживания жидкости молекулами гиалуроновой кислоты. Вследствие этого были предприняты многочисленные попытки модификации гиалуроновой кислоты.
Инъекционные производные гиалуроновой кислоты часто сочетают с подходящим анестетиком, например, лидокаином, чтобы уменьшать боль или неудобства, которые испытывает пациент, вследствие инъекционной процедуры.
Описание изобретения
Задача настоящего изобретения заключается в том, чтобы предложить улучшенную инъекционную композицию гиалуроновой кислоты для медицинских и/или немедицинских приложений.
Композиции гиалуроновой кислоты, применяемые для инъекций, требуется стерилизовать перед применением. Стерилизацию осуществляют, как правило, посредством термической обработки, такой как обработка в автоклаве. Термическая обработка, как правило, приводит к уменьшению жесткости или вязкости композиции гиалуроновой кислоты. Как упомянуто выше, инъекционные производные гиалуроновой кислоты часто сочетают с подходящим анестетиком, например, лидокаином, чтобы уменьшать боль или неудобства, которые испытывает пациент, вследствие инъекционной процедуры. Согласно наблюдениям, добавление некоторых обычно применяемых анестетиков, например, лидокаина, противодействует влиянию термической обработки на реологические свойства композиции гиалуроновой кислоты таким образом, что полученная в результате композиция становится более жесткой или вязкой, чем гель без лидокаина. Это изменение реологических свойств может оказаться неблагоприятным в некоторых приложениях, например, в приложениях, где требуемой или желательной является неглубокая инъекция геля, и/или где требуемой или желательной является кожа очень малой толщины. Примеры таких приложений включают восстановление кожи и увеличение мягких тканей, например, заполнение морщин или улучшение контура лица или тела, посредством инъекций геля гиалуроновой кислоты.
В настоящее время было обнаружено, что добавление в относительно небольшом количестве производного аскорбиновой кислоты в композицию гиалуроновой кислоты, включающую местный анестетик, выбранный из группы, состоящей из местных анестетиков амидного и сложноэфирного типов, способных эффективно подавлять «увеличение вязкости» композиции гиалуроновой кислоты, вызываемое местным анестетиком при стерилизации композиции в автоклаве. Таким образом, добавление в относительно небольшом количестве производного аскорбиновой кислоты в композицию гиалуроновой кислоты, включающую местный анестетик, может способствовать применению меньшей толщины кожи для инъекций без увеличения усилия, которое требуется для введения композиции, и без внесения изменений в компонент гиалуроновой кислоты. Кроме того, уменьшение вязкости и/или модуля упругости G' раствора является благоприятным в приложениях, где композицию впрыскивают неглубоко от поверхности кожи, например, для восстановления кожи или пластики мягких тканей, например, заполнения морщин или улучшения контура лица или тела, посредством инъекций геля гиалуроновой кислоты.
Воздействие производного аскорбиновой кислоты на вязкость и/или модуль упругости G' композиции продемонстрировано для немодифицированной гиалуроновой кислоты и модифицированной, например, сшитой, гиалуроновой кислоты, и это доказывает, что данное воздействие является общим для всех композиций, включающих гиалуроновую кислоту.
Помимо благоприятного воздействия на вязкость и/или модуль упругости G' композиции, добавление производного аскорбиновой кислоты в композицию может также обеспечивать и дополнительные преимущества. Аскорбиновая кислота (также известная как витамин C) и ее производные могут выступать как восстановители и поглотители агрессивных окислителей и радикалов. Поскольку аскорбиновая кислота и ее производные способны улучшать образование коллагена, они могут улучшать морфологию кожи. Они способны также улучшать образование эпидермального барьера, сокращать трансэпидермальные потери воды, ускорять заживление ран и, таким образом, играть важную роль в предотвращении старения кожи и связанных с этим состояний сухости кожи. Аскорбиновая кислота и ее производные известны своими противовоспалительными и светозащитными свойствами, а также своим воздействием на восстановление кожи от повреждений, связанных с ультрафиолетовым излучением. Кроме того, было показано, что аскорбиновая кислота и ее производные способны клинически улучшать дерматологические состояния, которые включают воспаление в качестве компонента процесса заболевания, такие как псориаз и астеатотическая экзема. Поскольку аскорбиновая кислота и ее производные способны подавлять образование меланина, они могут также производить эффект отбеливания кожи, и клинически доказано, что они улучшают состояние при меланозе кожи и ограниченном предраковом меланозе. Они могут также способствовать росту волос. Кроме того, предположено, что аскорбиновая кислота и ее производные обладают противораковыми свойствами.
Добавление производного аскорбиновой кислоты в композицию гиалуроновой кислоты, как правило, не производит никакого воздействия или производит незначительное воздействие на устойчивость композиции. А именно, было отмечено, что добавление производного аскорбиновой кислоты не повышает устойчивость композиции гиалуроновой кислоты. Исследования авторов настоящего изобретения показали, что добавление производного аскорбиновой кислоты может иногда приводить к небольшому уменьшению устойчивости композиции гиалуроновой кислоты. Однако авторы настоящего изобретения обнаружили, что преимущества, связанные с добавлением производного аскорбиновой кислоты перевешивают уменьшение устойчивости, вызванное ее добавлением в некоторых случаях. Чтобы избежать нежелательного уменьшения устойчивости композиции гиалуроновой кислоты концентрацию производного аскорбиновой кислоты следует поддерживать ниже максимальных концентраций, как описано ниже.
Согласно аспектам, проиллюстрированным в настоящем документе, предложена инъекционная композиция гиалуроновой кислоты, включающая:
гиалуроновую кислоту,
местный анестетик, выбранный из группы, состоящей из местного анестетика амидного и сложноэфирного типов или их сочетания, и
производное аскорбиновой кислоты в количестве, которое предотвращает или уменьшает воздействие на вязкость и/или модуль упругости G' композиции, вызванное местным анестетиком при термической стерилизации.
Термин «инъекционная» означает, что композиция гиалуроновой кислоты получена в форме, которая является подходящей для парентеральной инъекции, например, в мягкую ткань, такую как кожа, пациента или другого лица. Инъекционная композиция должна быть стерильной и свободной от компонентов, которые способны вызывать неблагоприятные реакции при введении в мягкую ткань, такую как кожа, пациента или другого лица. Это подразумевает отсутствие или лишь весьма низкую степень иммунной реакции, которая возникает у человека в результате лечения. Таким образом, у человека в результате лечения возникают лишь весьма слабые нежелательные местные или системные эффекты, или эти эффекты полностью отсутствуют.
Вязкость и/или модуль упругости G' композиции гиалуроновой кислоты можно измерять, применяя разнообразные способы, которые хорошо известны специалисту в данной области техники. Вязкость можно измерять, например, как вязкость при нулевом сдвиге (η0) методом ротационной вискозиметрии, применяя реометр Bohling VOR (измерительная система C14 или PP 30, промежуток 1,00 мм). Могут также оказаться применимыми и другие способы измерения вязкости. Модуль упругости G' можно измерять, например, применяя реометр Bohling VOR (измерительная система PP 30, промежуток 1,00 мм) и осуществляя изменение деформации, для определения области линейной вязкоупругости (LVR), а затем измерение вязкоупругих свойств в пределах LVR. Могут также оказаться применимыми и другие способы измерения модуля упругости G'.
Инъекционная композиция гиалуроновой кислоты предпочтительно является водной, и гиалуроновая кислота, местный анестетик и производное аскорбиновой кислоты предпочтительно набухают, растворяются или диспергируются в водной фазе.
Инъекционная композиция гиалуроновой кислоты включает гиалуроновую кислоту. Гиалуроновая кислота может представлять собой модифицированную, например, разветвленную или сшитую гиалуроновую кислоту. Согласно определенным вариантам осуществления, гиалуроновая кислота представляет собой сшитую гиалуроновую кислоту. Согласно специфическим вариантам осуществления, гиалуроновая кислота представляет собой гель гиалуроновой кислоты.
Если не определены другие условия, термин «гиалуроновая кислота» заключает в себе все варианты и сочетания вариантов гиалуроновой кислоты, гиалуроната или гиалуронана, имеющих разнообразные длины цепей и состояния заряда, а также разнообразные химические модификации, включая сшивание. Таким образом, данный термин также заключает в себе разнообразные гиалуронатные соли гиалуроновой кислоты с разнообразными противоионами, такой как гиалуронат натрия. Данный термин также заключает в себе разнообразные модификации гиалуроновой кислоты, такие как окисление, например, окисление групп -CH2OH в группы -CHO и/или -COOH; окисление перйодатом вицинальных гидроксильных групп, после чего необязательно следует восстановление, например, восстановление групп -CHO в группы -CH2OH или сочетание с аминами и образование иминов, за которым следует восстановление до вторичных аминов; сульфатирование; деамидирование, необязательно с последующим деаминированием или образованием амидов с новыми кислотами; этерификация; сшивание; замещения разнообразными соединениями, например, с применением сшивающего реагента или сочетание под действием карбодиимида; в том числе сочетание различных молекул, таких как белки, пептиды и активные компоненты лекарственных средств, с гиалуроновой кислотой; и деацетилирование. Другие примеры модификаций представляют собой реакции сочетания изомочевины, гидразида, бромциана, моноэпоксида и моносульфона.
Гиалуроновую кислоту можно получать из разнообразных источников животного и неживотного происхождения. Источники неживотного происхождения включают дрожжи и предпочтительно бактерии. Молекулярная масса одной молекулы гиалуроновой кислоты, как правило, находится в интервале от 0,1 до 10 МДа, но возможны и другие молекулярные массы.
В определенных вариантах осуществления концентрация указанной гиалуроновой кислоты находится в интервале от 1 до 100 мг/мл. В некоторых вариантах осуществления концентрация указанной гиалуроновой кислоты находится в интервале от 2 до 50 мг/мл. В специфических вариантах осуществления концентрация указанной гиалуроновой кислоты находится в интервале от 5 до 30 мг/мл или в интервале от 10 до 30 мг/мл. В определенных вариантах осуществления гиалуроновая кислота является сшитой. Сшитая гиалуроновая кислота включает сшивки между цепями гиалуроновой кислоты, что создает непрерывную сетку из молекул гиалуроновой кислоты, которые соединяются друг с другом посредством ковалентных сшивок, физического переплетения цепей гиалуроновой кислоты и разнообразных взаимодействий, таких как электростатические взаимодействия, водородные связи и силы Ван-дер-Ваальса (van der Waals).
Сшивание гиалуроновой кислоты можно осуществлять посредством модификации, сшивающим химическим реагентом. Сшивающий химический реагент можно, например, выбирать из группы, состоящей из дивинилсульфона, полиэпоксиды и диэпоксиды. Согласно вариантам осуществления, сшивающий химический реагент выбирают из группы, состоящей из 1,4-бутандиолдиглицидилового эфира (BDDE), 1,2-этандиолдиглицидилового эфира (EDDE) и диэпоксиоктана. Согласно предпочтительному варианту осуществления, сшивающий химический реагент представляет собой 1,4-бутандиолдиглицидиловый эфир (BDDE).
Сшитое производное гиалуроновой кислоты предпочтительно является биосовместимым. Это подразумевает, что у получающего лечение пациента возникает лишь весьма слабая иммунная реакция, или никакая иммунная реакция не возникает. Таким образом, у получающего лечение пациента возникают лишь весьма слабые нежелательные местные или системные эффекты, или данные эффекты не возникают.
Сшитое производное гиалуроновой кислоты согласно настоящему изобретению может представлять собой гель или гидрогель. Таким образом, его можно рассматривать как нерастворимую в воде, но в существенной степени разбавленную сшитую систему молекул гиалуроновой кислоты, когда воздействует жидкость, как правило, водная жидкость.
Гель содержит, главным образом, жидкость, которая может составлять, например, от 90 до 99,9 мас.% воды, но ведет себя подобно твердому веществу, вследствие трехмерной сетки сшитой гиалуроновой кислоты. Вследствие значительного содержания в нем жидкости, гель является структурно гибким и похожим на естественную ткань, что делает его весьма полезным в качестве клеточного каркаса для технологии культивирования ткани и для пластики ткани.
Как упомянуто выше, сшивание гиалуроновой кислоты для образования сшитого геля гиалуроновой кислоты можно осуществлять, например, посредством модификации сшивающим химическим реагентом, применяя, например, 1,4-бутандиолдиглицидиловый эфир (BDDE). Концентрация гиалуроновой кислоты и степень сшивания влияют на механические свойства, например, модуль упругости G', а также на свойства устойчивости геля. Сшитые гели гиалуроновой кислоты часто характеризуют термином «степень модификации». Степень модификации гелей гиалуроновой кислоты, как правило, находится в интервале между 0,1 и 15 мол.%. Было обнаружено, что воздействие производного аскорбиновой кислоты на вязкость и/или модуль упругости G' композиции согласно настоящему изобретению является особенно выраженным в сшитых гелях гиалуроновой кислоты с низкой степенью модификации. Наиболее выраженное воздействие возникает в гелях гиалуроновой кислоты, у которых степень модификации составляет 2 мол.% или менее, в том числе 1,5 мол.% или менее, в том числе 1,25 мол.% или менее, например, в интервале от 0,1 до 2 мол.%, в том числе в интервале от 0,2 до 1,5 мол.%, в том числе в интервале от 0,3 до 1,25 мол.%, по сравнению с более сшитыми гелями гиалуроновой кислоты. Степень модификации (мол.%) представляет собой количество сшивающего реагента (реагентов), которое связано с HA, т.е. молярное количество связанного сшивающего реагента (реагентов) по отношению к суммарному молярному количеству повторяющихся дисахаридных звеньев HA. Степень модификации отражает степень, в которой гиалуроновая кислота является химически модифицированной сшивающим реагентом. Все условия для реакции сшивания и подходящие аналитические методики для определения степени модификации хорошо известны специалисту в данной области техники, который способен легко регулировать эти и другие факторы, имеющие отношение к делу, и тем самым, обеспечивать подходящие условия, чтобы получать степень модификации в интервале от 0,1 до 2% и подтверждать характеристики полученного в результате продукта по отношению к степени модификации. Например, сшитый 1,4-бутандиолдиглицидиловым эфиром (BDDE) гель гиалуроновой кислоты можно получать согласно способу, который описан в примерах 1 и 2 опубликованной международной патентной заявки WO 9704012.
В предпочтительном варианте осуществления гиалуроновая кислота в составе композиции присутствует в форме сшитого геля гиалуроновой кислоты, который сшит сшивающим химическим реагентом, причем концентрация указанной гиалуроновой кислоты находится в интервале от 10 до 30 мг/мл, и степень модификации указанным сшивающим химическим реагентом находится в интервале от 0,1 до 2 мол.%.
Гели гиалуроновой кислоты могут также включать часть гиалуроновой кислоты, которая не является сшитой, т.е. не соединена с трехмерной сеткой сшитой гиалуроновой кислоты. Однако оказывается предпочтительным, чтобы, по меньшей мере, 50 мас.%, предпочтительно, по меньшей мере, 60 мас.%, предпочтительнее, по меньшей мере, 70 мас.% и наиболее предпочтительно, по меньшей мере, 80 мас.% гиалуроновой кислоты в гелевой композиции составляло часть сетки сшитой гиалуроновой кислоты.
Инъекционная композиция гиалуроновой кислоты дополнительно включает местный анестетик, выбранный из группы, состоящей из местных анестетиков амидного и сложноэфирного типов или их сочетания. Местный анестетик представляет собой лекарственное средство, которое вызывает обратимую местную анестезию и потерю болевого возбуждения нервных волокон. Когда анестетик применяют по отношению к специфическим нервным путям (нервная блокада), можно производить такие эффекты, как аналгезия (потеря болевого ощущения) и паралич (потеря мышечной силы). Местный анестетик можно вводить в композицию гиалуроновой кислоты, чтобы уменьшить боль или неудобства, которые испытывает пациент, вследствие инъекционной процедуры. В технике хорошо известны, и признаны группы местных анестетиков амидного типа (также обыкновенно называются термином «аминоамид») и местных анестетиков сложноэфирного типа (также обыкновенно называются термином «аминоэфир»).
Молекулы местных анестетиков амидного и сложноэфирного типов имеют простую химическую структуру, которую образуют ароматическая часть, присоединенная амидной или сложноэфирной связью к боковой цепи основания. Единственное исключение представляет собой бензокаин, в котором отсутствуют основные группы. Все остальные анестетики представляют собой слабые основания, у которых значения pKa находятся, главным образом, в интервале от 8 до 9, таким образом, что они являются в значительной степени, но не полностью ионизированными при физиологических значениях pH. Вследствие их аналогичной структуры можно предполагать, что они производят аналогичные химические и физические воздействия на композицию гиалуроновой кислоты.
Согласно определенным вариантам осуществления, местный анестетик выбирают из группы, состоящей из местных анестетиков амидного и сложноэфирного типов, например, бупивакаина, бутаниликаина, картикаина, цинхокаина (дибукаин), клибукаина, этилпарапиперидиноацетиламинобензоата, этидокаина, лигнокаина (лидокаин), мепивакаина, оксетазаина, прилокаина, ропивакаина, толикаина, тримекаина, вадокаина, артикаина, левобупивакаина, амилокаина, кокаина, пропанокаина, хлормекаина, циклометикаина, проксиметакаина, аметокаина (тетракаин), бензокаина, бутакаина, бутоксикаина, бутиламинобензоата, хлорпрокаина, диметокаина (ларокаин), оксибупрокаина, пиперокаина, паретоксикаина, прокаина (новокаин), пропоксикаина, трикаина или их сочетания.
Согласно определенным вариантам осуществления, местный анестетик выбирают из группы, состоящей из местных анестетиков амидного типа, например, бупивакаина, бутаниликаина, картикаина, цинхокаина (дибукаин), клибукаина, этилпарапиперидиноацетиламинобензоата, этидокаина, лигнокаина (лидокаин), мепивакаина, оксетазаина, прилокаина, ропивакаина, толикаина, тримекаина, вадокаина, артикаина, левобупивакаина или их сочетания. Согласно некоторым вариантам осуществления, местный анестетик выбирают из группы, состоящей из бупивакаина, лидокаина, и ропивакаина, или их сочетания.
Согласно специфическим вариантам осуществления, местный анестетик представляет собой лидокаин. Лидокаин представляет собой хорошо известное вещество, которое широко применяют в качестве местного анестетика в инъекционных композициях, таких как композиции гиалуроновой кислоты.
Концентрацию амидного или сложноэфирного местного анестетика может выбирать специалист в данной области техники в пределах терапевтически соответствующих интервалов концентраций каждого конкретного местного анестетика или их сочетаний.
В определенных вариантах осуществления концентрация указанного местного анестетика находится в интервале от 0,1 до 30 мг/мл. В некоторых вариантах осуществления концентрация указанного местного анестетика находится в интервале от 0,5 до 10 мг/мл.
Когда лидокаин применяют в качестве местного анестетика, лидокаин может присутствовать в концентрации, которая находится предпочтительно в интервале от 1 до 5 мг/мл, предпочтительнее в интервале от 2 до 4 мг/мл, в том числе эта концентрация может составлять приблизительно 3 мг/мл.
Инъекционная композиция гиалуроновой кислоты дополнительно включает производное аскорбиновой кислоты. Термин «производное аскорбиновой кислоты» при применении в настоящем документе означает аскорбиновую кислоту или производные аскорбиновой кислоты, включающие общую химическую структуру аскорбиновой кислоты. Таким образом, производное аскорбиновой кислоты может представлять собой соединение, имеющее химическую структуру:
Производное аскорбиновой кислоты композиции может представлять собой аскорбиновую кислоту или соединение, структурно родственное аскорбиновой кислоте и/или полученное на ее основе.
Сама аскорбиновая кислота может оказаться полезной в некоторых приложениях, но вследствие своей низкой устойчивости она может находить лишь ограниченное применение в некоторых практических приложениях.
Производное аскорбиновой кислоты может растворяться в воде. Растворимость производного аскорбиновой кислоты в воде в атмосферных условиях может предпочтительно оказаться достаточной, чтобы обеспечивать растворение в желательной концентрации производного аскорбиновой кислоты в композиции. Растворимость растворимого в воде производного аскорбиновой кислоты в воде в атмосферных условиях может предпочтительно оказаться достаточной, чтобы обеспечивать концентрацию, составляющую 0,001 мг/мл или более и предпочтительнее 0,01 мг/мл или более, в композиции гиалуроновой кислоты.
Производное аскорбиновой кислоты может оказаться способным к образованию аскорбиновой кислоты или аскорбата в условиях организма (in vivo), например, посредством ферментативного разложения, которое осуществляют фосфатазы, гликозидазы и другие ферменты. Таким образом, согласно варианту осуществления, производное аскорбиновой кислоты может образовывать аскорбиновую кислоту или аскорбат при помещении в условия живого организма (in vivo).
В некоторых вариантах осуществления, производное аскорбиновой кислоты выбирают из группы, состоящей из фосфатного сложного эфира аскорбиновой кислоты, карбоксилатного сложного эфира аскорбиновой кислоты, сульфата аскорбиновой кислоты, сульфонатного сложного эфира аскорбиновой кислоты, карбоната аскорбиновой кислоты, а также замещенной ацеталем или кеталем аскорбиновой кислоты, или их сочетания.
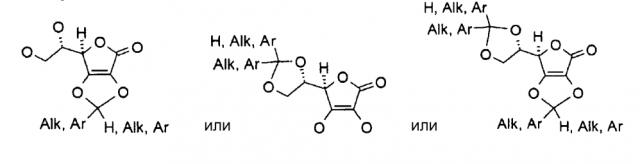
Производное аскорбиновой кислоты может представлять собой, например, соединение, имеющее общую формулу:
где R1, R2, R3, R4, независимо друг от друга, представляют собой атомы H или органические заместители. Соединение I может представлять собой, например, фосфатный сложный эфир аскорбиновой кислоты, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
где X представляет собой H, алкил, алкенил, алкинил, арил, амин, спирт, гликозид или
где n может составлять от 0 до 500.
Противоионы могут представлять собой, но не ограничиваются этим, Na+, K+, Ca2+, Al3+, Li+, Zn2+ или Mg2+.
Соединение I может представлять собой, например, карбоксилатный сложный эфир аскорбиновой кислоты, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
где Y представляет собой H, алкил, алкенил, алкинил, арил, амин, спирт, гликозид, сложный эфир аминокислоты или
где n может составлять от 0 до 500.
Соединение I может представлять собой, например, сульфат аскорбиновой кислоты, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
Противоионы могут представлять собой, но не ограничиваются этим, Na+, K+, Ca2+, Al3+, Li+, Zn2+ или Mg2+.
Соединение I может представлять собой, например, сульфонатный сложный эфир аскорбиновой кислоты, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
где Z представляет собой H, алкил, алкенил, алкинил, арил, амин, спирт, гликозид или
где n может составлять от 0 до 500.
Соединение I может представлять собой, например, карбонат аскорбиновой кислоты, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
где U представляет собой H, алкил, алкенил, алкинил, арил, амин, спирт, гликозид или
где n может составлять от 0 до 500.
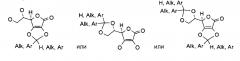
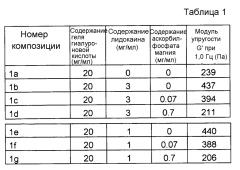
Соединение I может представлять собой, например, замещенную ацеталем или кеталем аскорбиновую кислоту, где, по меньшей мере, один из R1, R2, R3 и R4 представляет собой
где W, W′ и W″ представляют собой H, алкил, алкенил, алкинил, арил, амин, спирт, или углеводный остаток, например:
Соединение I может представлять собой, например, замещенную ацеталем или кеталем аскорбиновую кислоту, имеющую общую формулу:
где H представляет собой атом водорода, Alk представляет собой алкил, и Ar представляет собой арил.
В некоторых вариантах осуществления производное аскорбиновой кислоты выбирают из группы, состоящей из аскорбилфосфата, аскорбилсульфата, и аскорбилгликозида, или их сочетания.
В определенных вариантах осуществления производное аскорбиновой кислоты выбирают из группы, состоящей из аскорбилфосфата и аскорбилгликозида, или их сочетания.
В некоторых вариантах осуществления аскорбилфосфат выбирают из группы, состоящей из аскорбилфосфата натрия (SAP) и аскорбилфосфата магния (MAP), или их сочетания. Аскорбилфосфаты превращаются в витамин C в условиях организма (in vivo) посредством ферментативного гидролиза, осуществляемого фосфатазами.
В некоторых вариантах осуществления производное аскорбиновой кислоты представляет собой аминоалкил аскорбилфосфат. В определенных вариантах осуществления производное аскорбиновой кислоты представляет собой аминопропиласкорбилфосфат.
В некоторых вариантах осуществления производное аскорбиновой кислоты представляет собой аскорбилглюкозид. Аскорбилглюкозид превращается в витамин C в условиях организма (in vivo) посредством ферментативного гидролиза, который осуществляют глюкозидазы.
В некоторых вариантах осуществления производное аскорбиновой кислоты представляет собой метилсиланоласкорбат.
В некоторых вариантах осуществления производное аскорбиновой кислоты представляет собой ацетонид L-аскорбиновой кислоты.
Производные аскорбиновой кислоты, описанные в настоящем документе, могут присутствовать в непротонированной или полностью или частично протонированной форме, или в форме фармацевтически приемлемой соли. В частности, термины «аскорбилфосфат», «аскорбилсульфат», «аминоалкиласкорбилфосфат», «аминопропиласкорбилфосфат», «аскорбилгликозид» и «аскорбилглюкозид» при применении в настоящем документе предназначены для описания соединений в непротонированной или полностью или частично протонированной форме, или в форме фармацевтически приемлемой соли. Примеры подходящих противоионов включают, но не ограничиваются этим, ионы алюминия, кальция, лития, магния, калия, натрия и цинка.
Концентрацию производного аскорбиновой кислоты может выбирать специалист в данной области техники в зависимости от конкретного применяемого производного аскорбиновой кислоты.
В определенных вариантах осуществления концентрация указанного производного аскорбиновой кислоты находится в интервале от 0,001 до 15 мг/мл. В определенных вариантах осуществления концентрация указанного производного аскорбиновой кислоты находится в интервале от 0,001 до 10 мг/мл. В некоторых вариантах осуществления концентрация указанного производного аскорбиновой кислоты находится в интервале от 0,01 до 5 мг/мл. Концентрация указанного производного аскорбиновой кислоты, превышающая 0,01 мг/мл, является предпочтительной, поскольку она обеспечивает более значительное уменьшение вязкости и/или модуля упругости G' композиции гиалуроновой кислоты. Концентрация указанного производного аскорбиновой кислоты ниже 5 мг/мл является предпочтительной, поскольку более высокие концентрации могут приводить к нежелательному уменьшению устойчивости композиции гиалуроновой кислоты без дополнительных преимуществ.
Требуемая концентрация производного аскорбиновой кислоты может изменяться в пределах определенных выше интервалов в зависимости от конкретного применяемого производного аскорбиновой кислоты. В качестве примера, подходящая концентрация аскорбилфосфата натрия (SAP) или аскорбилфосфата магния (MAP) может находиться в интервале от 0,01 до 1 мг/мл, в то время как подходящая концентрация аскорбилглюкозида может находиться в интервале от 0,1 до 5 мг/мл.
Таким образом, согласно варианту осуществления, производное аскорбиновой кислоты представляет собой аскорбилфосфат натрия (SAP) или аскорбилфосфат магния (MAP), концентрация которого находится в интервале от 0,01 до 1 мг/мл и предпочтительно в интервале от 0,01 до 0,5 мг/мл.
Согласно еще одному варианту осуществления, производное аскорбиновой кислоты представляет собой аскорбилглюкозид, концентрация которого находится в интервале от 0,01 до 1 мг/мл, предпочтительно в интервале от 0,01 до 0,8 мг/мл, и предпочтительнее в интервале от 0,05 до 0,4 мг/мл.
Как упомянуто выше, согласно наблюдениям, добавление производного аскорбиновой кислоты не приводит к повышению устойчивости композиции гиалуроновой кислоты. Другими словами, инъекционная композиция гиалуроновой кислоты согласно настоящему изобретению не проявляет повышенной устойчивости по сравнению с такой же композицией без производного аскорбиновой кислоты.
Термин «устойчивость» при применении в настоящем документе предназначен для описания способности композиции гиалуроновой кислоты к сопротивлению разложению в процессе хранения и погрузки перед применением. Известно, что введение дополнительных компонентов в гиалуроновую кислоту или гель гиалуроновой кислоты может воздействовать на устойчивость указанной гиалуроновой кислоты или геля гиалуроновой кислоты. Устойчивость содержащей гиалуроновой кислоты или гель гиалуроновой кислоты композиции можно определять, применяя ряд различных способов. Способы определения устойчивость включают, но не ограничиваются этим, исследование однородности, цвета, прозрачности, pH, содержания геля и реологических свойств композиции. Устойчивость композиции гиалуроновой кислоты часто определяют путем наблюдения или измерения одного или более из указанных параметров с течением времени. Устойчивость можно определять, например, посредством измерения вязкости и/или модуля упругости G' композиции гиалуроновой кислоты с течением времени. Вязкость можно измерять, например, как вязкость при нулевом сдвиге (η0) методом ротационной вискозиметрии, применяя реометр Bohling VOR (измерительная система C14 или PP 30, промежуток 1,00 мм). Могут также оказаться применимыми и другие способы измерения вязкости. Модуль упругости G' можно измерять, например, применяя реометр Bohling VOR (измерительная система PP 30, промежуток 1,00 мм) и осуществляя изменение деформации, для определения области линейной вязкоупругости (LVR), а затем измерение вязкоупругих свойств в пределах LVR. Могут также оказаться применимыми и другие способы измерения модуля упругости G'.
В более конкретном варианте осуществления предложена инъекционная композиция гиалуроновой кислоты, включающая водный гель гиалуроновой кислоты, содержащий от 2 до 50 мг/мл гиалуроновой кислоты; от 0,5 до 10 мг/мл лидокаина; и от 0,01 до 5 мг/мл производного аскорбиновой кислоты выбранный из группы, состоящей из аскорбилфосфата и аскорбилгликозида, или их сочетания.
В более конкретном варианте осуществления предложена инъекционная композиция гиалуроновой кислоты, включающая водный гель гиалуроновой кислоты, содержащий от 2 до 50 мг/мл гиалуроновой кислоты; от 0,5 до 10 мг/мл лидокаина; и от 0,01 до 5 мг/мл аскорбилфосфата, например, аскорбилфосфата натрия или магния.
В еще одном более конкретном варианте осуществления предложена инъекционная композиция гиалуроновой кислоты, включающая водный гель гиалуроновой кислоты, содержащий от 2 до 50 мг/мл гиалуроновой кислоты; от 0,5 до 10 мг/мл лидокаина; и от 0,01 до 5 мг/мл аскорбилгликозида, например, аскорбилглюкозида.
В некоторых вариантах осуществления, композицию подвергают стерилизации. В определенных вариантах осуществления композиция является стерилизованной, т.е. композицию подвергают термической и/или паровой обработке, чтобы стерилизовать композицию. В некоторых вариантах осуществления композицию подвергают стерилизации путем обработки в автоклаве или аналогичной термической или паровой стерилизации. Стерилизацию, например, обработку в автоклаве, можно осуществлять при значении F0 ≥ 4.
Значение F0 процесса стерилизации насыщенным паром представляет собой смертность, выраженную как эквивалентное время в минутах при температуре 121ºC и обеспечиваемую путем обработки продукта в его конечном контейнере, по отношению к микроорганизмам, у которых значение Z составляет 10.
Когда композиции гиалуроновой кислоты подвергают стерилизации посредством термической или паровой обработки, вязкость и/или модуль упругости G', как правило, снижается. Когда местный анестетик амидного или сложноэфирного типа добавляют в композицию гиалуроновой кислоты, это снижение вязкости и/или модуля упругости G' пода