Молочная олигосахаридно-галактоолигосахаридная композиция для детской смеси, содержащая растворимую олигосахаридную фракцию, присутствующую в молоке, и имеющая низкое содержание моносахаридов, и способ получения композиции
Иллюстрации
Показать всеИзобретение относится к продуктам для детского питания. Заявленная смесь олигосахаридов получена из коровьего молока и содержит группу растворимых олигосахаридов, содержащих растворимую олигосахаридную фракцию, обнаруживаемую в коровьем молоке, и β-галактоолигосахариды, образованные под действием β-галактозидазы на лактозу, присутствующую в олигосахаридах коровьего молока. Причем смесь имеет общее содержание моносахаридов менее 5% масс./об. А соотношение лактоза:общее количество олигосахаридов составляет менее 10. Также предложены содержащая смесь олигосахаридов питательная композиция, применение данной композиции для повышения иммунной защиты и/или снижения риска инфекций, и/или уменьшения случаев пищевой аллергии и связанного с пищевой аллергией воздействия на здоровье, способ получения смеси олигосахаридов и продукт, полученный этим способом. Изобретение позволяет получать смесь для детского питания с пониженным уровнем моносахаридов, эффективную в качестве пребиотика, имеющую олигосахаридный профиль как у женского грудного молока. 5 н. и 16 з.п. ф-лы, 3 ил., 4 табл., 4 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к смеси олигосахаридов, полученной из коровьего молока, а также к пищевым продуктам, особенно к детской смеси, содержащей указанную смесь олигосахаридов (OS), и к способу получения указанной смеси олигосахаридов.
Уровень техники
В толстом кишечнике человека обитает широкий спектр бактерий, оказывающих как положительное, так и отрицательное воздействие на физиологию кишечника, а также другие системные воздействия. Преобладающие группы бактерий, обнаруженные в толстом кишечнике, включают род Bacteroides (бактероиды), в частности Bifidobacteria, Eubacteria, Clostridia и Lactobacilli. Данные бактерии проявляют активность, варьирующую в зависимости от доступности субстрата, окислительно-восстановительного потенциала, pH, парциального давления О2 и их распределения в толстом кишечнике. В большинстве случаев кишечные бактерии можно подразделить на виды, оказывающие либо потенциально вредное, либо полезное воздействие на организм хозяина. Патогенные воздействия (которые могут быть вызваны, например, Clostridia или Bacteroides) включают диарею, инфекции, поражение печени, канцерогенез и гнилостные процессы в кишечнике. Полезное для здоровья действие может быть обусловлено ингибированием роста вредных бактерий, стимуляцией иммунных функций, улучшением пищеварения и абсорбцией незаменимых нутриентов и синтезом витаминов. Желательно увеличение количества и/или усиление активности групп бактерий (таких как Bifidobacteria и Lactobacilli), которые обладают полезными для здоровья свойствами. Эти «хорошие бактерии», которые оказывают благотворное воздействие на организм хозяина, называются «иробиотиками». Пробиотики включают многие виды бактерий, но, как правило, выбираются из четырех родов бактерий: Lactobacilllus acidophilic, Bifidobacteria, Lactococcus и Pediococcus.
Польза для здоровья, связанная с пробиотическими бактериями, такими как Lactobacilli или Bifidobacteria включают усиленную системную клеточную иммунную реакцию, например повышение образования антител и фагоцитарной (пожирающей или уничтожающей активности белых кровяных клеток (лейкоцитов). Некоторые пробиотические бактериальные штаммы вызывают активизацию иммунной системы, тем самым предотвращая или уменьшая степень инфицирования. Некоторые пробиотики связывают с предотвращением аллергии, а также со снижением тяжести аллергии. Сообщалось об эффективности нескольких штаммов в облегчении течения кишечных расстройств, особенно диареи.
Относительно конкретного случая младенцев непосредственно перед рождением полагают, что желудочно-кишечный тракт младенца является стерильным. В процессе родов он контактирует с бактериями пищеварительного тракта и кожи матери и начинает заселяться ими. Существуют значительные различия в составе микробиоты кишечника, обусловленные питанием грудных детей. Микрофлора фекалий грудных детей, вскармливаемых материнским молоком, характеризуется преобладанием популяций бифидобактерий с некоторыми видами Lactobacillus, тогда как грудные дети, вскармливаемые молочными смесями, имеют более сложную микробиоту, в которой обычно присутствуют виды Bifidobacteria и виды Bacteroides, Clostridia и Streptococci. После отъема от груди состав микробиоты кишечника постепенно приближается к составу микробиоты взрослого человека.
Материнское молоко рекомендовано всем младенцам. Однако в некоторых случаях грудное вскармливание бывает неудовлетворительным или безуспешным по медицинским причинам, или же мать предпочитает не кормить грудью. Для таких ситуаций были разработаны детские смеси.
Для создания здоровой кишечной бактериальной микрофлоры, аналогичной микрофлоре детей на грудном вскармливании, желательно дополнять детскую смесь пробиотиками. Примеры пробиотиков, используемых в настоящее время в детских смесях, включают Lactobacillus rhamnosus АТСС 53103 от компании Valio Оу, Финляндия, под торговой маркой LGG; Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus paracasei CNCM 1-2116, Lactobacillus johnsonii CNCM 1-1225, Streptococcus salivarius DSM 13084, продаваемых BLIS Technologies Limited, Новая Зеландия, под наименованием K12; Bifidobacterium lactis CNCM 1-3446, продаваемый в частности компанией Christian Hansen, Дания, под торговой маркой Bb12; Bifidobacterium longum АТСС ВАА-999, продаваемый Morinaga Milk Industry Co. Ltd., Япония, под торговой маркой ВВ536; Bifidobacterium breve, продаваемый Danisco под торговой маркой Bb-03; Bifidobacterium breve, продаваемый Morinaga под торговой маркой M-16V; Bifidobacterium infantis, продаваемый Procter & Gamble Co. под торговой маркой Bifantis; и Bifidobacterium breve, продаваемый Institut Rosell (Lallemand) под торговой маркой R0070.
Эти пробиотики могут вводиться в количестве от приблизительно одного до приблизительно двадцати миллиардов колониеобразующих единиц (КОЕ) в день для поддержания здоровой кишечной микрофлоры, предпочтительно от приблизительно 5 миллиардов до приблизительно 10 миллиардов живых бактерий в день.
Другим фактором, влияющим на здоровую кишечную бактериальную микрофлору, является присутствие пребиотиков в кишечнике. Пребиотики являются неперевариваемыми пищевыми ингредиентами, которые выборочно стимулируют рост и/или активность пробиотиков в толстой кишке, тем самым улучшая здоровье организма хозяина. Пребиотики являются неперевариваемыми в том смысле, что они не разлагаются и не поглощаются желудком или тонкой кишкой и, таким образом, проходят неповрежденными в толстую кишку, где выборочно ферментируются полезными бактериями. Примеры пребиотиков включают некоторые олигосахариды, такие как фруктоолигосахариды (FOS) и галактоолигосахариды (GOS).
Женское молоко, как известно, содержит большее количество неусваиваемых олигосахаридов, чем большинство других видов животного молока. Фактически, неусваиваемые олигосахариды представляют собой третий из наиболее значительно представленных твердых компонентов грудного молока (после лактозы и липидов), встречающийся в концентрации 12-15 г/л в молозиве и 5-8 г/л в зрелом молоке. Олигосахариды женского молока (НМО) являются исключительно устойчивыми к ферментативному гидролизу, что говорит о том, что эти олигосахариды могут проявлять жизненно важные функции, не связанные непосредственно с их калорийностью.
Таким образом, пребиотики действуют синергически с пробиотиками для обеспечения значительной пользы для здоровья младенца. Пребиотики не только выборочно стимулируют рост пробиотиков, которые добавляют в детскую смесь, но также могут способствовать росту эндогенных пробиотиков, способных действовать синергически с добавляемыми пробиотиками.
Таким образом, польза для здоровья, обеспечиваемая описанными выше пробиотиками, усиливается присутствием пребиотиков.
Таким образом, по мере улучшения понимания состава женского молока было также предложено добавлять пребиотики в детскую смесь. Эти пребиотики, как правило, вводят в количествах, достаточных для положительного стимулирования здоровой микрофлоры в кишечнике и начала размножения этих «хороших» бактерий. Обычные содержания составляют от приблизительно 1 до приблизительно 10 г на порцию или от приблизительно 5% до приблизительно 40% рекомендуемой суточной дозы пищевых волокон для младенца.
Поэтому в продаже имеются различные детские смеси с добавлением пребиотиков, таких как, например, фруктоолигосахариды и галактоолигосахариды.
Тем не менее такие смеси представляют собой только приближение к смеси олигосахаридов, присутствующей в женском молоке. В женском молоке обнаружено более 100 различных олигосахаридных компонентов, некоторые из них пока еще либо не найдены, либо обнаружены только в небольших количествах в молоке животных, например коровьем молоке. Некоторые сиалилированные олигосахариды и фукозилированные олигосахариды присутствуют как в коровьем молоке, так и в молозиве, но только в очень небольших количествах.
В патенте EP 0975235 B1 описана синтетическая питательная композиция, содержащая один или несколько олигосахаридов женского молока, в которой НМО в композиции выбирают из группы из восьми НМО (3-фукозиллактозы, лакто-N-фукопентаозы III, лакто-N-фукопентаозы II, дифукозиллактозы, 2'-фукозиллактозы, лакто-N-фукопентаозы I, лакто-N-тетраозы и лакто-N-фукопентаозы V), в данном европейском патенте показано, что, по большому счету, олигосахариды защищают младенцев от вирусных и бактериальных инфекций органов дыхания, желудочно-кишечного и урогенитального трактов.
В патентной заявке US 2003/0129278 описана смесь олигосахаридов на основе олигосахаридов, полученных из одного или нескольких видов молока животных, отличающаяся тем, что она содержит по меньшей мере две фракции олигосахаридов, каждая из которых состоит, по меньшей мере, из двух различных олигосахаридов. Состав олигосахаридов в смеси олигосахаридов отличается от состава олигосахаридов в молоке одного или нескольких животных, из которого олигосахаридные фракции были экстрагированы.
В патенте EP 0458358 описан способ получения сухого обезжиренного молока, содержащего 10-15 масс.% галактоолигосахаридов, включающий:
(i) концентрирование обезжиренного молока с получением концентрированного молока с содержанием сухих веществ 20-50 масс.%,
(ii) добавление β-галактозидазы к концентрированному молоку для инициирования ферментативной реакции,
(iii) нагревание полученной реакционной смеси от 30 секунд до 15 минут до температуры 70-85°C для прекращения ферментативной реакции, и
(iv) распылительную сушку смеси после прекращения реакции.
В патенте авторов настоящего изобретения WO 2006/087391 описаны смесь олигосахаридов, полученная из молока животных, и способ получения указанной смеси олигосахаридов. Смесь олигосахаридов является эффективной в качестве пребиотика, особенно в кишечнике человека, и имеет олигосахаридный профиль, более близкий к профилю женского молока, чем олигосахаридный профиль, обеспечиваемый смесями фрукто- и галактоолигосахаридов.
При разработке пребиотических детских смесей желательно создавать смесь олигосахаридов, имеющую олигосахаридный профиль, наиболее близкий к олигосахаридному профилю исходного молока, по меньшей мере в качественном выражении. Относительные содержания олигосахаридов могут варьировать. Это означает, что смесь олигосахаридов должна содержать растворимую фракцию всех олигосахаридов, присутствующих в молоке. Под «растворимой фракцией» подразумеваются все различные олигосахариды, которые обычно растворимы в молоке. Относительные содержания различных растворимых олигосахаридов в исходном молоке не обязательно должны сохраняться в смеси олигосахаридов.
Кроме того, желательно поддерживать низкое соотношение лактоза/олигосахариды, чтобы избежать введения ненужных высоких количеств лактозы, а также уменьшить количество дополнительных OS, необходимых для достижения желаемого уровня олигосахаридов в детской смеси. Кроме того, смесь олигосахаридов должна иметь очень низкое содержание белка, чтобы не сильно влиять на аминокислотный профиль детской смеси.
Задачей изобретения является обеспечение смеси олигосахаридов, которая является эффективной в качестве пребиотика, особенно в кишечнике человека, и которая имеет олигосахаридный профиль, более близкий к аналогичному профилю женского молока, чем олигосахаридный профиль, обеспечиваемый смесями фрукто- и галактоолигосахаридов, и имеющей очень низкое содержание моносахаридов. Таким образом, задачей изобретения является обеспечение смеси олигосахаридов, содержащей растворимую фракцию олигосахаридов, присутствующих в молоке, из которого получают смесь олигосахаридов. В контексте настоящего изобретения «смесь олигосахаридов, полученная из коровьего молока», означает, что олигосахариды получают из коровьего молока. Таким образом, различные растворимые олигосахариды, присутствующие в исходном молоке, также присутствуют и в конечной смеси олигосахаридов по изобретению, однако не обязательно в тех же самых соотношениях.
Другой задачей изобретения является создание смеси олигосахаридов, которая имеет относительно высокую концентрацию олигосахаридов, обычно 20-50 масс.%.
Существует потребность в пищевом продукте, особенно предназначенном для детей, младенцев и/или новорожденных, который помогает обеспечить нормальный иммунный или противовоспалительный статус или частично устраняет или уменьшает пищевые аллергические реакции.
Существует потребность в создании пищевого продукта, который эффективен в качестве пребиотика, особенно в кишечнике человека.
Существует потребность в пищевом продукте, который обеспечивает указанные выше преимущества при сохранении сбалансированного нормального метаболизма у индивидуума.
Существует потребность в улучшении условий в кишечнике человека с помощью немедикаментозного вмешательства, которое совместимо с уязвимыми индивидуумами, такими как младенцы или дети раннего возраста.
Существует потребность в пищевом продукте, который обеспечивает оральную толерантность к аллергенам.
Существует потребность в олигосахаридном ингредиенте с очень низким содержанием молочного белка, который можно добавлять в детскую смесь в виде сиропа или порошка без какого-либо носителя.
Сущность изобретения
Настоящее изобретение относится к смеси олигосахаридов, полученных из коровьего молока, содержащей:
a) группу растворимых олигосахаридов, включающих растворимую олигосахаридную фракцию, обнаруживаемую в коровьем молоке (олигосахариды коровьего молока или CMOS);
b) β-галактоолигосахариды, образованные под действием β-галактозидазы на лактозу, присутствующую в олигосахаридах коровьего молока и, возможно, также на другие олигосахариды коровьего молока,
смесь, имеющая общее содержание моносахаридов менее 5% масс./об., предпочтительно менее 3%, и соотношение лактозагобщее количество олигосахаридов менее 10, предпочтительно менее 3.
Смесь имеет следующий состав моно-, ди- и олигосахаридов, выраженный в процентах сухого вещества:
c) лактоза 30-60%;
d) глюкоза 0,5-2,5%;
e) галактоза 0,5-2,5%;
f) олигосахариды и β-галактоолигосахариды 20-50%;
g) сиалиллактоза 0,2-2%.
Другим аспектом настоящего изобретения является способ получения смеси OS. Стадии включают:
a) концентрирование депротеинизированного материала коровьего молока до 50-75% общего содержания сухих веществ (TS);
b) подвергание концентрированного молочного материала стадии удаления лактозы с получением раствора, имеющего соотношение лактоза: олигосахариды менее 100;
c) необязательное осветление указанного раствора;
d) обработку необязательно осветленного раствора β-галактозидазой для получения жидкости, содержащей β-галактоолигосахариды;
e) необязательную деминерализацию, например, путем прохождения раствора через колонку со слабым катионитом и, необязательно, через колонку со смешанным сорбентом и/или анионообменную колонку;
f) проведение нанофильтрации, которая может осуществляться перед или после необязательной стадии деминерализации, и должна выполняться после или одновременно с обработкой β-галактозидазой.
В дополнительном аспекте изобретение обеспечивает продукт, получаемый способом по изобретению.
Смесь OS по изобретению обладает преимущественными свойствами. Она имеет температуру стеклования (Tg) в диапазоне 70-85°C, когда указанная смесь имеет влагосодержание 2,5%. Данное физическое свойство позволяет смеси быть легко высушенной распылением, без комкования или прилипания, в отсутствие носителя. Кроме того, смесь OS по изобретению является менее склонной к реакциям Майяра по сравнению с не подвергавшимися нанофильтрации GOS-содержащими смесями OS. Относительно высокая температура Tg при таком влагосодержании обеспечивает лучшую физическую стабильность при хранении.
Смесь OS по изобретению может быть включена в питательную композицию, например в стартовую детскую смесь, детскую смесь, детское питание, зерновые композиции (каши) для младенцев, детскую смесь для подросших детей или молочную смесь для детей 1-3 лет, предпочтительно в стартовую детскую смесь.
Поэтому такая питательная композиция является задачей настоящего изобретения.
Другим аспектом изобретения является применение питательных композиций, содержащих смесь OS по изобретению, для усиления иммунной защиты и/или снижения риска инфекций и/или уменьшения случаев пищевой аллергии и связанного с пищевой аллергией воздействия на здоровье.
Краткое описание чертежей
Фигура 1:
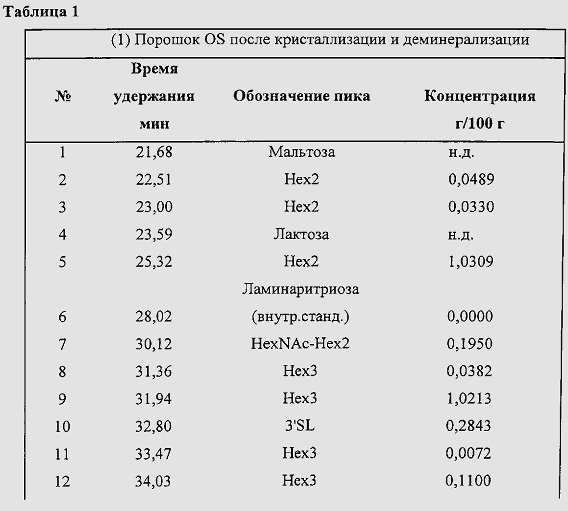
Общую растворимую фракцию олигосахаридов коровьего молока (CMOS) и смесей олигосахаридов коровьего молока/β-галактоолигосахаридов (CMOS-GOS) определяли по ВЭЖХ в трех стадиях способа Примера 1. ВЭЖХ-хроматограммы соответствуют данным, полученным для образцов: (1) порошка OS после частичного удаления лактозы путем кристаллизации и деминерализации; (2) OS-GOS, образованных путем гидролиза с β-галактозидазой для образования GOS; и (3) нанофильтрованных OS-GOS после нанофильтрации (соответствующих нано-OS-GOS в Примере 2). Для того чтобы хроматограммы могли быть построены примерно в одинаковом графическом масштабе, образцы (2) OS-GOS и (3) нанофильтрованных OS-GOS разбавляли в 20 и 10 раз соответственно.
Фигура 2:
Температуру стеклования (Tg) измеряли для порошков CMOS-GOS с 30% мальтодекстринового носителя (показаны черным цветом), CMOS-GOS с 30% лактозы (показаны пунктиром) и нанофильтрованной смеси CMOS-GOS согласно изобретению (показана серым цветом). Влагосодержание образцов определяли методом Карла Фишера. Не удалось получить значения для температур стеклования CMOS-GOS в отсутствие носителя, поскольку образцы нельзя было высушить до требуемого уровня влажности без добавления носителя. Тем не менее данные, как представляется, указывают на то, что в отсутствие носителя, значение Tg для не подвергавшихся нанофильтрации CMOS-GOS будет составлять примерно 35-40°C. Определения Tg проводились с помощью дифференциальной сканирующей калориметрии (DSC)
Фигура 3:
Процентное содержание блокированного лизина (за счет реакции Майяра) определяли в трех детских смесях, подробно описанных в табл. 2. Измерения проводили перед (показано серым цветом) и после (показано черным цветом) распылительной сушки. Распылительную сушку проводили при 92°C. На графике столбцы «CMOS Vivinal» представляют данные для жидкого концентрата (серый цвет) и порошка (черный цвет) детских смесей, к которым добавляли не подвергавшуюся нанофильтрации GOS-фракцию (Vivinal® GOS от FrieslandCampina) и не подвергавшуюся нанофильтрации CMOS фракцию (см. табл. 2). Столбцы «Нано-CMOS-GOS, влажное добавление» представляют данные для детских смесей (жидкий концентрат и порошок), в которые добавляли нанофильтрованную смесь CMOS-GOS согласно изобретению в виде влажной смеси. Столбцы «Нано-CMOS-GOS, сухое добавление» представляют данные для детской смеси (жидкий концентрат и порошок), в которую добавляли нанофильтрованную смесь CMOS-GOS согласно изобретению в виде сухого порошка.
Раскрытие изобретения
Определения:
В данном описании приведенные ниже термины имеют следующие значения.
Термин «младенец» означает ребенка младше 12 месяцев.
Термин «ребенок младшего возраста» означает ребенка в возрасте от одного до трех лет.
Термин «детская смесь» означает пищевой продукт, предназначенный специально для питания младенцев в течение первых четырех-шести месяцев жизни и удовлетворяющий сам по себе потребности в пище этой категории лиц (статья 2 директивы Европейской комиссии 2006/141/ЕС от 22 декабря 2006 года по детским смесям и детским смесям для подросших детей).
Термин «детская смесь для подросших детей» означает пищевой продукт, предназначенный специально для питания младенцев в возрасте старше четырех месяцев, и составляющий основной жидкостный компонент во все более разнообразном рационе этой категории лиц.
Термин «стартовая детская смесь» означает пищевой продукт, предназначенный специально для питания младенцев в течение первых четырех месяцев жизни.
Термин «детское питание» означает пищевой продукт, предназначенный специально для питания младенцев в течение первых лет жизни.
Термин «зерновая композиция (каша) для младенцев» означает пищевой продукт, предназначенный специально для питания младенцев в течение первых лет жизни.
Термин «молочная смесь для детей 1-3 лет» означает напиток на основе молока, адаптированный к конкретным потребностям в питании детей младшего возраста.
Термин «повышение пероральной толерантности к аллергенам» означает снижение чувствительности к аллергенам при приеме внутрь.
Термин «питательная композиция» означает композицию для питания субъекта. Данную питательную композицию обычно принимают перорально или внутривенно, и она обычно включает липиды или источник жира и источник белка.
Термин «синтетическая композиция» означает композицию, полученную с помощью химических и/или биологических (например, ферментов) средств, которая может быть химически идентична смеси, встречающейся естественным образом в молоке млекопитающих.
Термин «гипоаллергенная композиция» означает композицию, которая вряд ли будет вызывать аллергические реакции.
Термин «олигосахарид» означает сахаридный полимер, содержащий небольшое количество (обычно от двух до десяти) моносахаридных компонентов.
Термин «сиалилированный олигосахарид» означает олигосахарид, содержащий остаток сиаловой кислоты.
Термин «пребиотик» означает неперевариваемые углеводы, которые благотворно влияют на организм хозяина путем выборочной стимуляции роста и/или активности полезных бактерий, таких как бифидобактерии в толстой кишке человека {Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J. Nutr. 1995; 125:1401-12).
Термин «пробиотик» означает препараты микробных клеток или компоненты микробных клеток с благоприятным влиянием на здоровье или самочувствие организма-хозяина (Salminen S, Ouwehand A. Bermo Y. et al. "Probiotics: how should they be defined' Trends Food Sci. Technol. 1999:10 107-10).
«Аллергия» означает аллергию, которая была диагностирована врачом и которую можно лечить периодически или более длительным образом. «Пищевая аллергия» является аллергией в отношении питательной композиции.
Термин «олигосахаридный профиль» означает своеобразие состава олигосахаридов.
Все процентные содержания являются массовыми, если не указано иное.
Олигосахариды:
Олигосахариды (OS) определены в настоящем описании как олисахариды, встречающиеся естественным образом в молоке животных и имеющие степень полимеризации (DP) в диапазоне от 3 до 20. Данные олигосахариды растворимые в молоке. Все последующие ссылки на олигосахариды в тексте относятся к растворимым (в молоке) олигосахаридам, если не указано иное. Настоящее изобретение предлагает смесь олигосахаридов, полученную из коровьего молока, которая имеет соотношение лактоза (DP=2):олигосахариды менее 20, более предпочтительно менее 10 и предпочтительно между 8 и 1,25. Это соответствует снижению содержания лактозы в смеси олигосахаридов в 4-200 раз по сравнению с исходным коровьим молоком, что эквивалентно повышению соотношения между олигосахаридами и лактозой в 4-200 раз. Таким образом, смесь имеет такой же олигосахаридный профиль (т.е. общую растворимую олигосахаридную фракцию), как и профиль в молоке, из которого она была получена (т.е. из которого она произошла), но с гораздо более концентрированным содержанием олигосахаридов.
Смесь олигосахаридов по изобретению также содержит β-галактоолигосахариды (GOS), образующиеся в результате действия β-галактозидазы, главным образом, на лактозу, и также в некоторых случаях, но в гораздо меньшей степени, на некоторые из растворимых олигосахаридов, присутствующих в коровьем молоке (олигосахариды коровьего молока или CMOS). Таким образом, в варианте осуществления β-галактоолигосахариды образуются в результате действия β-галактозидазы на лактозу и на олигосахариды коровьего молока. В ходе получения смеси олигосахаридов добавляют фермент. Какие именно или до какой степени CMOS подвергаются действию фермента, авторами настоящего изобретения не определялось. Таким образом, относительные содержания различных олигосахаридов в смеси олигосахаридов по изобретению могут отличаться от относительных содержаний в коровьем молоке, из которого смесь получена. Фермент β-галактозидаза обладает двоякой активностью: он расщепляет лактозу на моносахариды, галактозу и глюкозу, и, во-вторых, за счет активности трансферазы, он катализирует последующее образование галактоолигосахаридов (GOS). Эти олигосахариды состоят из мономеров глюкозы и галактозы, имеющих степень полимеризации (DP) от 3 до 10, и, как известно, обладают пребиотической активностью.
Существуют более двадцати различных структур GOS, присутствующих в смеси олигосахаридов по настоящему изобретению.
Олигосахаридный профиль может быть охарактеризован по данным ВЭЖХ, масс-спектрометрии и другими способами. В соответствии с предпочтительным способом ВЭЖХ, олигосахариды, присутствующие в образцах, экстрагируются водой при 70°C. Экстрагированные OS флуоресцентно метят по реакции (2 ч при 65°C) амида 2-антраниловой кислоты через образование основания Шиффа. Двойную связь далее восстанавливают путем взаимодействия с цианоборогидридом натрия для получения стабильного олигосахаридно- аминобензамидного (OS-AB) производного. Меченые экстракты разбавляют ацетонитрилом перед введением в ВЭЖХ-флуориметр, оснащенный ловушкой. Разделение осуществляется на колонке Amide-80 3 мкм, 4,6×150 мм, и меченые OS обнаруживаются флуориметром при: Ex 330 нм, Em 420 нм. Количественное определение различных OS выполняется путем калибровки OS-2AB отклика при использовании мальтотриозы в качестве внешнего стандарта и ламинаритриозы в качестве внутреннего стандарта.
На фиг. 1 представлена общая растворимая олигосахаридная фракция в смеси, определенная описанным выше методом ВЭЖХ, для трех последовательных стадий получения смеси OS Примера 1: (1) CMOS после частичного удаления лактозы путем кристаллизации и деминерализации; (2) после гидролиза β-галактозидазой для образования GOS; и (3) после нанофильтрации (соответствует нано-CMOS-GOS в Примере 2). Так выглядит олигосахаридный профиль. Для того чтобы хроматограммы могли быть построены примерно в одинаковом графическом масштабе, образцы (2) OS-GOS и (3) нанофильтрованных OS-GOS разбавляли в 20 и 10 раз соответственно.
Перечень олигосахаридов, определенных по данным ВЭЖХ, приведен в табл. 1. Не все олигосахариды были идентифицированы, но профили в трех хроматограммах очень похожи. Это подтверждает, что группу CMOS исходного коровьего молока действительно присутствует в смеси OS изобретения. Авторы изобретения обратили внимание, что 3'SL пик (соответствующий сиалилолигосахариду 3'-сиалиллактозе) в большей степени заметен на хроматограмме (1), а не на хроматограммах (2) и (3). Полагают, что в ходе стадии гидролиза CMOS бета-галактозидазой один из образованных GOS имеет время удержания, очень близкое ко времени удержания 3'SL, и это мешает отделению 3'SL пика. Авторы изобретения показали, что пики при 32,29 мин (1) и 32,20 мин (2) не являются 3'SL, но скорее представляют структуру GOS (данные не показаны).
Пик, связанный с сиалилолигосахаридом 6'L (Neu5Ac(α2-6)Gal(β1-4)Glc) в хроматограмме (1), больше не виден на хроматограмме (2) из-за разбавления образца CMOS-GOS.
Hex=Гексоза, Hex 2-6=количество гексоз, эквивалентное ди-, три-, тетра-, пента-, гексасахаридам
Смесь OS по изобретению имеет общее содержание моносахаридов менее 5% масс./об., предпочтительно менее 3% масс./об.
Данная смесь может вводиться в пищевые продукты для детей или взрослых и оказывать пребиотическое, иммуномодулирующее и защитное действие.
Хотя смесь олигосахаридов по изобретению получают из коровьего молока, молоко также может быть получено от животного любого вида, в частности от коров, коз, буйволиц, кобыл, слоних, верблюдиц и овец.
Способ получения смеси олигосахаридов:
Исходный материал:
Исходным материалом в способе получения смеси олигосахаридов по изобретению является депротеинизированный молочный материал, такой как молоко, из которого удалены белки, или молочная сыворотка, либо любой обработанный или модифицированный сывороточный материал, из которого удалены сывороточные белки. Такие материалы включают кислую сыворотку и сладкую сыворотку. Предпочтительными исходными материалами являются ультрафильтрат молока и ультрафильтрат сыворотки. Альтернативно исходным материалом может быть восстановленный порошок, например порошкообразный ультрафильтрат.
Исходный материал должен быть депротеинизированным продуктом, поскольку присутствие белков на стадии концентрирования может приводить к нежелательным реакциям Майяра и побурению. Депротеинизация исходного материала может проводиться любыми известными средствами, например осаждением кислотами, термическими способами, ионным обменом. Однако предпочтительно, чтобы удаление белка осуществлялось ультрафильтрацией, в ходе которой из исходного материала удаляются и липиды.
Значение pH исходного материала может составлять от 3 до 7,5, хотя pH в диапазоне от 5 до 6 является предпочтительным, так как способствует предотвращению гидролиза олигосахаридов, например десиалилирования сиалиллактозы, и также снижению риска реакций побурения.
а. Концентрирование исходного материала
Депротеинизированный молочный материал концентрируют до 50 до 75% общего содержания сухих веществ (TS), предпочтительно от 55 до 60% TS, любыми известными средствами, при условии, что температура не повышается до уровня, при котором может происходить гидролиз (например, десиалилирование) олигосахаридов. Концентрирование предпочтительно проводится при температурах от 50°C до 90°C, более предпочтительно от 50°C до 75°C. Выпаривание является одним из предпочтительных способов, которое проводится при давлении от 80 до 200 мбар. В данном способе температура не повышается выше 60°C, что гарантирует отсутствие вредного воздействия на олигосахариды. Альтернативно, если исходный материал представляет собой порошок, то концентрирование до требуемого уровня может достигаться соответствующим восстановлением порошка.
b. Удаление лактозы
Предпочтительно, стадию удаления лактозы выполняют путем кристаллизации и удаления кристаллов лактозы. Например, кристаллизация лактозы может проводиться в концентрированном исходном материале путем охлаждения концентрированного материала с добавлением или без добавления затравки кристаллов. Кристаллы лактозы удаляются затем любым известным способом, например центрифугированием, фильтрацией и/или декантацией. Альтернативный способ отделения лактозы от олигосахаридов основан на разнице в растворимости. Исходный материал подвергается распылительной сушке, после чего добавляется вода для растворения олигосахаридов, в то время как лактоза остается в кристаллизованной форме.
Полученный раствор обогащен большим количеством олигосахаридов, при этом отношение олигосахариды:лактоза в нем в 2-200 раз превышает указанное отношение, определенное в молоке, из которого указанный раствор был получен.
Раствор может подвергаться повторному концентрированию как описано выше, и далее может осуществляться стадия удаления лактозы. Этот процесс может повторяться многократно по мере необходимости. Конечное отношение лактозаголигосахариды составляет менее 250, предпочтительно менее 125, более предпочтительно менее 100, еще более предпочтительно менее 20, наиболее предпочтительно менее 10.
Данная стадия может осуществляться в соответствии с известными способами.
c. Осветление жидкости
Данная стадия является необязательной и может осуществляться любым способом, известным специалисту, например центрифугированием.
d. Обработка депротеинизированного раствора β-галактозидазой для получения раствора, содержащего β-галактоолигосахариды (GOS)
Соответственно раствор может обрабатываться β-галактозидазой перед концентрированном молочного материала (стадия (а)) и/или после стадии(й) удаления лактозы (стадия (b)). Предпочтительно это происходит после завершения стадии(й) удаления лактозы. Предпочтительно используется β-галактозидаза, продуцируемая Aspergillus oryzae. Такой фермент коммерчески доступен в виде Lactase F от Amano, Япония, или в виде концентрата Enzeco Fungal Lactase от Enzyme Development Corporation (EDC), Нью-Йорк, США. Активность фермента, измеряемая в соответствии с методом FCCIV (Международного производственного стандарта), может составлять от 1000 до 30000 ед./кг лактозы. Обработка ферментом может проводиться при pH в диапазоне от 3 до 7 и температуре от 4°C до 70°C на исходном материале с концентрацией лактозы от 5 до 70 г/100 г общего содержания сухих веществ (TS) при концентрации фермента 0,5-10 г/кг смеси олигосахаридов.
Предпочтительно, около 1,5 г фермента используют на 1 кг сухого вещества смеси олигосахаридов, и время инкубации составляет от 1 до 8 часов при 20-70°C. После использования фермент может инактивироваться нагреванием.
После обработки 0,5-6 мг β-галактозидазой на 1 г TS раствора, имеющего содержание TS 25-50% и приблизительно 15-40% лактозы, образующийся в результате раствор может содержать приблизительно 1-4% олигосахаридов, приблизительно 9-25% GOS, приблизительно 15-30% лактозы, приблизительно 5-15% галактозы и приблизительно 2-15% глюкозы. Отношение олигосахариды: β-галактоолигосахариды (GOS) предпочтительно находится в диапазоне от 1:2 до 1:25, более предпочтительно от 1:5 до 1:20.
e. Стадия деминерализации
Данная стадия является необязательной. Раствор может быть деминерализован любыми известными способами, например ионным обменом, электродиализом, ультрафильтрацией или сочетанием данных способов. Например, материал может быть пропущен через колонку со слабым катионитом и колонку со смешанным сорбентом и/или анионообменную колонку, с последующим электродиализом или нанофильтрацией. Данную стадию деминерализации можно проводить при значениях pH, соответствующих нейтральному или кислому диапазону. Она может выполняться перед или после стадии гидролиза (d). Она также может выполняться частично перед гидролизом и частично после гидролиза.
f. Стадия нанофильтрации
Данная стадия имеет важное значение для способа изобретения. При нанофильтрации из раствора удаляются одновалентные катионы и анионы и моносахариды. Желательно удалять моносахариды из смеси, поскольку (i) они не обладают пребиотической активностью и (ii) они вызывают нежелательные реакции с белками, когда пребиотический ингредиент используется для получения детских смесей. Например, моносахариды могут привести к реакции Майяра, в которой лизиновые остатки белков блокируются, тем самым уменьшая питательное качество детской смеси. Лизин является незаменимой аминокислотой, которая должна быть представлена в рационе питания, а блокированный лизин не доступен для организма. Таким образом, желательно уменьшить количество случаев реакции Майяра в процессе получения детской смеси.
Кроме того, чем ниже концентрация моносахаридов в смеси, тем выше может быть концентрация олигосахаридов.
Неожиданно авторы изобретения обнаружили также, что более низкие содержания моносахаридов позволяют высушивать смесь олигосахаридов как есть, без добавления носителя. Как правило, CMOS-GOS смеси требуют присутствия 25-35% носителя (такого как, например, мальтодекстрин или лактоза), для получения порошка. Необязательность носителя для получения порошка является значительным преимуществом при получении и использовании CMOS-GOS смесей по изобретению.
После нанофильтрации образующийся в результате раствор должен иметь концентрацию моносахаридов менее 5% масс./об., предпочтительно менее 3% масс./об., и отношение лактоза:олигосахариды менее 20, предпочтительно менее 10.
Нанофильтрация осуществляется путем прохождения раствора через мембрану с размером пор, достаточно малым для удержания олигосахаридов, но достаточно большим для пропускания моносахаридов. Для этой цели могут использоваться известные в области техники коммерческие мембраны с границей отсечки по молекулярному весу в диапазоне 200-1000 Дальтон. Среди прочих, в качестве неограничивающего примера мембран, которые могут использоваться, можно при