Вирионы аденоассоциированного вируса с вариантным капсидом и способы их использования
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, вирусологии и медицины. Предложены вирионы аденоассоциированного вируса (AAV) с вариантным капсидным белком, где вирионы AAV демонстрируют большую инфекционность ретинальной клетки, когда вводятся интравитреальной инъекцией, по сравнению с AAV дикого типа. Также описаны способы доставки генного продукта в ретинальную клетку индивидуума и способы лечения глазных болезней. 6 н. и 18 з.п. ф-лы, 25 ил., 2 табл., 3 пр.
Реферат
Перекрестная ссылка на родственные заявки
[0001] Эта заявка испрашивает приоритет предварительной заявки на патент США №61/478,355, поданной апреля 22, 2011, описание которой во всей полноте включено в настоящую заявку путем ссылки.
Заявление относительно федерально спонсируемого исследования
[0002] Это изобретение было сделано при государственной поддержке под Грантом № EY016994-02 и EY1018241, предоставленным Национальным офтальмологическим институтом Национального института здравоохранения. Государство обладает определенными правами на изобретение.
Уровень техники
[0003] Фоторецепторы являются первыми нейронами в сетчатке, которые получают и обрабатывают визуальную информацию, преобразовывая видимую электромагнитную радиацию в гиперполяризованные ответы через фототрансдукцию. Подавляющее большинство унаследованных ретинальных болезней приводит к потере этих клеток или непосредственно, например, в доминантных мутациях, которые влияют на укладку белка родопсина, или косвенно, например, в рецессивных мутациях, влияющих на ретинальные метаболические циклы в пигментном эпителии сетчатки (RPE).
[0004] AAV принадлежит семейству Parvoviridae и роду Dependovirus, представители которого требуют совместного инфицирования с вирусом-помощником, таким как аденовирус, для активирования репликации, AAV порождает латентную инфекцию в отсутствие помощника. Вирионы состоят из 25 нм икосаэдрического капсида, охватывающего одноцепочечную геномную ДНК, состоящую из 4,9 тысяч нуклеотидов, с двумя открытыми рамками считывания: rep и cap. Неструктурный ген rep кодирует четыре регуляторных белка, важных для вирусной репликации, тогда как cap кодирует три структурных белка (VP1-3), которые собираются в 60-мерную капсидную оболочку. Этот вирусный капсид содействует способности векторов AAV преодолевать многие биологические барьеры вирусной трансдукции, включая связывание рецепторов клеточной поверхности, эндоцитоз, внутриклеточную миграцию и распаковывание в ядре.
Литература
[0005] Патентная публикация США №2005/0053922; патентная публикация США №2009/0202490; Allocca et al. (2007) J. Virol. 81:11372; Boucas et al. (2009) J. Gene Med. 11:1103.
Сущность изобретения
[0006] Настоящее раскрытие обеспечивает вирионы аденоассоциированного вируса (AAV) с измененным капсидным белком, отличающийся тем, что вирионы AAV демонстрируют большую инфекционность клетки сетчатки, когда вводятся путем интравитреальной инъекции, по сравнению с AAV дикого типа. Настоящее раскрытие также обеспечивает способы доставки генного продукта в клетку сетчатки индивидуума и способы лечения глазных болезней.
Краткое описание чертежей
[0007] На фигуре 1 представлена репрезентативная трехмерная модель AAV2, содержащего случайный гептамер после аминокислоты 587.
[0008] На фигуре 2 изображены более значительные уровни интравитреальной трансдукции вариантом 7М8 AAV2 (справа) относительно AAV2 (слева).
[0009] На фигуре 3 представлены репрезентативные флюоресцентные изображения криосрезов сетчатки, показывающие экспрессию зеленого флуоресцентного белка (GFP), возникающую вследствие 7М8 переноса гена GFP под контролем убиквитарного промотора CAG (слева) или фоторецептор специфического промотора Rho (справа).
[0010] На фигуре 4 изображены фоторецепторные клетки GFP+ на миллион клеток сетчатки, как подсчитано поточной цитометрией, после трансдукции 7М8 или 7М8, несущих 4 тирозиновые мутации (7m8.4YF).
[0011] На фигуре 5 представлена аминокислотная последовательность VP1 AAV2 (SEQ ID №1).
[0012] На фигуре 6 представлены аминокислотные последовательности, соответствующие аминокислотам 570-610 AAV2 (фигура 5) капсидного белка VP1 AAV различных серотипов AAV.
[0013] На фигурах 7A-I изображены структурные улучшения в мышиной сетчатке Rs1h-/- после переноса гена.
[0014] На фигурах 8A-D изображено функциональное спасение волн А и В электроретинограммы после доставки гена RS1.
[0015] На фигурах 9А-Е изображены устойчивые улучшения толщины сетчатки, измеренной спустя 10 месяцев после лечения 7m8-rho-RS1.
[0016] На фигуре 10 представлена аминокислотная последовательность ретиношизина.
[0017] На фигуре 11 представлена аминокислотная последовательность нейротрофического фактора головного мозга.
[0018] На фигуре 12 представлена аминокислотная последовательность RPE65.
[0019] На фигурах 13А-С представлена нуклеотидная последовательность конструкта 7m8-rho-RS1.
[0020] На фигуре 14 представлена аминокислотная последовательность периферина-2.
[0021] На фигуре 15 представлена аминокислотная последовательность периферина.
[0022] На фигуре 16 представлена аминокислотная последовательность регуляторного взаимодействующего белка-1 ГТФазы пигментной дистрофии сетчатки.
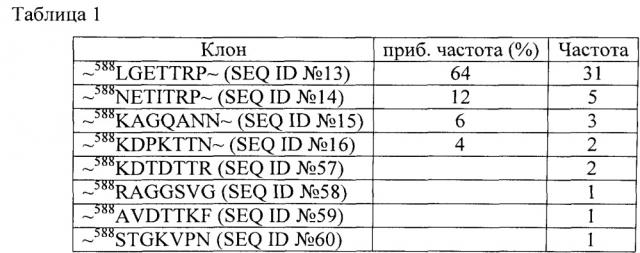
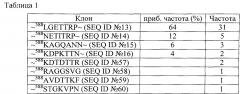
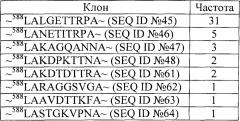
[0023] На фигурах 17А-С представлено выравнивание аминокислотных последовательностей участков петли IV капсидного белка AAV (петля GH). Сайты встраивания показаны жирным шрифтом и подчеркиванием.
[0024] На фигурах 18А-С представлено выравнивание аминокислотных последовательностей участков петли капсидного белка GH AAV с гетерологичными пептидными встраиваниями.
[0025] На фигуре 19 представлено флуоресцентное изображение дна, показывающее экспрессию GFP в центре сетчатки примата спустя 9 недель после введения 7m8, несущего GFP под управлением промотора коннексина-36.
Определения
[0026] Термин "ретинальная клетка" может относиться в настоящем документе к любому из клеточных типов, которые содержит сетчатка, такому как ретинальные клетки ганглия, амакринные клетки, горизонтальные клетки, биполярные клетки и клетки фоторецептора, включая палочки и колбочки, глиальные клетки Мюллера, клетки пигментного эпителия сетчатки.
[0027] "AAV" является аббревиатурой для аденоассоциированного вируса и может быть использована для обозначения самого вируса или его производных. Термин охватывает все подтипы и природного происхождения, и рекомбинантные формы, за исключением случаев, когда требуется иное. Аббревиатура "rAAV" относится к рекомбинантному аденоассоциированному вирусу, также именуемого рекомбинантным вектором AAV (или "вектор rAAV"). Термин "AAV" включает AAV тип 1 (AAV-1), AAV тип 2 (AAV-2), AAV тип 3 (AAV-3), AAV тип 4 (AAV-4), AAV тип 5 (AAV-5), AAV тип 6 (AAV-6), AAV тип 7 (AAV-7), AAV тип 8 (AAV-8), птичий AAV, бычий AAV, псовый AAV, конский AAV, приматный AAV, неприматный AAV и овечий AAV. "Приматный AAV" относится к AAV, который инфицирует приматов, "неприматный AAV" относится к AAV, который инфицирует неприматных млекопитающих, "бычий AAV" относится к AAV, который инфицирует жвачных млекопитающих и пр.
[0028] Геномные последовательности различных серотипов AAV, также как и последовательности природных концевых повторов (TR), белков Rep и капсидных субъединиц известны из уровня техники. Такие последовательности могут быть найдены в литературе или общедоступных базах данных, таких как GenBank. Смотри, например, номера доступов GenBank NC_002077 (AAV-1), AF063497 (AAV-1), NC_001401 (AAV-2), AF043303 (AAV-2), NC_001729 (AAV-3). NC_001829 (AAV-4), U89790 (AAV-4), NC_006152 (AAV-5), AF513851 (AAV-7), AF513852 (AAV-8) и NC_006261 (AAV-8); сведения которых включены в настоящий документ путем ссылки касательно последовательностей нуклеиновых кислот и аминокислот AAV. Смотри также, например, Srivistava et al. (1983) J. Virology 45:555; Chiorini et al. (1998) J. Virology 71:6823; Chiorini et al. (1999) J. Virology 73:1309; Bantel-Schaal et al. (1999) J. Virology 73:939; Xiao et al. (1999) J. Virology 73:3994; Muramatsu et al. (1996) Virology 221:208; Shade et al., (1986) J. Virol. 58:921; Gao et al. (2002) Proc. Nat. Acad. Sci. USA 99:11854; Moris et al. (2004) Virology 33:375-383; международные патентные публикации WO 00/28061, WO 99/61601, WO 98/11244; и патент США №6156303.
[0029] "Вектор rAAV", как использовано в настоящем документе, относится к вектору AAV, содержащему полинуклеотидную последовательность, которая происходит не от AAV (т.е., полинуклеотид, ксеногенный к AAV), обычно последовательность, представляющую интерес для генетической трансформации клетки. В основном, гетерологичный полинуклеотид является фланкированным, по меньшей мере, одной или обычно двумя последовательностями инвертированных концевых повторов AAV (ITR). Термин вектор rAAV охватывает как части вектора rAAV, так и векторные плазмиды rAAV. Вектор rAAV может быть либо одноцепочечным (ssAAV), либо самокомплементарным (scAAV).
[0030] "Вирус AAV" или "частица вируса AAV", или "частица вектора rAAV" относится к частице вируса, состоящей из, по меньшей мере, одного капсидного белка AAV (обычно всех капсидных белков AAV дикого типа) и инкапсулированного полинуклеотида вектора rAAV. Если частица содержит гетерологичный полинуклеотид (т.е. полинуклеотид, не являющийся геномом AAV дикого типа, такой как трансген, который будет доставлен в клетку млекопитающего), обычно упоминается как "частица вектора rAAV" или просто "вектор rAAV". Таким образом, получение частицы rAAV обязательно включает получение вектора rAAV как такового, и вектор содержится в пределах частицы rAAV.
[0031] "Упаковывание" относится к серии внутриклеточных событий, которые приводят к сборке и инкапсулированию частицы AAV.
[0032] Гены "rep" и "cap" AAV относятся к полинуклеотидным последовательностям, кодирующим репликацию и капсидирующие белки аденоассоциированного вируса. "Rep" и "cap" AAV именуются в настоящем документе как "упаковочные гены" AAV.
[0033] "Вирус-помощник" для AAV относится к вирусу, который позволяет AAV (например, AAV дикого типа) реплицироваться и упаковываться с помощью клетки млекопитающего. Ряд таких вирусов-помощников для AAV известны из уровня техники, включая аденовирусы, герпевирусы и проксивирусы, такие как вирус коровьей оспы. Аденовирусы охватывают много различных подгрупп, хотя обычно используется аденовирус 5 типа, подгруппы С. Известны многочисленные аденовирусы человека, нечеловеческих млекопитающих и птичьего происхождения и доступные из депозитариев, таких как АТСС. Вирусы семейства герпеса включают, например, вирусы герпеса простого (HSV) и вирусы Эпштейн-Барра (EBV), а также вирусы цитомегалии (CMV) и вирусы псевдобешенства (PRV); которые также доступны из депозитария АТСС.
[0034] "Хелперная вирусная функция(и) относится к функции(ям), закодированной в геноме вируса-помощника, который позволяет AAV реплицироваться и упаковываться (в сочетании с другими необходимыми условиями для репликации и упаковывания, описанными в настоящем документе). Как описано в настоящем документе, "хелперная вирусная функция" может обеспечивать ряд путей, включая обеспеченные вирусами-помощниками или обеспеченные, например, полинуклеотидными последовательностями, кодирующими необходимую функцию(и) в клетке-продуценте в пути. Например, плазмиду или другой вектор экспрессии, содержащий нуклеотидные последовательности, кодирующие один или более аденовирусных белков, трансфектируют в клетку-продуцент вместе с вектором rAAV.
[0035] "Инфекционный" вирус или вирусная частица является вирусом, который содержит компетентно собранный вирусный капсид и способен доставить полинуклеотидный компонент в клетку, для которой вирусный вид является тропическим. Термин не обязательно подразумевает любую репликационную способность вируса. Методы подсчета инфекционных вирусных частиц описаны в другом разделе в этом описании и в уровне техники. Вирусная инфекционность может быть выражена как отношение инфекционных вирусных частиц ко всем вирусным частицам. Способы определения отношения инфекционных вирусных частиц ко всем вирусным частицам известны из уровня техники. Смотри, например, Grainger et al. (2005) Mol. Ther. 11:S337 (описывающий анализ инфекционного титра TCID50); и Zolotukhin et al. (1999) Gene Ther. 6:973. Смотри также Примеры.
[0036] "Репликационно компетентный" вирус (например, репликационно компетентный AAV) относится к фенотипичному вирусу дикого типа, который является инфекционным, а также способен реплицироваться в инфицированной клетке (то есть, в присутствии вируса-помощника или хелперных вирусных функций). В случае AAV, репликационная компетенция обычно требует присутствия функциональных упаковочных генов AAV. В целом, векторы rAAV, как описано в настоящем документе, являются репликационно некомпетентными в клетках млекопитающих (особенно в клетках человека) из-за отсутствия одного или более упаковочных генов AAV. Обычно, такие векторы rAAV испытывают недостаток в любых последовательностях упаковочных генов AAV, чтобы минимизировать возможность того, что репликационная компетенция AAV генерируется рекомбинацией между упаковочными генами AAV и поступающим вектором rAAV. Во многих вариантах осуществления изобретения препараты вектора rAAV, как описано в данном документе, являются такими, что почти не содержат репликационно компетентного AAV (rcAAV, также именуемый как RCA) (например, меньше, чем приблизительно 1 rcAAV на 102 частиц rAAV, меньше, чем приблизительно 1 rcAAV на 104 частиц rAAV, меньше, чем приблизительно 1 rcAAV на 108 частиц rAAV, меньше, чем приблизительно 1 rcAAV на 1012 частиц rAAV или rcAAV отсутствует).
[0037] Термин "полинуклеотид" относится к полимерной форме нуклеотидов любой длины, включая дезоксирибонуклеотиды или рибонуклеотиды или их аналоги. Полинуклеотиды могут содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды и нуклеотидные аналоги, и могут быть прерванными ненуклеотидными компонентами. Если имеются, то модификации нуклеотидной структуре могут придаваться до или после сборки полимера. Термин полинуклеотид, как использовано в настоящем документе, относится взаимозаменяемо к дву- и одноцепочечным молекулам. Если не определено и не требуется иное, то любой вариант осуществления изобретения, описанного в настоящем документе, которое является полинуклеотидом, охватывает как двуцепочечную форму, так и каждую из двух комплементарных одноцепочечных форм, известных или предсказанных для составления двуцепочечной формы.
[0038] Реакции гибридизации нуклеиновых кислот могут проводиться в условиях разной "жесткости". Условия, повышающие жесткость реакции гибридизации широко известны и опубликованы в уровне техники. Смотри, например, Sambrook et al. Molecular Cloning, A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989, включенный в настоящий документ путем ссылки. Например, смотри страницу 7.52 в Sambrook et al. Примеры соответствующих условий включают (в порядке повышающейся жесткости): температуры инкубации 25°С, 37°С, 50°С и 68°С; буферные концентрации 10 × SSC, 6 × SSC, 1 × SSC, 0,1 × SSC (где 1 × SSC является 0,15 М NaCl и 15 мМ цитратным буфером) и их эквиваленты с использованием других буферных систем; концентрации формамида 0%, 25%, 50% и 75%; время инкубирования от 5 минут до 24 часов; 1, 2 или более стадий отмывания; инкубационное время отмывки 1, 2 или 15 минут; и отмывочные растворы 6 × SSC, 1 × SSC, 0.1 × SSC или деионизированная вода. Примером жестких условий гибридизации является гибридизация при 50°С или выше и 0,1 × SSC (15 мМ хлорида натрия/1,5 мМ цитрата натрия). Другим примером жестких условий гибридизации является инкубирование в течение ночи при 42°С в растворе: 50% формамида, 1 × SSC (150 мМ NaCl, 15 мМ цитрата натрия), 50 мМ фосфата натрия (рН 7,6), 5 × раствора Денхардта, 10% сульфата декстрана и 20 мкг/мл денатурированной, расщепленной ДНК из молок лососевых, с последующим отмыванием фильтров в 0,1 × SSC при приблизительно 65°C. Как другой пример, жесткие условия гибридизации включают: предварительную гибридизацию в течение от 8 часов до ночи при 65°С в растворе, содержащем 6Х SSC (1X SSC является 0,15 М NaCl, 0,015 М цитрата Na; рН 7,0), 5Х раствора Денхардта, 0,05% фосфата натрия и 100 мкг/мл ДНК спермы сельди; гибридизация в течение 18-20 часов при 65°С в растворе, содержащем 6Х SSC, 1X раствора Денхардта, 100 мкг/мл тРНК дрожжей и 0,05% фосфата натрия; отмывание фильтров при 65°С в течение одного часа в растворе, содержащем 0,2Х SSC и 0,1% SDS (додецилсульфата натрия).
[0039] Жесткие условия гибридизации являются условиями гибридизации, которые, по меньшей мере, столь же жесткие как представленные выше условия. Другие жесткие условия гибридизации известны из уровня техники и также могут быть применены для идентификации нуклеиновых кислот этого определенного варианта осуществления изобретения.
[0040] "Tm" является температурой в градусах Цельсия, при которой 50% полинуклеотидного дуплекса, образованного комплементарными нитями, соединенными водородными связями в антипараллельном направлении спариванием оснований Уотсона-Крика, диссоциирует в одиночную нить в условиях эксперимента. Tm может быть предсказана согласно стандартной формуле, такой как:
[0041] Tm=81,5+16,6 log[X+]+0,41 (% G/C)-0,61 (% F)-600/L
[0042] где [Х+] является концентрацией катионов (особенно ионов натрия, Na+ в моль/л; (% G/C) является количеством остатков G и С как процент всех остатков в дуплексе;
(% F) является процентным содержанием формамида в растворе (вес/об); и
L является количеством нуклеотидов в каждой нити дуплекса.
[0043] Полинуклеотид или полипептид имеют определенную процентную "идентичность последовательности" с другим полинуклеотидом или полипептидом, обозначающую что, при выравнивании этот процент оснований или аминокислот является таким же при сравнении этих двух последовательностей. Подобие последовательностей может быть определено многими различными способами. Для определения идентичности последовательностей последовательности могут выравниваться с использованием методов и компьютерных программ, включая BLAST, доступный из всемирной компьютерной сети с ncbi.nlm.nih.gov/BLAST/. Другим алгоритмом выравнивания является FASTA, доступный из пакета Genetics Computing Group (GCG) из Madison, Wisconsin, USA, находящегося в полной собственности филиала Oxford Molecular Group, Inc. Другие методы выравнивания описаны в Methods in Enzymology, vol. 266: Computer Methods for Macromolecular Sequence Analysis (1996), ed. Doolittle, Academic Press, Inc., a division of Harcourt Brace & Co., San Diego, California, USA. Особенно интересными являются программы выравнивания, которые разрешают пропуски в последовательности. Алгоритм Смита-Уотермана является одним из типов алгоритма, который разрешает пропуски при выравнивании последовательностей. Смотри Meth. Mol. Biol. 70:173-187 (1997). Также, программа GAP, использующая метод выравнивания Нидлмана-Вунша, может быть применена для выравнивания последовательностей. См. J. Mol. Biol. 48:443-453 (1970)
[0044] Представляющей интерес является программа BestFit, использующая алгоритм локальной гомологии Смита и Уотермана (Advances in Applied Mathematics 2:482-489 (1981), для определения идентичности последовательностей. Штраф за образование пропусков будет обычно заключаться в пределах от 1 до 5, обычно от 2 до 4 и во многих вариантах осуществления изобретения будет составлять 3. Штраф за продолжения пропуска будет обычно заключаться в пределах от приблизительно 0,01, до 0,20, и во многих случаях будет составлять 0,10. Программа содержит параметры, используемые по умолчанию, определенные с помощью последовательностей, введенных для сравнения. Предпочтительно, идентичность последовательностей определяется с помощью параметров по умолчанию, определенных программой. Эта программа доступна также из пакета Genetics Computing Group (GCG) из Madison, Wisconsin, USA.
[0045] Другой представляющей интерес программой является алгоритм FastDB. FastDB описан в Current Methods в Sequence Comparison и Analysis, Macromolecule Sequencing и Synthesis, Selected Methods и Applications, pp.127-149, 1988, Alan R. Liss, Inc. Процент идентичности последовательностей рассчитывают с помощью FastDB, исходя из следующих параметров:
[0046] штраф за нарушение комплементарности: 1.00;
[0047] штраф за пропуск в последовательности: 1.00;
[0048] штраф за размер пропуска: 0.33; и
[0049] штраф за стыки: 30.0.
[0050] "Ген" относится к полинуклеотиду, содержащему, по меньшей мере, одну открытую рамку считывания, которая способна кодировать определенный белок после транскрипции и трансляции.
[0051] "Генный продукт" является молекулой, полученной в результате экспрессии определенного гена. Генные продукты включают, например, полипептид, аптамер, интерферирующую РНК, мРНК и т.п.
[0052] "Малые интерферирующие РНК" или "короткие интерферирующие РНК " или миРНК являются РНК-дуплексами нуклеотидов, которые ориентированы на представляющий интерес ген ("ген-мишень"). "РНК-дуплекс" относится к структуре, образованной комплементарным спариванием между двумя участками молекулы РНК. миРНК является "нацеленной" на ген, в котором нуклеотидная последовательность части дуплекса миРНК комплементарна нуклеотидной последовательности нацеленного гена. В некоторых вариантах осуществления изобретения длина дуплекса миРНК составляет меньше чем 30 нуклеотидов. В некоторых вариантах осуществления изобретения дуплекс может составлять 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11 или 10 нуклеотидов в длину. В некоторых вариантах осуществления изобретения длина дуплекса составляет 19-25 нуклеотидов в длину. РНК-дуплексная часть миРНК может быть частью шпилькообразной структуры. В дополнение к дуплексной части шпилькообразная структура может содержать петлевую часть, находящуюся между двумя последовательностями, образующими дуплекс.Длина петли может меняться. В некоторых вариантах осуществления изобретения петля является в 5, 6, 7, 8, 9, 10, 11, 12 и 13 нуклеотидов в длину. Шпилькообразная структура может также содержать 3' или 5' "липкие" части. В некоторых вариантах осуществления изобретения "липкий" конец является 3' или 5' концом 0, 1, 2, 3, 4 или 5 нуклеотидов в длину.
[0053] "Короткая шпилечная РНК" или кшРНК является полинуклеотидным конструктом, который может быть получен для экспрессии интерферирующих РНК, таких как миРНК.
[0054] "Рекомбинант" в применении к полинуклеотиду означает, что полинуклеотид является продуктом различных комбинаций клонирования, этапов рестрикции или лигирования и других процедур, которые приводят к конструкту, который отличается от найденного в природе полинуклеотида. Рекомбинантный вирус является вирусной частицей, содержащей рекомбинантный полинуклеотид. Термины соответственно включают репликации оригинального полинуклеотидного конструкта и потомство оригинального вирусного конструкта.
[0055] "Регуляторный элемент" или "регуляторная последовательность" является нуклеотидной последовательностью, вовлеченной во взаимодействие молекул, которая способствует функциональному регулированию полинуклеотида, включая репликацию, дупликацию, транскрипцию, сплайсинг, трансляцию или деградацию полинуклеотида. Регулирование может влиять на частоту, скорость или специфику процесса и может быть улучшающим или ингибирующим по природе. Известные из уровня техники элементы включают, например, регулирующие транскрипцию последовательности, такие как промоторы и энхансеры. Промотор является участком ДНК, способным в определенных условиях к связыванию РНК-полимеразы и инициированию транскрипции кодирующей области, обычно располагаемой по ходу транскрипции (в направлении 3') от промотора.
[0056] "Функционально связанный" относится к непосредственному соседству генетических элементов, причем элементы находятся в контакте, позволяющем им работать ожидаемым способом. Например, промотор функционально связан с кодирующей областью, если промотор помогает инициировать транскрипцию кодирующей последовательности. Между промотором и кодирующей областью, до тех пор, пока поддерживается эта функциональная связь, могут находиться интроны.
[0057] "Экспрессионный вектор" является вектором, содержащем область, которая кодирует целевой пептид и используется для осуществления экспрессии белка в намеченной клетке-мишени. Экспрессионный вектор также содержит регуляторные элементы, функционально связанные с кодирующей областью для облегчения экспрессии белка в клетке-мишени. Комбинацию регуляторных элементов и гена или генов, с которыми они функционально связаны для экспрессии, иногда называют "кассетой экспрессии", большое количество которых известно и доступно из уровня техники или может быть легко создано из компонентов, доступных из уровня техники.
[0058] "Гетерологичный" означает полученный из генотипно отличной единицы от той остальной единицы, с которой он сравнивается. Например, полинуклеотид, введенный генно-инженерным способом в плазмиду или вектор, полученный из разных видов, является гетерологичным полинуклеотидом. Промотор, удаленный из его природной кодирующей последовательности и функционально связанный с кодирующей последовательностью, с которой он в природе не связан, является гетерологичным промотором. Так, например, rAAV, который включает гетерологичную нуклеиновую кислоту, кодирующую гетерологичный генный продукт, является rAAV, включающим нуклеиновую кислоту, обычно не содержащуюся во встречающемся в природе вирусе, AAV дикого типа, и кодируемый гетерологичный генный продукт является генным продуктом, обычно некодируемым встречающимся в природе вирусом, AAV дикого типа.
[0059] Термины "генетическое изменение" и "генетическая модификация" (и их грамматические варианты) используются взаимозаменяемо в данном документе для обозначения процесса, при котором генетический элемент (например, полинуклеотид) вводят в клетку отличным от митоза или мейоза способом. Элемент может быть гетерологичным к клетке или может быть дополнительной копией или усовершенствованной версией элемента, уже существующего в клетке. Генетическое изменение может быть осуществлено, например, путем трасфектирования клетки рекомбинантной плазмидой или другим полинуклеотидом с помощью любого процесса, известного из уровня техники, такого как электропорация, кальций-фосфатная преципитация или контактирование с полинуклеотид-липосомным комплексом. Генетическое изменение также может быть осуществлено, например, путем трансдукции или инфекции вируса ДНК или РНК или вирусного вектора. Обычно генетический элемент вводится в хромосому или минихромосому в клетке; но любое изменение, изменяющее фенотип и/или генотип клетки и ее потомства, включено в этот термин.
[0060] Клетка является так называемой "стабильно" измененной, трансфектированной, генетически модифицированной или трансформированной генетической последовательностью, если последовательность доступна для выполнения ее функции во время продленной культуры клеток in vitro. Обычно такая клетка является «наследственно» измененной (генетически модифицированной) в том отношении, что вводится генетическое изменение, которое также наследуется потомством измененной клетки.
[0061] Термины "полипептид", "пептид" и "белок" используются в настоящем документе взаимозаменяемо для обозначения полимеров аминокислот любой длины. Термины также охватывают модифицированный аминокислотный полимер, например, образованием дисульфидных связей, гликолизацией, липидизацией, фосфорилированием или конъюгацией с маркирующим компонентом. Полипептиды, такие как анти-ангиогенные полипептиды, нейропротекторные полипептиды и подобное, когда обсуждаются в контексте доставки генного продукта субъекту-млекопитающему, и их композиции, относятся, соответственно, к интактному полипептиду или любому его фрагменту или генно-инженерному производному, сохраняющему желаемую биохимическую функцию интактного белка. Подобным образом, указания на нуклеиновые кислоты, кодирующие анти-ангиогенные полипептиды, нуклеиновые кислоты, кодирующие нейропротекторные полипептиды, и другие такие нуклеиновые кислоты для использования в доставке генного продукта субъекту-млекопитающему (которые могут называться "трансгенами" и будут доставлены в клетку-реципиент), включают полинуклеотиды, кодирующие интактный полипептид или любой фрагмент или генно-инженерное производное, обладающие желаемой биохимической функцией.
[0062] "Выделенная" плазмида, нуклеиновая кислота, вектор, вирус, вирион, клетка-хозяин или другое вещество относится к получению вещества, лишенного, по меньшей мере, некоторых других компонентов, которые могут также присутствовать, откуда вещество или подобное вещество происходит или изначально получено. Так, например, выделенное вещество может быть получено с использованием методов очистки для его обогащения из исходной смеси. Обогащение может быть измерено на абсолютном базисе, таком как вес на объем раствора, или оно может быть измерено относительно второго, потенциально интерферирующего вещества, присутствующего в исходной смеси. Увеличивающиеся обогащения вариантов осуществления этого описания являются в возрастающей степени более выделенными. Выделенная плазмида, нуклеиновая кислота, вектор, вирус, клетка-хозяин или другое вещество являются в некоторых вариантах осуществления изобретения очищенными, например, от приблизительно 80% до приблизительно 90% чистоты, по меньшей мере, приблизительно 90% чистоты, по меньшей мере, приблизительно 95% чистоты, по меньшей мере, приблизительно 98% чистоты или, по меньшей мере, приблизительно 99%, или более чистоты.
[0063] Как использовано в настоящем документе, термины "терапия", "лечение" или подобные относятся к получению желательного фармакологического и/или физиологического эффекта. Эффект может быть профилактическим с точки зрения полного или частичного предотвращения болезни или ее симптомов и/или может быть терапевтическим с точки зрения частичного или полного излечивания от болезни и/или неблагоприятного воздействия, относящегося к болезни. "Лечение", как использовано в настоящем документе, охватывает любое лечение болезни у млекопитающего, особенно у человека, и включает: (а) препятствование возникновению болезни у субъекта, предрасположенного к заболеванию или с повышенным риском приобретения заболевания, но у которого болезнь еще не диагностирована; (b) ингибирование болезни, то есть, остановку ее развития; и (с) облегчение болезни, то есть, вызов регресса болезни.
[0064] Термины "индивидуум", "хозяин", "субъект" и "пациент" в настоящем документе используются взаимозаменяемо, относятся к млекопитающим, включая, человеческие и нечеловеческие приматы, включая человекообразных обезьян и людей; млекопитающих спортивных животных (например, лошади); млекопитающих сельскохозяйственных животных (например, овцы, козы и т.д.); млекопитающих домашних животных (собаки, кошки и т.д.); и грызуны (например, мыши, крысы, и т.д.), но не ограничиваются перечисленными.
[0065] Прежде чем дальше описывать настоящее изобретение следует понимать, что это изобретение не ограничивается описанными конкретными вариантами осуществления, и как таковые, они могут, конечно, изменяться. Также следует понимать, что терминология, используемая в настоящем документе, предназначена исключительно для описания конкретных вариантов осуществления изобретения, а не для его ограничения, поскольку объем настоящего изобретения будет ограничиваться только приложенной формулой.
[0066] В случаях, когда предусмотрен диапазон значений, следует понимать, что каждое промежуточное значение, с точностью до десятой единицы нижнего предела, между верхним и нижним пределом такого диапазона или любое другое указанное или промежуточное значение в этом установленном диапазоне, охвачено изобретением, если контекст ясно не указывает иное. Верхние и нижние пределы этих меньших диапазонов могут независимо включаться в меньшие диапазоны и также охватываться изобретением с учетом любого специально исключенного предела в установленном диапазоне. Когда установленный диапазон включает один или оба предела, то диапазоны, исключающие один из двух или оба эти указанные пределы, также включены в изобретение.
[0067] Если не указано иное, то все технические и научные термины, использованные в настоящем документе, имеют те же значения, как и обычно понятные для специалиста в области техники, к которой относится изобретение. Хотя любые методы и материалы, подобные или эквивалентные тем, что описаны в настоящем документе, могут также использоваться в практике или тестировании настоящего изобретения, теперь описаны предпочтительные методы и материалы. Все публикации, указанные в настоящем документе, включены в данную заявку путем ссылки для раскрытия и описания методов и/или материалов, в связи с которыми цитируются публикации
[0068] Нужно отметить, что, как использовано в настоящем документе и в приложенной формуле, формы единственного числа включают формы множественного числа, если контекст ясно не указывает на иное. Так, например, ссылка на "вирион рекомбинантного AAV" включает ряд таких вирионов, а ссылка на "фоторецепторную клетку" включает ссылку на одну или более фоторецепторных клеток и их эквиваленты, известные специалисту в данной области техники, и т.д. Нужно дополнительно отметить, что формула может быть составлена так, чтобы исключить любой необязательный элемент. В таковом качестве это высказывание призвано служить ранее упомянутой основой для использования такой исключительной терминологии как "исключительно", "только" и т.п. в связи с перечислением элементов формулы изобретения или использованием негативных признаков.
[0069] Следует принимать во внимание, что некоторые особенности изобретения, которые для ясности описаны в контексте отдельных вариантов осуществления, могут также предусматриваться в комбинации в единственном варианте осуществления. И наоборот, различные особенности изобретения, которые для краткости описаны в контексте единственного варианта осуществления, могут также предусматриваться отдельно или в любой пригодной субкомбинации. Все комбинации вариантов осуществления, относящиеся к изобретению, определенно охвачены данным изобретением и раскрыты в настоящем документе так же, как если бы каждая комбинация была в нем индивидуально и явно раскрыта. Кроме того, все субкомбинации различных вариантов осуществления изобретения и их элементов также определенно охвачены данным изобретением и раскрыты в настоящем документе так же, как если бы каждая такая подкомбинация была в нем индивидуально и явно раскрыта.
[0070] Публикации, рассмотренные в данном документе, предоставлены исключительно на момент их раскрытия до даты подачи настоящей заявки. Ничто в данном документе не должно истолковываться как допуск, что данное изобретение не наделено правом предшествовать такой публикации по причине более раннего изобретения. Также даты предоставленных публикаций могут отличаться от фактических годов издания, которые, возможно, нуждаются в независимом подтверждении.
Подробное описание
[0071] В настоящем описании предложены вирионы аденоассоциированного вируса (AAV) с измененным (вариантным) капсидным белком, причем вирионы AAV демонстрируют большую инфекционность ретинальной клетки, когда вводятся интравитреальной инъекцией, по сравнению с AAV дикого типа, когда вводятся интравитреальной инъекцией. В настоящем описании дополнительно предложены способы доставки генного продукта в ретинальную клетку у индивидуума и способы лечения болезни глаз.
[0072] Ретинальна клетка может быть фоторецептором (например, палочки; колбочки), ганглиозной клеткой сетчатки (RGC), клеткой Мюллера (глиальная клетка Мюллера), биполярной клеткой, амакринной клеткой, горизонтальной клеткой или клеткой пигментного эпителия сетчатки (RPE).
ВАРИАНТНЫЕ КАПСИДНЫХ БЕЛКИ AAV
[0073] В настоящем описании предложены вариантные капсидные белки AAV, отличающийся тем, что вариантный капсидный белок AAV содержит вставку из приблизительно 5 аминокислот до приблизительно 11 аминокислот в сайте встраивания в петле GH капсидного белка или петле IV, по сравнению с соответствующим капсидным белком родительского AAV, и где вариантный капсидный белок, когда присутствует в вирионе AAV, предоставляет повышенную инфекционность ретинальной клетки по сравнению с инфекционностью ретинальной клетки вирионом AAV, содержащим соответствующий родительский капсидный белок AAV. В некоторых случаях ретинальная клетка является фоторецепторной клеткой (например, палочки; колбочки). В других случаях ретинальная клетка является RGC. В других случаях ретинальная клетка является клеткой RPE. В других случаях ретинальная клетка является клеткой Мюллера. Другие ретинальные клетки включают амакринные клетки, биполярные клетки и горизонтальные клетки. "Вставка из приблизительно 5 аминокислот до приблизительно 11 аминокислот" также именуемая в настоящем документе как "пептидная вставка" (например, вставка гетерологичного пептида). "Соответствующий родительский капсидный белок AAV" относится к капсидному белку AAV того же серотипа AAV без пептидной вставки.
[0074] Сайт встраивания находится в петле GH или петле IV капсидного белка AAV, например, в доступной для растворителя части петли GH или петли IV капсидного белка AAV. Для петли GH/ петли IV капсида AAV, смотри, например, van Vliet et al. (2006) Mol. Ther. 14:809; Padron et al. (2005) J. Virol. 79:5047; и Shen et al. (2007) Mol. Ther. 15:1955. Например, сайт встраивания может находиться в пределах аминокислот 411-650 капсидного белка AAV, как указано на фигурах 17А и 17B. Например, сайт встраивания м